Nội dung bài học Amoniac và muối amoni tìm hiểu về cấu tạo phân tử, tính chất vật lí (tính tan, tỉ khối, màu, mùi), ứng dụng chính, amoniac trong phòng thí nghiệm và trong công nghiệp . Tính chất hoá học của amoniac: Tính bazơ yếu (tác dụng với nước, dung dịch muối, axit) và tính khử (tác dụng với oxi, clo). Cách điều chế NH3. Tính chất vật lí (trạng thái, màu sắc, tính tan). Tính chất hoá học (phản ứng với dung dịch kiềm, phản ứng nhiệt phân) và ứng dụng của muối amoni.
Hình 1: Sơ đồ cấu tạo của phân tử NH3
Video 1: Sự hòa tan của Amoniac trong nước
Dung dịch NH3 đậm đặc trong phòng thí nghiệm có nồng độ 25% (N = 0,91g/cm3).
Tác dụng với nước
NH3 + H2O \(\rightleftharpoons\) NH4++ OH-
Tác dụng với dung dịch bazơ
AlCl3 + 3NH3 + 3 H2O → Al(OH)3 \(\downarrow\) + 3 NH4Cl
Al3++3NH3+3H2O → Al(OH)3 \(\downarrow\) + 3NH4+
Tác dụng với axít
2NH3 + H2SO4 → (NH4)2SO4
NH3 (k) + HCl (k) → NH4Cl
(không màu) (ko màu) (khói trắng)
Video 2: Amoniac tác dụng với axit clohidric
Trong phân tử NH3, N có số oxi hóa là -3. Nitơ có các số oxi hóa là -3,0,+1,+2,+3,+4,+5. Như vậy trong các phản ứng hóa học khi có sự thay đổi số oxi hóa, số oxi hóa của N trong NH3 chỉ có thể tăng lên → thể hiện tính khử.
Tác dụng với oxi
Video 3: Thí nghiệm giữa NH3 và Oxi
NH3 được tạo ra từ phản ứng của NH4Cl và CaO
Khí O2 được tạo ra từ phản ứng của KClO3 và MnO2
Tác dụng với Clo
2NH3 + 3Cl2 → N2 + 6 HCl
Nếu NH3 dư : NH3 + HCl → NH4Cl (khói trắng)
* Kết luận: Amoniac có các tính chất hoá học cơ bản: Tính bazơ yếu và Tính khử
N2 + 3H2 2NH3 \(\triangle H < 0\)
Muối amoni là chất tinh thể ion gồm cation amoni NH4+ và anion gốc axít. Ví dụ: NH4Cl, (NH4)2SO4 , (NH4)2CO3
(NH4)2SO4 + 2NaOH → Na2SO4 + 2NH3 + 2H2O.
Phương trình ion thu gọn: NH4+ + OH- → NH3 + H2O → Điều chế NH3 trong Phòng thí nghiệm và nhận biết muối amoni.
NH4Cl (r) NH3 (k) + HCl (k).
(NH4)2CO3 (r) NH3 (k) + NH4HCO3(r).
NH4HCO3(r) NH3(k) + CO2(k) + H2O
NH4NO2 N2 + 2H2O
NH4NO3 N2O + 2H2O
Để nhận biết các dung dịch: NH4NO3, (NH4)2SO4, K2SO4 đựng trong các lọ mất nhãn ta dùng:
Hỗn hợp X gồm N2 và H2 có tỉ khối so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác) thu được hỗn hợp Y có tỉ khối so với He bằng 2. Hiệu suất của phản ứng tổng hợp NH3 là:
MX = 7,2. Áp dụng quy tắc đường chéo ta có: \(n_{H_2}:n_{N_2}=4:1\)
⇒ Giả sử ban đầu có 4 mol H2 và 1 mol N2 trong X
N2 + 3H2 ↔ 2NH3
x → x → 2x
⇒ sau phản ứng: nY = 2x + (1 - x) + (4 - 3x) = 5 - 2x mol
Bảo toàn khối lượng: mX = mY
⇒ 5 × 7,2 = (5 - 2x) × 2 × 4
⇒ x = 0,25 mol
⇒ H% (tính theo N2) = 25%
Cho các phản ứng sau:
4NH3 + 5O2 → 4NO + 6H2O (1)
NH3 + H2SO4 → NH4HSO4 (2)
2NH3 + 3CuO → 3Cu + N2\(\uparrow\) + 3H2O (3)
8NH3 + 3Cl2 → N2 + 6NH4Cl (4)
NH3 + H2S → NH4HS (5)
2NH3 + 3O2 → 2N2\(\uparrow\) + 6H2O (6)
NH3 + HCl → NH4Cl (7)
Số phản ứng trong đó NH3 không đóng vai trò là chất khử là:
Các phản ứng mà có sự tăng số oxi hóa của N ⇒ NH3 thể hiện tính khử. Các phản ứng không có hiện tượng trên là: 2, 5, 7.
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 8có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Khí nào dưới đây làm xanh quỳ tím ẩm?
Khi nhiệt phân, muối nitrat nào sau đây có thể không thu được khí O2?
Để nhận biết các dung dịch muối (đựng riêng biệt trong các ống nghiệm): Al(NO3)3, (NH4)2SO4, NH4NO3, MgCl2 có thể dùng dung dịch:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 8.
Bài tập 1 trang 37 SGK Hóa học 11
Bài tập 2 trang 37 SGK Hóa học 11
Bài tập 3 trang 37 SGK Hóa học 11
Bài tập 4 trang 37 SGK Hóa học 11
Bài tập 5 trang 37 SGK Hóa học 11
Bài tập 6 trang 37 SGK Hóa học 11
Bài tập 7 trang 37 SGK Hóa học 11
Bài tập 8 trang 38 SGK Hóa học 11
Bài tập 8.1 trang 11 SBT Hóa học 11
Bài tập 8.2 trang 11 SBT Hóa học 11
Bài tập 8.3 trang 11 SBT Hóa học 11
Bài tập 8.4 trang 11 SBT Hóa học 11
Bài tập 8.5 trang 12 SBT Hóa học 11
Bài tập 8.6 trang 12 SBT Hóa học 11
Bài tập 8.7 trang 12 SBT Hóa học 11
Bài tập 8.8 trang 12 SBT Hóa học 11
Bài tập 8.9 trang 13 SBT Hóa học 11
Bài tập 8.10 trang 13 SBT Hóa học 11
Bài tập 8.11 trang 13 SBT Hóa học 11
Bài tập 8.12 trang 13 SBT Hóa học 11
Bài tập 1 trang 47 SGK Hóa học 11 nâng cao
Bài tập 2 trang 47 SGK Hóa học 11 nâng cao
Bài tập 3 trang 47 SGK Hóa học 11 nâng cao
Bài tập 4 trang 47 SGK Hóa học 11 nâng cao
Bài tập 5 trang 47 SGK Hóa học 11 nâng cao
Bài tập 6 trang 47 SGK Hóa học 11 nâng cao
Bài tập 7 trang 48 SGK Hóa học 11 nâng cao
Bài tập 8 trang 48 SGK Hóa học 11 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Khí nào dưới đây làm xanh quỳ tím ẩm?
Khi nhiệt phân, muối nitrat nào sau đây có thể không thu được khí O2?
Để nhận biết các dung dịch muối (đựng riêng biệt trong các ống nghiệm): Al(NO3)3, (NH4)2SO4, NH4NO3, MgCl2 có thể dùng dung dịch:
Thành phần của dung dịch NH3 gồm:
Cho hình vẽ mô tả thí nghiệm như sau:
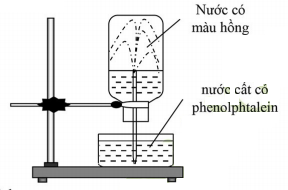
Hình vẽ mô tả thí nghiệm để chứng minh:
Nito trong chất nào sau đâu vừa có tính oxi hóa vừa có tính khử?
Để làm khô, sạch khí NH3 có lẫn hơi nước người ta dùng:
Tã lót trẻ em sau khi giặt vẫn giữ lại 1 lượng nhỏ amoniac. Để khử sạch amoniac nên dùng chất gì sau đây cho vào nước xả cuối cùng để giặt?
Phân bón nào sau đây làm tăng độ chua của đất?
Hỗn hợp X gồm N2 và H2 có tỉ khối so với H2 bằng 3,6. Sau khi tiến hành phản ứng tổng hợp amoniac trong bình kín (có xúc tác bột Fe) thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Hiệu suất phản ứng tổng hợp amoniac là:
Mô tả và giải thích hiện tượng xảy ra trong thí nghiệm chứng minh rằng ammoniac tan nhiều trong nước.
Hoàn thành sơ đồ chuyển hóa sau đây và viết các phương trình hóa học:
Khí A (+H2O)→ Dung dịch A (+ HCl) → B + (NaOH)→ Khí A + (HNO3) → C (to)→ D + H2O
Biết rằng A là hợp chất của nitơ.
Hiện nay, để sản xuất ammoniac, người ta điều chế nitơ và hiđro bằng cách chuyển hóa có xúc tác một hỗn hợp gồm không khí, hơi nước và khí metan (thành phần chính của khí thiên nhiên). Phản ứng giữa khí metan và hơi nước tạo ra hiđro và cacbon đioxit. Để loại khí oxi và thu khí nitơ, người ta đốt khí metan trong một thiết bị kín chứa không khí.
Hãy viết các phương trình hóa học của phản ứng điều chế hiđro, loại khí oxi và tổng hợp khí ammoniac.
Trình bày phương pháp hóa học để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4. Viết phương trình hóa học của các phản ứng đã dùng.
Muốn cho cân bằng của phản ứng tổng hợp amoniac chuyển dịch sang phải, cần phải đồng thời:
A. Tăng áp suất và tăng nhiệt độ.
B. Giảm áp suất và giảm nhiệt độ.
C. Tăng áp suất và giảm nhiệt độ.
D. Giảm áp suất và tang nhiệt độ.
Trong phản ứng nhiệt phân các muối NH4NO2 và NH4NO3, số oxi hóa của nitơ biến đổi như thế nào? Nguyên tử nitơ trong ion nào của muối đóng vai trò chất khử và nguyên tử nitơ trong ion nào của muối đóng vai trò chất oxi hóa?
Cho dung dịch NaOH dư vào 150,0 ml dung dịch (NH4)2SO4 1,00 M, đun nóng nhẹ.
a) Viết phương trình hóa học ở dạng phân tử và dạng ion rút gọn.
b) Tính thể tích khí (đktc) thu gọn.
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,0 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25,0%. Các thể tích khí được đo ở đktc.
A. 44,8 lít N2 và 134,4 lít H2
B. 22,4 lít N2 và 134,4 lít H2
C. 22,4 lít N2 và 67,2 lít H2
D. 44,8 lít N2 và 67,2 lít H2
Trong dung dịch, amoniac là một bazơ yếu là do
A. amoniac tan nhiều trong nước.
B. phân tử amoniac là phân tử có cực.
C. khi tan trong nước, amoniac kết hợp với nước tạo ra các ion NH4+ và OH−.
D. khi tan trong nước, chỉ một phần nhỏ các phân tử amoniac kết hợp với ion H+ của nước, tạo ra các ion NH4+ và OH−.
Dãy nào dưới đây gồm các chất chứa nguyên tử nitơ có khả năng vừa thể hiện tính khử vừa thể hiện tính oxi hoá khi tham gia phản ứng?
A. NH3, N2O5, N2, NO2
B. NH3, NO, HNO3, N2O5
C. N2, NO, N2O, N2O5
D. NO2, N2, NO, N2O3
Trong các phản ứng hóa học dưới đây, ở phản ứng nào amonic không thể hiện tính khử?
A. Khí amoniac tác dụng với đồng (II) oxit nung nóng tạo ra N2, H2O và Cu.
B. Khi amoniac tác dụng với khí hiđro clorua.
C. Khi amoniac tác dụng với khí clo.
D. Đốt cháy amoniac trong oxi.
Trong các dãy chất dưới đây, dãy nào gồm các chất đều phản ứng với NH3 trong điều kiện thích hợp?
A. Dung dịch HCl, dung dịch AlCl3, Cu, O2.
B. Dung dịch HNO3, dung dịch ZnCl2, dung dịch KOH, Cl2.
C. Dung dịch H2SO4, dung dịch FeCl3, O2, Cl2.
D. Dung dịch H3PO4, dung dịch CuCl2, dung dịch NaOH, O2.
Phản ứng tổng hợp amoniac là phản ứng thuận nghịch:
N2(k) + 3H2(k) ⇔ 2NH3(k)
ΔH = -92 kJ
Cân bằng của phản ứng này chuyển dịch như thế nào khi thay đổi một trong các điều kiện sau đây ? Giải thích.
1. Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống.
2. Giảm nhiệt độ.
3. Thêm khí nitơ.
4. Dùng chất xúc tác thích hợp.
Cho lượng khí amoniac đi từ từ qua ống sứ chứa 3,2 g CuO nung nóng đến khi phản ứng xảy ra hoàn toàn, thu được chất rắn A và một hỗn hợp khí. Chất rắn A phản ứng vừa đủ với 20,0 ml dung dịch HCl 1,00M.
1. Viết phương trình hoá học của các phản ứng.
2. Tính thể tích khí nitơ (đktc) được tạo thành sau phản ứng.
Trong những nhận xét dưới đây về muối amoni, nhận xét nào đúng?
A. Muối amoni là chất tinh thể ion, phân tử gồm cation amoni và anion hiđroxit.
B. Tất cả các muối amoni đều dễ tan trong nước, khi tan phân li hoàn toàn thành cation amoni và anion gốc axit.
C. Dung dịch muối amoni tác dụng với dung dịch kiềm đặc, nóng cho thoát ra chất khí làm quỳ tím hoá đỏ.
D. Khi nhiệt phân muối amoni luôn luôn có khí amoniac thoát ra.
Phản ứng nào dưới đây là phản ứng oxi hóa - khử?
A. (NH4)2SO4 + 2NaOH → 2NH3↑ + H2O + Na2SO4
B. NH4HCO3 to→ NH3↑ + CO2↑ + H2O
C. NH4Cl to→ NH3↑ + HCl↑
D. NH4NO3 to→ N2O + 2H2O
Trong các phản ứng nhiệt phân muối amoni dưới đây, phản ứng nào không là phản ứng oxi hóa - khử?
A. NH4NO2 → N2 + 2H2O
B. NH4NO3 → N2O + 2H2O
C. NH4HCO3 → NH3 + CO2 + H2O
D. (NH4)2Cr2O7 → N2 + Cr2O3 + 4H2O
Hoàn thành các phương trình hoá học sau đây:
1. ? + OH− → NH3 + ?
2. (NH4)3PO4 to→ NH3 + ?
3. NH4Cl + NaNO2 to→ ? + ? + ?
4. (NH4)2Cr2O7 to→ N2 + Cr2O3 + ?
Chỉ được dùng một kim loại, hãy trình bày cách phân biệt các dung dịch muối sau đây: NH4NO3, (NH4)2SO4, K2SO4. Viết phương trình hoá học của các phản ứng xảy ra.
Cho dung dịch Ba(OH)2 đến dư vào 75 ml dung dịch muối amoni sunfat.
1. Viết phương trình hoá học của phản ứng dưới dạng ion.
2. Tính nồng độ mol của các ion trong dung dịch muối ban đầu, biết rằng phản ứng tạo ra 17,475 g một chất kết tủa. Bỏ qua sự thuỷ phân của ion amoni trong dung dịch.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Với hiệu suất phản ứng tổng hợp amoniac 35% thì có thể thu được bao nhiêu lít khí amoni từ 5 lít không khí ( giả sử trong không khí, nito chiếm 80% thể tích), biết các khí đo ở cùng điều kiện nhiệt độ và áp suất?
A. 8 lít NH3
B. 3,5 lít NH3
C. 2,8 lít NH3
D. 10 lít NH3
Câu trả lời của bạn
5 lít không khí có : 1 lít O2
4 lít N2
pthh N2 + 3H2 ➜ 2NH3
4
VNH3 = 4.35%/2 = 0,7 l
CÂU 1.cho 5.4 gam AL tác dụng với dd HNO3 loãng dư, thu V lít khí NxOy ở ( đktc) là sản phẩm khử duy nhất có tỉ khối hơi NxOy so với khí H2 là 14 . Gía trị V là ?
CÂU 2.cho m gam Zn tác dụng với đ HNO3 loãng dư thu được 2.912 lít khí N2O ỏ đktc la san pham khu duy nhất . Gía trị m ?
Câu trả lời của bạn
1. NH3 dư + Cl2 ->
2. NH3+ FECL3 + H2O ->
3. NH3 DƯ + CUCL2 + H20 ->
4. Fe2O3 + HNO3 đ ->
5. Fe3O4 + HNO3 đ ->
6. AL + HNO3 đặc nguội ->
Câu trả lời của bạn
1. 8NH3 + 3Cl2 → H2 + 6NH4Cl
2. 3H2O + 3NH3 + FeCl3 → 3NH4Cl + Fe(OH)3
3. 2H2O + 2NH3 + CuCl2 → Cu(OH)2 + 2NH4Cl
4. Fe2O3 + 6HNO3 → 2Fe(NO3)2 + 3H2O
5. 28HNO3 + 3Fe3O4 → 14H2O + NO + 9Fe(NO3)3
6. Không có phản ứng xảy ra.
thank you 
cho mình hỏi tại sao muối NH4HCO3 lại có thể làm xốp bánh ?
Câu trả lời của bạn
nh4hco3 khi nấu lên phân hủy tạo nh3 và co2 thoát ra bên ngoài đẩy lớp bột bánh làm bánh xopp
dung dịch X chứa các ion NH4, Fe3+, SO4, NO3. cho 100ml X tác dụng dd Ba(OH)2 dư đun nhẹ được 4,48l khí và 57,3g kết tủa. mặt khác khi làm khô cẩn thận 100ml dd X thu được 34,6g muối kha. tính nồng độ mol có trong dd X
Câu trả lời của bạn
X là hỗn hợp của N2 và H2 có tỉ khối so với H2 là 6.2. Nung nóng X trong 1 bình kín có xt thu được hỗn hợp khí có dX/H2 là 7.75 . Hiệu suất phản ứng tổng hợp NH3 là ?????
Câu trả lời của bạn
![[âIMG]](https://dapanhay.com/filemanager/data-images/48968221_197540147776936_5032274874186334208_n.jpg?_nc_cat=103&_nc_ht=scontent.fdad1-1.fna&oh=ba7a0048891688cae9b6328499af5bd7&oe=5CCD8587)
alo alo, mn ơi, Câu này nan giải này, làm sao giờ :D
Tã lót trẻ em sau khi giặt thường vẫn còn sót lại một lượng nhỏ amoniac, dễ làm cho trẻ bị viêm da, thậm chí mẩn ngứa, tấy đỏ. Để khử sạch amoniac nên dùng chất gì sau đây cho vào nước xả cuối cùng để giặt ?
A. Phèn chua B. Giấm ăn C. Muối ăn D. Gừng tươi
Câu trả lời của bạn
hi hi 
hihi. Hóa ứng dụng mà. Khó phải rồi ^^
Tã lót trẻ em sau khi giặt thường lưu lại lượng amoniac và bột giặt mà mắt thường không nhìn thấy được. Với số lượng chất hoá học còn xót lại này rất có thể làm cho da bị viêm, thậm chí bị sưng tấy đau ngứa. Bởi vậy, khi giặt tã lót, nếu nhỏ vào nước giặt một vài giọt giấm ăn, các loại chất trên sẽ được khử sạch.
(Chưa test thử nên ko chắc nhé. Nhà không có trẻ con . haha)
Chế Anh Trần "còn xót lại" haha 
trong phòng thí nghiệm khí amoniac được điều chế bằng cách cho muối amoniac tác dụng với dung dịch kiềm đun nóng nhẹ . hình vẽ nào sau đây biểu diễn phương pháp thu khí NH3 tốt nhất
Câu trả lời của bạn
Em muốn tải hình ảnh lên thì chọn hình ảnh => tải lên => chọn tệp => tải lên máy chủ => Đồng ý
Như này nè:
sau đó
Dung dịch X chứa 0,2 mol Ca2+; 0,08 mol Cl- ; z mol HCO3- và t mol NO3-. Cô cạn X rồi nung đến khối lượng không đổi, thu được 16,44 gam chất rắn Y. Nếu thêm t mol HNO3 vào X rồi đun dung dịch đến cạn thì thu được muối khan có khối lượng là
A. 20,60 gam. B. 30,52 gam. C. 25,56 gam. D. 19,48 gam.
Câu trả lời của bạn
Sau khi cô cạn và nung đến khối lượng không đổi X thì: 2HCO3- → CO32- + CO2 ↑ → O2- + CO2↑
NO3- → NO2-
=> chất rắn gồm : CaO , CaCl2 , Ca(NO2)2
0,2 mol Ca2+ ; 0,08 mol Cl- ; 0,5z mol O2- ; t mol NO2-
=> mY = 16,44 = 0,2.40 + 0,08.35,5 + 0,5z.16 + 46t (1)
Lại có : Trong Y bảo toàn điện tích : 2nCa = nCl + nHCO3 + nNO3
=> 2.0,2 = 0,08 + z + t (2)
Từ (1) và (2) => z = 0,24 mol ; t = 0,08 mol Khi cho t mol HNO3 vào X :
HNO3 + HCO3- → CO2 + H2O + NO3-
Còn lại: 0,16 mol HCO3-, 0,2 mol Ca2+ ; 0,08 mol Cl-
Cô cạn thì : 2HCO3 - → CO2 + CO32- (nCO32- = ½ n HCO3 = 0,08 mol)
=> mrắn = mCa + mCO3 + mNO3 + mCl = 25,56g
1/ Nung nóng 0,5 mol hỗn hợp X gồm H2 , N2 trong bình kín có xúc tác thích hợp, sau một thời gian thu được hỗn hợp Y. Cho 1/2 Y đi qua ống đựng Cuo dư nong nóng thấy khối lượng chất rắn trong ống giảm nhiều nhất là 3,2 g. Tỉ khối hơi của Y so với X
2/ Cho V(l) NH3 phản ứng vừa đủ với 200 ml dung dịch Al2(SO4)3 xM sau phản ứng lọc kết tủa và cho vào 10 ml dung dịch NaOH 2M thì kết tủa vừa hết. Giá trị của V, x lần lượt là ?
Câu trả lời của bạn
Bài 1:
3CuO+2NH3−−−>3Cu+N2+3H2O
3x/2------x
CuO+H2−−−>Cu+H2OCuO+H2−−−>Cu+H2O
(b-3x)/2--(b-3x)/2
==> mol O = b/2 = 0,2 ==> b = 0,4
Gọi a, b là mol N2 và H2 có trong X
==> trong Y có 2x mol NH3, (a-x) mol N2 dư và (b-3x) mol H2 dư
Y + CuO ---> Cu + NH3 + H2O + N2
==> toàn bộ H2 trong X sẽ chuyển thành H2O sau phản ứng
==> mol rắn giảm = mol O = mol H2O = số mol H2 = b = 2*3,2/16 = 0,4 => a = 0,1
Khối lượng X = 2*0,4 + 28*0,1 = 3,6 => phân tử lượng X = 3,6/0,5 = 7,2
dX/H2 = 7,2/2 = 3,6
Ca dao Việt Nam có câu:
“Lúa chim lấp ló ngoài bờ
Hễ nghe tiếng sấm phất cờ mà lên”
Mang ý nghĩa hóa học gì ?
Câu ca dao có nghĩa là: Khi vụ lúa chiêm đang trổ đồng mà có trận mưa rào kèm theo sấm chớp thì rất tốt và cho năng suất cao. Vì sao vậy ?
Câu trả lời của bạn
Do trong không khí có khoảng 80% Nitơ và 20 % oxi. Khi có sấm chớp( tia lửa điện) thì:
2N2 + O2 → 2NO
Sau đó:
2NO + O2 → 2NO2
Khí NO2 hòa tan trong nước:
4NO2 + O2 + H2O → 4HNO3
HNO3 → H+ + NO3-
(Đạm)
Nhờ có sấm chớp ở các cơn mưa giông, mỗi năm trung bình mỗi mẫu đất được cung cấp khoảng 6-7 kg nitơ.
cho 5,6 g fe vao dd hno3 sau pu thu duoc khi no va dd a chua 22,34 g muoi (khong co muoi amoni) tinh Vno va Nhno3
Câu trả lời của bạn
Nhno3 ????????????????
tinh so mol hno3 nhat nheo

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *