Nội dung bài học Anken tìm hiểu về đồng đẳng, đồng phân, danh pháp anken; Tính chất vật lí, hóa học của anken như phản ứng cộng (cộng hidro, cộng halogen, cộng HX, ...), hiểu về quy tắc Maccopnhicop, phản ứng trùng hợp, phản ứng oxi hóa hoàn toàn và không hoàn toàn; điều chế và ứng dụng anken.
(Từ C2H4, theo khái niệm đồng đẳng: C2H4(CH2)k → C2+kH4+2k đặt 2 + k = n thì công thức phân tử chung của anken là: CnH2n (\(n \ge 2\))
a) Đồng phân cấu tạo
CH2=CH-CH2-CH3
CH3-CH=CH-CH3
b) Đồng phân hình học
Điều kiện: \(\begin{array}{l} {R_1} \ne {R_2}\\ {R_3} \ne {R_4} \end{array}\)
;
a) Tên thông thường
Tên anken = Tên ankan đổi đuôi an thành ilen
Ví dụ :
CH2=CH2: Etilen
CH2=CH-CH3 Propilen
b) Tên thay thế
Tên anken = Tên ankan đổi đuôi an thành en
*Quy tắc:
Số chỉ vị trí nhánh + tên nhánh + tên C mạch chính + số chỉ liên kết đôi + en
*Ví dụ:
CH2=CH2: Eten
CH2=CH-CH3 : Propen
CH2=CH-CH2-CH3 But-1-en
CH3-CH=CH-CH3 But-2-en
Hình 1: Mô hình phân tử etilen
Đặc điểm cấu tạo của anken có một liên kết đôi C=C (gồm một liên kết \(\sigma\) bền vững và một liên kết \(\pi\) kém bền)
Dự đoán tính chất hóa học của anken
Liên kết đôi là trung tâm phản ứng.
Phản ứng phá vỡ liên kết \(\pi\) kém bền.
Phản ứng cộng là phản ứng trong đó phân tử hợp chất hữu cơ kết hợp với phân tử khác tạo thành phân tử hợp chất mới.
a) Cộng hiđrô (Phản ứng hiđro hoá)
CnH2n + H2 CnH2n+2
CH2=CH2 + H2 CH3-CH3
CH3-CH=CH2 + H2 
CH3-CH2-CH3
b) Cộng halogen (Phản ứng halogen hoá)
CnH2n + Br2 → CnH2nBr2
Anken làm mất màu của dung dịch brom → Phản ứng này dùng để nhận biết anken.
Video 1: Etilen tác dụng với dung dịch Brom
CH2=CH2 + Br2 → BrCH2 - CH2Br
(Màu nâu đỏ) 1,2-đibrometan
(Không màu)
c) Cộng HX (X là OH, Cl, Br,…)
CH2=CH2 + HBr → CH3-CH2Br
CH2=CH2 + H-OH CH3-CH2OH
Qui tắc Mac-côp-nhi-côp:
Trong phản ứng cộng HX vào liên kết đôi,nguyên tử H (hay phần mang điện tích dương) chủ yếu cộng vào nguyên tử cacbon bậc thấp hơn (có nhiều H hơn), còn nguyên tử hay nhóm nguyên tử X (phần mang điện tích âm) cộng vào nguyên tử cacbon bậc cao hơn (có ít H hơn).
nCH2=CH2 [- CH2–CH2 -]n
a) Oxi hoá hoàn toàn
Phản ứng đốt cháy anken: số mol CO2 = số mol H2O
b) Oxi hoá không hoàn toàn
Anken làm mất màu dd KMnO4 → Dùng để nhận biết anken
Etilen được điều chế từ ancol etylic theo phương trình:
C2H5OH CH2=CH2 + H2O
Video 2: Điều chế etilen từ ancol etylic
Anken được điều chế từ ankan
CnH2n+2 CnH2n + H2
Hình 2: Ứng dụng của anken
Số đồng phân cấu tạo của C4H8 là:
Hỗn hợp X gồm H2 và một anken (là chất khí ở điều kiện thường) có số mol bằng nhau. Dẫn X qua Ni nung nóng, thu được hỗn hợp Y có tỉ khối so với He bằng 11,6. Hiệu suất của phản ứng hiđro hóa là:
Giả sử X gồm 1 mol H2 và 1 mol CnH2n
CnH2n + H2 → CnH2n+2
x → x x (mol)
Sau phản ứng còn: (1 – x) mol H2; (1 – x) mol CnH2n và x mol CnH2n+2
mX = mY ⇒ 14n + 2 = (2 – x)11,6 × 4
Do x < ⇒ 14n + 2 > 46,4 ⇒ n > 3,16
Mà anken này ở thể khí ⇒ n ≤ 4 ⇒ n = 4 TM
⇒ x = 0,75 mol
⇒ Hpứ = 75%
Đốt cháy hoàn toàn 8,96 lít (đktc) hỗn hợp hai anken X và Y là đồng đẳng liên tiếp thu được m gam nước và (m+39)gam CO2. Công thức phân tử của hai anken X và Y là?
Đốt cháy anken cho \(n_{H_{2}O}=n_{CO_{2}}\rightarrow \frac{m}{18}=\frac{m+39}{44}\Rightarrow m=27\)
\(n_{CO_{2}}=\frac{27+39}{44}=1,5 mol,n_{hh}=\frac{8,96}{22,4}=0,4 mol\)
Đặt hai công thức chung của hai anken là:
\({C_{\overline n }}{H_{2\overline n }} + \frac{{3\bar n}}{2}{O_2} \to \bar nC{O_2} + \bar n{H_2}O\)
\(0,4\hspace{80pt}0,4\bar{n}\)
\(n_{CO_{2}}=0,4\bar{n}=1,5\Rightarrow \bar{n}=3,75\)
Công thức hai anken là: C4H8 và C3H6
Bài 4:
Hỗn hợp khí X gồm H2 và một anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất. Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của anken là:
\(\\ M_{X} = 18,3; \ M_{Y}= 26 \\ n_{X} = 1 \ mol \Rightarrow m_{Y}=m_{X}=9,1.2=18,2 \ g \\ n_{Y} = \frac{18,2}{26}=0,7 \ mol \Rightarrow n_{H_{2} \ pu}= 1-0,7=0,3 \ mol\)
\(\\ \Rightarrow Y\left\{\begin{matrix} C_{n}H_{2n+2} : 0,3 \\ H_{2}:0,4 \ \ \ \ \ \ \ \end{matrix}\right. \\ (14n+2).0,3 +2. 0,4 =18,2 \Rightarrow n=4 \Rightarrow anken: C_{4}H_{8}\)
Anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất CH3–CH=CH–CH3
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 29có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Trong các đồng đẳng của etilen thì chất nào có %C = 85,71%
Điều chế etilen trong phòng thí nghiệm từ C2H5OH (H2SO4 đặc,\(t^{o}\geq 170^{o}C\)) thường có lẫn các oxit như CO2, SO2. Chọn một trong số các chất sau để loại bỏ CO2, SO2?
Số đồng phân cấu tạo của hidrocacbon có công thức phân tử C5H10 là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 29.
Bài tập 1 trang 132 SGK Hóa học 11
Bài tập 2 trang 132 SGK Hóa học 11
Bài tập 3 trang 132 SGK Hóa học 11
Bài tập 4 trang 132 SGK Hóa học 11
Bài tập 5 trang 132 SGK Hóa học 11
Bài tập 6 trang 132 SGK Hóa học 11
Bài tập 29.1 trang 44 SBT Hóa học 11
Bài tập 29.2 trang 44 SBT Hóa học 11
Bài tập 29.3 trang 44 SBT Hóa học 11
Bài tập 29.4 trang 44 SBT Hóa học 11
Bài tập 29.5 trang 45 SBT Hóa học 11
Bài tập 29.6 trang 45 SBT Hóa học 11
Bài tập 29.7 trang 45 SBT Hóa học 11
Bài tập 29.8 trang 45 SBT Hóa học 11
Bài tập 29.9 trang 45 SBT Hóa học 11
Bài tập 29.10 trang 45 SBT Hóa học 11
Bài tập 29.11 trang 45 SBT Hóa học 11
Bài tập 29.12 trang 46 SBT Hóa học 11
Bài tập 29.13 trang 46 SBT Hóa học 11
Bài tập 29.14 trang 46 SBT Hóa học 11
Bài tập 1 trang 158 SGK Hóa học 11 nâng cao
Bài tập 2 trang 158 SGK Hóa học 11 nâng cao
Bài tập 3 trang 158 SGK Hóa học 11 nâng cao
Bài tập 4 trang 158 SGK Hóa học 11 nâng cao
Bài tập 5 trang 158 SGK Hóa học 11 nâng cao
Bài tập 1 trang 164 SGK Hóa học 11 nâng cao
Bài tập 2 trang 164 SGK Hóa học 11 nâng cao
Bài tập 3 trang 164 SGK Hóa học 11 nâng cao
Bài tập 4 trang 164 SGK Hóa học 11 nâng cao
Bài tập 5 trang 164 SGK Hóa học 11 nâng cao
Bài tập 6 trang 164 SGK Hóa học 11 nâng cao
Bài tập 7 trang 165 SGK Hóa học 11 nâng cao
Bài tập 8 trang 165 SGK Hóa học 11 nâng cao
Bài tập 9 trang 165 SGK Hóa học 11 nâng cao
Bài tập 10 trang 165 SGK Hóa học 11 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Trong các đồng đẳng của etilen thì chất nào có %C = 85,71%
Điều chế etilen trong phòng thí nghiệm từ C2H5OH (H2SO4 đặc,\(t^{o}\geq 170^{o}C\)) thường có lẫn các oxit như CO2, SO2. Chọn một trong số các chất sau để loại bỏ CO2, SO2?
Số đồng phân cấu tạo của hidrocacbon có công thức phân tử C5H10 là:
Cho 2 anken tác dụng với H2O xúc tác dung dịch H2SO4 thu được 2 ancol (rượu). 2 anken đó là:
Số liên kết \(\sigma\) (xích ma) có trong một phân tử propen là?
Hỗn hợp X gồm H2 và C2H4 có tỉ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng, thu được hỗn hợp Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hiđro hóa là:
Cho hỗn hợp hai anken đồng đẳng kế tiếp nhau tác dụng với nước (có H2SO4 làm xúc tác) thu được hỗn hợp Z gồm hai rượu (ancol) X và Y. Đốt cháy hoàn toàn 1,06 gam hỗn hợp Z sau đó hấp thụ toàn bộ sản phẩm cháy vào 2 lít dung dịch NaOH 0,1M thu được dung dịch T trong đó nồng độ của NaOH bằng 0,05M. Công thức cấu tạo thu gọn của X và Y là:
Đốt cháy hoàn toàn 8,96 lít (đkc) hỗn hợp M gồm 2 anken đồng đẳng liên tiếp X; Y (MX < MY) rồi dẫn toàn bộ sản phẩm cháy lần lượt qua bình I đựng P2O5 dư và bình II đựng dung dịch Ca(OH)2 dư thấy khối lượng bình 1 tăng m gam và khối lượng bình II tăng (m + 39) gam. Phần trăm khối lượng anken Y trong M là:
Hỗn hợp X gồm etilen và propilen với tỷ lệ thể tích tương ứng 3 : 2. Hidrat hóa hoàn toàn 1 thể tích X thu được hỗn hợp ancol Y trong đó tỷ lệ về khối lượng các ancol bậc 1 so với bậc 2 là 28 : 15. Thành phần phần trăm về khối lượng của các ancol iso-propylic trong Y là:
Để khử hoàn toàn 200 ml dung dịch KMnO4 0,2M tạo thành chất rắn màu đen cần V lít khí C2H4 (đktc). Giá trị tối thiểu của V là
So sánh anken với ankan về đặc điểm cấu tạo và tính chất hóa học. Cho thí dụ minh họa?
Ứng với công thức C5H10 có bao nhiêu đồng phân cấu tạo?
A. 4
B. 5
C. 3
D. 7
Viết phương trình hóa học của phản ứng xảy ra khi:
a) Propilen tác dụng với hidro, đun nóng (xúc tác Ni).
b) But-2-en tác dụng với hirdo clorua.
c) Metylpropen tác dụng với nước có xúc tác axit.
d) Trùng hợp but-1-en.
Trình bày phương pháp hóa học để:
a) Phân biệt metan và etilen.
b) Tách lấy khí metan từ hỗn hợp etilen.
c) Phân biệt hai bình không dán nhãn đựng hexan và hex-1-en.
Viết phương trình hóa học của các phản ứng đã dùng.
Chất nào sau đây làm mất màu dung dịch brom?
A. Butan
B. But-1-en
C. Cacbon đioxit
D. Metylpropan
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,90gam.
a) Viết các phương trình hóa học và giải thích các hiện tượng ở thí nghiệm trên.
b) Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
Hợp chất sau có tên là gì?
A. 2-đimetylpent-4-en.
B. 2,2-đimetylpent-4-en.
C. 4-đimetylpent-l-en.
D. 4,4-đimetylpent-l-en.
Hợp chất sau có tên là gì?
A. 3-metylenpentan
B. 1,1-đietyleten
C. 2-etylbut-1-en
D. 3-etylbut-3-en
Nhận xét sau đây là sai ?
A. Tất cả các anken đều có công thức là CnH2n.
B. Tất cả các chất có công thức chung CnH2n đều là anken.
C. Tất cả các anken đều làm mất màu dung dịch brom.
D. Tất cả các anken đều làm mất màu dung dịch KMnO4.
Hợp chất 2,4-đimetylhex-1-en ứng với công thức cấu tạo nào cho dưới đây?
A. 
B. 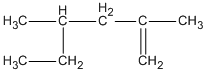
C. 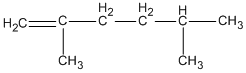
D. 
Để phân biệt etan và eten, dùng phản ứng nào cho dưới đây là thuận tiện nhất ?
A. Phản ứng đốt cháy
B. Phản ứng cộng với hiđro
C. Phản ứng với nước brom
D. Phản ứng trùng hợp
Chất X có công thức phân tử C4H8. X có thể làm mất màu dung dịch brom và khi tác dụng với HCl tạo ra một sản phẩm duy nhất. Tên chất X đó là
A. xiclobutan.
B. but-1-en.
C. but-2-en.
D. 2 metylprop-1-en.
Trình bày phương pháp hoá học để phân biệt ba khí: etan, etilen và cacbon đioxit.
Hỗn hợp khí A chứa một ankan và một anken, Khối lượng hỗn hợp A là 9 gam và thể tích là 8,96 lít. Đốt cháy hoàn toàn A, thu được 13,44 lít CO2. Các thể tích được đo ở đktc.
Xác định công thức phân tử và phần trăm thể tích từng chất trong A.
0,7 g một anken có thể làm mất màu 16,0 g dung dịch brom (trong CCl4) có nồng độ 12,5%.
1. Xác định công thức phân tử chất A.
2. Viết công thức cấu tạo của tất cả các đồng phân cấu tạo ứng với công thức phân tử tìm được. Ghi tên từng đồng phân.
Hỗn hợp khí A chứa eten và hiđro. Tỉ khối của A đối với hiđro là 7,5. Dẫn A đi qua chất xúc tác Ni nung nóng thì A biến thành hỗn hợp khí B có tỉ khối đối với hiđro là 9,0.
Tính hiệu suất phản ứng cộng hiđro của eten.
Hỗn hợp khí A chứa hiđro và một anken. Tỉ khối của A đối với hiđro là 6,0. Đun nóng nhẹ hỗn hợp A có mặt chất xúc tác Ni thì A biến thành hỗn hợp khí B không làm mất màu nước brom và có tỉ khối đối với hiđro là 8,0.
Xác định công thức phân tử và phần trăm thể tích của từng chất trong hỗn hợp A và hỗn hợp B.
Hỗn hợp khí A chứa hiđro và 2 anken kế tiếp nhau trong dãy đồng đẳng. Tỉ khối của A đối với hiđro là 8,26. Đun nóng nhẹ hỗn hợp A có mặt chất xúc tác Ni thì A biến thành hỗn hợp khí B không làm mất màu nước brom và có tỉ khối đối với hiđro là 11,80.
Xác định công thức phân tử và phần trăm thể tích của từng chất trong hỗn hợp A và hỗn hợp B.
Hỗn hợp khí A chứa hiđro, một ankan và một anken. Dẫn 13,44 lít A đi qua chất xúc tác Ni nung nóng thì thu được 10,08 lít hỗn hợp khí B. Dẫn B đi qua bình đựng nước brom thì màu của dung dịch nhạt đi, khối lượng của bình tăng thêm 3,15 g. Sau thí nghiệm, còn lại 8,4 lít hỗn hợp khí C có tỉ khối đối với hiđro là 17,80. Biết các thể tích được đo ở đktc và các phản ứng đều xảy ra hoàn toàn.
Xác định công thức phân tử và phần trăm thể tích của từng chất trong mỗi hỗn hợp A, B và C.
Hỗn hợp khí A chứa hiđro, một ankan và một anken. Đốt cháy hoàn toàn 100 ml A, thu được 210 ml khí CO2. Nếu đun nóng nhẹ 100 ml A có mặt chất xúc tác Ni thì còn lại 70 ml một chất khí duy nhất. Các thể tích khí đều đo ở cùng một điều kiện.
1. Xác định công thức phân tử và phần trăm thể tích của từng chất trong hỗn hợp A.
2. Tính thể tích oxi vừa đủ để đốt cháy hoàn toàn 100 ml A.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Xét 1 mol hỗn hợp X ⟹ mX = 9,1.2 = 18,2 gam.
BTKL: mX = mY = 18,2 gam ⟹ nY = 18,2 : 26 = 0,7 mol.
Do Y không làm mất màu nước brom ⟹ anken phản ứng hết và H2 dư.
⟹ nanken = nH2 phản ứng = nX - nY = 1 - 0,7 = 0,3 mol
⟹ nH2 trong X = 1 - 0,3 = 0,7 mol
⟹ Manken = (18,2 – 0,7.2)/0,3 = 56 (C4H8)
Mà anken cộng HBr tạo ra sp duy nhất nên anken phải có cấu tạo đối xứng
⟹ CTCT: CH3CH=CHCH3
Câu trả lời của bạn
Ta có nCH4 = nCO2 = 0,126 mol
=> VCH4 = 2,8224
=> %VCH4 = 2,8224 .100% / 10,8 = 26,13%
=> % VAnken = 73,87%
Câu trả lời của bạn
MX = 15
→ nC2H4 : nH2 = 13 : 13 = 1 : 1
Giả sử nC2H4 = nH2 = 1 mol ⟹ hiệu suất có thể tính theo C2H4 hoặc H2.
PTHH: C2H4 + H2 → C2H6
Ban đầu: 1 1 (mol)
Phản ứng: x → x → x (mol)
Sau phản ứng: (1-x) (1-x) x (mol)
⟹ nY = (1-x) + (1-x) + x = 2 - x (mol)
Bảo toàn khối lượng: mX = mY ⟹ 2 + 28 = 4.5.(2 - x) ⟹ x = 0,5 mol.
⟹ H% = \(\dfrac{{0,5}}{1}.100\% \) = 50%.
Câu trả lời của bạn
Đặt công thức chung của 2 anken đồng đẳng kế tiếp là: \({C_{\overline n }}{H_{2\overline n }}\)
PTHH: \({C_{\overline n }}{H_{2\overline n }} + {H_2}O\xrightarrow{{}}{C_{\overline n }}{H_{2\overline n + 1}}OH\)(Z) (1)
Đốt cháy 1,06 gam Z thu được CO2 và H2O
Hấp thụ CO2 vào dd NaOH, sau phản ứng thu được dd NaOH có nồng độ 0,05M → NaOH đã dùng dư. NaOH dư nên khi hấp thụ CO2 vào chỉ tạo muối Na2CO3
PTHH: CO2 + 2NaOH → Na2CO3 + H2O (2)
nNaOH bđ = V.CM đầu = 2.0,1 = 0,2 (mol)
nNaOH dư = V.CM sau = 2.0,05 = 0,1 (mol)
→ nNaOH pư = nNaOH bđ - nNaOH dư = 0,2 – 0,1 = 0,1 (mol)
Theo PTHH (2): \({n_{C{O_2}}} = \frac{1}{2}{n_{NaOH\,pu}} = \frac{1}{2}.0,1 = 0,05\,(mol)\)
PTHH đốt cháy hh ancol Y:
\({C_{\overline n }}{H_{2\overline n + 1}}OH + \frac{{3\overline n + 1}}{2}{O_2}\xrightarrow{{{t^0}}}{\overline n _{C{O_2}}} + (\overline n + 1){H_2}O\) (3)
Theo PTHH (3) ta có: \(n{C_{\overline n }}{H_{2\overline n + 1}}OH = \frac{1}{{\overline n }}{n_{C{O_2}}} = \frac{1}{{\overline n }}.0,05 = \frac{{0,05}}{{\overline n }}\,\,(mol)\)
Ta có: nY. MY = mY
\(\begin{array}{l} \to \frac{{0,05}}{{\overline n }}\,\,.(14\overline n + 18) = 1,06\\ \to 14\overline n + 18 = 21,2\overline n \\ \to 7,2\overline n = 18\\ \to \overline n = \frac{{18}}{{7,2}} = 2,5\end{array}\)
Vì 2 anken đồng đẳng kế tiếp nên 2 ancol cũng đồng đẳng kế tiếp → CTCT thu gọn 2 ancol là: C2H5OH và C3H7OH
Câu trả lời của bạn
m tăng = mC3H6 = 4,2 g
=> nC2H6 + nC3H8 = nHỗn hợp – nC3H6 = 0,2 – 0,1 = 0,1 (1)
=> %VC3H6 = nC3H6.100%/ nhh = 50%
=> khí đốt là C2H6 và C3H8
=> BTNT H : => 6nC2H6 + 8nC3H8 = 2nH2O = 0,72(2)
=> Từ (1) và (2) => nC2H6 = 0,04 ; nC3H8 = 0,06
Vậy phần trăm thể tích mỗi khí là: etan (20%), propan (30%) và propen (50%)
Câu trả lời của bạn
Câu trả lời của bạn
Vì bình kín => mX = mY
=> Mx.nx = My.ny
=>2.9,25.1 = 2.10.ny
=> ny = 0,925 mol
=> nH2 pứ = nX – nY = 1 – 0,925 = 0,075 mol
Câu trả lời của bạn
Hydrocacbon X → ancol Y no => X là anken
a mol Y + Na → 0,5a mol H2 => trong Y chỉ có 1 nhóm OH
Z là đồng phân cùng nhóm chức với Y => Z cũng là ancol no đơn chức
Z → T → Y. Ta thấy 2 ancol đồng phân chuyến hóa cho nhau chỉ có thể thông qua anken => Như vậy X và T là 2 anken đồng phân
Chỉ có C4H8 mới có đồng phân và ở thể khí.
=> Z và Y có dạng C4H10O
Thỏa mãn sơ đồ Z → T → Y chỉ có :
CH3CH2CH2CH2OH -> CH3CH2CH=CH2 -> CH3CH2CH(OH)CH3
=> X phải là CH3-CH=CH-CH3
Câu trả lời của bạn
nanken = 0,4 mol
Đốt cháy anken: nCO2 = nH2O = x mol
Bình 1 hấp thụ H2O ⟹ mH2O = mbình 1 tăng ⟹ m = 18x (1)
Bình 2 hấp thụ CO2 ⟹ mCO2 = mbình 2 tăng ⟹ m + 39 = 44x (2)
Lấy (2) - (1) được: 39 = 26x ⟹ x = 1,5 mol
⟹ \(\bar C = \dfrac{{{n_{C{O_2}}}}}{{{n_{hh}}}} = \dfrac{{1,5}}{{0,4}} = 3,75\)
Vì là 2 anken đồng đẳng kế tiếp và MX < MY ⟹ C3H6 (X) và C4H8 (Y).
Ta có hệ phương trình: \(\left\{ \begin{array}{l}{n_X} + {n_Y} = {n_{hh}} = 0,4\\3{n_X} + 4{n_Y} = {n_{C{O_2}}} = 1,5\end{array} \right. \to \left\{ \begin{array}{l}{n_X} = 0,1\\{n_Y} = 0,3\end{array} \right.\)
Trong cùng điều kiện, phần trăm thể tích chính là phần trăm về số mol
⟹ \(\% {V_Y} = \dfrac{{0,3}}{{0,4}}.100\% = 75\% \)
Câu trả lời của bạn
2-hiđroxi-2-metyl propanal có CTCT là CH3-C(OH)(CH3)-CHO.
⟹ Z là CH3-C(OH)(CH3)-CH2OH
⟹ Y là CH3-C(Br)(CH3)-CH2Br
⟹ X là CH3-C(CH3)=CH2 (isobutilen)
Câu trả lời của bạn
C2H4 ; CH3CH=CHCH3 (cis, trans)
=> có 3 anken thỏa mãn
Câu trả lời của bạn
nX = 3,36/22,4 = 0,15 mol
mX = m bình tăng = 8,4 mol
→ MX = mX : nX = 8,4 : 0,15 = 56
Gọi CTPT của X là CnH2n → 14n = 56 → n = 4
→ CTPT X: C4H8
Do X cộng HBr thu được 1 sản phẩm duy nhất nên X có cấu tạo đối xứng
→ CTCT X: CH3-CH=CH-CH3 (But-2-en)
Câu trả lời của bạn
Khi anken tác dụng vs nước thì sp tạo thành sẽ tuân theo quy tắc Maccopnhicop: Nhóm OH cộng vào C bậc cao hơn, H sẽ cộng vào C bậc thấp hơn => liên kết đôi nằm ở vị trí thứ 2
=> CTCT anken: CH3-CH=CH(C2H5)- CH2- CH3 có tên gọi là 3-etylpent-2-en.
A propilen và isobutilen.
B propen và but-1-en.
C etilen và propilen.
D propen và but-2-en.
Câu trả lời của bạn
2 anken thể khí + H2O => 4 ancol
=> mỗi anken tạo ra 2 ancol
Vì không có ancol bậc 3 => Loại isobutilen (CH2=C(CH3)2)
Propen cộng H2O thu được 2 sản phẩm
Etilen cộng H2O thu được 1 sản phẩm
But-1-en cộng H2O thu được 2 sản phẩm
But-2-en cộng H2O thu được 1 sản phẩm
Như vậy chỉ có đáp án B thỏa mãn đề bài
Câu trả lời của bạn
2 anken thể khí + H2O => 4 ancol
=> mỗi anken tạo ra 2 ancol
Vì không có ancol bậc 3 => Loại isobutilen (CH2=C(CH3)2)
Propen cộng H2O thu được 2 sản phẩm
Etilen cộng H2O thu được 1 sản phẩm
But-1-en cộng H2O thu được 2 sản phẩm
But-2-en cộng H2O thu được 1 sản phẩm
Như vậy chỉ có đáp án B thỏa mãn đề bài
Câu trả lời của bạn
Câu trả lời của bạn
6.Viết pư điều chế :
a. Etylen từ EtylClorua
b. Etylen từ Etanol
c.Propen từ isopropylclorua
d. Propen từ ancol propylic
e.Polyetylen từ etanol
f. Etylenglycol từ 1,2 điclo etan
6.Thực hiện pư theo sơ đồ :
1 2 3 4 5
a. Etan -> Etylclorua -> Etylen -> Etanol -> Eten -> Etylenglycol
1 2 3 4
b. Ancol etylic -> Etylen -> Etylclorua -> Etylen -> 1,2- đibrometan
1 2 3 4 5 6
c.Propan -> propen -> isopropylclorua -> Propen -> propan-2- ol -> Propen -> Polipropylen
Câu trả lời của bạn
Dẫn từ từ 8,4g hỗn hợp X gồm but1en và but2en lội chậm qua bình đựng dung dịch Br2 khi kết thúc phản ứng thấy có 24g brom phản ứng. Xác định thành phần phần trăm khối lượng but-1-en và but-2-en có trong hỗn hợp X
Câu trả lời của bạn
Câu trả lời của bạn

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *