Nội dung bài học Amoniac và muối amoni tìm hiểu về cấu tạo phân tử, tính chất vật lí (tính tan, tỉ khối, màu, mùi), ứng dụng chính, amoniac trong phòng thí nghiệm và trong công nghiệp . Tính chất hoá học của amoniac: Tính bazơ yếu (tác dụng với nước, dung dịch muối, axit) và tính khử (tác dụng với oxi, clo). Cách điều chế NH3. Tính chất vật lí (trạng thái, màu sắc, tính tan). Tính chất hoá học (phản ứng với dung dịch kiềm, phản ứng nhiệt phân) và ứng dụng của muối amoni.
Hình 1: Sơ đồ cấu tạo của phân tử NH3
Video 1: Sự hòa tan của Amoniac trong nước
Dung dịch NH3 đậm đặc trong phòng thí nghiệm có nồng độ 25% (N = 0,91g/cm3).
Tác dụng với nước
NH3 + H2O \(\rightleftharpoons\) NH4++ OH-
Tác dụng với dung dịch bazơ
AlCl3 + 3NH3 + 3 H2O → Al(OH)3 \(\downarrow\) + 3 NH4Cl
Al3++3NH3+3H2O → Al(OH)3 \(\downarrow\) + 3NH4+
Tác dụng với axít
2NH3 + H2SO4 → (NH4)2SO4
NH3 (k) + HCl (k) → NH4Cl
(không màu) (ko màu) (khói trắng)
Video 2: Amoniac tác dụng với axit clohidric
Trong phân tử NH3, N có số oxi hóa là -3. Nitơ có các số oxi hóa là -3,0,+1,+2,+3,+4,+5. Như vậy trong các phản ứng hóa học khi có sự thay đổi số oxi hóa, số oxi hóa của N trong NH3 chỉ có thể tăng lên → thể hiện tính khử.
Tác dụng với oxi
Video 3: Thí nghiệm giữa NH3 và Oxi
NH3 được tạo ra từ phản ứng của NH4Cl và CaO
Khí O2 được tạo ra từ phản ứng của KClO3 và MnO2
Tác dụng với Clo
2NH3 + 3Cl2 → N2 + 6 HCl
Nếu NH3 dư : NH3 + HCl → NH4Cl (khói trắng)
* Kết luận: Amoniac có các tính chất hoá học cơ bản: Tính bazơ yếu và Tính khử
N2 + 3H2 2NH3 \(\triangle H < 0\)
Muối amoni là chất tinh thể ion gồm cation amoni NH4+ và anion gốc axít. Ví dụ: NH4Cl, (NH4)2SO4 , (NH4)2CO3
(NH4)2SO4 + 2NaOH → Na2SO4 + 2NH3 + 2H2O.
Phương trình ion thu gọn: NH4+ + OH- → NH3 + H2O → Điều chế NH3 trong Phòng thí nghiệm và nhận biết muối amoni.
NH4Cl (r) NH3 (k) + HCl (k).
(NH4)2CO3 (r) NH3 (k) + NH4HCO3(r).
NH4HCO3(r) NH3(k) + CO2(k) + H2O
NH4NO2 N2 + 2H2O
NH4NO3 N2O + 2H2O
Để nhận biết các dung dịch: NH4NO3, (NH4)2SO4, K2SO4 đựng trong các lọ mất nhãn ta dùng:
Hỗn hợp X gồm N2 và H2 có tỉ khối so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác) thu được hỗn hợp Y có tỉ khối so với He bằng 2. Hiệu suất của phản ứng tổng hợp NH3 là:
MX = 7,2. Áp dụng quy tắc đường chéo ta có: \(n_{H_2}:n_{N_2}=4:1\)
⇒ Giả sử ban đầu có 4 mol H2 và 1 mol N2 trong X
N2 + 3H2 ↔ 2NH3
x → x → 2x
⇒ sau phản ứng: nY = 2x + (1 - x) + (4 - 3x) = 5 - 2x mol
Bảo toàn khối lượng: mX = mY
⇒ 5 × 7,2 = (5 - 2x) × 2 × 4
⇒ x = 0,25 mol
⇒ H% (tính theo N2) = 25%
Cho các phản ứng sau:
4NH3 + 5O2 → 4NO + 6H2O (1)
NH3 + H2SO4 → NH4HSO4 (2)
2NH3 + 3CuO → 3Cu + N2\(\uparrow\) + 3H2O (3)
8NH3 + 3Cl2 → N2 + 6NH4Cl (4)
NH3 + H2S → NH4HS (5)
2NH3 + 3O2 → 2N2\(\uparrow\) + 6H2O (6)
NH3 + HCl → NH4Cl (7)
Số phản ứng trong đó NH3 không đóng vai trò là chất khử là:
Các phản ứng mà có sự tăng số oxi hóa của N ⇒ NH3 thể hiện tính khử. Các phản ứng không có hiện tượng trên là: 2, 5, 7.
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 8có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Khí nào dưới đây làm xanh quỳ tím ẩm?
Khi nhiệt phân, muối nitrat nào sau đây có thể không thu được khí O2?
Để nhận biết các dung dịch muối (đựng riêng biệt trong các ống nghiệm): Al(NO3)3, (NH4)2SO4, NH4NO3, MgCl2 có thể dùng dung dịch:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 8.
Bài tập 1 trang 37 SGK Hóa học 11
Bài tập 2 trang 37 SGK Hóa học 11
Bài tập 3 trang 37 SGK Hóa học 11
Bài tập 4 trang 37 SGK Hóa học 11
Bài tập 5 trang 37 SGK Hóa học 11
Bài tập 6 trang 37 SGK Hóa học 11
Bài tập 7 trang 37 SGK Hóa học 11
Bài tập 8 trang 38 SGK Hóa học 11
Bài tập 8.1 trang 11 SBT Hóa học 11
Bài tập 8.2 trang 11 SBT Hóa học 11
Bài tập 8.3 trang 11 SBT Hóa học 11
Bài tập 8.4 trang 11 SBT Hóa học 11
Bài tập 8.5 trang 12 SBT Hóa học 11
Bài tập 8.6 trang 12 SBT Hóa học 11
Bài tập 8.7 trang 12 SBT Hóa học 11
Bài tập 8.8 trang 12 SBT Hóa học 11
Bài tập 8.9 trang 13 SBT Hóa học 11
Bài tập 8.10 trang 13 SBT Hóa học 11
Bài tập 8.11 trang 13 SBT Hóa học 11
Bài tập 8.12 trang 13 SBT Hóa học 11
Bài tập 1 trang 47 SGK Hóa học 11 nâng cao
Bài tập 2 trang 47 SGK Hóa học 11 nâng cao
Bài tập 3 trang 47 SGK Hóa học 11 nâng cao
Bài tập 4 trang 47 SGK Hóa học 11 nâng cao
Bài tập 5 trang 47 SGK Hóa học 11 nâng cao
Bài tập 6 trang 47 SGK Hóa học 11 nâng cao
Bài tập 7 trang 48 SGK Hóa học 11 nâng cao
Bài tập 8 trang 48 SGK Hóa học 11 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Khí nào dưới đây làm xanh quỳ tím ẩm?
Khi nhiệt phân, muối nitrat nào sau đây có thể không thu được khí O2?
Để nhận biết các dung dịch muối (đựng riêng biệt trong các ống nghiệm): Al(NO3)3, (NH4)2SO4, NH4NO3, MgCl2 có thể dùng dung dịch:
Thành phần của dung dịch NH3 gồm:
Cho hình vẽ mô tả thí nghiệm như sau:
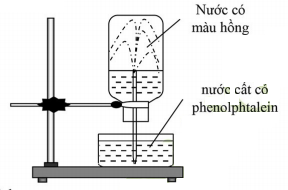
Hình vẽ mô tả thí nghiệm để chứng minh:
Nito trong chất nào sau đâu vừa có tính oxi hóa vừa có tính khử?
Để làm khô, sạch khí NH3 có lẫn hơi nước người ta dùng:
Tã lót trẻ em sau khi giặt vẫn giữ lại 1 lượng nhỏ amoniac. Để khử sạch amoniac nên dùng chất gì sau đây cho vào nước xả cuối cùng để giặt?
Phân bón nào sau đây làm tăng độ chua của đất?
Hỗn hợp X gồm N2 và H2 có tỉ khối so với H2 bằng 3,6. Sau khi tiến hành phản ứng tổng hợp amoniac trong bình kín (có xúc tác bột Fe) thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Hiệu suất phản ứng tổng hợp amoniac là:
Mô tả và giải thích hiện tượng xảy ra trong thí nghiệm chứng minh rằng ammoniac tan nhiều trong nước.
Hoàn thành sơ đồ chuyển hóa sau đây và viết các phương trình hóa học:
Khí A (+H2O)→ Dung dịch A (+ HCl) → B + (NaOH)→ Khí A + (HNO3) → C (to)→ D + H2O
Biết rằng A là hợp chất của nitơ.
Hiện nay, để sản xuất ammoniac, người ta điều chế nitơ và hiđro bằng cách chuyển hóa có xúc tác một hỗn hợp gồm không khí, hơi nước và khí metan (thành phần chính của khí thiên nhiên). Phản ứng giữa khí metan và hơi nước tạo ra hiđro và cacbon đioxit. Để loại khí oxi và thu khí nitơ, người ta đốt khí metan trong một thiết bị kín chứa không khí.
Hãy viết các phương trình hóa học của phản ứng điều chế hiđro, loại khí oxi và tổng hợp khí ammoniac.
Trình bày phương pháp hóa học để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4. Viết phương trình hóa học của các phản ứng đã dùng.
Muốn cho cân bằng của phản ứng tổng hợp amoniac chuyển dịch sang phải, cần phải đồng thời:
A. Tăng áp suất và tăng nhiệt độ.
B. Giảm áp suất và giảm nhiệt độ.
C. Tăng áp suất và giảm nhiệt độ.
D. Giảm áp suất và tang nhiệt độ.
Trong phản ứng nhiệt phân các muối NH4NO2 và NH4NO3, số oxi hóa của nitơ biến đổi như thế nào? Nguyên tử nitơ trong ion nào của muối đóng vai trò chất khử và nguyên tử nitơ trong ion nào của muối đóng vai trò chất oxi hóa?
Cho dung dịch NaOH dư vào 150,0 ml dung dịch (NH4)2SO4 1,00 M, đun nóng nhẹ.
a) Viết phương trình hóa học ở dạng phân tử và dạng ion rút gọn.
b) Tính thể tích khí (đktc) thu gọn.
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,0 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25,0%. Các thể tích khí được đo ở đktc.
A. 44,8 lít N2 và 134,4 lít H2
B. 22,4 lít N2 và 134,4 lít H2
C. 22,4 lít N2 và 67,2 lít H2
D. 44,8 lít N2 và 67,2 lít H2
Trong dung dịch, amoniac là một bazơ yếu là do
A. amoniac tan nhiều trong nước.
B. phân tử amoniac là phân tử có cực.
C. khi tan trong nước, amoniac kết hợp với nước tạo ra các ion NH4+ và OH−.
D. khi tan trong nước, chỉ một phần nhỏ các phân tử amoniac kết hợp với ion H+ của nước, tạo ra các ion NH4+ và OH−.
Dãy nào dưới đây gồm các chất chứa nguyên tử nitơ có khả năng vừa thể hiện tính khử vừa thể hiện tính oxi hoá khi tham gia phản ứng?
A. NH3, N2O5, N2, NO2
B. NH3, NO, HNO3, N2O5
C. N2, NO, N2O, N2O5
D. NO2, N2, NO, N2O3
Trong các phản ứng hóa học dưới đây, ở phản ứng nào amonic không thể hiện tính khử?
A. Khí amoniac tác dụng với đồng (II) oxit nung nóng tạo ra N2, H2O và Cu.
B. Khi amoniac tác dụng với khí hiđro clorua.
C. Khi amoniac tác dụng với khí clo.
D. Đốt cháy amoniac trong oxi.
Trong các dãy chất dưới đây, dãy nào gồm các chất đều phản ứng với NH3 trong điều kiện thích hợp?
A. Dung dịch HCl, dung dịch AlCl3, Cu, O2.
B. Dung dịch HNO3, dung dịch ZnCl2, dung dịch KOH, Cl2.
C. Dung dịch H2SO4, dung dịch FeCl3, O2, Cl2.
D. Dung dịch H3PO4, dung dịch CuCl2, dung dịch NaOH, O2.
Phản ứng tổng hợp amoniac là phản ứng thuận nghịch:
N2(k) + 3H2(k) ⇔ 2NH3(k)
ΔH = -92 kJ
Cân bằng của phản ứng này chuyển dịch như thế nào khi thay đổi một trong các điều kiện sau đây ? Giải thích.
1. Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống.
2. Giảm nhiệt độ.
3. Thêm khí nitơ.
4. Dùng chất xúc tác thích hợp.
Cho lượng khí amoniac đi từ từ qua ống sứ chứa 3,2 g CuO nung nóng đến khi phản ứng xảy ra hoàn toàn, thu được chất rắn A và một hỗn hợp khí. Chất rắn A phản ứng vừa đủ với 20,0 ml dung dịch HCl 1,00M.
1. Viết phương trình hoá học của các phản ứng.
2. Tính thể tích khí nitơ (đktc) được tạo thành sau phản ứng.
Trong những nhận xét dưới đây về muối amoni, nhận xét nào đúng?
A. Muối amoni là chất tinh thể ion, phân tử gồm cation amoni và anion hiđroxit.
B. Tất cả các muối amoni đều dễ tan trong nước, khi tan phân li hoàn toàn thành cation amoni và anion gốc axit.
C. Dung dịch muối amoni tác dụng với dung dịch kiềm đặc, nóng cho thoát ra chất khí làm quỳ tím hoá đỏ.
D. Khi nhiệt phân muối amoni luôn luôn có khí amoniac thoát ra.
Phản ứng nào dưới đây là phản ứng oxi hóa - khử?
A. (NH4)2SO4 + 2NaOH → 2NH3↑ + H2O + Na2SO4
B. NH4HCO3 to→ NH3↑ + CO2↑ + H2O
C. NH4Cl to→ NH3↑ + HCl↑
D. NH4NO3 to→ N2O + 2H2O
Trong các phản ứng nhiệt phân muối amoni dưới đây, phản ứng nào không là phản ứng oxi hóa - khử?
A. NH4NO2 → N2 + 2H2O
B. NH4NO3 → N2O + 2H2O
C. NH4HCO3 → NH3 + CO2 + H2O
D. (NH4)2Cr2O7 → N2 + Cr2O3 + 4H2O
Hoàn thành các phương trình hoá học sau đây:
1. ? + OH− → NH3 + ?
2. (NH4)3PO4 to→ NH3 + ?
3. NH4Cl + NaNO2 to→ ? + ? + ?
4. (NH4)2Cr2O7 to→ N2 + Cr2O3 + ?
Chỉ được dùng một kim loại, hãy trình bày cách phân biệt các dung dịch muối sau đây: NH4NO3, (NH4)2SO4, K2SO4. Viết phương trình hoá học của các phản ứng xảy ra.
Cho dung dịch Ba(OH)2 đến dư vào 75 ml dung dịch muối amoni sunfat.
1. Viết phương trình hoá học của phản ứng dưới dạng ion.
2. Tính nồng độ mol của các ion trong dung dịch muối ban đầu, biết rằng phản ứng tạo ra 17,475 g một chất kết tủa. Bỏ qua sự thuỷ phân của ion amoni trong dung dịch.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
chia m(g) hỗn hợp NH4Cl và (NH4)2SO4 làm 2 phần bằng nhau
-phần 1 cho tác dụng với dung dịch NaOH đun nóng thu được 1,729 lít khí (đktc)
-phần 2 : cho tác dụng với BaCl2 dư tạo 6,99 lít kết tủa
tìm % khối lượng mỗi chất trong hỗn hợp ban đầu
Câu trả lời của bạn
viet dde bai cung sai
tả lót của em bé sau khi giặc sạch vẫn lưu giữ 1 lương amoniac để loại bỏ hoàn toàn thì trong nước xả cuối ta nên cho vào chất gì để làm sạch?
Câu trả lời của bạn
Ta có thể dùng CH3COO
Do amoniac có tính bazo nên dùng axit nhẹ để trung hòa, mặt khác axit acetic trong giấm ăn khử mùi khai đặc trưng của amoniac nên cho vao chất giấm ăn để làm sạch.
Cho amoniac NH3 tác dụng với õi ở nhiệt độ cao có xúc tác thích hợp sinh ra nito oxit NO và nước. Phương trình hóa học là 4NH3 + 5O2 ---> 4NO + 6H2OO. Trong phản ứng trên, NH3 đóng vai trò
A. Chất oxi hóa
B. Chất khử
C. Vừa oxi hóa và khử
D. Chất tạo môi trường
Câu trả lời của bạn
B
Tại sao người ta không dùng NH4HCO3 trong công nghệ chữa cháy mà lại dùng những chất khác?
Câu trả lời của bạn
Là vì muối này dễ bị phân hủy ở nhiệt độ cao tạo NH3. Khi nồng độ khí NH3 trong không khí lớn thì gây hại cho cơ thể con ng. Vì vậy ko dùng được
NH4HCO3 \(\rightarrow\)NH3+ CO2 + H2O
Điều chế HNO3 trong công nghiệp theo sơ đồ:
NH3 --> NO--->NO2-----> HNO3
a) Viết phương trình phản ứng và ghi rõ điều kiện.
b) Tính thể tích NH3 (ở đktc) chứa 15% tạp chất không cháy cần thiết để thu được 10 kg HNO3 31,5%. Biết hiệu suất của quá trình là 79,356%.
Câu trả lời của bạn
a/ 4NH33O2-> 4NO +6H2O (nhiệt độ, xúc tác)
2NO + O2 -> 2NO2 (nhiệt độ thường)
2NO2 + H2O +(\(\dfrac{1}{2}\)) O2 -> 2HNO3
b/ Khối lượng HNO3 nguyên chất là:
mHNO3 = 3,15 (kg)
NH3-----> NO------>NO2------>HNO3
17--------------->63
0,85 (kg)<--------------3,15 (kg)
Lượng NH3 thực tế là:
mNH3 = \(\dfrac{0,85.100}{79.356}.\dfrac{100}{85}=1,26\left(kg\right)\)
V(NH3) = \(\dfrac{1,26}{17}.22,4=1,66\left(m^3\right)\)
Hoà tan m gam hỗn hợp NH4Cl và (NH4)2SO4 có tỉ lệ số mol NH4Cl:(NH4)2SO4 =1:2 vào nước được dung dịch A. Cho dung dịch A tác dụng với dung dịch NaOH dư đun nóng thu được 13,44 lít NH3 (đktc). Tính giá trị m
Câu trả lời của bạn
Một bình kín dung tích không đổi chứ 10 lít hh N2 và H2 theo tỉ lệ 2:3 về thể tích. Thực hiện tổng hợp NH3 sau phản ứng đưa về đk ban đầu thấy áp suất trong bình giảm 15%. Thể tích NH3 thu được là:
A 1,5 lít B 1,0 lít C 2,25 lít D 1,765 lít
Câu trả lời của bạn
1 .Cho m gam amonisunfat tác dụng hoàn toàn với NAOH dư. Đun nóng thu được sp khí A. Hấp thụ hoàn toàn khí trên vào dung dịch chứa 3.92g H3PO4. Tính khối lượng muối thu được
a) trong trường hợp m=1.32
b) trong trường hợp m=3.96g
Câu trả lời của bạn
a. m=1,32; nH3PO4=0,04
(NH4)2SO4 + 2NaOH -> 2NH3\(\uparrow\) + Na2SO4
0,01.....................................0,02
NH3 + H2O \(⇌\) NH4+ + OH-
Đặt \(T=\dfrac{n_{OH}}{n_{H3PO4}}\)
- T\(\ge\) tạo muối photphat (PO43-)
- 3>T>2 tạo muối photphat và hidrophotphat (HPO42-)
- T=2 tạo muối hidrophotphat (HPO42-)
- 2>T> 1 tạo muối hidrophotphat và đihidrophotphat (H2PO4-) - T\(\le\) tạo muối đihidrophotphat (em có thể viết gộp các TH dấu bằng lại để chỉ còn 3 TH) Đối với câu a: T=0,02/0,04=1/2 => tạo muối đihidrophotphat NH3 + H3PO4 -> NH4(H2PO4) 0,02........0.02..............0.02 => mmuoi= 2,3 g b. xét T rồi viết PTHH. Làm tương tự như câu a: Thực hiện phản ứng giữa H2 và N2 (tỉ lệ mol 4:1), trong bình kín có xúc tác, thu được hỗn hợp khí có áp suất giảm 9% so với ban đầu ( trong cùng điều kiện). Tính Hiệu suất phản ứng.
Câu trả lời của bạn
Cho 1,12 lít khí NH3 (đktc) tác dụng vói 16 gam CuO nug nóng.Sau phản uéng còn lại chất rắn X (các PỨ xảycra hoàn toàn). Thể tích HCL 0,5 M cần để PỨ hoàn toàn với X là bao nhiêu
Câu trả lời của bạn
nNH3=0.05 mol
nCuO=0.2 mol
3CuO+2NH3->3Cu+N2+3H2O
0.075 0.05
nCuO dư=0.125
CuO+2HCl->CuCl2+H2
0.125 0.25
->VHCl=0.25/0.5=0.5L
Thể tích khí O2 (đktc) cần để đốt cháy 6,8 gam NH3 tạo thành khí NO và H2O
Câu trả lời của bạn
nNH3=0.4 mol
4NH3+502->4NO+6H2O
0.4 0.5
->VO2=11,2 l
Cho hỗn hợp N2, H2 được lấy theo tỉ lệ thể tích là 3:7 thêm xúc tác và đun nóng để phản ứng xảy ra thu được hỗn hợp khí Y. Hiệu suất phản ứng tổng hợp NH3 là 25%, khối lượng mol phân tử của hỗn hợp Y :
A. 10,60 B. 10,77 C. 11,53 D. 11,09
Câu trả lời của bạn
N2+3H2\(\rightarrow\)2NH3
Gọi số mol N2=3 mol, số mol H2 là 7 mol
Tỉ lệ: \(\dfrac{3}{1}>\dfrac{7}{3}\)Tính các chất theo H2
\(n_{H_2\left(pu\right)}=\dfrac{25}{100}.7=1,75mol\)
\(n_{H_2\left(dư\right)}=7-1,75=5,25mol\)
\(n_{N_2\left(Pu\right)}=\dfrac{1}{3}n_{H_2}=\dfrac{1,75}{3}mol\)
\(n_{N_2\left(dư\right)}=3-\dfrac{1,75}{3}=\dfrac{7,25}{3}mol\)
\(n_{NH_3}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.1,75=\dfrac{7}{6}mol\)
\(\overline{M}=\dfrac{m_{hh}}{n_{hh}}=\dfrac{5,25.2+28.\dfrac{7,25}{3}+17\dfrac{7}{6}}{5,25+\dfrac{7,25}{3}+\dfrac{7}{6}}\approx11,09\)
Đáp án D
Cho 11,7 gam kali vào 600 ml dung dịch NH4Cl 1M thu được V lít hỗn hợp khí (đktc) có tỉ khối so với hiđrô là d. Tính giá trị của V, d.
Câu trả lời của bạn
K + H2O ---> KOH + H2
KOH + NH4CL ---> KCl + NH3 + H2O
Đến đây Ok rồi nhé.
cho 5 lít N2 và 15 lít H2 vào một bình kín dung tích không đổi .ở 00C ,áp suất trong bình là P1 atm .đun nóng bình một thời gian thì thấy có 20% N2 tham gia phản ứng , đưa bình về nhiệt độ ban đầu thấy áp suất trong bình lúc này là P2.tỉ lệ P1 và P2 là
Câu trả lời của bạn
Dẫn 0.896 lít ( đktc) khí NH3 đi qua ống sứ đựng 32 gam CuO nung nóng đến khi pứ hoan toàn, thu đc chất rắn Y và a mol khí N2 a) Xđ phần trăm khối lượng của Cu trong Y b) Cho toàn bộ a mol khí N2 trên vào bình kín chứa H2 đc hh khí Z có tỉ khối so với H2 bằng 6.2. Đun nóng Z 1 thời gian( có xúc tác).Tính V NH3 thu đươc (đktc), biết H pứ tổng hợp NH3 là 25%
Câu trả lời của bạn
2NH3 + 3CuO \(\rightarrow\) 3Cu + N2 + 3H2O
\(n_{NH_3}=\dfrac{0,896}{22,4}=0,04mol\)
\(n_{CuO}=\dfrac{32}{80}=0,4mol\)
\(n_{Cu}=n_{CuO\left(pu\right)}=\dfrac{3}{2}n_{NH_3}=0,06mol\)
nCuO(dư)=0,4-0,06=0,34mol
mY=0,06.64+0,34.80=31,04 gam
%Cu=\(\dfrac{0,06.64.100}{31,04}\approx12,37\%\)
%CuO=87,63%
\(n_{N_2}=\dfrac{1}{3}n_{NH_3}=\dfrac{0,04}{3}mol\)
\(\overline{M_Z}=6,2.2=12,4\)
- Gọi số mol H2 là x. Ta có:\(\dfrac{17.\dfrac{0,04}{3}+2x}{\dfrac{0,04}{3}+x}=12,4\)
\(\rightarrow\)17.0,04+6x=12,4(0,04+3x)\(\rightarrow\)0,68+6x=0,496+37,2x\(\rightarrow\)31,2x=0,184
\(\rightarrow\)x=0,006 mol
N2+3H2\(\rightarrow\)2NH3
\(\dfrac{\dfrac{0,04}{3}}{1}>\dfrac{0,006}{3}\)
\(n_{NH_3}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.\dfrac{25}{100}.0,006=0,001mol\)
\(V_{NH_3}=0,001.22,4=0,0224l\)
Khi tổng hợp NH3 từ N2 và H2 (điều kiện thích hợp) thấy rằng nồng độ khi cân bằng của N2 là 0,02M ,H2:2M ,NH3:0.6M.Hằng số cân bằng của phản ứng là :
A.3,25 B.2,25 C.2 D.1,25
Câu trả lời của bạn
N2+3H2\(\rightarrow\)2NH3
Kcb=\(\dfrac{\left[NH_3\right]^2}{\left[N_2\right].\left[H_2\right]^3}=\dfrac{0,6^2}{0,02.2^3}=2,25\)
Đáp án B
sau quá trình tổng hợp NH3 từ N2 và H2 ( VH2:VN2=3:1), thấy áp suất trog bình giảm 10% so với áp suất ban đầu. biết nhiệt độ trước và sau phản ứng không đổi.phần trăm theo thể tích của N2, H2, NH3 trong hỗn hợp khí thu được sau phản ứng lần lượt là bao nhiêu?
m.n giải giúp em với ạ
Câu trả lời của bạn
1.NH3 khong tac dung duoc voi chat nao sao day?
A. O2
B. H2SO4
C. Cl2
D. NaOH
2. Cho 3gam mot kim loai co hoa tri 2 tan hoan toan trong dd HNO3 dac nong thu duoc 5.6 lit NO2( la san pham khu duy nhat o dktc). Kim loai do la
A. Zn
B. Mg
C. Fe
D. Cu
3. Cho 0.1mol H3PO4 vao dubg dich chua 0.35mol KOH. Dung dich thu duoc co cac chat
A. H3PO4, KH2PO4
B. K3PO4, KOH
C. K3PO4, K2HPO4
D. K2HPO4, KH2PO4
4. Dung dich loang(du) nao sau day tac dung voi kim loai sat tao thanh muoi sat 3
A. HNO3
B. H2SO4
C. HCl
D. H3PO4
C.on m.n nhiu
Câu trả lời của bạn
1d 2b 3a 4a
Nhận biết Ba(OH)2 , H2SO4 , NH4CL , ( NH4)2SO4 , NH3 chỉ dùng quỳ tím . Giúp mình với
Câu trả lời của bạn
ba(oh)2 chuyển xanh
h2so4,nh4cl,(nh4)so4 chuyển dỏ
dung dich NH3 quỳ tím chuyển màu xanh nha
Ba(OH)2 quy tím hóa xanh
H2SO4 hóa đỏ
NH4Cl, NH4)2SO4 không đổi màu
dùng quỳ tím thì ta thấy :
+, Ba(OH)2 hóa xanh
+, H2SO4 sẽ hóa đỏ
+, NH4Cl, (NH4)2SO4 và NH3 sẽ không đổi màu .
Dùng Ba(OH)2 cho tác dụng với ba chất còn lại thì ta thấy:
1, Đối với dd NH4Cl thì xuất hiện khí có mùi khai bay ra .pt
2 NH4Cl + Ba(OH)2 \(\rightarrow\) BaCl2 +2 NH3\(\uparrow\) +2 H2O
2, Đối với (NH4)2SO4 thì xuất hiện kết tủa trắng và có khí mùi khai bay ra.pt
(NH4)2SO4 + Ba(OH)2 \(\rightarrow\) BaSO4\(\downarrow\) + 2NH3\(\uparrow\) +2H2O
3, Đối với NH3 thì không phản ứng.
Trộn 8 lít H2 với 3 lít N2 rồi đun nóng với chất xúc tác bột sắt. Sau phản ứng thu được 9 lít hh khí. Tính hiệu suất phản ứng. Các thể tích đo ở cùng điều kiện nhiệt độ, áp suất.
Câu trả lời của bạn
3H2+N2->2NH3
Gọi x là VN2 pư
=>VN2 dư= 3-x
VH2 dư=8-3x
VNH3=2x
=>3-x+8-3x+2x=9
=>x=1
H=\(\dfrac{1\cdot100}{3}=33,3\%\)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *