Nội dung Bài Luyện tập Hiđrocacbon thơm giúp HS biết được những điểm giống nhau và khác nhau về tính chất hóa học của các hiđrocacbon thơm với các ankan, anken, tính chất hóa học của các hiđrocacbon thơm.
Với R: nhóm ankyl
(thế nguyên tử hiđro)
Nhận biết các chất lỏng riêng biệt: ancol etylic, clorofom, benzen bằng 1 thuốc thử nào sau đây?
Dùng H2O ⇒ benzen phân lớp còn 2 chất còn lại tan.
Sau đó cho 2 chất còn lại vào benzen. Vì benzen tan rất kém trong nước và rượu nên sẽ phân lớp nếu có ancol etylic và tan tốt trong dung môi hữu cơ là clorofom.
Cho sơ đồ phản ứng sau:
\(Toluen \xrightarrow[1:1]{+Cl_2\ (as)} X \xrightarrow[]{+NaOH,t^0} Y \xrightarrow[]{+CuO,t^0} Z \xrightarrow[]{dd\ AgNO_3/NH_3} T\)
Biết rằng X, Y, Z, T là những sản phẩm chính. Công thức cấu tạo của chất T là:
\(\\C_6H_5CH_3 \xrightarrow[1:1]{+Cl_2,as} C_6H_5CH_2Cl \xrightarrow[]{+NaOH,t^0} C_6H_5CH_2OH\\ C_6H_5CH_2OH \xrightarrow[]{+CuO,t^0} C_6H_5CHO \xrightarrow[]{dd.AgNO_3/NH_3} C_6H_5COONH_4\)
Cho 27,6 gam hợp chất thơm X có công thức C7H6O3 tác dụng với 800 ml dung dịch NaOH 1M thu được dung dịch Y. Để trung hòa toàn bộ Y cần 100 ml dung dịch H2SO4 1M thu được dung dịch Z. Khối lượng chất rắn khan thu được khi cô cạn dung dịch Z là:
Có nNaOH = 0,8 mol; n\(\tiny H_2SO_4\) trung hòa = 0,1 mol
⇒ nNaOH phản ứng với X = 0,8 – 0,1 × 2 = 0,6 mol = 3nX
⇒ X phải có CT là HCOO-C6H4-OH
⇒ Chất rắn sau cô cạn có: 0,1 mol Na2SO4; 0,2 mol HCOONa; 0,2 mol C6H4(ONa)2
⇒ m = 58,6 g
Hỗn hợp chất X gồm các thành phần C, O, H chứa vòng benzen. Cho 6,9 gam X vào 360 ml dung dịch NaOH 0,5M (dư 20% so với lượng cần phản ứng) đến phản ứng hoàn toàn, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn. Mặt khác, đốt cháy hoàn toàn 6,9 g X cần vừa đủ 7,84 lít O2 (đktc) thu được 15,4 gam CO2. Biết X có công thức phân tử trùng với công thức đơn giản nhất. Giá trị của m là:
Khi đốt X: \(n_{O_2}= 0,35\) mol ⇒ theo DLBTKL: \(m_{H_2O} = m_X + m_{O_2} - m_{CO_2}\)
⇒ \(n_{H_2O} = 0,15\) mol và \(n_{CO_2} = 0,35\) mol
Trong X: \(n_C= 0,35\) mol;
\(n_H= 0,3\) mol; ⇒ \(n_C:n_H:n_O= 7:6:3\)
\(n_O=2n_{CO_2} +n_{H_2O} - 2n_{O_2}=0,15\) mol
Do X có CTPT trùng với CTDG nhất ⇒ X là C7H6O3
Có nNaOH = 0,18 mol ⇒ nNaOH phản ứng = 0,15 mol = 3nX
⇒ X có công thức cấu tạo là HCOO-C6H4-OH
HCOO-C6H4-OH + 3NaOH → HCOONa + C6H4(ONa)2 + 3H2O
⇒ m rắn = m NaOH dư + m HCOONa + m \(\tiny C_6H_4(ONa)_2\) = 12,3 g
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 36có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Trong các câu sau, câu nào không đúng?
Chất sau đây có tên gọi là gì?
Cho ba chất lỏng trong ba ống nghiệm riêng biệt: benzen, toluen và stiren. Dùng hoá chất nào sau đây để phân biệt chúng?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 36.
Bài tập 1 trang 162 SGK Hóa học 11
Bài tập 2 trang 162 SGK Hóa học 11
Bài tập 3 trang 162 SGK Hóa học 11
Bài tập 4 trang 162 SGK Hóa học 11
Bài tập 5 trang 162 SGK Hóa học 11
Bài tập 6 trang 162 SGK Hóa học 11
Bài tập 36.1 trang 55 SBT Hóa học 11
Bài tập 36.2 trang 55 SBT Hóa học 11
Bài tập 36.3 trang 56 SBT Hóa học 11
Bài tập 36.4 trang 56 SBT Hóa học 11
Bài tập 36.5 trang 56 SBT Hóa học 11
Bài tập 36.6 trang 56 SBT Hóa học 11
Bài tập 36.7 trang 56 SBT Hóa học 11
Bài tập 36.8 trang 57 SBT Hóa học 11
Bài tập 36.9 trang 57 SBT Hóa học 11
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Trong các câu sau, câu nào không đúng?
Chất sau đây có tên gọi là gì?
Cho ba chất lỏng trong ba ống nghiệm riêng biệt: benzen, toluen và stiren. Dùng hoá chất nào sau đây để phân biệt chúng?
Cho chuỗi biến hoá sau:
CTPT của A, B, C lần lượt là:
Lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng hết với Clo (xúc tác Fe), hiệu suất của phản ứng đạt 80% là:
Đốt cháy hoàn toàn 4,6 gam toluen, sản phẩm thu được cho đi qua bình đựng dung dịch Ca(OH)2 dư. Khối lượng kết tủa tạo thành là:
Cho 1,28 gam naphtalen tác dụng hết với axit nitric tạo thành 1-nitronaptalen. Khối lượng sản phẩm tạo thành là:
Stiren tác dụng với dung dịch Brom dư tạo thành 1,2-đibromphenyletan có CTCT là:
Khối lượng Brom đủ để phản ứng hết với 1,04 gam stiren là:
Cho 39 gam benzen vào 100 gam HNO3 63% sau đó thêm axit H2SO4 đặc vào và đun nóng. Tính khối lượng nitrobenzen thu được nếu hiệu suất của phản ứng đạt 80%.
61,5 gam
49,2 gam
Đốt cháy hoàn toàn 2,9 gam hỗn hợp X gồm hai hiđrocacbon kế tiếp nhau trong dãy đồng đẳng của benzen thu được 9,68 gam CO2. Vậy công thức của 2 aren là:
C7H8 và C8H10
C8H10 và C9H12
C9H12 và C10H14
Viết công thức cấu tạo và gọi tên các hiđrocacbon thơm có công thức phân tử C8H10, C8H8. Trong số các đồng phân đó, đồng phân nào phản ứng được với: dung dịch brom, hiđrobromua? Viết phương trình hoá học của phản ứng xảy ra.
Trình bày phương pháp hóa học của các phản ứng hóa học đặc biệt các chất lỏng sau: benzen, stiren, toluene và hex – 1 – in.
Viết phương trình hóa học của các phản ứng điều chế etilen, axetilen từ metan; điều chế clobenzen và nitrobenzen từ benzen và các chất vô cơ khác.
Cho 23,0 kg toluen tác dụng với hỗn hợp axit HNO3 đặc, dư (xúc tác axit H2SO4 đặc). Giả sử toàn bộ toluene chuyển thành 2,4,6 – trinitrotoluen (TNT).
Hãy tính:
a) Khối lượng TNT thu được.
b) Khối lượng axit HNO3 đã phản ứng.
Ankylbenzen X có phần trăm khối lượng cacbon bằng 91,31%.
a) Tìm công thức phân tử của X.
b) Viết công thức cấu tạo, gọi tên chất X.
Hiđrocacbon X ở thể lỏng có tỉ lệ phần trăm khối lượng H xấp xỉ 7,7%. X tác dụng được với dung dịch brom. Công thức nào sau đây là công thức phân tử của X?
A. C2H2
B. C4H4
C. C6H6
D. C8H8
Có bốn tên gọi : o-xilen, o-đimetylbenzen, 1,2-đimetylbenzen, etylbenzen. Đó là tên của
A. 1 chất.
B. 2 chất.
C. 3 chất.
D. 4 chất.
Có 5 công thức cấu tạo:
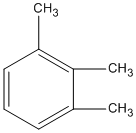
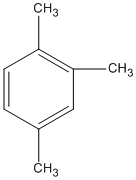
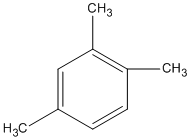
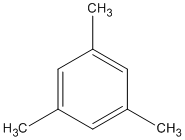
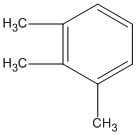
Đó là công thức của mấy chất ?
A. 1 chất.
B. 2 chất.
C. 3 chất.
D. 4 chất.
Nhận xét nào dưới đây không đúng?
A. Benzen và toluen đều không có phản ứng với dung dịch nước brom.
B. Benzen và toluen đều có phản ứng thế với brom khi có xúc tác Fe.
C. Benzen và toluen đều có thể tham gia phản ứng cộng.
D. Toluen tham gia phản ứng thế nguyên tử H của vòng benzen khó hơn benzen.
Nếu cho toluen tác dụng với brom trong điều kiện chiếu sáng và đun nóng nhẹ, sản phẩm chính là
A. 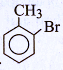
B. 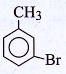
C. 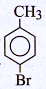
D. 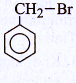
Cho vào ống nghiệm 2 ml nước brom. Nhỏ từ từ vào ống nghiệm đó 1 ml benzen. Trong ống nghiệm có 2 lớp chất lỏng : lớp dưới có thể tích lớn hơn và có màu vàng nâu, lớp trên không màu. Lắc kĩ ống nghiệm để hai lớp đó trộn vào nhau và sau đó để yên ống nghiệm. Trong ống lại thấy 2 lớp chất lỏng : lớp dưới có thể tích lớn hơn và không màu, lớp trên có màu.
Hãy giải thích những hiện tượng vừa nêu.
A là một đồng đẳng của benzen có tỉ khối hơi so với metan bằng 5,75.
A tham gia các quá trình chuyển hóa theo sơ đồ sau:
Trên sơ đồ chỉ ghi các chất sản phẩm hữu cơ (phản ứng còn có thể tạo ra các chất vô cơ).
Hãy viết phương trình hóa học của các quá trình chuyển hóa. Các chất hữu cơ viết dưới dạng công thức cấu tạo, kèm theo tên gọi.
Chất A là một đồng đẳng của benzen. Khi đốt cháy hoàn toàn 1,5 g chất A, người ta thu được 2,52 lít khí CO2 ( ở đktc ).
1. Xác định công thức phân tử chất A.
2. Viết các công thức cấu tạo có thể có của A kèm theo tên tương ứng.
3. Khi A tác dụng với Br2 có chất xúc tác Fe và nhiệt độ thì một nguyên tử H đính với vòng benzen bị thay thế bởi Br, tạo ra dẫn xuất monobrom duy nhất. Xác định công thức cấu tạo đúng của A.
Hỗn hợp M chứa benzen và xiclohexen. Hỗn hợp M có thể làm mất màu tối đa 75,0 g dung dịch brom 3,2%. Nếu đốt cháy hoàn toàn hỗn hợp M và hấp thụ tất cả sản phẩm cháy vào dung dịch Ca(OH)2 (lấy dư) thì thu được 21 g kết tủa. Tính phần trăm khối lượng từng chất trong hỗn hợp M.
Hỗn hợp A gồm hiđro và hơi benzen. Tỉ khối của A so với metan là 0,6. Dẫn A đi qua chất xúc tác Ni nung nóng thì chỉ xảy ra phản ứng làm cho một phần benzen chuyển thành xiclohexan. Hỗn hợp sau phản ứng có tỉ khối hơi so với metan là 0,75.
Tính xem bao nhiêu phần trăm benzen đã chuyển thành xiclohexan.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Nếu tư duy theo hướng tính khối lượng của từng muối, sau đó suy ra tổng khối lượng của chúng thì rất phức tạp, vì rất khó để xác định xem dung dịch X được tạo thành từ các muối nào. Còn nếu sử dụng hệ quả 2 của định luật bảo toàn khối lượng thì vấn đề sẽ được giải quyết đơn giản hơn nhiều. Ta có:
\({{m}_{\text{mu }\!\!\grave{\mathrm{e}}\!\!\text{ i}}}={{m}_{C{{u}^{2+}}}}+{{m}_{N{{a}^{+}}}}+{{m}_{SO_{4}^{2-}}}+{{m}_{C{{l}^{-}}}}+{{n}_{NO_{3}^{-}}}\)
\(\Leftrightarrow {{m}_{\text{mu }\!\!\grave{\mathrm{e}}\!\!\text{ i}}}=0,2.64+0,1.23+0,15.96+0,1.35,5+0,1.62=39,25\,\,gam\)
Câu trả lời của bạn
Theo giả thiết: Z gồm hai chất khí đều làm xanh giấy quỳ ẩm, nên suy ra Z gồm hai chất có tính bazơ. Vì \({{\overline{M}}_{Z}}=13,75.2=27,5\text{ g}/mol\) nên Z chứa một chất là NH3, chất còn lại là amin. Hai chất trong X là CH3COONH4 và HCOOH3NCH3.
Phương trình phản ứng:
\(\begin{align}
& C{{H}_{3}}COON{{H}_{4}}+NaOH\xrightarrow{{{t}^{o}}}C{{H}_{3}}COONa+N{{H}_{3}}+{{H}_{2}}O~~~~~~~(1) \\
& \text{ }x~\text{ }\xrightarrow{{}}\text{ }x\text{ }\xrightarrow{{}}\text{ }x\text{ }\xrightarrow{{}}\text{ }x\text{ (mol)} \\
\end{align}\)
\(\begin{align}
& HCOO{{H}_{3}}NC{{H}_{3}}+NaOH\xrightarrow{{{t}^{o}}}HCOONa+C{{H}_{3}}N{{H}_{2}}~+{{H}_{2}}O~~~~~(2) \\
& \text{ }y~~~\xrightarrow{{}}~\text{ }y~~~\text{ }\xrightarrow{{}}~~\text{ }y~~\xrightarrow{{}}~\text{ }y\text{ (mol)} \\
\end{align}\)
Theo giả thiết và các phản ứng (1), (2), ta có:
\(\xrightarrow{\text{gi }\!\!\P\!\!\text{ thi }\!\!\tilde{\mathrm{O}}\!\!\text{ t}}\left\{ \begin{align}
& {{n}_{Z}}=0,2\text{ mol} \\
& {{\overline{M}}_{Z}}=27,5\text{ g}/mol \\
\end{align} \right.\Leftrightarrow \left\{ \begin{align}
& x+y=\frac{4,48}{22,4}=0,2 \\
& \frac{17x+31y}{x+y}=27,5 \\
\end{align} \right.\Rightarrow \left\{ \begin{align}
& x=0,05\text{ mol} \\
& y=0,15\text{ mol} \\
\end{align} \right.\)
Trong Y chứa CH3COONa và HCOONa. Khi cô cạn dung dịch Y thu được khối lượng muối khan là:
\({{m}_{\text{mu }\!\!\grave{\mathrm{e}}\!\!\text{ i}}}={{m}_{C{{H}_{3}}COONa}}+{{m}_{HCOONa}}=0,05.82+0,15.68=14,3\,\,gam\)
Câu trả lời của bạn
Áp dụng bảo toàn khối lượng, ta có:
\({{m}_{\text{F}{{\text{e}}_{\text{x}}}{{O}_{y}}}}+{{m}_{{{\text{H}}_{\text{2}}}S{{O}_{4}}}}={{m}_{F{{e}_{2}}{{(S{{O}_{4}})}_{3}}}}+{{m}_{S{{O}_{2}}}}+{{m}_{{{H}_{2}}O}}\)
\(\Leftrightarrow {{m}_{\text{F}{{\text{e}}_{\text{x}}}{{O}_{y}}}}+0,75.98=0,225.400+0,075.64+0,75.18\Leftrightarrow {{m}_{\text{F}{{\text{e}}_{\text{x}}}{{O}_{y}}}}=34,8\,\,gam\)
Câu trả lời của bạn
\({{n}_{HCl}}=2{{n}_{{{H}_{2}}S{{O}_{4}}}}=2{{n}_{{{H}_{2}}O}}\Rightarrow {{n}_{{{H}_{2}}S{{O}_{4}}}}={{n}_{{{H}_{2}}O}}=\frac{1}{2}{{n}_{HCl}}=\frac{1}{2}.0,39.2=0,39\,\,mol\)
Áp dụng bảo toàn khối lượng, ta có:
\({{m}_{X}}+{{m}_{{{H}_{2}}S{{O}_{4}}}}={{m}_{\text{mu }\!\!\grave{\mathrm{e}}\!\!\text{ i sunfat}}}+{{m}_{{{H}_{2}}O}}\)
\( \Leftrightarrow 23,42 + 0,39.98 = {m_{{\rm{mu\`e i sunfat}}}} + 0,39.18 \Leftrightarrow {m_{{\rm{mu\`e i sunfat}}}} = 54,62\,\,gam\)
Câu trả lời của bạn
\( \Leftrightarrow 0,015.44 + 0,02(40 + 56) = {m_{{\rm{ch\^E t r\raise.5ex\hbox{$\scriptstyle 3$}\kern-.1em/
\kern-.15em\lower.25ex\hbox{$\scriptstyle 3$} n}}}} + 0,015.18 \Rightarrow {m_{{\rm{ch\^E t r\raise.5ex\hbox{$\scriptstyle 3$}\kern-.1em/
\kern-.15em\lower.25ex\hbox{$\scriptstyle 3$} n}}}} = \,\,2,31\,\,gam\)
Câu trả lời của bạn
\({n_{KCl\,\,trong\,\,X}} = \frac{{{n_{KCl\,\,trong\,\,Z}}}}{5} = 0,2\,\,mol \Rightarrow \% {m_{KCl}}_{\,trong\,\,X}\frac{{0,2.74,5}}{{82,3}}.100\% = 18,1\% \)
Câu trả lời của bạn
\( \Leftrightarrow 0,08.108 + {m_{Cu}} + (5,85 - 0,04.65) = 7,76 + 10,53 \Leftrightarrow {m_{Cu}} = 6,4\,\,gam\)
Câu trả lời của bạn
Xét hai trường hợp và tính toán theo phản ứng:
(1). Phản ứng tạo ra hai muối NaH2PO4 và Na2HPO4.
(2). Phản ứng tạo ra hai muối Na2HPO4 và Na3PO4.
Câu trả lời của bạn
Phản ứng xảy ra khi đun nóng dung dịch X:
\(2HCO_{3}^{-}\xrightarrow{{{t}^{o}}}CO_{3}^{2-}+C{{O}_{2}}~+~{{H}_{2}}O\) (1)
Theo giả thiết và (1), ta có: \({{n}_{C{{O}_{2}}}}={{n}_{{{H}_{2}}O}}=0,1\,\,mol.\)
Áp dụng bảo toàn khối lượng, ta có:
\({{m}_{X}}={{m}_{k\tilde{O}t\text{ t }\!\!\tilde{\mathrm{n}}\!\!\text{ a}}}+{{m}_{ch\hat{E}t\text{ r }\!\!{\scriptscriptstyle 3\!/\!{ }_4}\!\!\text{ n}}}+{{m}_{C{{O}_{2}}}}+{{m}_{{{H}_{2}}O}}\)
\(\Leftrightarrow {{m}_{X}}=3,68+13,88+0,1.44+0,1.18=23,76\,\,gam\)
Câu trả lời của bạn
\( \Leftrightarrow {m_X} + 294 = 331,2 + 13,4 \Rightarrow {m_X} = 50,6\,\,gam\)
Câu trả lời của bạn
\({n_{HN{O_3}}} = {n_{NO_3^ - \,\,tao{\rm{ muoi}}}} + {n_{NO}} = 0,48 + 0,16 = 0,64\,\,mol \Rightarrow {V_{dd\,\,HN{O_3}\,\,1M}} = 0,64\)
Câu trả lời của bạn
\(\begin{array}{l}
C{\% _{Cu{{(N{O_3})}_2}}} = \frac{{0,1.188}}{{89}}.100\% = 21,12\% {\rm{ }}\\
C{\% _{Fe{{(N{O_3})}_3}}} = \frac{{0,1.242}}{{89}}.100\% = 27,19\%
\end{array}\)
Câu trả lời của bạn
BTKL: m hh đầu = mX => 0,35.26 + 0,65.2 = nX.8.2 => nX = 0,65 mol
=> n giảm = nH2 pư = 0,35 + 0,65 – 0,65 = 0,35 mol
Mặt khác: nC2H2 dư = nAg2C2 = 12 : 240 = 0,05 mol
BT liên kết π: 2nC2H2 bđ = nH2 pư + 2nC2H2 dư + n π(Y) => 2.0,35 = 0,35 + 2.0,05 + n π(Y)
=> n π(Y) = 0,25 mol
=> nBr2 = n π(Y) = 0,25 mol
Câu trả lời của bạn
Đốt cháy ankan: nankan = nH2O – nCO2
Đốt cháy anken: nH2O = nCO2
=> Đốt cháy hỗn hợp ankan, anken thì nankan = nH2O – nCO2 = 0,05 mol
=> nanken = 0,15 mol => %nanken = 75%
Câu trả lời của bạn
BTNT “C”: nC = nCO2 = 0,6 mol
Bảo toàn khối lượng: mX = mC + mH => mH = 8 – 0,6 .12 = 0,8 => nH = 0,8 mol
BTNT “H”: nH2O = nH : 2 = 0,4 mol
nankin = nCO2 – nH2O = 0,6 – 0,4 = 0,2 mol
=> Số C trung bình = 0,6 : 0,2 = 3
Do 2 ankin ở đk thường tồn tại ở thể khí => có số C ≤ 4
=> hỗn hợp X chứa 2 ankin là C2H2 (0,1 mol) và C4H6 (0,1 mol)
mAgC≡CAg = 24 g
Do lượng Kết tủa > 25 g => C4H6 cũng tạo kết tủa
=> CTCT của C4H6 là HC≡C-CH2-CH3
Câu trả lời của bạn
Hỗn hợp gồm ankan và anken khi đốt cháy hoàn toàn sẽ thu được nCO2 < nH2O.
Hỗn hợp X không thể gồm ankan và anken
Câu trả lời của bạn
Giả sử V1 và V2 tương ứng với số mol n1 và n2 (n2 – n1 = 0,5)
=> n1.X + n2.Y = 107,5
Và n2.X + n1.Y = 91,25
Trừ 2 phương trình cho nhau :
(n1 – n2)X - (n1 – n2)Y = 16,25
=> 0,5.Y – 0,5.23,5 = 16,25
=>Y = 56 (C4H8)
Câu trả lời của bạn
But-2-en có cấu tạo đối xứng, khi cộng nước thu được 1 ancol duy nhất:
CH3-CH=CH-CH3 + H2O → CH3-CH(OH)-CH2-CH3
Câu trả lời của bạn
CH3COONa + NaOH → CH4 + Na2CO3
=> nY = nmuối axetat = 0,21 mol
=> V = 4,704 lít
Câu trả lời của bạn
Các chất làm mất màu dung dịch KMnO4 là 4 chất: eten; axetilen; toluen; stiren
(các chất có liên kết kép ngoài vòng benzen hoặc phần nhánh hidrocacbon của vòng benzen)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *