Bài học chủ yếu rèn luyện kỹ năng viết phương trình phản ứng trao đổi giữa các chất điện li dạng đầy đủ và dạng ion thu gọn. Vận dụng kiến thức để dự đoán chiều hướng của phản ứng trao đổi giữa các chất điện li và làm một số dạng bài tập cơ bản.
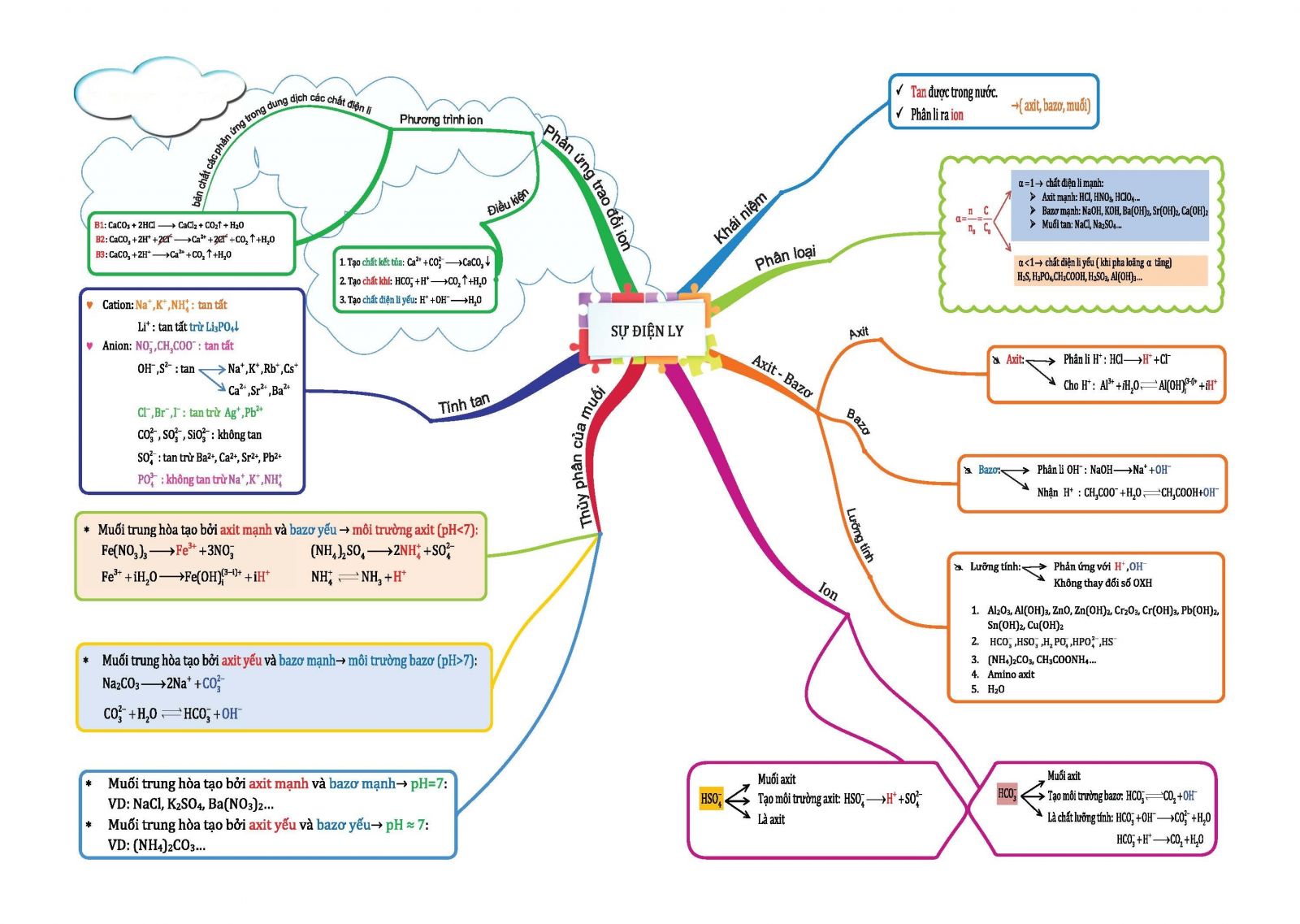 Hình 1: Sơ đồ tư duy Hóa học "Sự điện li"
Hình 1: Sơ đồ tư duy Hóa học "Sự điện li"
Axit là chất khi tan trong nước phân li ra ion H+
Bazơ là chất khi tan trong nước phân li ra ion OH-
Hiđroxit lưỡng tính là chất khi tan trong nước vừa có thể phân li theo kiểu axit, vừa có thể phân li theo kiểu bazơ.
Hầu hết các muối khi tan trong nước phân li hoàn toàn thành cation kim loại (hoặc NH4+) và anion gốc axit.
Nếu gốc axit còn chứa hiđro axit thì nó sẽ tiếp tục phân li yếu ra cation H+ và anion gốc axit.
Dùng phản ứng trao đổi ion để tách:
a, ion Mg2+ ra khỏi dung dịch chứa các chất tan Mg(NO3)2 và KNO3
b, ion PO43- ra khỏi dung dịch chứa các chất tan K3PO4 và KNO3
a, Mg(NO3)2 + 2KOH →Mg(OH)2 ↓+ 2KNO3
b, K3PO4 + 3AgNO3 → Ag3PO4 ↓+ 3KNO3
Trong y học,dược phẩm Nabica (NaHCO3) là chất dùng để trung hòa bớt lượng dư axit HCl trong dạ dày.
a, Viết PTHH dưới dạng phân tử và ion rút gọn của phản ứng.
b, Nồng độ axit HCl trong dạ dày 0,035M, tính thể tích dung dịch HCl được trung hòa và thể tích CO2 (đktc) sinh ra khi uống 0,336g NaHCO3.
NaHCO3 + HCl → NaCl + CO2 + H2O (1)
HCO3- + H+ → CO2 + H2O
Tính số mol NaHCO3 rồi dựa vào PTHH (1) suy ra số mol CO2 và HCl rồi tính thể tích
VCO2 = 0,0896 lít; VHCl = 0,114 lít
Hòa tan 0,887g NaCl và KCl trong nước, xử lý dung dịch thu được bằng một lượng dư dung dịch AgNO3 thu được 1,913g kết tủa. Tính thành phần phần trăm của mỗi chất trong hỗn hợp.
NaCl + AgNO3 → AgCl↓ + NaNO3
KCl + AgNO3 → AgCl↓ + KNO3
Gọi x, y lần lượt là số mol của NaCl và KCl, dựa vào khối lượng hỗn hợp ta có pt và dựa vào số mol kết tủa ta có thêm phương trình nữa, giải hệ tìm x,y →tính khối lượng KCl rồi tính %KCl, %NaCl = 100 - %KCl
Hệ: \(\left\{ \begin{array}{l} 58,5x + 74,5y = 0,887\\ x + y = 0,0133 \end{array} \right.\)→ x= 0,00659 mol; y = 0,00671 mol→ mKCl = 0,5g
→%mKCl = 56,4%, %mNaCl = 43,6%
Cho 400g dung dịch H2SO4 49% vào nước được 2 lít dung dịch A.
a, Tính nồng độ mol ion H+ trong dung dịch A.
b, Tính thể tích dd NaOH 1,8M cần thêm vào dd A để thu được dung dịch có pH = 1, pH = 7, pH =13
a,Tính khối lượng H2SO4 →tính số mol H2SO4→ lấy số mol chia thể tích ra nồng độ H2SO4 = 1M
H2SO4→ 2H+ + SO42-
1M 2M
[H+]ddA = 2M
b, số mol H2SO4 = 2 mol nên số mol H+ = 4 mol, số mol NaOH = 1,8 VddNaOH (mol)
nên nOH- = 1,8V, bản chất của quá trình trung hòa là
H+ + OH- → H2O ,vì thu được dd có pH = 1 < 7 nên môi trường là axit, số mol H+ dư
4 mol > 1,8VddNaOH
nH+ dư = 4 - 1,8VddNaOH (1)
pH = 1 → [H+]= 10-1 M = 0,1M, Vddsau = VddA + VNaOH = 2+ VddNaOH , →nH+ dư = 0,1 (2+ VddNaOH) (2)
Từ (1) và (2) có: 4-1,8VddNaOH = 0,1 . (2+ VddNaOH) → VddNaOH = 2 lít
pH = 7 thì môi trường trung tính nH+ = nOH- →4 = 1,8VddNaOH→ VddNaOH = 2,2 lít
pH = 13>7, môi trường bazơ, số mol OH- dư: nOH- dư = 1,8VddNaOH- 4 (1)
pH = 13 → [H+]= 10-13 M→ [OH-] = \(\frac{{{{10}^{ - 14}}}}{{{{10}^{ - 13}}}}\) = 0,1M→nOH- dư = 0,1 (2+ VddNaOH) (2)
Cho biết giá trị pH của các dung dịch sau:
Na2CO3, KCl, CH3COONa, NaHSO4, AlCl3, Na2S, C6H5ONa, NH4Cl. Giải thích?
ion trung tính(mạnh) không bị thủy phân, các ion trung tính gồm gốc của axit mạnh (HCl, HBr, HI, HNO3, H2SO4
, HClO3, HClO4 ) và cation của bazơ mạnh( KOH, NaOH, Ca(OH)2, Ba(OH)2)
Na2CO3→2Na+ + CO32-
Na+ là cation của bazơ mạnh nên không bị thủy phân, CO32- gốc axit yếu nên bị thủy phân
CO32- + H2O ⇄HCO3- + OH-, môi trường bazơ nên pH >7
KCl → K+ + Cl- , ion mạnh không bị thủy phân, môi trường trung tính, pH = 7
CH3COONa→ CH3COO- + Na+
CH3COO- + H2O ⇄CH3COOH + OH--, môi trường bazơ nên pH >7
NaHSO4 → Na+ + HSO4-
HSO4- ⇄H+ + SO42- (hoặc HSO4- + H2O ⇄H3O+ + SO42- (H3O+ chính là H+) môi trường axit nên pH <7
AlCl3→ Al3+ + 3Cl-
Al3+ + H2O ⇄Al(OH)2+ + H+ → môi trường axit nên pH <7
Na2S→ 2Na+ + S2-
S2- + H2O ⇄HS- + OH- → môi trường bazơ nên pH >7
C6H5ONa →C6H5O- + Na+
C6H5O- + H2O ⇄ C6H5OH + OH- → môi trường bazơ nên pH >7
NH4Cl→ NH4+ + Cl-, NH4++ H2O ⇄NH3 + H3O+→ môi trường axit nên pH <7
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 5có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Dãy chất nào sau đây là các chất điện li mạnh?
Trong dung dịch H2S (dung môi là nước) có thể chứa
Một dung dịch có [ OH- ]= 10-5 M. Môi trường của dung dịch này là
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 5.
Bài tập 1 trang 23 SGK Hóa học 11
Bài tập 2 trang 23 SGK Hóa học 11
Bài tập 3 trang 23 SGK Hóa học 11
Bài tập 4 trang 23 SGK Hóa học 11
Bài tập 5 trang 23 SGK Hóa học 11
Bài tập 6 trang 23 SGK Hóa học 11
Bài tập 7 trang 23 SGK Hóa học 11
Bài tập 5.1 trang 8 SBT Hóa học 11
Bài tập 5.2 trang 8 SBT Hóa học 11
Bài tập 5.3 trang 8 SBT Hóa học 11
Bài tập 5.4 trang 8 SBT Hóa học 11
Bài tập 5.5 trang 8 SBT Hóa học 11
Bài tập 5.6 trang 8 SBT Hóa học 11
Bài tập 5.7 trang 8 SBT Hóa học 11
Bài tập 5.8 trang 9 SBT Hóa học 11
Bài tập 5.9 trang 9 SBT Hóa học 11
Bài tập 5.10 trang 9 SBT Hóa học 11
Bài tập 5.11 trang 9 SBT Hóa học 11
Bài tập 1 trang 23 SGK Hóa học 11 nâng cao
Bài tập 2 trang 23 SGK Hóa học 11 nâng cao
Bài tập 3 trang 23 SGK Hóa học 11 nâng cao
Bài tập 4 trang 23 SGK Hóa học 11 nâng cao
Bài tập 5 trang 23 SGK Hóa học 11 nâng cao
Bài tập 6 trang 23 SGK Hóa học 11 nâng cao
Bài tập 7 trang 23 SGK Hóa học 11 nâng cao
Bài tập 8 trang 23 SGK Hóa học 11 nâng cao
Bài tập 9 trang 23 SGK Hóa học 11 nâng cao
Bài tập 10 trang 23 SGK Hóa học 11 nâng cao
Bài tập 1 trang 30 SGK Hóa học 11 nâng cao
Bài tập 2 trang 30 SGK Hóa học 11 nâng cao
Bài tập 3 trang 31 SGK Hóa học 11 nâng cao
Bài tập 4 trang 31 SGK Hóa học 11 nâng cao
Bài tập 5 trang 31 SGK Hóa học 11 nâng cao
Bài tập 6 trang 31 SGK Hóa học 11 nâng cao
Bài tập 7 trang 31 SGK Hóa học 11 nâng cao
Bài tập 8 trang 31 SGK Hóa học 11 nâng cao
Bài tập 9 trang 31 SGK Hóa học 11 nâng cao
Bài tập 10 trang 31 SGK Hóa học 11 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Dãy chất nào sau đây là các chất điện li mạnh?
Trong dung dịch H2S (dung môi là nước) có thể chứa
Một dung dịch có [ OH- ]= 10-5 M. Môi trường của dung dịch này là
Cho 1 giọt quỳ tím lần lượt vào từng dung dịch các muối có cùng nồng độ 0,1M sau : NH4Cl (1), Al2(SO4)3 (2), K2CO3 (3), KNO3 (4) dung dịch có xuất hiện màu đỏ là ?
Sắp xếp các dung dịch sau : H2SO4 (1), CH3COOH (2), KNO3 (3), Na2CO3 (4) ( có cùng nồng độ mol) theo thứ tự độ pH tăng dần :
Cho 200 ml dung dịch KOH 2M trung hòa V ml dung dịch H2SO4 2M . Giá trị V = ?
Cho 200 ml dung dịch gồm KOH 2M và Ca(OH)2 1M trung hòa V ml dung dịch H2SO4 0,5M . Giá trị V = ?
Tính pH của dung dịch chứa 0,4 gam NaOH trong 100 ml .
Cho các chất: NaOH, HF, HBr, CH3COOH, C2H5OH, C12H22O11 (saccarozơ), CH3COONa, NaCl, NH4NO3. Tổng số chất thuộc chất điện li và chất điện li mạnh là?
Một dung dịch có [H+] = 0,001 M. Tính [OH–] và pH của dung dịch?
Viết phương trình điện li của các chất sau: K2S, Na2HPO4, NaH2PO4, Pb(OH)2, HBrO, HF, HCIO4.
Một dung dịch có [H+] = 0,01 M. Tính [OH–] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm? Hãy cho biết màu của quỳ tím trong dung dịch này.
Một dung dịch có pH = 9,0. Tính nồng độ mol của các ion H+ và OH– trong dung dịch. Hãy cho biết màu của phenolphtalein trong dung dịch này.
Viết các phương trình phân tử và ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau:
a) Na2CO3 + Ca(NO3)2
b) FeSO4 + NaOH (loãng)
c) NaHCO3 + HCI
d) NaHCO3+ NaOH
e) K2CO3+ NaCI
g) Pb(OH)2 (r) + HNO3
h) Pb(OH)2 (r) + NaOH
i) CuSO4 + Na2S
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi:
A. Các chất phản ứng phải là những chất dễ tan.
B. Các chất phản ứng phải là những chất điện li mạnh.
C. Một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
D. Phản ứng không phải là thuận nghịch.
Kết tủa CdS được tạo thành trong dung dịch bằng các cặp chất nào dưới đây?
A. CdCl2 + NaOH
B. Cd(NO3)2 + H2S
C. Cd(NO3)2 + HCl
D. CdCl2 + Na2SO4
Viết phương trình hoá học (dưới dạng phân tử và ion rút gọn) của phản ứng trao đổi ion trong dung dịch tạo thành từng kết tủa sau: Cr(OH)3; Al(OH)3; Ni(OH)2
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong đó là :
A. [H+] = 1.10-4 M.
B. [H+] = 1.10-5 M.
C. [H+] > 1.10-5 M.
D. [H+] < 1.10-5 M.
Dung dịch axit mạnh một nấc X nồng độ 0,010 mol/l có pH = 2 và dung dịch bazơ mạnh một nấc Y nồng độ 0,010 mol/l có pH = 12. Vậy:
A. X và Y là các chất điện li mạnh.
B. X và Y là các chất điện li yếu.
C. X là chất điện li mạnh, Y là chất điện li yếu.
D. X là chất điện li yếu, Y là chất điện li mạnh.
Dung dịch axit mạnh H2SO4 0,10M có :
A. pH = 1.
B. pH < 1.
C. pH > 1.
D. [H+] > 0,2M.
Dung dịch chất A có pH = 3. Cần thêm V2 ml nước vào V1 ml dung dịch chất A để pha loãng thành dung dịch có pH = 4. Biểu thức liên hệ giữa V1 và V2 là
A. V2 = 9V1
B. V2 = 10V1
C. V1 = 9V2
D. V2 = V1/10
Nồng độ H+ trong rượu vang là 3,2.10-4 M. Sau khi mở nút chai để hở trong không khí một tháng, nồng độ H+ là 1.10-3M. Hỏi pH của rượu vang tăng lên hay giảm xuống sau khi để trong không khí ?
Viết phương trình dạng phân tử ứng với phương trình ion rút gọn sau:
1. Ba2+ + CO32− → BaCO3↓
2. Fe3+ + 3OH− → Fe(OH)3↓
3. NH4+ + OH− → NH3↑ + H2O
4. S2− + 2H+ → H2S↑
5. HClO + OH− → ClO- + H2O
6. CO2 + 2OH− → CO32− + H2O
Viết phương trình dạng phân tử và ion rút gọn của các phản ứng trong dung dịch theo sơ đồ sau:
1. Pb(NO3)2 + ? → PbCl2↓ + ?
2. Sn(OH)2 + ? → Na2SnO2↓ + ?
3. MgCO3 + ? → MgCl2 + ?
4. HPO42− + ? → H3PO4 + ?
5. FeS + ? → FeCl2 + ?
6. Fe2(SO4)3 + ? → K2SO4 + ?
Hoà tan hoàn toàn 0,12 g Mg trong 100,0 ml dung dịch HCl 0,20 M. Tính pH của dung dịch sau khi phản ứng kết thúc (thể tích dung dịch biến đổi không đáng kể).
Trong nước biển, magie là kim loại có hàm lượng lớn thứ hai sau natri. Mỗi kilogam nước biển chứa khoảng 1,3 g magie dưới dạng các ion Mg2+. Ở nhiều quốc gia, magie được khai thác từ nước biển. Quá trình sản xuất magie từ nước biển gồm các giai đoạn sau:
1. Nung đá vôi thành vôi sống.
2. Hoà tan vôi sống trong nước biển tạo ra kết tủa Mg(OH)2.
3. Hoà tan kết tủa Mg(OH)2 trong dung dịch HCl.
4. Điện phân MgCl2 nóng chảy
Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn (nếu có) của quá trình sản xuất trên.
Nước chứa nhiểu ion Ca2+ và Mg2+ là nước cứng. Nước chứa ít hoặc không chứa các ion Ca2+ và Mg2+ là nước mềm. Nước cứng không phù hợp cho việc sử dụng trong công nghiệp và sinh hoạt. Trong nước thường chứa các hợp chất Ca(HCO3)2, Mg(HCO3)2, CaCl2 và MgCl2 hoà tan.
Để loại các ion Ca2+ và Mg2+ dưới dạng Ca(HCO3)2, Mg(HCO3)2 và MgCl2 người ta cho sữa vôi Ca(OH)2 vào nước sẽ tạo ra các kết tủa CaCO3 và Mg(OH)2.
Để loại Ca2+ dưới dạng CaCl2 người ta hoà tan Na2CO3 vào nước sẽ tạo kết tủa CaCO3.
Hãy viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng trên.
Có 6 dung dịch đựng trong 6 lọ mất nhãn: Mg(NO3)2, Zn(NO3)2, Pb(NO3)2, AlCl3, KOH và NaCl. Chỉ dùng thêm dung dịch AgNO3 và một thuốc thử nữa, hãy trình bày cách nhận biết từng dung dịch. Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng nhận biết đó.
Viết các biểu thức tính hằng số phân li axit Ka hoặc hằng số phân li bazơ Kb của các axit và bazơ sau: HClO, BrO-, HNO2, NO2-.
Đối với dung dịch axit yếu HNO2 0,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào sau đây là đúng?
A. pH > 1,00;
B. pH = 1,00;
C. [H+] > [NO2-];
D. [H+] < [NO2-];
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Các quá trình điện li:
HNO2 \(\overset {} \leftrightarrows \) H+ + NO2- Ka = 4.10-4
H2O \(\overset {} \leftrightarrows \) H+ + OH- Kw = 10-14
Ta thấy: Ka.Ca = 0,2.4.10-4 = 8.10-5 > > Kw = 10-14. Do vậy sự phân li của H2O tạo ra H+ là không đáng kể. Vì vậy bỏ qua sự điện li của H2O. Dung dịch chỉ có sự điện li của HNO2
HNO2 \(\overset {} \leftrightarrows \) H+ + NO2- Ka = 4.10-4
ban đầu: 0,2
phân li: x x x
cân bằng: (0,2 - x) x x
Ta có:\(Ka = {{{\rm{[}}{H^ + }{\rm{]}}.{\rm{[}}N{O_2}^ - {\rm{]}}} \over {{\rm{[}}HN{O_2}]}} = {{{x^2}} \over {0,2 - x}} = {4.10^{ - 4}}(*)\)
Giải phương trình bậc 2
→ x2 + 4.10-4x - 0,2.4.10-4 = 0
→ x = 8,7465.10-3 (M)
→ [H+] = x = 8,7465.10-3 (M)
→ pH = -lg[H+] = -lg(8,7465.10-3) = 2,058
Câu trả lời của bạn
Các phản ứng tạo kết tủa:
H2SO4 + BaCl2 → BaSO4↓ + 2 HCl
H2O + SO3 + BaCl2 → BaSO4↓ + 2 HCl
NaHSO4 + BaCl2 → BaSO4↓ + NaCl + HCl
Na2SO3 + BaCl2 → BaSO3↓ + 2 NaCl
K2SO4 + BaCl2 → BaSO4 ↓ + 2 KCl
Câu trả lời của bạn
Các chất phản ứng: HNO3, Na2SO4, Ca(OH)2, KHSO4
PTHH:
2HNO3 + Ba(HCO3)2 → Ba(NO3)2 + 2H2O + 2CO2
Na2SO4 + Ba(HCO3)2 → BaSO4 ↓ + 2NaHCO3
Ca(OH)2 + Ba(HCO3)2 → BaCO3 ↓ + CaCO3 ↓ + 2H2O
2KHSO4 + Ba(HCO3)2 → BaSO4 ↓ + K2SO4 + 2CO2 + 2H2O
1) NaHSO4 + NaHSO3
2) Na3PO4 + K2SO4
3) AgNO3 + Fe(NO3)2
4) C6H5ONa + H2O
5) CuS + HNO3
6) BaHPO4 + H3PO4
7) NH4Cl + NaNO2 (đun nóng)
8) Ca(HCO3)2 + NaOH
9) NaOH + Al(OH)3
10) MgSO4 + HCl.
Số phản ứng xảy ra là
Câu trả lời của bạn
1) NaHSO4 + NaHSO3 → Na2SO4 + H2O + SO2
2) Na3PO4 + K2SO4 → Không phản ứng
3) AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag
4) C6H5ONa + H2O → Không phản ứng
5) CuS + HNO3 → Không phản ứng
6) BaHPO4 + H3PO4 → Ba(H2PO4)2
7) NH4Cl + NaNO2 (đun nóng) → NaCl + N2 + 2H2O
8) Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + 2H2O
9) NaOH + Al(OH)3 → NaAlO2 + 2H2O
10) MgSO4 + HCl → Không phản ứng
Vậy có 6 phản ứng xảy ra.
A NH4+, Na+, K+.
B Cu2+, Mg2+, Al3+.
C Fe2+, Zn2+, Al3+ .
D Fe3+, HSO4-.
Câu trả lời của bạn
B và C có phản ứng 2Al3+ + 3CO32- + 3H2O → 2Al(OH)3↓ + 3CO2
D có phản ứng 2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3↓ + 3CO2
Đáp án A
A AgNO3, BaCl2, Al2(SO4)3, Na2CO3.
B AgCl, Ba(NO3)2, Al2(SO4)3, Na2CO3.
C AgNO3, BaCl2, Al2(CO3)3, Na2SO4.
D Ag2CO3, Ba(NO3)2, Al2(SO4)3, NaNO3.
Câu trả lời của bạn
B. AgCl là chất kết tủa
C. Al2(CO3)3 không tồn tại bị thủy phân thành Al(OH)3 và giải phóng khí CO2
D. Ag2CO3 là chất kết tủa
Đáp án A
Câu trả lời của bạn
Phản ứng 1; 2; 3; 4 là phản ứng axit - bazơ.
1) H+ + OH- → H2O
2) 3H+ + Al(OH)3 → Al3+ + 3H2O
3) Ba2+ + SO42- → BaSO4
4) SO3 + 2OH- → SO42- + H2O
Câu trả lời của bạn
1, 2 và 4.
Câu trả lời của bạn
Các chất phản ứng: (NH4)2SO4, MgCl2, FeCl2
A Na+, Mg2+, NO3-, SO42-.
B Ba2+, Al3+, Cl-, HSO4-.
C Cu2+, Fe3+, SO42-, Cl-.
D K+, NH4+, Cl-, PO43-.
Câu trả lời của bạn
HSO4-→ H+ + SO42-
Ba2+ + SO42- → BaSO4 ↓
=> dd B không tồn tại
Đáp án B
A NH4+ ; Na+; HCO3- ; OH-.
B Fe2+ ; NH4+ ; NO3- ; SO42-.
C Na+; Fe2+ ; H+ ; NO3-.
D Cu2+; K+ ; OH- ; NO3-.
Câu trả lời của bạn
Các ion không phản ứng với nhau có thể cùng tồn tại trong một dung dịch.
A loại vì NH4+ + OH- → NH3 + H2O; HCO3- + OH- → CO32- + H2O
C loại vì 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
D loại vì Cu2+ + 2OH- → Cu(OH)2
Đáp án B
A Na+, NH4+, SO42-, Cl-.
B Mg2+, Al3+, NO3-, Cl-.
C Ag+, Mg2+, NO3-, Br-.
D Fe3+, Ag+, NO3-, CH3COO-.
Câu trả lời của bạn
Do xảy ra phản ứng Ag+ + Br- → AgBr↓
Đáp án C
A Ba2+ + SO42- → BaSO4
B Ba2+ + HPO42- + SO42- + 2H+ → BaSO4 + H3PO4
C HPO42- + 2H+ → H3PO4
D Ba2+ + PO43- + SO42- + 3H+ → BaSO4 + H3PO4
Câu trả lời của bạn
Ba2+ + HPO42- + SO42- + 2H+ → BaSO4 + H3PO4
A FeS + 2HCl → FeCl2 + H2S.
B 2CH3COOH + K2S → 2CH3COOK + H2S.
C 2NaHSO4 + Na2S → 2Na2SO4 + H2S.
D BaS + H2SO4 → BaSO4 + H2S.
Câu trả lời của bạn
- Xét A: FeS + 2HCl → FeCl2 + H2S ↑
⟹ PT ion rút gọn: FeS + 2H+ → Fe2+ + H2S
- Xét B: 2CH3COOH + K2S → 2CH3COOK + H2S ↑
⟹ PT ion rút gọn: 2CH3COOH + S2- → 2CH3COO- + H2S ↑
- Xét C: 2NaHSO4 + Na2S → 2Na2SO4 + H2S ↑
⟹ PT ion rút gọn: 2H+ + S2- → H2S ↑
- Xét D: BaS + H2SO4 → BaSO4 ↓ + H2S
⟹ PT ion rút gọn: BaS + 2H+ + SO42- → BaSO4 ↓ + H2S ↑
A NaNO3, AlCl3, BaCl2, NaOH, KOH.
B BaCl2, NaOH, FeCl3, Fe(NO3)3, KCl.
C NaHCO3, BaCl2, Na2S, Na2CO3, KOH.
D Na2S, Cu(OH)2, Na2CO3, FeCl2, NaNO3.
Câu trả lời của bạn
A. NaHSO4 không phản ứng với NaNO3
B. NaHSO4 không phản ứng với FeCl3, Fe(NO3)3 , KCl.
C. Tất cả các chất đều phản ứng với NaHSO4
D. NaHSO4 không phản ứng với NaNO3, FeCl2
Đáp án C
Câu trả lời của bạn
Ba(OH)2 + Ca(HCO3)2 → CaCO3 + BaCO3 +2 H2O
Câu trả lời của bạn
\({V_2}{.10^{ - b}} = {V_1}{.10^{ - a}} \Rightarrow \frac{{{V_2}}}{{{V_1}}} = \frac{{{{10}^{ - 1}}}}{{{{10}^{ - 4}}}} = 1000 \Rightarrow {V_2} = 1000.{V_1} \Rightarrow {V_{{H_2}O}} = {V_2} - {V_1} = 999.{V_1} = 1998.ml\)
Câu trả lời của bạn
\({V_2}{.10^{ - b}} = {V_1}{.10^{ - a}} \Rightarrow \frac{{{V_2}}}{{{V_1}}} = \frac{{{{10}^{ - 3}}}}{{{{10}^{ - 5}}}} = 100 \Rightarrow {V_2} = 100.{V_1}\)
Câu trả lời của bạn
\(\left\{ \begin{array}{l}
{H^ + }:0,1\\
O{H^ - }:0,15
\end{array} \right. \Rightarrow n_{O{H^ - }}^{du} = 0,05 \Rightarrow \left[ {O{H^ - }} \right] = 0,1 \Rightarrow pOH = 1 \Rightarrow pH = 13\)
Câu trả lời của bạn
\(\left\{ \begin{align}
& {{n}_{HCl}}=0,{{2.10}^{-3}} \\
& {{n}_{NaOH}}=a \\
\end{align} \right.\to pH=11\Rightarrow pOH=3\) dư NaOH
\(NaOH+HCl\to NaCl+{{H}_{2}}O\Rightarrow a-{{2.10}^{-4}}={{2.10}^{-4}}\Rightarrow a={{4.10}^{-4}}\Rightarrow {{m}_{NaOH}}=0,016.g\)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *