Nội dung bài giảng giúp các em hs hệ thống hóa kiến thức các hiđrocacbon quan trọng: ankan, anken, ankin và ankylbenzen về đặc điểm cấu tạo tính chất vật lý, tính chất hóa học, tính đặc trưng và ứng dụng.
|
| ANKAN | ANKEN | ANKIN | ANKYLBENZEN |
| 1. CTPT | CnH2n+2 (n ≥ 1) | CnH2n (n ≥ 2) | CnH2n - 2 (n ≥ 2) | CnH2n - 6 (n ≥ 6) |
| 2. Đặc điểm cấu tạo | - Chỉ có liên kết đơn. | - Có 1 liên kết đôi C=C. | - Có một liên kết ba C≡C. | - Có vòng benzen. |
| 3. Đồng phân | - Mạch cacbon. | - Mạch cacbon. - Vị trí liên kết đôi - Hình học. | - Mạch cacbon. - Vị trí liên kết ba. | - Mạch cacbon của nhánh ankyl - Vị trí tương đối của các nhóm ankyl. |
| 4. Lí tính | - Ở điều kiện thường; từ C1 đến C4 là chất khí, C5 đến C17 là chất lỏng và còn lại là chất rắn. - Không màu. - Không tan trong nước. - Nhiệt độ sôi, nhiệt độ nóng chảy tăng dần khi phân tử khối tăng. | |||
| ANKAN | ANKEN | ANKIN | ANKYLBENZEN | |
| Phản ứng thế | Phản ứng thế với halogen | Phản ứng thế bằng ion kim loại | Phản ứng thế halogen, nitro hóa | |
| Phản ứng tách | Phản ứng đehiđro hóa, crackinh | |||
| Phản ứng cộng | Phản ứng với halogen, HX, H2 | Phản ứng với halogen, HX, H2 theo 2 giai đoạn | Phản ứng với H2, Cl2 | |
| Phản ứng trùng hợp | Phản ứng | Phản ứng đime hóa, trime hóa | ||
| Phản ứng oxi hóa không hoàn toàn (phản ứng với KMnO4) | Phản ứng | Phản ứng | Benzen: không làm mất màu Ankylbenzen: làm mất màu khi đun nóng | |
| Phản ứng cháy | nCO22O | nCO2=nH2O | nCO2>nH2O | nCO2 > nH2O |
Hình: Sơ đồ chuyển hóa giữa các loại hidrocacbon
Crackinh hoàn toàn V lít ankan X thu được hỗn hợp Y gồm 0,1V lít C3H8; 0,6V lít CH4; 1,8V lít các hidrocacbon khác. Tỉ khối của Y so với H2 là 14,4. Dẫn 1 mol Y đi qua bình chứa dung dịch Brom dư, phản ứng kết thúc thấy khối lượng bình tăng m gam. Biết các thể tích khí đo ở cùng điều kiện, chỉ có ankan tham gia phản ứng crackinh. Giá trị của m là:
Do tỉ lệ mol cũng bằng tỉ lệ thể tích ở cùng điều kiện nên nếu xét 1 mol Y
\(\Rightarrow n_Y = n_{C_3H_8} + n_{CH_4} + n_{HC khac} = 0,1n_X + 0,6n_X + 1,8n_X\)
⇒ nX = 0,4 mol
Bảo toàn khối lượng: mX = mY = 2 × 14,4 × 1 = 28,8 g
⇒ MX = 72 g ⇒ X là C5H12
Các phản ứng cracking xảy ra:
+/ C5H12 → CH4 + C4H8
+/ C5H12 → C3H8 + C2H4
+/ C5H12 → C2H6 + C3H6
+/ C3H8 → CH4 + C2H4 (*) ⇒ C5H12 → CH4 + 2C2H4
⇒ ở PT (*) có: \(n_{C_2H_4} = 2(n_Y - 2n_X )= 0,4\ mol\)
\(\Rightarrow n_{C_4H_8} = 0,04\ mol;\ n_{C_3H_8} = 0,04\ mol\)
\(\Rightarrow n_{C_2H_4} = 0,44\ mol \Rightarrow n_{HC\ khac} = n_{C_4H_8} + n_{C_2H_4} + n_{C_2H_6} + n_{C_3H_6}\)
\(\Rightarrow n_{C_2H_6} = n_{C_3H_6} = 0,12\ mol\)
⇒ Brom phản ứng được với C4H8; C3H6; C2H4.
⇒ mtăng \(= m_{C_4H_8} + m_{C_2H_4} + m_{C_3H_6} = 19,6\ g\)
Cho hỗn hợp hai anken đồng đẳng kế tiếp nhau tác dụng với nước (có H2SO4 làm xúc tác) thu được hỗn hợp Z gồm hai rượu (ancol) X và Y. Đốt cháy hoàn toàn 1,06 gam hỗn hợp Z sau đó hấp thụ toàn bộ sản phẩm cháy vào 2 lít dung dịch NaOH 0,1M thu được dung dịch T trong đó nồng độ của NaOH bằng 0,05M. Công thức cấu tạo thu gọn của X và Y là (Cho: H = 1; C = 12; O = 16; thể tích dung dịch thay đổi không đáng kể)
Gọi CTPT trung bình 2 anken là \(C_{\bar{n}} H_{2\bar{n}}\)
(\(\Rightarrow\) ancol tương ứng \(C_{\bar{n}} H_{2\bar{n} +2}O\))
+ Đốt cháy: \(C_{\bar{n}} H_{2\bar{n}+2}O\ +\frac{3\bar{n}}{2}O_2\rightarrow \bar{n}CO_2+(\bar{n}+1)H_2O\)
+ Do sản phẩm cháy đi vào NaOH sau đó còn dư bazo nên CO2 tạo muối Na2CO3:
2NaOH + CO2 → Na2CO3 + H2O
\(\Rightarrow 0,5\times n_{NaOH \ pu} = n_{CO2} = 0,5\times 2\times (0,1 - 0,05) = 0,05\) (mol)
\(\Rightarrow C_{\bar{n}} H_{2\bar{n}+2}O=\frac{0,05}{\bar{n}}\) (mol)
\(\Rightarrow M_{C_{\bar{n}} H_{2\bar{n} +2}O}=14\bar{n}+18=\frac{1,06}{\frac{0,05}{\bar{n}}}\Rightarrow \bar{n}=2,5\)
\(\Rightarrow\) Mà 2 anken là đồng đẳng liên tiếp
\(\Rightarrow\) chúng là C2H5OH và C3H7OH
Hấp thụ vừa đủ hỗn hợp khí X gồm etilen và propilen vào dung dịch KMnO4 31,6% ở nhiệt độ thấp thu được dung dịch Y chỉ chứa 3 chất tan là etilenglicol, propan-1-2-điol, kali hidroxit và kết tủa Z. Trong dung dịch Y nồng độ % của etilenglicol là 6,906%. Phần trăm hối lượng prpilen trong X là:
Gọi khối lượng anken hấp thụ là m g có x mol etilen và y mol propen.
⇒ m = 28x + 42y
Giả sử có 100g dung dịch thuốc tím ⇒ n\(\tiny KMnO_4\) = 0,2 mol
Các quá trình:
+ Cho e: anken → diol + 2e
+ Nhận e: MnO4- + 2H2O + 3e → MnO2 + 4OH-
⇒ n e trao đổi = 2x + 2y = 0,2 × 3 = 0,6 mol (1)
⇒ m rắn không tan = 17,4 g
⇒ m dd sau = m dd thuốc tím + m anken – m rắn = 82,6 + m
⇒ C% etilenglicol = \(\frac{62x}{82,6 +28x + 42y}\) = 0,06906 (2)
Từ 1 và 2 ⇒ x = 0,104 mol; y= 0,196 mol
%m propilen (X) = 73,75%
Đốt cháy hoàn toàn 4,64 gam một hiđrocacbon X (chất khí ở điều kiện thường) rồi đem toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng dung dịch Ba(OH)2. Sau các phản ứng thu được 39,4 gam kết tủa và khối lượng phần dung dịch giảm bớt 19,912 gam. Công thức phân tử của X là:
\(m_{\downarrow} = 39,4 \ gam\)
Khối lượng dung dịch giảm bớt 19,912 gam
\(\\ \Rightarrow m_{\downarrow} - (m_{CO_{2}} + m_{H_{2}O}) = 19,912 \\ \Rightarrow m_{CO_{2}} + m_{H_{2}O} = 19,488 \\ m_{C} + m_{H} = m_{hh} = 4,64 \\ X: C_{x}H_{y} \\ \left\{\begin{matrix} 12x+y = 4,64 \ \ \ \ \ \ \ \\ 44x + 18.\dfrac{y}{2} = 19,488 \end{matrix}\right. \Rightarrow \left\{\begin{matrix} x = 0,348 \\ y = 0,464 \end{matrix}\right. \\ x : y = 0,348:0,464 = 3:4 \Rightarrow C_{3}H_{4}\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 38có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho dãy chuyển hoá sau: \(CH_{4} \xrightarrow[]{ \ \ \ } A \xrightarrow[]{ \ \ \ } B \xrightarrow[]{ \ \ \ } C \xrightarrow[]{ \ \ \ } Cao \ su \ buna.\) Công thức phân tử của B là:
Có bao nhiêu chất ứng với CTPT C4H8 mà khi hiđro hóa với xúc tác Ni nung nóng cho sản phẩm là butan?
Hai hidrocacbon A và B có cùng công thức phân tử C5H12 tác dụng với Cl2 theo tỉ lệ mol 1 : 1 thì A tạo ra 1 dẫn xuất duy nhất còn B tạo ra hỗn hợp 4 dẫn xuất. Tên gọi của A và B lần lượt là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 38.
Bài tập 1 trang 172 SGK Hóa học 11
Bài tập 2 trang 172 SGK Hóa học 11
Bài tập 3 trang 172 SGK Hóa học 11
Bài tập 4 trang 172 SGK Hóa học 11
Bài tập 5 trang 172 SGK Hóa học 11
Bài tập 38.1 trang 59 SBT Hóa học 11
Bài tập 38.2 trang 59 SBT Hóa học 11
Bài tập 38.3 trang 59 SBT Hóa học 11
Bài tập 38.4 trang 93 SBT Hóa học 12
Bài tập 38.5 trang 60 SBT Hóa học 11
Bài tập 38.6 trang 60 SBT Hóa học 11
Bài tập 38.7 trang 60 SBT Hóa học 11
Bài tập 38.8 trang 60 SBT Hóa học 11
Bài tập 38.9 trang 60 SBT Hóa học 11
Bài tập 1 trang 207 SGK Hóa học 11 nâng cao
Bài tập 2 trang 207 SGK Hóa học 11 nâng cao
Bài tập 3 trang 207 SGK Hóa học 11 nâng cao
Bài tập 4 trang 207 SGK Hóa học 11 nâng cao
Bài tập 5 trang 207 SGK Hóa học 11 nâng cao
Bài tập 6 trang 207 SGK Hóa học 11 nâng cao
Bài tập 7 trang 207 SGK Hóa học 11 nâng cao
Bài tập 8 trang 207 SGK Hóa học 11 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho dãy chuyển hoá sau: \(CH_{4} \xrightarrow[]{ \ \ \ } A \xrightarrow[]{ \ \ \ } B \xrightarrow[]{ \ \ \ } C \xrightarrow[]{ \ \ \ } Cao \ su \ buna.\) Công thức phân tử của B là:
Có bao nhiêu chất ứng với CTPT C4H8 mà khi hiđro hóa với xúc tác Ni nung nóng cho sản phẩm là butan?
Hai hidrocacbon A và B có cùng công thức phân tử C5H12 tác dụng với Cl2 theo tỉ lệ mol 1 : 1 thì A tạo ra 1 dẫn xuất duy nhất còn B tạo ra hỗn hợp 4 dẫn xuất. Tên gọi của A và B lần lượt là:
Dẫn từ từ C2H4 vào dung dịch KMnO4, hiện tượng quan sát được là:
Cho hình vẽ mô tả thí nghiệm điều chế Y từ dung dịch X:
Hình vẽ trên minh họa phản ứng nào sau đây?
Khi crackinh hoàn toàn một thể tích ankan X thu được ba thể tích hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 12. Công thức phân tử của X là:
Hỗn hợp khí X gồm CH4, C2H2 có \(\overline{M}_X = 23,5\). Trộn V (lít) X với V1 (lít) hiđrocacbon Y được 107,5 gam hỗn hợp khí Z. Trộn V1 (lít) X với V (lít) hiđrocacbon Y được 91,25 gam hỗn hợp khí F. Biết V1 – V = 11,2 (lít) (các khí đều đo ở đktc). Công thức của Y là:
Hỗn hợp X gồm axetilen và vinyl axetilen có tỉ khối so với hidro là 19,5. Lấy 4,48l X (đktc) trộn với 0,09mol H2 rồi cho vào bình kín có sẵn chất xúc tác Ni, đốt nóng, sau các phản ứng hoàn toàn thu được hỗn hợp Y chỉ gồm các hidrocacbon. Dẫn Y qua dung dịch chứa 0,2mol AgNO3 trong dung dịch NH3 dư, sau khi AgNO3 hết thu được 22,35g kết tủa và có 20,16l khí Z ở đktc thoát ra. Z phản ứng tối đa m gam brom trong CCl4 .Giá trị của m là:
Hỗn hợp X gồm propen và axetilen. Cho 5,6 lit hỗn hợp khí X tác dụng với dung dịch Brom dư, thấy có 72g brom phản ứng. Mặt khác cho 4,48 lit X tác dụng với dung dịch AgNO3 dư /NH3 thu được m gam kết tủa, các khí đều đo ở điều kiện tiêu chuẩn. Giá trị của m là:
Hỗn hợp X gồm 2 hiđrocacbon mạch hở, điều kiện thường ở thể khí, trong phân tử hơn kém nhau một liên kết π. Lấy 0,56 lít X (đktc) tác dụng với brom dư (trong CCl4) thì có 14,4 gam brom phản ứng. Nếu lấ y 2,54 gam X tác dụng hết với lượng dư dung dịch AgNO3 trong NH3 thì thu được khối lượng kết tủa là:
Nhà máy khí Dinh Cố có 2 sản phẩm chính: khí hoá lỏng cung cấp cho thị trường và khí đốt cung cấp cho nhà máy điện Phú Mỹ.
a) Thành phần chính của mỗi sản phẩm đó là gì?
b) Có nên chuyển tất cả lượng khí khai thác được thành khí hoá lỏng hay không, vì sao?
Dầu mỏ hiện ta đang khai thác được chứa rất ít benzen. Em chọn phương án sản xuất benzen nào dưới đây, vì sao? Viết các phương trình hoá học của phản ứng xảy ra

Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
A. \({p_1} = \frac{{47}}{{48}}p.\)
B. p1 = p.
C. \({p_1} = \frac{{16}}{{17}}p.\)
D. \({p_1} = \frac{3}{5}p.\)
Câu trả lời của bạn
Đốt A: CxHy + \(\left( {x + \frac{y}{4}} \right){O_2}\) → xCO2 + \(\frac{y}{2}{H_2}O\)
Vì phản ứng chỉ có N2, H2O, CO2→ các hiđrocacbon bị cháy hết và O2 vừa đủ.
Chọn \({n_{{C_x}{H_y}}} = 1\) →nB = 15 mol → \({n_{{O_2}\,p.u}} = x + \frac{y}{4} = \frac{{15}}{5} = 3\) mol.
→ \({n_{{N_2}}} = 4{n_{{O_2}}} = 12\,\,mol\)
→ \(\left\{ \begin{gathered}
x + \frac{y}{4} = 3 \hfill \\
x:{y \mathord{\left/
{\vphantom {y {2 = 7:4}}} \right.
\kern-\nulldelimiterspace} {2 = 7:4}} \hfill \\
\end{gathered} \right.\) → x = 7/3 ; y = 8/3
Vì nhiệt độ và thể tích không đổi nên áp suất tỉ lệ với số mol khí, ta có:
\(\frac{{{p_1}}}{p} = \frac{{{7 \mathord{\left/
{\vphantom {7 3}} \right.
\kern-\nulldelimiterspace} 3} + {4 \mathord{\left/
{\vphantom {4 3}} \right.
\kern-\nulldelimiterspace} 3} + 12}}{{1 + 15}} = \frac{{47}}{{48}} \to {p_1} = \frac{{47}}{{48}}p.\)
→ Đáp án A
Đốt cháy hoàn toàn a gam hỗn hợp X hai hiđrocacbon A, B thu được \(\frac{{132.a}}{{41}}\) gam CO2 và \(\frac{{45a}}{{41}}\,\,gam\,\,{H_2}O\). Nếu thêm vào hỗn hợp X một nửa lượng A có trong hỗn hợp X rồi đốt cháy hoàn toàn thì thu được \(\frac{{165a}}{{41}}\,\,gam\,\,C{O_2}\) và \(\frac{{60,75a}}{{41}}\,\,gam\,\,{H_2}O\). Biết A, B không làm mất mầu nước Br2.
Câu trả lời của bạn
Chọn a = 41 gam.
Đốt X → \({n_{C{O_2}}} = \frac{{132}}{{44}}\,\,\, = \,\,\,3\,\,mol\) và \({n_{{H_2}O}} = \frac{{45}}{{18}}\,\, = 2,5\,\,mol\).
Đốt \(\left( {X + \frac{1}{2}A} \right) \to {n_{C{O_2}}} = \frac{{165}}{{44}} = 3,75\,\,mol\) và \({n_{{H_2}O}} = \frac{{60,75}}{{18}} = 3,375\,\,\,mol\).
Đốt \(\frac{1}{2}A\) thu được (3,75 - 3) = 0,75 mol CO2 và (3,375 - 2,5) = 0,875 mol H2O.
Đốt cháy A thu được \({n_{C{O_2}}} = 1,5\,\,\,mol\) và \({n_{{H_2}O}} = 1,75\,\,\,mol\).
vì \({n_{{H_2}O}} > {n_{C{O_2}}}\) → A thuộc loại ankan, do đó:
\({C_n}{H_{2n + 2}}\,\,\, + \,\,\,\,\frac{{3n + 1}}{2}{O_2}\,\,\, \to \,\,\,\,nC{O_2}\,\,\, + \,\,\,\left( {n + 1} \right){H_2}O\)
→ \(\frac{{{n_{C{O_2}}}}}{{{n_{{H_2}O}}}} = \frac{n}{{n + 1}} = \frac{{1,5}}{{1,75}}\) → n = 6→ A là C6H14.
→ Đáp án D
a) D thuộc loại hiđrocacbon nào
A. CnH2n+2.
B. CmH2m-2.
C. CnH2n.
D. CnHn.
b) Giá trị m là
A. 2,75 gam.
B. 3,75 gam.
C. 5 gam.
D. 3,5 gam.
Câu trả lời của bạn
a) Chọn a = 82 gam
Đốt X và m gam D (CxHy) ta có:
\(\left\{ \begin{gathered}
{n_{C{O_2}}} = \frac{{275}}{{44}} = 6,25\,\,\,mol \hfill \\
{n_{{H_2}O}} = \frac{{94,5}}{{18}} = 5,25\,\,\,mol \hfill \\
\end{gathered} \right.\)
C6H14 + 19/2O2 → 6CO2 + 7H2O
C6H6 + 15/2O2 → 6CO2 + 3H2O
Đốt D: \({C_x}{H_y}\,\,\, + \,\,\,\left( {x + \frac{y}{4}} \right){O_2}\,\,\,\, \to \,\,\,\,xC{O_2}\,\,\, + \,\,\,\frac{y}{2}{H_2}O\)
Đặt ta có: 86b + 78b = 82
→ b = 0,5 mol.
Đốt 82 gam hỗn hợp X thu được:
\({n_{C{O_2}}} = 0,5 \times \left( {6 + 6} \right) = 6\,\,mol\)
\({n_{{H_2}O}} = 0,5 \times \left( {7 + 3} \right) = 5\,\,mol\)
→ Đốt cháy m gam D thu được:
\(\begin{gathered}
{n_{C{O_2}}} = 6,25 - 6 = 0,25\,\,mol \hfill \\
{n_{{H_2}O}} = 5,25 - 5 = 0,25\,\,mol \hfill \\
\end{gathered} \)
Do \({n_{C{O_2}}} = {n_{{H_2}O}}\) → D thuộc CnH2n. → Đáp án C
b) mD = mC + mH = 0,25.(12 + 2) = 3,5 gam. → Đáp án D

Câu trả lời của bạn
Câu trả lời của bạn
A. 0,09
B. 0,01
C. 0,08
D. 0,02
Câu trả lời của bạn
Nhận xét: hỗn hợp X gồm ankan và anken, khi đốt cháy anken cho số mol H2O và CO2 bằng nhau, do đó chênh lệch giữa số mol H2O và CO2 chính là số mol ankan.
nAnkan = nH2O - nCO2 = \(\frac{{4,14}}{{18}} - \frac{{6,16}}{{44}} = 0,09\)
nAnken = nX - nankan = \(\frac{{2,24}}{{22,4}} - 0,09\) = 0,01 mol

Câu trả lời của bạn
A. C2H2; C3H4
B. C3H6; C4H8
C. C2H4; C3H6
D. C2H6; C3H8
Câu trả lời của bạn
Kết tủa là BaCO3, ta có nCO2 = nBaCO3 = 147,75 : 197 = 0,75 mol ⇒ mCO2= 33 gam.
Khối lượng bình tăng là mCO2 + mH2O = 46,5 → mH2O = 13,5 gam ⇒ nH2O = 0,75 mol.
nH2O = nCO2 ⇒ anken. Số nguyên tử C trung bình 2 chất là 0,57 : 0,3 = 2,5 ⇒ C2H4; C3H6.
A. C2H6 và 10
B. C2H4 và 11
C. C3H8 và 9
D. CH4 và 12
Câu trả lời của bạn
nO2 = 7,68 : 32 = 0,24 mol
Khối lượng bình 1 tăng chính là khối lượng nước ⇒ nH2O = 4,32 : 18 = 0,24 mol
Bảo toàn nguyên tố O có 2nO2 = 2nCO2 + nH2O ⇒ \(nC{O_2} = \frac{{2.0,24 - 0,24}}{2} = 0,12 < n{H_2}O\)
Vậy X là ankan và nX = nH2O - nCO2 = 0,12 mol ⇒ số nguyên tử C của X là \(\frac{{nC{O_2}}}{{nX}} = \frac{{0,12}}{{0,12}} = 1\).
Kết tủa thu được là CaCO3, ta có nCaCO3 = nCO2 = 0,12 → mCaCO3 = 12 gam. Đáp án D.
A. C3H6
B. C4H8
C. C5H10
D. C5H8
Câu trả lời của bạn
nBr2 = 8 : 160 = 0,05 mol ⇒ X phản ứng cộng với Br2 tỉ lệ 1:1.
Sản phẩm phản ứng cộng là dẫn xuất đibrom (CxHyBr2) có số mol = 0,05.
\(\% Br = \frac{{160}}{{12x + y + 160}} = 69,56\% \) ⇒ 12x + y = 70 ⇒ C5H10.
Đáp án C.
A. 1,64
B. 5,28
C. 3,28
D. 3,48
Câu trả lời của bạn
Cho hỗn hợp X (C2H2 và H2) qua bột Ni nung nóng thu được hỗn hợp Z (C2H6 và H2 dư) và Z’ (C2H4 và C2H2 dư).
Ta có mZ = mC (trong Z) + mH (trong Z) = 12.nCO2 + 2nH2O = 1,84 gam
Khối lượng bình brom tăng chính là khối lượng Z’
mZ' = mX = mZ = 0,12.26 + 0,18.2 - 18,4 = 1,64 gam
Đáp án A.
A. 4,2 gam
B. 5,4 gam
C. 13,2 gam
D. 18,6 gam
Câu trả lời của bạn
dX/H2 = MX : 2 = 21 ⇒ MX = 42. Gọi công thức trung bình của 3 chất là C3Hx.
Khi đó 12.3 + x = 42 ⇒ x = 6.
C3H6 + 9/2O2 → 3CO2 + 3H2O
0,1 0,3 0,3
Khối lượng bình tăng là mCO2 + mH2O = 0,3.(44+18) = 18,6 gam. Đáp án D
A. 11,58
B. 15,58
C. 11,85
D. 18,55
Câu trả lời của bạn
nAnkan = 8,8 : 44 = 0,2 mol ⇒ nAnkan pư = 0,2.90% = 0,18 mol và có 0,02 mol ankan dư.
Nhận xét: số mol sản phẩm mới tạo ra gấp đôi số mol ankan phản ứng.
⇒ số mol khí trong A là 0,18.2 + 0,02 = 0,38 mol.
Bảo toàn khối lượng có mA = mC3H8 = 8,8 gam ⇒ MA = 8,8 : 0,38 = 23,26 gam → MA = 8,8 : 0,38 = 23,26 gam
→ dA/H2 = 11,58
Đáp án A.
A. 5,8 gam
B. 6,96 gam
C. 8,7 gam
D. 10,44 gam
Câu trả lời của bạn
Crackinh hoàn toàn isobutan thu được hỗn hợp CH4 và C3H6.
Số mol anken phản ứng với brom là nAnken = nBr2 = 6,4 : 160 = 0,04 mol ⇒ manken = 1,68 gam.
Khối lượng hỗn hợp khí B là \(\frac{{4,704}}{{22,4}}.\frac{{117}}{7}.2 = 7,02g\)
Bảo toàn khối lượng có misobutan = mC3H6 + mB = 1,68 + 7,02 = 8,7 gam.
Đáp án C.
Câu trả lời của bạn
A. Br2
B. NaOH
C. NaCl
D. AgNO3 trong NH3
Câu trả lời của bạn
Đáp án A
A. C4H9OH, CH3COOCH3, C2H5COOH
B. C3H7OH, CH3COOH, HCOOCH3
C. CH3COOCH3, C4H9OH, C2H5COOH
D. CH3COOH, C3H7OH, HCOOCH3
Câu trả lời của bạn
Đáp án C
Nhiệt độ sôi: este < ancol < axit do ancol, axit có liên kết hydro
Câu trả lời của bạn
Vào khoảng những năm 1940 - 1948 người ta phát hiện thấy rằng axit 2,4 - điclophenoxiaxetic (2,4-D) , axit 2,4,5 -triclophenoxiaxetic (2,4,5-T) ở nồng độ cỡ phần triệu có tác dụng kích thích sự sinh trưởng thực vật nhưng ở nồng độ cao hơn chúng có tác dụng tiêu diệt cây cỏ. Từ đó chúng được sản xuất ở quy mô công nghiệp dùng làm chất diệt cỏ phát quang rừng rậm. Trong quá trình sản xuất 2,4-D và 2,4,5-T luôn tạo ra một lượng nhỏ tạp chất là đioxin. Đó là một chất cực độc, tác dụng ngay ở nồng độ cực nhỏ (cỡ phần tỉ) , gây ra những tai hoạ cực kì nguy hiểm (ung thư, quái thai, dị tật…).
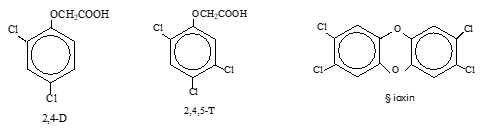
Trong cuộc chiến tranh ở Việt Nam , Đế quốc Mĩ rải xuống Miền Nam nước ta hàng vạn tấn chất độc màu da cam trong đó chứa 2,4-D , 2,4,5-T và đioxin mà hậu quả của nó vẫn còn cho đến ngày ngay.
A. 1-etyl-3-metylbenzen.
B. 1,3,5-trimetylbenzen.
C. Propylbenzen.
D. Cumen.
Câu trả lời của bạn
X phải có tính chất đối xứng
Đáp án B

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *