Nội dung bài Luyện tập Hợp chất hữu cơ, công thức phân tử và công thức cấu tạo ôn tập, hệ thống lại về Hợp chất hữu cơ: Khái niệm, phân loại, đồng đẳng, đồng phân, liên kết trong phân tử. Phản ứng của hợp chất hữu cơ. Rèn luyện kĩ năng giải bài tập xác định CTPT, viết CTCT của một số chất hữu cơ đơn giản, nhận dạng một vài loại phản ứng của các chất hữu cơ đơn giản.
1. Hợp chất hữu cơ là hợp chẩt của cacbon (trừ CO, CO2, muối cacbonat, xianua, cacbua, ...)
2. Hợp chất hữu cơ được chia thành hidrocacbon và dẫn xuất hidrocacbon.
3. Liên kết hóa học trong phân tử hợp chất hữu cơ thường là liên kết cộng hóa trị.
4. Các loại công thức biểu diễn công thức hợp chất hữu cơ.
5. Các loại phản ứng hay gặp trong hóa học hữu cơ là phản ứng thế, phản ứng cộng, phản ứng tách.
6. Đồng đẳng, đồng phân
| Công thức phân tử | Công thức cấu tạo | Tính chất | |
| Chất đồng đẳng | Khác nhau một hay nhiều nhóm -CH2 | Tương tự nhau | Tương tự nhau |
| Chất đồng phân | Giống nhau | Khác nhau | Khác nhau |
Một hợp chất hữu cơ Y khi đốt cháy thu được CO2 và H2O có số mol bằng nhau; đồng thời lượng oxi cần dùng bằng 4 lần số mol của Y. Tìm CTPT của Y biết trong Y chỉ có 1 nguyên tử oxi.
\(\begin{array}{l} {n_{C{O_2}}} = {n_{{H_2}O}} \Rightarrow CTPT:{C_x}{H_{2x}}O\\ {C_x}{H_{2x}}O + \left( {\frac{{3x - 1}}{2}} \right){O_2} \to xC{O_2} + x{H_2}O\\ {n_{{O_2}}} = 4{n_Y} \Rightarrow \frac{{3x - 1}}{2} = 4 \Rightarrow x = 3\\ CTPT:{C_3}{H_6}O \end{array}\)
Đốt cháy hoàn toàn một hợp chất hữu cơ chứa C, H, Cl sinh ra 0,22g CO2 và 0,09g H2O. Khi xác định clo trong lượng chất đó bằng dd AgNO3, người ta thu được 1,435 g AgCl. Xác định CTPT của hợp chất hữu cơ nói trên biết tỉ khối hơi của nó so với hydro bằng 42,5
\(\begin{array}{l} {n_{C{O_2}}} = 0,005{\rm{ }}mol;{n_{{H_2}O}} = 0,005{\rm{ }}mol;{n_{Cl}} = {n_{AgCl}} = 0,01{\rm{ }}mol\\ \Rightarrow {n_C} = 0,005{\rm{ }}mol;{n_H} = 2.0,005 = 0,01{\rm{ }}mol\\ C:H:Cl = {n_C}:{n_H}:{n_{Cl}} = 0,005:0,01:0,01 = 1:2:2\\ CTPT:{(C{H_2}C{l_2})_n}\\ {d_{HC/{H_2}}} = 42,5 \Rightarrow {M_A} = 42,5.2 = 85\\ \Rightarrow 85n = 85 \Leftrightarrow n = 1 \Rightarrow CTPT:{\rm{ C}}{{\rm{H}}_2}C{l_2} \end{array}\)
Đốt cháy hoàn toàn 18g chất hữu cơ A cần vừa đủ 16,8 lít O2 thu được CO2 và hơi nước có tỷ lệ thể tích = 3: 2. Xác định CTPT của A, biết số nguyên tử oxi trong A không vượt quá 2?
\(\begin{array}{l} {n_{{O_2}}} = 0,75mol\\ \left\{ \begin{array}{l} C{O_2}(a{\rm{ }}mol)\\ {H_2}O{\rm{ }}(b{\rm{ }}mol) \end{array} \right.\\ \frac{a}{b} = \frac{3}{2} \Leftrightarrow 2a - 3b = 0{\rm{ }}(1)\\ {m_{C{O_2}}} + {m_{{H_2}O}} = {m_A} + {m_{{O_2}}}\\ \Leftrightarrow 44a + 18b = 18 + 0,75.32 = 42{\rm{ }}(2)\\ \left\{ \begin{array}{l} a = 0,75{\rm{ }}mol\\ b = 0,5{\rm{ }}mol \end{array} \right. \end{array}\)
\(\begin{array}{l} \Rightarrow {n_C} = {n_{C{O_2}}} = 0,75mol;{\rm{ }}{{\rm{n}}_H} = 2{n_{{H_2}O}} = 2.0,5 = 1{\rm{ }}mol\\ {n_{O(A)}} = ({n_{O(C{O_2})}} + {n_O}_{({H_2}O)}) - {n_{O({O_2})}}\\ \Rightarrow {n_{O(A)}} = (2.{n_{C{O_2}}} + {n_{{H_2}O}}) - 2{n_{{O_2}}}\\ \Leftrightarrow {n_{O(A)}} = 0,5{\rm{ }}mol\\ C{\rm{ }}:{\rm{ }}H{\rm{ }}:{\rm{ }}O{\rm{ }} = {\rm{ }}{n_C}:{\rm{ }}{n_H}:{\rm{ }}{n_O} = {\rm{ }}0,75{\rm{ }}:{\rm{ }}1{\rm{ }}:{\rm{ }}0,5{\rm{ }} = {\rm{ }}1,5{\rm{ }}:{\rm{ }}2{\rm{ }}:{\rm{ }}1 = {\rm{ }}3{\rm{ }}:{\rm{ }}4{\rm{ }}:{\rm{ }}2\\ \Rightarrow CTPT:{\rm{ }}{\left( {{C_3}{H_4}{O_2}} \right)_n} \end{array}\)
So số nguyên tử oxi không vượt quá 2 nên n = 1 ⇒ CTPT là: C3H4O2
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 24có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Chất có CTPT C6H10O4. Công thức nào sau đây là công thức đơn giản nhất:
Đốt cháy hoàn toàn hợp chất hữu cơ nào sau đây thì sản phẩm thu được khác với các chất còn lại?
Cho thí nghiệm như hình vẽ để phân tích hợp chất hữu cơ. Hãy cho biết thí nghiệm trên dùng để xác định nguyên tố nào:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 24.
Bài tập 1 trang 107 SGK Hóa học 11
Bài tập 2 trang 107 SGK Hóa học 11
Bài tập 3 trang 107 SGK Hóa học 11
Bài tập 4 trang 107 SGK Hóa học 11
Bài tập 5 trang 107 SGK Hóa học 11
Bài tập 6 trang 107 SGK Hóa học 11
Bài tập 7 trang 107 SGK Hóa học 11
Bài tập 8 trang 107 SGK Hóa học 11
Bài tập 24.1 trang 34 SBT Hóa học 11
Bài tập 24.2 trang 35 SBT Hóa học 11
Bài tập 24.3 trang 35 SBT Hóa học 11
Bài tập 24.4 trang 35 SBT Hóa học 11
Bài tập 24.5 trang 35 SBT Hóa học 11
Bài tập 24.6 trang 36 SBT Hóa học 11
Bài tập 24.7 trang 36 SBT Hóa học 11
Bài tập 24.8 trang 36 SBT Hóa học 11
Bài tập 1 trang 121 SGK Hóa học 11 nâng cao
Bài tập 2 trang 121 SGK Hóa học 11 nâng cao
Bài tập 3 trang 121 SGK Hóa học 11 nâng cao
Bài tập 4 trang 121 SGK Hóa học 11 nâng cao
Bài tập 5 trang 121 SGK Hóa học 11 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Chất có CTPT C6H10O4. Công thức nào sau đây là công thức đơn giản nhất:
Đốt cháy hoàn toàn hợp chất hữu cơ nào sau đây thì sản phẩm thu được khác với các chất còn lại?
Cho thí nghiệm như hình vẽ để phân tích hợp chất hữu cơ. Hãy cho biết thí nghiệm trên dùng để xác định nguyên tố nào:
Trong những dãy chất sau, dãy nào có các chất là đồng phân của nhau:
Đốt cháy hoàn toàn 6 gam hợp chất A thu được 8,8 gam CO2 và 3,6 gam H2O.Tìm công thức thực nghiệm của A.
Công thức phân tử của metylơgenol là?
Chất X có công thức phân tử C6H10O4. Công thức nào sau đây là công thức đơn giản nhất của X ?
Số công thức cấu tạo có thể có ứng với các công thức phân tử C2H7N là
Lycopen có công thức phân tử C40H56, là chất màu đỏ trong quả cà chua, có cấu tạo mạch hở, chỉ chứa liên kết đôi và liên kết đơn trong phân tử. Số kết đôi đó có trong phân tử licopen là
Đốt cháy hoàn toàn 8,9 gam hợp chất hữu cơ X, thu được 6,73 lít CO2 (đktc) ; 1,12 lít N2 (đktc) và 6,3 gam H2O. biết X có công thức phân tử trùng với công thức đơn giản nhất . Công thức phân tử của X là
Chất nào sau đây là hiđrocacbon? Là dẫn xuất của hiđrocacbon?
a) CH2O
b)C2H5Br
c) CH2O2
d) C6H5Br
e) C6H6
g) CH3COOH.
Từ ơogenol (trong tinh dầu hương nhu) điều chế được metylơgenol (M = 178 g/mol) là chất dẫn dụ côn trùng. Kết quả phân tích nguyên tố của metylơgenol cho thấy: %C = 74,16%; %H = 7,86%, còn lại là oxi.
Lập công thức đơn giản nhất, công thức phân tử của metylơgenol.
Viết công thức cấu tạo của các chất có công thức phân tử sau: CH2Cl2 (một chất), C2H4O2 (ba chất), C2H4Cl2 (hai chất)?
Chất X có công thức phân tử C6H10O4. Công thức nào sau đây là công thức đơn giản nhất của X?
A. C3H5O2
B. C6H10O4
C. C3H10O2
D. C12H20O8
Hãy viết công thức cấu tạo có thể có của các đồng đẳng của ancol etylic có công thức phân tử C3H8O và C4H10O.
Cho các chất sau: C3H7-OH, C4H9-OH, CH3-O-C2H5, C2H5-O-C2H5. Những cặp chất nào có thể là đồng đẳng hoặc đổng phân của nhau?
Các phản ứng sau đây thuộc loại phản ứng nào (phản ứng thế, phản ứng cộng, phản ứng tách)?
a) C2H6 + Cl2 → C2H5Cl + HCl
b) C4H8 + H2O → C4H10O
c) C2H5Cl → C2H4 + HCl
d) 2C2H5OH → C2H5OC2H5 + H2O
Viết phương trình hoá học của các phản ứng xảy ra trong các trường hợp sau và cho biết các phản ứng đó thuộc loại phản ứng nào (phản ứng thế, phản ứng cộng, phản ứng tách).
a) Etilen tác dụng với hiđro có Ni làm xúc tác và đun nóng.
b) Đun nóng axetilen ở 600°C với bột than làm xúc tác thu được benzen.
c) Dung dịch ancol etylic để lâu ngoài không khí chuyển thành dung dịch axit axetic (giấm ăn).
Cho dãy chất: CH4; C6H6; C6H5-OH; C2H5ZnI; C2H5PH2. Nhận xét nào đưới đây đúng ?
A. Các chất trong dãy đều là hiđrocacbon.
B. Các chất trong dãy đều là dẫn xuất của hiđrocacbon.
C. Các chất trong dãy đều là hợp chất hữu cơ.
D. Trong dãy có cả chất vô cơ và hữu cơ nhưng đều là hợp chất của cacbon.
Người ta lần lượt lấy mẫu thử của một trong bốn chất X, Y, Z, T và làm thí nghiệm như sau : Cho mẫu thử qua CuO đốt nóng (để đốt cháy hoàn toàn) rồi dẫn sản phẩm cháy qua CuSO4 khan sau đó qua dung dịch Ca(OH)2. Kết quả thí nghiệm cho thấy, mẫu X chỉ làm cho CuSO4 chuyển qua màu xanh, mẫu Y chỉ tạo kết tủa trắng ở bình chứa nước vôi, mẫu Z tạo hiện tượng như trên ở cả hai bình; còn mẫu T không tạo hiện tượng gì.
Kết luận nào đúng cho các thí nghiệm này là :
A. X chỉ chứa nguyên tố hiđro.
B. Y chỉ chứa nguyên tố cacbon
C. Z là một hiđrocacbon.
D. T là chất vô cơ.
Trong số các chất sau đây, chất nào là đồng đẳng của
A. HCOO-CH3
B. CH3-COO-CH3
C. HO-CO-CH2-CH3
D. H-COO-CH2-CH3
Phenol có công thức cấu tạo là 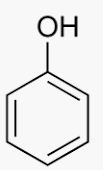
Trong các chất dưới đây, chất nào không là đồng đẳng của phenol?
A. 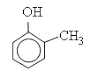
B. 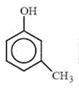
C. 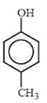
D. 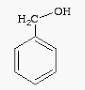
Trong số các chất dưới đây, chất nào không là đồng phân của
A. CH3-COO-CH3
B. H-COO-CH2-CH3
C. H-CO-CH2-CH2-OH
D. H-COO-CH2-CH2-CH3
1. Trong số các chất hữu cơ đã được học ở lớp 9, hãy kể ra 2 cặp chất có công thức phân tử khác nhau nhưng có cùng công thức đơn giản nhất.
2. Viết công thức cấu tạo của 2 chất có cùng công thức phân tử C4H10 và của 2 chất có cùng công thức phân tử C2H6O.
Hợp chất hữu cơ A có thành phần khối lượng của các nguyên tố như sau: C chiếm 24,24%; H chiếm 4,04%; Cl chiếm 71,72%.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A biết rằng tỉ khối hơi của A đối với CO2 là 2,25.
3. Dựa vào thuyết cấu tạo hoá học, hãy viết các công thức cấu tạo mà chất A có thể có ở dạng khai triển và dạng thu gọn.
Hỗn hợp M chứa hai chất hữu cơ thuộc cùng dãy đồng đẳng và hơn kém nhau 2 nguyên tử cacbon. Nếu làm bay hơi 7,28 g M thì thể tích hơi thu được đúng bằng thể tích của 2,94 g khí N2 ở cùng điều kiện. Để đốt cháy hoàn toàn 5,20 g hỗn hợp M cần dùng vừa hết 5,04 lít O2 (đktc). Sản phẩm cháy chỉ gồm CO2 và hơi nước với thể tích bằng nhau.
Hãy xác định công thức phân tử và phần trăm khối lượng từng chất trong hỗn hợp M.
Hãy điền từ ngữ thích hợp vào chỗ trống trong các câu sau:
a) Chưng cất dựa trên sự khác nhau về thành phần của hỗn hợp lỏng so với … tạo thành khi … hỗn hợp đó lỏng.
A. Hỗn hợp rắn
B. Hỗn hợp hơi
C. đun nóng
D. đun sôi
b) Người ta thường sử dụng Phương pháp chưng cất đối với các chất có … khác nhau. Chiết dựa vào sự khác nhau về … của các chất.
A. Độ tan
B. nhiệt độ nóng chảy
C. nhiệt độ sôi
D. thành phần
c) Người ta thường sử dụng Phương pháp chiết tách các chất lỏng … hoặc tách chất … ra khỏi chất rắn …
A. Độ tan
B. không tan
C. bay hơi
D. không trộn lẫn vào nhau
d) Tinh chế chất rắn bằng cách kết tinh trong dung môi dựa vào … theo nhiệt độ.
A. Sự thay đổi tỉ khối
B. sự kết tinh
C. sự thăng hoa
D. sự thay đổi độ tan.
Hãy thiết lập công thức phân tử của các hợp chất A và B ứng với các số liệu thực nghiệm sau (không ghi %O).
a) C: 49,40%; H: 9,8%; N:19,10%; dA/kk = 2,52
b) C: 54,54%; H: 9,09%; dB/CO2 = 2,00
Một hợp chất A chứa 54,8%C; 4,8%H, 9,3%N còn lại là O cho biết phân tử khối của nó là 153. Xác định công thức phân tử của hợp chất. vì sao phân tử khối của các hợp chất chứa C, H, O là số chẵn mà phân tử khối của A là lại là số lẻ (không kể phần thập phân)?
Phân tích nguyên tố một hợp chất hữu cơ A cho kết quả: 7097%, 10,15%H còn lại là O. Cho biết khối lượng mol phân tử của A là 340 g/mol. Xác định công thức phân tử của A. Hãy giải thích bài trên bằng hai cách dưới đây rút ra kết luận.
a) Qua công thức đơn giản nhất
b) Không qua công thức đơn giản nhất.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Đốt cháy hoàn toàn 0,6 gam một HCHC A. Cho sản phẩm cháy lần lượt qua bình đựng dd axit H2SO4 đặc (1) và bình đựng dung dịch axit Ca(OH)2 dư (2), thấy bình 1 tăng 0,81 gam, bình 2 có 3 gam kết tủa. Xác định công thức phân tử của A, biết thể tích hơi của 0,6 gam A bằng thể tích hơi của 0,48 gam oxi ở cùng điều kiện nhiệt độ và áp suất.
Câu trả lời của bạn
thể tích của 0,6 gam A = thể tích của 0,48 gam O2 ở cùng điều kiện
⇒ nA = n0,48 gam O2 = 0,48/32 = 0,015 mol
bình 1: cho qua H2SO4 đặc thì vì H2SO4 đặc háo nước nên nước bị giữ lại
⇒ mH2O = 0,81 gam ⇒ nH2O = 0,81/18 = 0,045 mol
⇒ nH = 2nH2O = 0,09 mol
bình 2: nCaCO3 = 3/100= 0,03 mol
⇒nC=nCO2 = nCaCO3 = 0,03 mol
vì sản phẩm cháy là CO2 và H2O nên trong A có C, H và có thể có O
mC + mH = 0,03.12 + 0,09.1 = 0,45 < mA =0,6 ⇒ trong A có O
mO = mA - (mC + mH)= 0,15 g
cách giải là vậy nhưng hình như đề sai nên nO tính không a kết quả đẹp cho lắm
phân tích hợp chất hửu cơ x thu được kết quả % của cacbon =40% phần trăm của hidro =6,67% còn lại là oxi.lập công thức đơn giản nhất cua ct hửu cơ
Câu trả lời của bạn
câu này dễ mà bạn, mk chỉ bạn cách làm nhé
-trc hết bạn tính cho mk %O2
-rồi dựa vào công thức %C/16 : %H/1 : %O/16
( ":" là dấu chia đấy nhá!!!)
-rút gọn đến số tối thiểu đó chính là CTDGN của nó đấy
Cho 5cm^3 CxHy ở thể khí với 30cm^3 O2 lấy dư vào khí nhiên kế .Sau khi bật tia lữa điện và làm lạnh, trong khí nhiên kế còn 20cm^3 mà 15cm^3 bị hấp thụ bởi KOH .Phần còn lại bị hấp thu bởi photpho.Lập công thức của hidrocacbon
(mình yếu hóa lăm mong các bạn trả lời nahnh giùm mình nha ,gấp lm ạ!)
Câu trả lời của bạn
..............CxHy + (x + y/4)O2 ---> x CO2 + y/2 H2O
ban đầu: 5------------------30
Pư:.........5-----------------5(x+y/4)
Sau Pư: 0 ----------30 - 5(x+y/4)--------5x --------5y/2
Ta có: KOH chỉ hấp thụ CO2 => 5x = 15 => x = 3.
Phần còn lại: 30 - 5(x+y/4) + 5y/2 = 20 - 15 => y = ...
Ai cho mình cách xác định công thức hóa học hộ đi.. Mình cần gấp lắm, cảm ơn trước nhé. ![]()
Câu trả lời của bạn
- Đặt CTDC
- Dựa theo dữ liệu đề cho tìm CTTN
- Biện luận suy ra CTPT
Phân tích 0,29 gam một hợp chất hữu cơ chỉ chứa C, H, O ta có %C = 62,06%; %H = 10,34%. Vậy khối lượng oxi trong hợp chất là:
Câu trả lời của bạn
Câu trả lời của bạn
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai hiđrocacbon thuộc cùng dãy đồng đẳng cần dùng V lít O2 và thu được 11.2 lít CO2 và 12.6 g H2O. Tính giá trị của m và V. Mọi người giúp em vs ạ
Câu trả lời của bạn
nCO2 = 0,5 (mol)
nH2O = 0,7 (mol)
Bảo toàn oxi suy ra nO2 = 0,85 (mol) ➝ 19,04 (l)
Đốt cháy hoàn toàn 3,99 gam chất hữu cơ X phải dùng vừa đủ 5,88 lít khí o2 (đktc). Sản phẩm cháy chỉ có co2 và h2o theo tỉ lệ
44: 15 về khối lượng. Tỉ khối hơi của X đối với O2 là 3,5625, công thức phân tử của X là
A. C6H12O2
B. C6H10O
C. C6H10O2
D. C5H10O2
Câu trả lời của bạn
8 CAU TREN HOI BAT LUC VOI MINH MONG CAC BAN GIUP
Nhớ hậu tạ nhá.
Bữa nào điểm kiểm tra cao nhớ khoe nha. Tụi mình sẽ rất vui vì điều đó. ^^
Bài này nhanh nhất là thông qua tỉ khối có M = 0,5625. 32 = 114 và kết luận đáp án C.
GIÚP MÌNH VỚI!!!!!!!!!,NHỚ GIẢI CHI TIẾT NHA Á HÍ HI
Đốt cháy 0.01 mol hợp chất hữu cơ A thu được sản phẩm cháy gồm khí cacbonic và hơi nước. Cho toàn bộ sản phẩm hấp thụ hoàn toàn vào bình đựng dung dịch Ca(OH)2 dư thì thấy thu được 10 gam kết tủa và khối lượng bình đựng dung dịch tăng thêm là 5.3 gam.Số mol CO2 so với số mol hợp chất A là:
A.2 b.3 c.4 d.5
Câu trả lời của bạn
Đề này có bị làm sao không vậy? Cho khối lượng kết tủa là CaCO3 có số mol kết tủa bằng số mol của CO2. Có Số mol hợp chất nữa thì hỏi làm cái gì nhỉ?
Mong quý Thầy cô giúp đỡ ạ.
Đốt cháy hoàn toàn 29,2 gam hỗn hợp X gồm andehit acrylic, metyl axetat, andehit axetic và etylen glicol thu được 1,15 mol CO2 và 23,4 gam H2O. Mặt khác, khi cho 36,5 gam hỗn hợp X trên tác dụng hết với dung dịch AgNO3 trong NH3 thì thu được tối đa m gam Ag. Giá trị gần nhất của m là
A. 43,5 B. 64,8 C. 53,9 D. 81,9
Câu trả lời của bạn
- Trong 29,2 (g) X chứa 0,2 mol CH3CHO và C2H3CHO vậy trong 36,5 (g) X chứa 0,25 mol CH3CHO và C2H3CHO.
- Cho 36,5 (g) X tác dụng với AgNO3 thì
\({n_{Ag}} = 2({n_{{C_2}{H_3}CHO}} + {n_{C{H_3}CHO}}) = 2{n_{{C_{\bar x}}{H_4}O}} = 0,5 \Rightarrow {m_{Ag}} = 54gam\)
Cho 5cm^3 CxHy ở thể khí với 30cm^3 O2 lấy dư vào khí nhiên kế .Sau khi bật tia lữa điện và làm lạnh, trong khí nhiên kế còn 20cm^3 mà 15cm^3 bị hấp thụ bởi KOH .Phần còn lại bị hấp thu bởi photpho.Lập công thức của hidrocacbon
(mình yếu hóa lăm mong các bạn trả lời nahnh giùm mình nha ,gấp lm ạ!)
Câu trả lời của bạn
ủa? Câu này Anh tỉ tỉ giải cho bạn rồi mà.
Đây này: https://dapanhay.com/hoi-dap/hoa-hoc-11/dai-cuong-ve-hoa-hoc-huu-co-dang-lap-cong-thuc-phan-tu-faq24143.html
1. Viết tất cả các đồng phân cis- và trans- của các chất có công thức phân tử là C3H4BrCl và các chất có công thức cấu tạo :R-CH=CH-CH=CH-R,
2.Thêm NH3dư vào dung dịch có 0.5 mol AgNO3 ta được dung dịch A. Cho từ từ 3 gam khí X vào A đến phản ứng hoàn toàn dược dung dịch B và chất rắn C . Thêm từ từ HI đến dư vào B thu được 23.5 gam kết tuarvangf và V lít khí Y ở đktc thoát ra . Biện luận để tìm X ,khối lượng chât rắn C và thể tích khí Y
3. Từ meetan điều chế xiclobutan
Câu trả lời của bạn
+ Vì X pư với AgNO3/NH3 có chất rắn C nên X là anđehit hoặc ank-1-in hoặc HCOOH. Nếu là ank-1-in thì khi cho HI vào B không có khí thoát ra ð X là anđehit hoặc HCOOH
+ Khi cho HI vào B thì ta có:
Ag+ + I- → AgI
Vì số nAgI = \(\frac{{23,5}}{{235}}\) =0,1 mol ⇒ số mol Ag+ còn lại trong B là 0,1 mol; vì có khí thoát ra nên phải có \(CO_3^{2 - }\). Do đó số mol Ag+ pư với khí X là 0,4 mol
⇒ số mol X là 0,2 mol (HCOOH) hoặc 0,1 mol (HCHO)
ð MX tương ứng là 15 đvC (3/0,2); 30 đvC (3/0,1). Ta thấy chỉ có HCHO phù hợp.
HCHO (NH4)2CO3 + 4Ag
0,1 0,1 0,4
\(CO_3^{2 - }\) + 2H+ → H2O + CO2↑
0,1 0,1
+ Khối lượng của C= mAg = 43,2 gam;
thể tích Y = 2,24 lít.
Metan → axetilen; metan → metanal sau đó:
2HCHO + CH CH → HO-CH2-C
CH → HO-CH2-C C-CH2-OH →HO-CH2- CH2-CH2-CH2-OH
C-CH2-OH →HO-CH2- CH2-CH2-CH2-OH
Cl-CH2- CH2-CH2-CH2-Cl
Câu 1:
có 4 loại đp là:
cis-cis; trans-trans; cis-trans; trans-cis có công thức cấu tạo: R-CH=CH-CH=CH-R’.
Hỗn hợp C2H2, C2H4, CH3-CH=CH2, C3H4. Đốt 6,1 gam hỗn hợp X bằng một lượng không khí vừa đủ thu được hỗn hợp khí và hơi Y gồm CO2, H2O và N2 trong đó CO2 chiếm 13,636% thể tích (giả sử không khí gồm 20% O2 và 80% N2 về thể tích). Hiđro hoá hoàn toàn 6,1 gam hỗn hợp X cần 6,272 lít khí H2 (đktc). Cho 0,54 mol hỗn hợp X có thể làm mất màu tối đa bao nhiêu gam Brom?
A. 137,6
B. 134,4
C. 132,8
D. 129,6
Câu trả lời của bạn
20.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol, thu được 13,44 lít khí CO2 (đktc) và 15,4 gam nước. Mặt khác cho m gam X tác
dụng với Na (dư) thu được 4,48 (lit) khí H2 (đktc). Giá trị của m là
A. 12,9
B. 15,3
C. 12,3
D. 16,9
Câu trả lời của bạn
mấy câu này mình làm thường sai đè nhiều lám.
Bạn có đó không? Kiểm tra lại giùm mình số liệu của nước. Vì đề đốt cháy không thể cho số mol lẻ kinh dị như vậy dc. Xem giùm mình nha.
Đề này phải là 15,3 ak bạn. Mình giải luôn như này:
Gọi công thức của 2 ancol là R(OH)a.
Bảo toàn nguyên tố H:
nH2=0,2 mol =>nOH = 0,4 mol.
=>mO trong ancol là 0,4*16 = 6,4 gam
Ta có:
nCO2= 0,6 ⇒ mC trong ancol là 0,6*12 = 7,2 gam
nH2O= 0,85 ⇒ mH trong ancol là 0,85*2=1,7 gam
Vậy m = 7,2+1,7+6,4 =15,3 gam
Đáp án B 
ĐỀ THI HÓA 12
Câu trả lời của bạn
đây bạn hình ảnh đầy đủ

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *