Nội dung bài giảng Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hóa học giúp học sinh hệ thống hoá lại các kiến thức trong chương như: tính chất của phi kim, tính chất của clo,C, Si, CO, CO2, H2CO3, muối cacbonat. Cấu tạo bảng tuần hoàn và sự biến đổi tuần hoàn tính chất của các nguyên tố trong chu kì, nhóm và ý nghĩa của bảng tuần hoàn.
Hình 1: Tính chất hóa học của phi kim
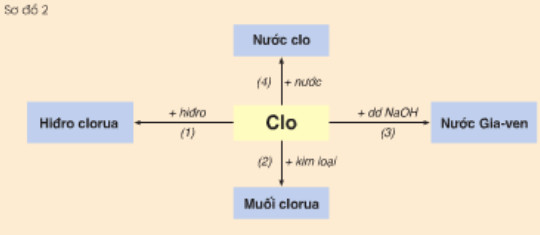
Hình 2: Tính chất hóa học của Clo
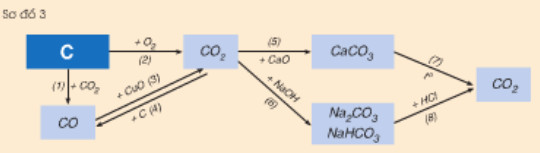
Hình 3: Tính chất hóa học của Cacbon và hợp chất của Cacbon
Trong một nhóm đi từ trên xuống tính kim loại của các nguyên tố tăng dần, tính phi kim của các nguyên tố giảm dần.
Biết cấu tạo nguyên tử → vị trí và tính chất của nguyên tố.
Hình 4: Ý nghĩa của Bảng tuần hoàn
Sau bài học cần nắm:
Tính chất hóa học của phi kim
Bảng tuần hoàn các nguyên tố hóa học
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 32có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Sản phẩm của phản ứng khi đốt cháy hoàn toàn lần lượt lưu huỳnh, hiđro, cacbon, photpho, trong khí oxi dư là:
Cho sơ đồ biến đổi sau: Phi kim → Oxit axit (1) → Oxit axit (2) → Axit
Dãy chất phù hợp với sơ đồ trên là:
Sục khí clo vào dung dịch KOH ở nhiệt độ thường, sản phẩm của phản ứng gồm:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 32.
Bài tập 1 trang 103 SGK Hóa học 9
Bài tập 2 trang 103 SGK Hóa học 9
Bài tập 3 trang 103 SGK Hóa học 9
Bài tập 4 trang 103 SGK Hóa học 9
Bài tập 5 trang 103 SGK Hóa học 9
Bài tập 6 trang 103 SGK Hóa học 9
Bài tập 32.1 trang 40 SBT Hóa học 9
Bài tập 32.2 trang 40 SBT Hóa học 9
Bài tập 32.3 trang 40 SBT Hóa học 9
Bài tập 32.4 trang 40 SBT Hóa học 9
Bài tập 32.5 trang 41 SBT Hóa học 9
Bài tập 32.6 trang 41 SBT Hóa học 9
Bài tập 32.7 trang 41 SBT Hóa học 9
Bài tập 32.8 trang 41 SBT Hóa học 9
Bài tập 32.9 trang 41 SBT Hóa học 9
Bài tập 32.10 trang 41 SBT Hóa học 9
Bài tập 32.11 trang 41 SBT Hóa học 9
Bài tập 32.12 trang 41 SBT Hóa học 9
Bài tập 32.13 trang 42 SBT Hóa học 9
Bài tập 32.14 trang 42 SBT Hóa học 9
Bài tập 32.15 trang 42 SBT Hóa học 9
Bài tập 32.16 trang 42 SBT Hóa học 9
Bài tập 32.17 trang 42 SBT Hóa học 9
Bài tập 32.18 trang 42 SBT Hóa học 9
Bài tập 32.19 trang 42 SBT Hóa học 9
Bài tập 32.20 trang 42 SBT Hóa học 9
Bài tập 32.21 trang 42 SBT Hóa học 9
Bài tập 32.22 trang 42 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Sản phẩm của phản ứng khi đốt cháy hoàn toàn lần lượt lưu huỳnh, hiđro, cacbon, photpho, trong khí oxi dư là:
Cho sơ đồ biến đổi sau: Phi kim → Oxit axit (1) → Oxit axit (2) → Axit
Dãy chất phù hợp với sơ đồ trên là:
Sục khí clo vào dung dịch KOH ở nhiệt độ thường, sản phẩm của phản ứng gồm:
Để chứng minh sự có mặt của khí CO và CO2 trong hỗn hợp, người ta dẫn hỗn hợp khí qua (1), sau đó dẫn khí còn lại qua (2) thấy có kết tủa màu đỏ xuất hiện. Hoá chất đem sử dụng ở (1), (2) lần lượt là:
Hàng năm, thế giới cần tiêu thụ khoảng 46 triệu tấn clo. Nếu lượng clo chỉ được điều chế từ muối ăn NaCl thì cần ít nhất bao nhiêu tấn muối?
Những chai, lọ bằng thủy tinh không được đựng dung dịch axit nào sau đây?
Chất dung để làm khô khí Cl2 ẩm là
Nguyên tố A có số hiệu nguyên tử là 11, chu kì 3, nhóm I trong bảng hệ thống tuần hoàn. A là:
Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32g oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4g chất rắn.
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của NaCl trong dung dịch A
Căn cứ vào sơ đồ sau:

Hãy viết phương trình hóa học với phi kim cụ thể là lưu huỳnh.
Hãy viết các phương trình hóa học biểu diễn tính chất hóa học của clo theo sơ đồ sau:
Hãy viết các phương trình hóa học biểu diễn tính chất hóa học của cacbon và một số hợp chất của nó theo sơ đồ sau:
Nguyên tố A có số hiệu nguyên tử là 11, chu kì 3, nhóm I trong bảng hệ thống tuần hoàn. Hãy cho biết:
- Cấu tạo nguyên tử của A.
- Tính chất hóa học đặc trưng của A.
- So sánh tính chất hóa học của A với các nguyên tố lân cận.
a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32g oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4g chất rắn.
b) Chất khí sinh ra được hấp thụ hoàn toàn trong dung dịch nước vôi trong có dư. Tính khối lượng kết tủa thu được.
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể?
Ngâm hỗn hợp các kim loại Al, Cu, Fe trong mỗi dung dịch sau :
a) Dung dịch CuSO4 (dư).
b) Dung dịch AgNO3 (dư).
c) Dung dịch FeSO4 (dư).
Viết các phương trình hoá học. Kim loại nào thu được trong mỗi trường hợp ?
Khi cho khí clo tác dụng với kim loại, em có nhận xét gì về mức độ hoạt động hoá học của nguyên tố clo. Cho thí dụ minh hoạ.
Có bốn mẫu khí A, B, C, D đựng riêng biệt trong các bình thủy tinh. Mỗi khí có một số tính chất trong các tính chất sau:
A. Cháy trong không khí tạo ra chất lỏng không màu (ở nhiệt độ thường), chất lỏng này làm cho đồng(II) sunfat khan màu trắng chuyển thành màu xanh.
B. Độc, cháy với ngọn lửa màu xanh, sinh ra chất khí làm đục nước vôi trong.
C. Không cháy nhưng làm cho ngọn lửa cháy sáng chói hơn.
D. Không cháy mà còn làm tắt ngọn lửa và làm quỳ tím ẩm hoá đỏ.
Khí nào nói trên là: hiđro, oxi , cacbon đioxit, cacbon oxit ?
Cặp nguyên tố nào sau đây dễ kết hợp với nhau để tạo thành một hợp chất ổn định ?
a) Zn, Ne
b) H, S
c) Br, Be
d) O, Na
e) K, Kr
Có 4 lá kim loại: sắt, đồng, nhôm, bạc. Làm thế nào để có thể nhận biết được mỗi kim loại bằng phương pháp hoá học. Viết các phương trình hoá học.
Trong phòng thí nghiệm có 3 lọ mất nhãn đựng ba chất bột trắng là: BaC03, NaCl, Na2C03. Làm thế nào để nhận ra hoá chất trong mỗi lọ với điều kiện chỉ dùng thêm dung dịch HCl loãng ?
Hình vẽ 3.5 là thiết bị điều chế khí clo trong phòng thí nghiệm.
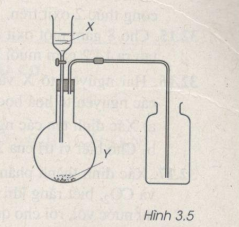
a) X và Y là những chất nào trong số các chất sau ?
X : H2O, dd HCl, dd H2SO4, dd NaOH, dd NaCl.
Y : NaCl, CaCO3, MnO2, CuCl2, Na2SO4, KMnO4.
b) Viết phương trình hoá học điều chế khí clo từ những chất đã chọn ở trên.
Một nguyên tố X tạo được các hợp chất sau: XH3, X205. Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố X cùng nhóm với
A. agon
B. nitơ
C. oxi
D. flo
Cho kim loại Al có dư vào 400 ml dung dịch HCl 1M. Dẫn khí tạo ra qua ống đựng CuO dư, nung nóng thì thu được 11,52 gam Cu. Tính hiệu suất của quá trình phản ứng.
Nung hỗn hợp CaCO3 và MgCO3 thu được 76 gam hai oxit và 33,6 lít CO2 (đktc). Tính khối lượng của hỗn hợp ban đầu.
Có hai lá kẽm khối lượng như nhau. Một lá cho vào dung dịch đồng(II) nitrat, lá kia cho vào dung dịch chì(II) nitrat. Sau cùng một thời gian phản ứng, khối lượng lá kẽm thứ nhất giảm 0,05 gam.
a) Viết các phương trình hoá học.
b) Khối lượng lá kẽm thứ 2 tăng hay giảm là bao nhiêu gam ? Biết rằng trong cả 2 phản ứng trên, khối lượng kẽm bị hoà tan bằng nhau.
Cho hỗn hợp 2 kim loại Fe và Cu tác dụng với khí clo dư thu được 59,5 gam hỗn hợp muối. Cũng lượng hỗn hợp trên cho tác dụng với lượng dư dung dịch HCl 10% thu được 25,4 gam một muối.
a) Tính phần trăm khối lượng mỗi muối trong hỗn hợp muối thu được.
b) Tính thể tích dung dịch HCl 10% (D = 1,0 g/ml) cần dùng.
Cho 23,6 gam hỗn hợp gồm Mg, Fe, Cu tác dụng vừa hết với 91,25 gam dung dịch HCl 20% thu được dung dịch A và 12,8 gam chất không tan.
Tính khối lượng các kim loại trong hỗn hợp ban đầu.
Nguyên tố A tạo được 2 loại oxit. Phần trăm về khối lượng của oxi trong 2 oxit lần lượt bằng 50% và 60%. Xác định nguyên tử khối của A và cho biết công thức 2 oxit trên.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Chiều tăng dần tính phi kim: cacbon, oxi, flo.
Câu trả lời của bạn
Chiều giảm dần tính kim loại: natri, magie, nhôm.
Câu trả lời của bạn
Nguyên tố franxi có tính kim loại mạnh nhất.
Nguyên tố flo có tính phi kim mạnh nhất.
Câu trả lời của bạn
Thứ tự tăng dần tính phi kim: silic, cacbon, nito, oxi.
Câu trả lời của bạn
Ô nguyên tố cho biết: số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố và nguyên tử khối của nguyên tố đó.
Câu trả lời của bạn
Nguyên tắc sắp xếp các nguyên tố trong một chu kì:những nguyên tố có cùng số lớp electron và được sắp xếp theo chiều điện tích hạt nhân tăng dần
Câu trả lời của bạn
Các nguyên tố nhóm I có 1 electron lớp ngoài cùng gồm: hidro, liti, natri, kali, rubidi, xesi, franxi.
Các nguyên tố nhóm II có 2 electron lớp ngoài cùng gồm: beri, magie, canxi, stronti, bari, radi.
Các nguyên tố nhóm VII có 7 electron lớp ngoài cùng gồm: flo, clo, brom, iot, poloni.
Câu trả lời của bạn
Các nguyên tố neon, agon thuộc nguyên tố khí hiếm.
Câu trả lời của bạn
Số hiệu nguyên tử (kí hiệu là Z) có số trị bằng số đơn vị điện tích nguyên tử (bằng số proton và bằng số electron trong nguyên tử) và là số thứ tự của nguyên tố trong bảng tuần hoàn.
Câu trả lời của bạn
Bảng tuần hoàn được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử
Các nguyên tố có cấu hình electron lớp ngoài cùng bằng nhau xếp thành 1 cột (nhóm)
Các nguyên tố có số lớp electron bằng nhau xếp thành 1 hàng (chu kì).
Câu trả lời của bạn
- Cho Y tan hoàn toàn trong dung dịch gồm KNO3 và H2SO4 (loãng), thu hỗn hợp hai khí có M = 16 (trong đó có một khí hóa nâu trong không khí) → Hai khí đó là NO và H2
- Do Y phản ứng với {KNO3, H2SO4 loãng} thu được NO
⟹ Y chứa hợp chất có Fe chưa đạt số oxi hóa +3
⟹ O2 phản ứng hết ⟹ Khí Z gồm CO2 và NO2
- Do phản ứng sinh ra H2 nên có phản ứng của Fe và H+ ⟹ NO3- phản ứng hết
Bảo toàn nguyên tố N → nNO = nKNO3 = 0,02 mol
Hỗn hợp khí NO và H2 có \(\overline M = 16\) → \(\overline M = \frac{{{m_{NO}} + {m_{H2}}}}{{{n_{NO}} + {n_{H2}}}} = \frac{{30.0,02 + 2{n_{{H_2}}}}}{{0,02 + {n_{{H_2}}}}} = 16 \to {n_{{H_2}}} = 0,02\left( {mol} \right)\)
- Đặt a, b lần lượt là số mol Fe2+, số mol Fe3+ trong muối. Đặt x là số mol O trong Y.
+ Bảo toàn điện tích dd muối → 2a + 3b + 0,02 = 0,3.2 (1)
+ Khối lượng muối sunfat → 56(a + b) + 39.0,02 + 96.0,3 = 42,46 (2)
Giải (1) (2) được a = 0,11 và b = 0,12
- Quy đổi Y thành Fe và O. Khi cho Y tác dụng {KNO3, H2SO4} thì quá trình cho - nhận e là:
Fe0 → Fe+2 + 2e O0 + 2e → O-2
Fe0 → Fe+3 + 3e N+5 + 3e → N+2
2H+ + 2e → H2
Áp dụng bảo toàn e → \(2{n_{F{{\rm{e}}^{2 + }}}} + 3{n_{F{{\rm{e}}^{3 + }}}} = 2{n_O} + 3{n_{NO}} + 2{n_{{H_2}}}\) → nO = 0,24 mol
Quy đổi X thành Fe (0,23 mol), NO3 (u mol) và CO3 (v mol)
Suy ra Z gồm NO2 (u mol) và CO2 (v mol)
Bảo toàn O → nO (Y) = u + v = 0,24 (mol) (3)
Từ \(\overline {{M_Z}} = 45\), dùng sơ đồ đường chéo suy ra u = v (4)
Giải hệ (3) và (4) ta có u = v = 0,12 (mol)
→ mX = 56.0,23 + 62.0,12 + 60.0,12 = 27,52 (g)
a) Xác định kim loại R và phần trăm theo khối lượng của Fe, R trong hỗn hợp A.
b) Cho toàn bộ dung dịch B ở trên tác dụng với V lít dung dịch NaOH 2M thì thu được kết tủa, lọc lấy kết tủa rồi nung nóng trong không khí đến khối lượng không đổi được 16,1 gam chất rắn. Biết rằng các phản ứng xảy ra hoàn toàn và toàn bộ lượng muối của Fe trong B đã phản ứng hết với NaOH. Tính giá trị của V.
Câu trả lời của bạn
a)
nHCl = 0,2.3,5 = 0,7 mol; nH2 = 0,3 mol
Nhận thấy: nH(HCl) > 2nH2 ⟹ HCl dư, KL hết
Giả sử 18,6 gam A chứa a mol Fe và b mol R
Fe + 2HCl → FeCl2 + H2
a → 2a → a
R + 2HCl → RCl2 + H2
b → 2b → b
(1) mhh = 56a + Rb = 18,6
(2) nH2 = a + b = 0,3
\(\xrightarrow{{\left( 1 \right) - 56 \times \left( 2 \right)}}\)\(\left( {R - 56} \right)b = 1,8 \to b = \frac{{1,8}}{{R - 56}}\)
Nhận thấy: 0 < b < 0,3 ⟹ \(0 < \frac{{1,8}}{{R - 56}} < 0,3 \Leftrightarrow 0,3.\left( {R - 56} \right) > 1,8 \Leftrightarrow R > 62\) (*)
- Khi cho 2,6 gam R phản ứng với 0,039 mol H2SO4:
R + H2SO4 → RSO4 + H2
Do R còn dư nên nR > nH2SO4 ⇔ \(\frac{{2,6}}{R} > 0,039 \Leftrightarrow R < 66,67\)(**)
Từ (*) (**) ⟹ R là kim loại Zn (R = 65)
Thay R = 65 vào (1) ta có \(\left\{ \begin{array}{l}56{\rm{a}} + 65b = 18,6\\a + b = 0,3\end{array} \right. \to \left\{ \begin{array}{l}a = 0,1\\b = 0,2\end{array} \right. \to \left\{ \begin{array}{l}\% {m_{F{\rm{e}}}} = \frac{{0,1.56}}{{18,6}}.100\% = 30,1\% \\\% {m_{Zn}} = 100\% - 30,1\% = 69,9\% \end{array} \right.\)
b)
Dung dịch B gồm: FeCl2 (0,1 mol); ZnCl2 (0,2 mol) và HCl dư (0,1 mol)
Theo đề bài toàn bộ muối Fe phản ứng hết với NaOH nên ta toàn Fe:
nFe2O3 = ½.nFe = 0,05 mol → mFe2O3 = 8 gam
→ mZnO = 16,1 - 8 = 8,1 gam → nZnO = 0,1 mol
*Trường hợp 1: Kết tủa Zn(OH)2 chưa bị hòa tan
HCl + NaOH → NaCl + H2O
0,1 → 0,1
FeCl2 + 2NaOH → Fe(OH)2 ↓
0,2 ← 0,1
ZnCl2 + 2NaOH → Zn(OH)2 ↓
0,2 ← 0,1
4Fe(OH)2 + O2 \(\xrightarrow{{{t^o}}}\) 2Fe2O3 + 4H2O
0,1 ← 0,05
Zn(OH)2 \(\xrightarrow{{{t^o}}}\) ZnO + H2O
0,1 ← 0,1
⟹ nNaOH = 0,1 + 0,2 + 0,2 = 0,5 mol
⟹ V = 0,25 lít
*Trường hợp 2: Kết tủa Zn(OH)2 bị hòa tan một phần
HCl + NaOH → NaCl + H2O
0,1 → 0,1
FeCl2 + 2NaOH → Fe(OH)2 ↓
0,2 ← 0,1
ZnCl2 + 2NaOH → Zn(OH)2 ↓
0,2 → 0,4 → 0,2
Zn(OH)2 + 2NaOH → Na2ZnO2 + 2H2O
(0,2-0,1) → 0,2
4Fe(OH)2 + O2 \(\xrightarrow{{{t^o}}}\) 2Fe2O3 + 4H2O
0,1 ← 0,05
Zn(OH)2 \(\xrightarrow{{{t^o}}}\) ZnO + H2O
0,1 ← 0,1
⟹ nNaOH = 0,1 + 0,2 + 0,4 + 0,2 = 0,9 mol
⟹ V = 0,45 lít
Câu trả lời của bạn
200 ml = 0,2 (lít) ⟹ nH2SO4 = VH2SO4 × CM H2SO4 = 0,2 × 1,5 = 0,3 (mol)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Theo PTHH: nNaOH = 2nH2SO4 = 2.0,3 = 0,6 (mol)
⟹ VNaOH = nNaOH : CM NaOH = 0,6 : 1,0 = 0,6 (lít) = 600 (ml)
⟹ V = 600 ml
Câu trả lời của bạn
(1) S + O2 \(\xrightarrow{{{t^o}}}\) SO2
(2) SO2 + O2 \(\xrightarrow{{xt{V_2}{O_5},{t^o}}}\) SO3
(3) SO3 + H2O → H2SO4
(4) H2SO4 + 2NaOH → Na2SO4 + 2H2O
Câu trả lời của bạn
Phần 1 + dd HCl
nhh khí(đktc) = 1,568/22,4 = 0,07 (mol); Mhh = 10×MH2 = 10.2 = 20 (g/mol)
⟹ mhh khí = n×M= 0,07.20 = 1,4 (g)
Fe(OH)3 + 3HCl → FeCl3 + 3H2O (1)
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O (2)
Fe + 2HCl → FeCl2 + H2↑ (3)
FeCO3 + 2HCl → FeCl2 + CO2↑+ H2O (4)
Hỗn hợp khí thu được gồm H2 và CO2.
Đặt \(\left\{ \begin{array}{l}{n_{{H_2}}} = a(mol)\\{n_{C{O_2}}} = b(mol)\end{array} \right. \Rightarrow \left\{ \begin{array}{l}{n_{hh}} = a + b = 0,07\\{m_{hh}} = 2a + 44b = 1,4\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a = 0,04 = {n_{{H_2}}}\\b = 0,03 = {n_{C{O_2}}}\end{array} \right.\)
Theo PTHH (3): nFe = nH2 = 0,04 (mol)
Theo PTHH (4): nFeCO3 = nCO2 = 0,03 (mol)
Phần 2:
Hỗn hợp 2 khí trong đó có SO2 ⟹ khí còn lại là CO2
nhh khí(đktc) = 2,688/22,4 = 0,12 (mol) ⟹ nSO2 = nhh - nCO2 = 0,12 – 0,03 = 0,09 (mol)
2Fe + 6H2SO4 (đặc) \(\xrightarrow{{{t^0}}}\)Fe2(SO4)3 + 3SO2 + 6H2O (5)
2FeCO3 + 4H2SO4 (đặc) \(\xrightarrow{{{t^0}}}\)Fe2(SO4)3 + SO2 + 2CO2 + 4H2O (6)
2Fe3O4 + 10H2SO4 (đặc) \(\xrightarrow{{{t^0}}}\)3Fe2(SO4)3 + SO2 + 10H2O (7)
2Fe(OH)3 + 3H2SO4 (đặc) \(\xrightarrow{{{t^0}}}\)Fe2(SO4)3 + 6H2O (8)
Vì thu được hỗn hợp muối sunfat nên có thể xảy ra phản ứng sau:
Fe + Fe2(SO4)3 → 3FeSO4 (9)
Ta có sơ đồ: X + H2SO4 (0,345 mol) → \(34,56(g)\left\{ \begin{array}{l}FeS{O_4}\\F{e_2}{(S{O_4})_3}\end{array} \right. + \left\{ \begin{array}{l}S{O_2}:0,09\,mol\\C{O_2}:0,03\,mol\end{array} \right. + {H_2}O\)
Bảo toàn nguyên tố S: nSO4(muối) = nH2SO4 – nSO2 = 0,345 – 0,09 = 0,225 (mol)
⟹ mFe(X) = mmuối sunfat – mSO4(muối) = 34,56 – 96.0,225 = 10,08 (g)
Vì 2Fe(OH)3 ⇔Fe2O3.3H2O và FeCO3 ⇔ FeO.CO2 nên nếu lược bỏ lượng CO2 (trong FeCO3) và lượng H2O (trong Fe(OH)3) ta sẽ có 2 sơ dồ như sau:
\(\left\{ \begin{array}{l}Fe:10,08\,(g)\\O:\,x(mol)\end{array} \right. + HCl \to m(g)\left\{ \begin{array}{l}FeC{l_2}\\FeC{l_3}\end{array} \right. + 0,04\,mol\,{H_2} + {H_2}O\,(1)\)
\(\left\{ \begin{array}{l}Fe:10,08\,(g)\\O:\,x(mol)\end{array} \right. + 0,345\,mol\,{H_2}S{O_4} \to \left\{ \begin{array}{l}FeS{O_4}\\F{e_2}{(S{O_4})_3}\end{array} \right.(0,255\,mol\,S{O_4}) + 0,09\,mol\,S{O_2} + {H_2}O\,(2)\)
BTNT “H”: nH2O(2) = nH2SO4 = 0,345 (mol
BTNT “O”: x + 0,345.4 = 0,255.4 + 0,09.2 + 0,345 ⟹ x = 0,165 (mol) ⟹ nH2O(1) = 0,165 (mol)
BTNT “H”: nHCl = 0,04.2 + 0,165.2 = 0,41 (mol) ⟹ nCl(muối) = 0,41 (mol)
⟹ m = 10,08 + 35,5.0,41 = 24,635 (g)
Lưu ý:
Bài toán không cho dữ liệu “sản phẩm không có muối amoni” như các đề thường thấy, nhưng theo tính chất cơ bản của sắt và hợp chất của sắt trong giới hạn chương trình xem như không tạo muối amoni”
Câu trả lời của bạn
Quy đổi hỗn hợp Fe, FeS, FeS2, S thành Fe (a mol) và S (b mol)
⟹ mhỗn hợp = 56a + 32b = 2,08 (1)
Quá trình trao đổi electron:
\(\mathop {F{\rm{e}}}\limits^0 \to \mathop {F{\rm{e}}}\limits^{ + 3} + 3{\rm{e}}\) \(\mathop S\limits^{ + 6} + 2{\rm{e}} \to \mathop S\limits^{ + 4} \)
\(\mathop S\limits^0 \to \mathop S\limits^{ + 6} + 6{\rm{e}}\)
Áp dụng bảo toàn e: 3nFe + 6nS = 2nSO2 ⟹ 3a + 6b = 2.\(\frac{{2,688}}{{22,4}}\) = 0,24 (2)
Giải hệ phương trình (1) (2) được a = 0,02 và b = 0,03
→ Dung dịch X chứa 0,01 mol Fe2(SO4)3
Khi cho dung dịch X phản ứng với NaOH dư, sau đó lọc và nung kết tủa đến khối lượng không đổi:
Fe2(SO4)3 + 6 NaOH → 2 Fe(OH)3 + 3 Na2SO4
0,01 → 0,02 (mol)
2 Fe(OH)3 Fe2O3 + 3 H2O
0,02 → 0,01 (mol)
→ Chất rắn thu được là Fe2O3 có khối lượng: mFe2O3 = 0,01.160 = 1,6 gam
Câu trả lời của bạn
\({n_{KMn{O_4}}} = \frac{{1,896}}{{158}} = 0,012\left( {mol} \right)\)
- Khi cho KMnO4 phản ứng với HCl đặc
(1) 2 KMnO4 + 16 HClđặc \(\xrightarrow{{{t^o}}}\) 2 KCl + 2 MnCl2 + 5 Cl2 + 8 H2O
0,012 → 0,03 mol
Bảo toàn nguyên tố Cl → nAgCl = 2nCl2 = 0,06 mol
⟹ mAgCl = 0,06.143,5 = 8,61 gam < 12,93 gam
⟹ Ngoài AgCl thì còn có kết tủa khác
⟹ Kim loại M có phản ứng với AgNO3
- Khi cho Cl2 tác dụng hết với kim loại M (có hóa trị n không đổi):
(2) n Cl2 + 2 M \(\xrightarrow{{{t^o}}}\) 2 MCln
0,03 → 0,06/n (mol)
→ Hỗn hợp chất rắn X gồm MCln (0,06/n mol) và M dư (a mol)
→ mX = \(\frac{{0,06}}{n}.\left( {M + 35,5n} \right) + a.M\) = 5,38 (1)
- Khi cho X tác dụng AgNO3 dư:
(3) MCln + n AgNO3 → n AgCl ↓ + M(NO3)n
0,06/n → 0,06 (mol)
(4) n M + 2n AgNO3 → n M(NO3)2 + 2n Ag ↓
a → 2a (mol)
→ mkết tủa = 8,61 + 108.2a = 12,93 (2)
Từ (2) ⟹ a = 0,02. Thay vào (1) ta được:
\(\begin{array}{l}\,\,\,\,\,\,\,\frac{{0,06}}{n}.\left( {M + 35,5n} \right) + 0,02.M = 5,38\\ \to 0,06M + 2,13n + 0,02M.n = 5,38n\\ \to M = \frac{{3,25n}}{{0,02n + 0,06}}\end{array}\)
Biện luận với n = 1, 2, 3 ta thấy n = 2 và M = 65 thỏa mãn
Vậy kim loại M là Kẽm (kí hiệu Zn)
Câu trả lời của bạn
nH2(đktc) = VH2/22,4 = 11,2/22,4 = 0,5 (mol)
PTHH: M + H2SO4 → MSO4 + H2↑
Theo PTHH: nM = nH2 = 0,5 (mol)
⟹ MM = mM/nM = 12/0,5 = 24 (g/mol)
⟹M là Mg
Câu trả lời của bạn
PTHH: 2NaOH + MgCl2 → Mg(OH)2↓ + 2NaCl
Kết tủa thu được là Mg(OH)2
Theo PTHH: nMg(OH)2 = 1/2 nNaOH = 1/2 .0,3 = 0,15 (mol)
⟹ mMg(OH)2 = nMg(OH)2×MMg(OH)2 = 0,15×(24+17.2)= 8,7 (g)
Câu trả lời của bạn
BaCO3 tan nhưng là rất ít luôn nên ng ta coi như ko tan.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *