Nội dung bài học giúp học sinh biết về các tính chất hóa học của axit HCl, H2SO4 loãng; Biết được cách viết phương trình phản ứng thể hiện tính chất chung của axit. H2SO4 đặc có những tính chất hoá học riêng: Tính oxi hoá (tác dụng với những kim loại kém hoạt động) tính háo nước, dẫn ra được những phản ứng minh họa cho những tính chất này. Những ứng dụng quan trọng của axit trong sản xuất, trong đời sống.
Làm quỳ tím chuyển sang màu đỏ
Tác dụng với kim loại: 2Al ( r) + 6HCl (dd) → 2 AlCl3 (dd) + 3H2 (k)
Tác dụng với Bazơ: Cu(OH)2(r)+2HCl(dd) → CuCl2(dd)+ 2H2O(l)
Tác dụng với oxit bazơ: CuO (r) + 2HCl (dd) → CuCl2(dd) + H2O
Tác dụng với muối: (Học trong bài 9)
Điều chế các muối
Làm sạch bề mặt kim loại trước khi hàn
Tẩy gỉ kim loại trước khi tráng, sơn, mạ kim loại
Chế biến thực phẩm, dược phẩm
Làm quỳ tím hoá đỏ
Tác dụng với kim loại → muối + nước.
Video 1: Phản ứng của Mg và dung dịch H2SO4
Tác dụng với bazơ → muối + nước
Video 2: Phản ứng giữa dung dịch Cu(OH)2 và H2SO4
Tác dụng với oxit bazơ → muối + nước
Video 3: Phản ứng giữa Fe2O3 và H2SO4
Tác dụng với muối
Tác dụng với kim loại
Video 4: Thí nghiệm Đồng với axit sunfuric loãng và đặc
Nhận xét: H2SO4 đặc tác dụng với nhiều kim loại khác → muối sunfat, không giải phóng khí H2
Tính háo nước
Video 5: Thí nghiệm chứng minh tính háo nước của axit sunfuric đặc
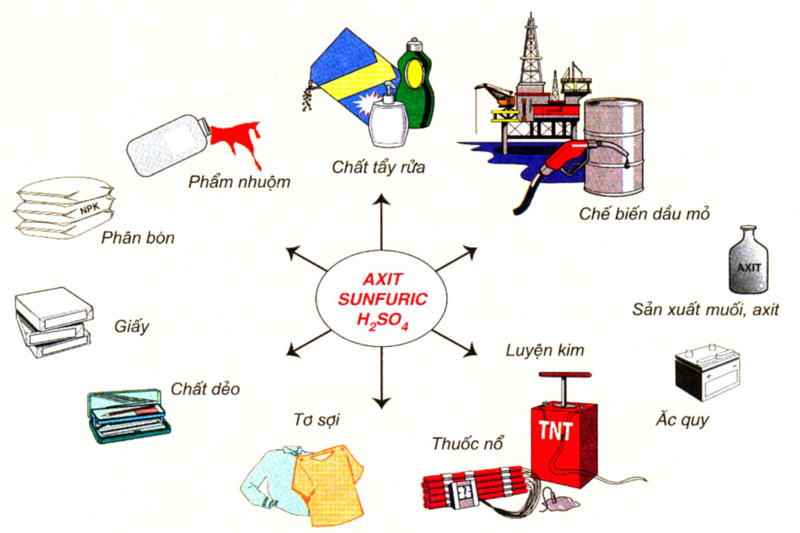
Hình 1: Ứng dụng của axit sunfuric
Trong Công nghiệp Axit sunfuric được sản xuất bằng phương pháp tiếp xúc.
a. Nguyên liệu: Lưu huỳnh hoặc Quặng Pyritsắt (FeS2)
b. Các công đoạn chính:
Video 6: Quy trình sản xuất Axit sunfuric
Video 7: Thí nghiệm giữa dung dịch BaCl2 và H2SO4
Hình 2: Tính chất hóa học của Axit sunfuric
Cần phải điều chế một lượng Đồng (II) sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric?
a, Axit sunfuric tác dụng với Đồng (II) oxit
b. Axit sunfuric đặc tác dụng với Đồng kim loại.
Viết các phương trình hóa học và giải thích
Phương trình hóa học a: CuO + H2SO4 → CuSO4 + H2O
Phương trình hóa học b: Cu + 2H2SO4 (đ) CuSO4 + SO2 + 2H2O
Ở phản ứng a tỉ lệ phản ứng của Cu : H2SO4 là 1: 1 nên sẽ tiết kiệm được axit hơn phản ứng b theo tỉ lệ 1:2.
Hơn nữa ở phản ứng 2 tạo thêm sản phẩm SO2 là khí độc, mùi hắc là nguyên nhân chính tạo ra mưa axit gây ô nhiễm môi trường.
Có 4 lọ không nhãn đựng 4 dung dịch không màu là: HCl, H2SO4, NaCl, Na2SO4. Hãy nhận biết dung dịch trong mỗi lọ bằng phương pháp hóa học. Viết các phương trình hóa học.
Trích dẫn một ít dung dịch của 4 chất để làm mẫu thử rồi lần lượt tiến hành lần lượt như sau:
| Thuốc thử | HCl | H2SO4 | NaCl | Na2SO4 |
| Qùy tím | Đỏ | Đỏ | - | - |
| dung dịch BaCl2 | - | kết tủa trắng | - | Kết tủa trắng |
Trung hòa 300ml dung dịch H2SO4 1,5M bằng dung dịch NaOH 40%
a. Tính khối lượng dung dịch NaOH cần dùng.
b. Nếu thay dung dịch NaOH bằng dung dịch KOH 5,6% (D = 1,045g/ml) thì lượng KOH cần dùng là bao nhiêu?
a. Phương trình hóa học: H2SO4 + 2NaOH → Na2SO4 + 2H2O
Số mol H2SO4 là: nH2SO4 = 0,3 . 1,5 = 0,45 mol
Khối lượng NaOH cần dùng: mNaOH = 2. 0,45. 40 = 36g.
Khối lượng dung dịch NaOH 40%: mdd = 36.10040 = 90g
b. Phương trình phản ứng: H2SO4 + 2KOH → K2SO4 + 2 H2O
Khối lượng KOH cần dùng: mKOH = 2 . 0,45 . 56 = 50,4g
Khối lượng dung dịch KOH: mdd = 50,4.1005,6 = 900g
Thể tích dung dịch KOH cần dùng: vdd = mddD = 9001,045 = 861,2 ml
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 4có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Để an toàn khi pha loãng H2SO4 đặc cần thực hiện theo cách:
Dung dịch axit clohiđric tác dụng với sắt tạo thành:
Dung dịch axit clohiđric tác dụng với đồng (II) hiđrôxit tạo thành dung dịch màu:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 4.
Bài tập 1 trang 19 SGK Hóa học 9
Bài tập 2 trang 19 SGK Hóa học 9
Bài tập 3 trang 19 SGK Hóa học 9
Bài tập 4 trang 19 SGK Hóa học 9
Bài tập 5 trang 19 SGK Hóa học 9
Bài tập 6 trang 19 SGK Hóa học 9
Bài tập 7 trang 19 SGK Hóa học 9
Bài tập 4.1 trang 6 SBT Hóa học 9
Bài tập 4.2 trang 6 SBT Hóa học 9
Bài tập 4.3 trang 7 SBT Hóa học 9
Bài tập 4.4 trang 7 SBT Hóa học 9
Bài tập 4.5 trang 7 SBT Hóa học 9
Bài tập 4.6 trang 7 SBT Hóa học 9
Bài tập 4.7 trang 7 SBT Hóa học 9
Bài tập 4.8 trang 7 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Để an toàn khi pha loãng H2SO4 đặc cần thực hiện theo cách:
Dung dịch axit clohiđric tác dụng với sắt tạo thành:
Dung dịch axit clohiđric tác dụng với đồng (II) hiđrôxit tạo thành dung dịch màu:
Oxit tác dụng được với axit clohiđric là:
Axit sunfuric đặc nóng tác dụng với đồng kim loại sinh ra khí:
Khi nhỏ từ từ H2SO4 đậm đặc vào đường chứa trong cốc hiện tượng quan sát được là:
Để nhận biết gốc sunfat (= SO4) người ta dùng muối nào sau đây ?
Pha dung dịch chứa 1 g NaOH với dung dịch chứa 1 g HCl sau phản ứng thu được dung dịch có môi trường:
Cho 5,6 g sắt tác dụng với axit clohiđric dư, sau phản ứng thể tích khí H2 thu được (ở đktc):
Từ 60 kg FeS2 sản xuất được bao nhiêu kg H2SO4 theo sơ đồ sau:
Có những chất: CuO, BaCl2, Zn, ZnO. Chất nào nói trên tác dụng với dung dịch HCl và dung dịch H2SO4 loãng, sinh ra:
a) Chất khí cháy được trong không khí?
b) Dung dịch có màu xanh lam?
c) Chất kết tủa màu trắng không tan trong nước và axit?
d) Dung dịch không màu và nước?
Viết tất cả các phương trình phản ứng.
Sản xuất axit sunfuric trong công nghiệp cần phải có những nguyên liệu chủ yếu nào? Hãy cho biết mục đích của mỗi công đoạn sản xuất axit sunfuric và dẫn ra những phản ứng hóa học.
Bằng cách nào có thể nhận biết từng chất trong mỗi cặp chất sau theo phương pháp hóa học:
a) Dung dịch HCl và dung dịch H2SO4.
b) Dung dịch NaCl và dung dịch Na2SO4.
c) Dung dịch Na2SO4 và dung dịch H2SO4.
Viết các phương trình phản ứng.
Bảng dưới đây cho biết kết quả của 6 thí nghiệm xảy ra giữa Fe và dung dịch H2SO4 loãng. Trong mỗi thí nghiệm người ta dùng 0,2 gam Fe tác dụng với thể tích bằng nhau của axit, nhưng có nồng độ khác nhau.

Những thí nghiệm nào chứng tỏ rằng:
a) Phản ứng xảy ra nhanh hơn khi tăng nhiệt độ?
b) Phản ứng xảy ra nhanh hơn khi tăng diện tích tiếp xúc?
c) Phản ứng xảy ra nhanh hơn khi tăng nồng độ axit?
Hãy sử dụng những chất có sẵn: Cu, Fe, CuO, KOH, C6H12O6 (glucozơ), dung dịch H2SO4loãng, H2SO4 đặc và những dụng cụ thí nghiệm cần thiết để làm những thí nghiệm chứng minh rằng:
a) Dung dịch H2SO4 loãng có những tính chất chung của axit.
b) H2SO4 đặc có những tính chất hóa học riêng.
Viết phương trình hóa học cho mỗi thí nghiệm.
Cho một khối lượng mạt sắt dư vào 50ml dung dịch HCl. Phản ứng xong thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học.
b) Tính khối lượng mạt sắt đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl đã dùng.
Hòa tan hoàn toàn 12,1g hỗn hợp bột CuO và ZnO cần 100ml dung dịch HCl 3M.
a) Viết các phương trình hóa học.
b) Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
c) Hãy tính khối lượng dung dịch H2SO4 có nồng độ 20 % để hòa tan hoàn toàn hỗn hợp các oxit trên.
Dung dịch H2SO4 loãng tác dụng được với các chất trong dãy:
A. CuO, BaCl2, NaCl, FeCO3
B. Cu, Cu(OH)2, Na2CO3, KCl
C. Fe, ZnO, MgCl2, NaOH
D. Mg, BaCl2, K2CO3, Al2O3
Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric ?
a) Axit sunfuric tác dụng với đồng(II) oxit.
b) Axit sunfuric đặc tác dụng với đồng kim loại.
Viết các phương trình hoá học và giải thích.
Cho những chất sau: đồng, các hợp chất của đồng và axit sunfuric. Hãy viết những phương trình hoá học điều chế đồng(II) sunfat từ những chất đã cho, cần ghi rõ các điều kiện của phản ứng.
Có 3 lọ không nhãn, mỗi lọ đựng một trong những chất rắn sau: CuO, BaCl2, Na2CO3. Hãy chọn một thuốc thử để có thể nhận biết được cả ba chất trên. Giải thích và viết phương trình hoá học.
Có 4 lọ không nhãn, mỗi lọ đựng một dung dịch không màu là: HCl, H2SO4, NaCl, Na2SO4. Hãy nhận biết dung dịch đựng trong mỗi lọ bằng phương pháp hoá học. Viết các phương trình hoá học.
Cho một lượng bột sắt dư vào 50 ml dung dịch axit sunfuric. Phản ứng xong, thu được 3,36 lít khí hiđro (đktc).
a) Viết phương trình hoá học.
b) Tính khối lượng sắt đã tham gia phản ứng.
c) Tính nồng độ moi của dung dịch axit sunfuric đã dùng.
Trung hoà 20 ml dung dịch H2SO4 1M bằng dung dịch NaOH 20%.
a) Viết phương trình hoá học.
b) Tính khối lượng dung dịch NaOH cần dùng.
c) Nếu trung hoà dung dịch axit sunfuric trên bằng dung dịch KOH 5,6%, có khối lượng riêng là 1,045 g/ml, thì cần bao nhiêu ml dung dịch KOH ?
Cho dung dịch HCl 0,5M tác dụng vừa đủ với 21,6 gam hỗn hợp A gồm Fe, FeO, FeCO3. Thấy thoát ra một hỗn hợp khí có tỉ khối đối với H2 là 15 và tạo ra 31,75 gam muối clorua.
a) Tính thể tích dung dịch HCl đã dùng.
b) Tính % khối lượng của mỗi chất trong hỗn hợp A.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
giúp em với ạ, em cần gấp lắm ạ
hoà tan hoà toàn 32g hỗn hợp gồm CuO và Fe2O3. Cần vừa đủ 400g dung dịch HCl x%. Sau phản ứng thu được 67g hỗn hợp 2 muối a) Tính %m mỗi kim loại trong hỗn hợp ban đầu b) Tính c. C) Tính c% sau phản ứng
Câu trả lời của bạn
người ta dùng 200 tấn quặng hemetit hàm lượng Fe2O3 là 30% thì sản xuất được 38 tấn gang. Biết rằng loại gang này chứa 95% Fe và trong lò cao có 2% mất theo xỉ. Tính hiệu suất của quá trình sản xuất
Câu trả lời của bạn
Câu trả lời của bạn
H2SO4 là axit sunfuric
Câu trả lời của bạn
Zn + 2HCl → ZnCl2 + H2 (1)
Zn + H2SO4 → ZnSO4 + H2 (2)
nHCl = 0,002 => nH2 (1) = 0,001 mol => V1 = 0,001 x 22,4 = 0,0224 lít
nH2SO4 = 0,002 => nH2 (2) = 0,002 mol => V2 = 0,002 x 22,4 = 0,0448 lít
=> V2 = 2V1.
Câu trả lời của bạn
pH = 7 thì dung dịch trung tính và ngược lại.
=> NaOH và HCl vừa hết.
NaOH + HCl → NaCl + H2O
Nghĩa là: nNaOH = nHCl => x = y.
Câu trả lời của bạn
Do X tác dụng với H2SO4 loãng, giải phóng H2 nên X không thể là Cu và Ag → loại A và B
Do H2 không khử được MgO để tạo thành Mg → loại C
Câu trả lời của bạn
Để pha loãng dung dịch H2SO4 đặc một cách an toàn phải
Câu trả lời của bạn
\(\begin{array}{l} Ba{(N{O_3})_2} + HCl \to kpu\\ Ba{(N{O_3})_2} + {H_2}S{O_4} \to BaS{O_4} \downarrow + HN{O_3} \end{array}\)
Câu trả lời của bạn
Mg + H2SO4 → MgSO4 + H2
0,4mol 0,4mol
=> m = 0,4.24 = 9,6g
Câu trả lời của bạn
n khí = 3,36/22,4 = 0,15 mol
Zn + 2HCl → ZnCl2 + H2
0,3 mol ⇔ 0,15 mol
CMHCl = 0,3/0,1 = 3M
Câu trả lời của bạn
n khí = 0,1 mol
Zn + 2HCl → ZnCl2 + H2
0,1 0,1 mol
-> mZn = 0,1.65 = 6,5 gam
Câu trả lời của bạn
Fe + 2HCl → FeCl2 + H2
nFe = 5,6/56 = 0,1 mol
Theo PT, ta có nH2 = nFe = 0,1 mol
=> VH2 = 0,1.22,4 = 2,24 lít
Câu trả lời của bạn
Nhỏ từ từ dung dịch BaCl2 vào dung dịch Na2SO4 ta thấy xuất hiện kết tủa màu trắng
Do BaCl2 + Na2SO4 → BaSO4(↓ trắng) + 2NaCl
Câu trả lời của bạn
Phân tử axit gồm có một hay nhiều nguyên tử hidro liên kết với gốc axit, các nguyên tử hidro này có thể thay thế bằng các nguyên tử kim loại.
Các chất thuộc loại axit là: H2SO4, HCl
Câu trả lời của bạn
Gốc axit của axit HNO3 là nhóm (NO3) có hóa trị I
Câu trả lời của bạn
pH = 3 < 7 → dung dịch có môi trường axit.
Câu trả lời của bạn
Chất dùng để phân biệt các dung dịch không màu: HCl, H2SO4 loãng, BaCl2 là qùy tím
(HCl, H2SO4 loãng, BaCl2) + quỳ tím ->
- Quỳ tím chuyển sang đỏ: (HCl, H2SO4) + BaCl2 -> kết tủa trắng là H2SO4, còn lại là HCl
- Quỳ tím không đổi màu: BaCl2
Câu trả lời của bạn
Dãy kim loại phản ứng được với dung dịch H2SO4 loãng là Mg, Fe, Zn.
H2SO4 không phản ứng với Cu, Ag, Pt.
Câu trả lời của bạn
Axit sunfuric: H2SO4.
Câu trả lời của bạn
H2SO3 là axit ít oxi
+ Axit có ít nguyên tử oxi: Tên axit = Axit + tên phi kim + ơ.
⇒ H2SO3 có tên gọi là: axit sunfurơ

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *