Nội dung bài học giúp củng cố các kiến thức đã học về tính chất của Gluxit, rèn luyện các kĩ năng thí nghiệm.
C6H12O6 + Ag2O \(\overset{NH_{3}}{\rightarrow}\) C6H12O7 (Axit gluconic) + 2Ag\(\downarrow\)
Sự hấp phụ Iod vào các khe trống trong tinh bột tạo màu xanh đen.
⇒ Phương pháp dùng để nhận biết Hồ tinh bột và ngược lại (dùng để nhận biết Iod)
Không dùng tay cầm trực tiếp hoá chất.
Không đổ hoá chất này vào hoá chất khác ngoài chỉ dẫn.
Không đổ lại hoá chất thừa lại lọ đựng ban đầu.
Không dùng hoá chất nếu không biết hoá chất gì.
Không nếm hoặc ngửi trực tiếp hoá chất.
Khi mở lọ hoá chất và lấy hoá chất không để dây ra bàn, dùng xong đậy nắp lại ngay.
Cách tiến hành, các em quan sát thí nghiệm sau:
Video 1: Phản ứng tráng bạc của Glucozơ
Có chất màu sáng bạc bám lên thành ống nghiệm
Do Ag sinh ra từ phản ứng bám lên thành ống nghiệm: C6H12O6 + Ag2O \(\overset{NH_{3}}{\rightarrow}\) C6H12O7 (Axit gluconic) + 2Ag\(\downarrow\)
Cách tiến hành, các em quan sát thí nghiệm sau:
Video 2: Phân biệt glucozơ, saccarozo và tinh bột
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 55có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Đun nóng dd chứa 9g glucozơ với dd AgNO3 đủ pứ trong dd NH3 thấy Ag tách ra. Tính lượng Ag thu được.
Khi lên men 360 gam glucozơ với hiệu suất 100%, khối lượng ancol etylic thu được là
Cho m gam glucozơ lên men, khí thoát ra được dẫn vào dd nước vôi trong dư thu được 55,2g kết tủa trắng. Tính khối lượng glucozơ đã lên men, biết hiệu suất lên men là 92%.
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Đun nóng dd chứa 9g glucozơ với dd AgNO3 đủ pứ trong dd NH3 thấy Ag tách ra. Tính lượng Ag thu được.
Khi lên men 360 gam glucozơ với hiệu suất 100%, khối lượng ancol etylic thu được là
Cho m gam glucozơ lên men, khí thoát ra được dẫn vào dd nước vôi trong dư thu được 55,2g kết tủa trắng. Tính khối lượng glucozơ đã lên men, biết hiệu suất lên men là 92%.
Thuỷ phân hòan toàn 1 kg tinh bột thu được:
Trong các nhận xét dưới đây, nhận xét nào đúng?
Tất cả các chất có công thức Cn(H2O)m đều là cacbohidrat.
Tất cả các cacbohidrat đều có công thức chung là Cn(H2O)m
Đa số các cacbohidrat có công thức chung là Cn(H2O)m
Phân tử các cacbohidrat đều có ít nhất 6 nguyên tử cacbon.
Glucozo không thuộc loại :
hợp chất tạp chức.
monosaccarit.
Dựa vào tính chất nào để kết luận tinh bột và xenlulozơ là những polime thiên nhiên có công thức (C6H10O5)n
Tinh bột và xenlulozơ khi bị đốt cháy đều cho CO2 và H2O theo tỉ lệ số mol 6:5.
Tinh bột và xenlulozơ khi bị thuỷ phân đến cùng đều cho glucozơ.
Tinh bột và xenlulozơ đều tan trong nước.
Thuỷ phân 1 kg khoai có chứa 20% tinh bột trong môi trường axit. Nếu hiệu suất của quá trình là 75% thì khối lượng glucozơ thu được là nhiêu?
Phân tử khối trung bình của PVC là 750000. Hệ số polime hoá của PVC là bao nhiêu ?
Phân tử khối trung bình của polietilen X là 420000. Hệ số polime hoá của PE là bao nhiêu ?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

Câu trả lời của bạn
Câu trả lời của bạn
Hoa phượng.
Câu trả lời của bạn
Hoa đào.
Câu trả lời của bạn
Hoa lục bình.
Câu trả lời của bạn
Hoa dạ hương.
Câu trả lời của bạn
Hoa điểm 10.
Câu trả lời của bạn
Hoa chuối.
Câu trả lời của bạn
Câu trả lời của bạn
Câu trả lời của bạn
Câu trả lời của bạn
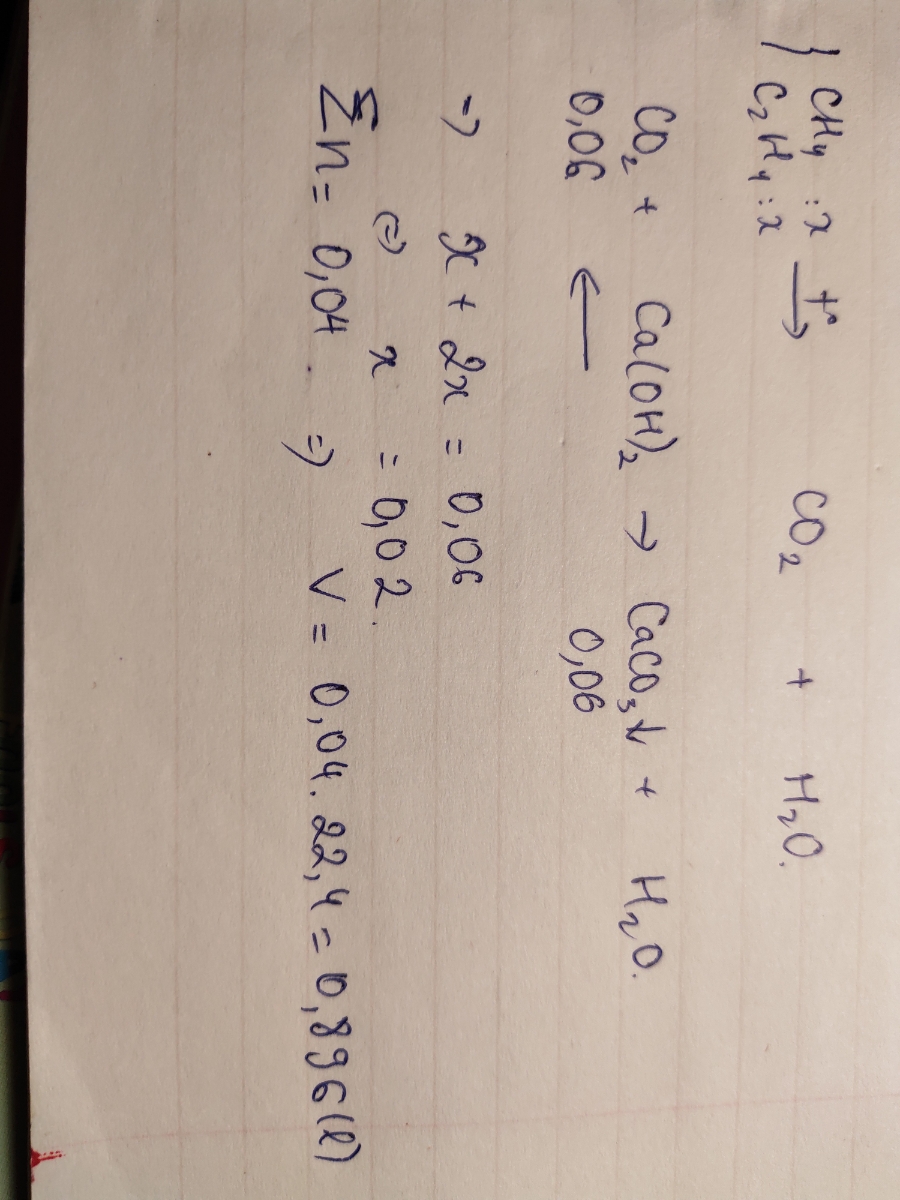
Cho 100g khí CO2 (được xem như là khí lý tưởng) ở 00C và 1,013.105 Pa. Xác định Q, A, ΔU và ΔH trong các quá trình sau. Biết Cp = 37,1 J/mol.K.
a. Giãn nở đẳng nhiệt tới thể tích 0,2 m3.
b. Giãn đẳng áp tới 0,2 m3.
c. Đun nóng đẳng tích tới khi áp suất bằng 2,026.105 Pa.
Cho 1 atm = 101325 Pa
Câu trả lời của bạn
Ta có: \(P_1=1,013.10^5Pa=0.99975atm\approx1atm\) ; \(T_1=273K;V_2=0.2m^3=200\left(l\right)\) ;
\(C_p=37,1\left(\frac{J}{mol.K}\right)\) ; \(n_{CO_2}=\frac{m_{CO_2}}{M_{CO_2}}=\frac{100}{44}=\frac{25}{11}\left(mol\right)\)
Vì theo dề bài CO2 được xem như là khí lý tưởng nên ta có phương trình trạng thái:
\(P_1.V_1=n.R.T_1\Rightarrow V_1=\frac{n_{CO_2}.R.T_1}{P_1}=\frac{\frac{25}{11}.0,082.273}{1}=50,88\left(l\right)\)
a) : Vì quá trình giãn nở đẳng nhiệt (T=T1) tới \(V_2\) nên biến thiên nội năng đẳng nhiệt của một quá trình là bằng 0 hay \(\Delta U_T=0\) và \(\Delta H_T=\Delta U_T=0\)
Như vậy ta có:
\(Q_T=A_T=n_{CO_2}.R.T.ln\frac{V_2}{V_1}=\frac{25.8,314.273}{11}.ln\frac{200}{50.88}=7061,14\left(J\right)\)
b) Quá trình giãn đẳng áp, gọi \(T_2\) là nhiệt độ của CO2 ở \(V_2\) ta có: \(\frac{V_1}{V_2}=\frac{T_1}{T_2}\Rightarrow T_2=\frac{273.200}{50.88}=1073,1\left(K\right)\)
Công dãn nở đẳng áp là : \(A_P=n_{CO_2}.R.\Delta T=\frac{25}{11}.8,314.\left(1073,1-273\right)=15118,25\left(J\right)\)
và ta cũng có \(\Delta H=Q_P=n_{CO_2}.C_p.\Delta T=\frac{25}{11}.37,1.\left(1073,1-273\right)=67462,98\left(J\right)\)
Suy ra: \(\Delta U_P=Q_P-n_{CO_2}.R.\Delta T=67462,98-15118,25=52344,73\left(J\right)\)
c) đun nóng đẳng tích tới \(P'_2=2,026.10^5\left(Pa\right)=1,9995\left(atm\right)\approx2\left(atm\right)\)
Vì quá trình là đẳng tích nên \(Q_V=\Delta U\) vá \(A_V=0\)
Ta có: \(\frac{T_1}{T'_2}=\frac{P_1}{P'_2}\Rightarrow T'_2=T'_1.\frac{P_2}{P_1}=273.\frac{2}{1}=546\left(K\right)\)
\(C_V=C_P-R=37,1-8,314=28,786\left(\frac{J}{mol.K}\right)\)
vậy \(Q_V=n_{CO_2}.C_V.\Delta T=\frac{25}{11}.28,786.\left(546-273\right)=17860,4\left(J\right)\)
Đối với khí lý tưởng: \(\Delta H=\Delta U+n_{CO_2}.R.\Delta T=17860,4+\frac{25}{11}.8,314.\left(546-273\right)=23018,86\left(J\right)\)

Câu trả lời của bạn
Em chào thầy! thầy ơi thầy cho em hỏi: nhiệt dụng mol khác nhiệt dung riêng ở chỗ nào ạ. và đơn vị của từng loại là gì ạ? Em cảm ơn thầy ạ!
Câu trả lời của bạn
Nhiệt dung riêng của một chất là một đại lượng vật lý có giá trị bằng nhiệt lượng cần truyền cho một đơn vị khối lượng chất đó để làm tăng nhiệt độ lên 1 °C. Trong hệ thống đo lường quốc tế, đơn vị đo của nhiệt dung riêng là Joule trên kilôgam trên Kelvin, J•kg−1•K−1 hay J/(kg•K), hoặc Joule trên mol trên Kelvin.
+ Nhiệt dung mol đẳng tích (ký hiệu Cv) là nhiệt dung tính trong quá trình biến đổi mà thể tích của hệ không đổi và được tính bằng δ.Q_v chia cho n.dT
+ Nhiệt dung mol đẳng áp (ký hiệu Cp) là nhiệt dung tính trong quá trình biến đổi mà áp suất của hệ không đổi và được tính bằng δ.Q_p chia cho n.dT
Nêu phương pháp hóa học nhận biết 4 dung dịch sau :glucozơ; Saccarozơ ;rượu etylic và axit axetic
Câu trả lời của bạn
- lấy mẫu , đánh dấu
- nhúng quỳ tím vào các mẫu thử
+ mẫu thử nào làm quỳ tím hóa đỏ -> axitxetic
+ mẫu thử nào k hiện tượng -> glucozo , saccarozo , rượu etylic (1)
- cho Na vào mẫu thử nhóm (1)
+ mẫu thử nào có khí bay lên -> rượu etylic
2C2H5OH + 2Na -> 2C2H5ONa + H2
+ mẫu thử nào ko hiện tượng -> glucozo và saccarozo (2)
- cho AgNO3/NH3 vào mẫu thử nhóm (2)
+ mẫu thử nào xuất hiện kết tủa trắng bạc -> glucozo
C6H12O6 + Ag2O --NH3--> C6H12O7 + 2Ag
+ mẫu thử nào ko hiện tượng -> saccarozo
Câu 1: Nhận biết rượu etylic, axit axetic, benzen. Viết PTHH.
Câu 2: Cho 7,8g Kali tác dụng với rượu etylic.
a) Viết PTHH
b) Tính m rượu etylic cần dùng.
c) Đun nóng 1g rượu etylic ở trên với 6g axit axetic (xt H2SO4). Một thời gian sau, thu được 5,28g etyl axetat. Tính hiệu suất phản ứng.
Câu trả lời của bạn
1.
- Lấy mẫu thử và đánh dấu
- Cho quỳ tím vào các mẫu thử
+ Mẫu thử làm quỳ hóa đỏ chất ban đầu là axit axetic
+ Mẫu thử không hiện tương chất ban đầu là rượu etylic, bezen (I)
- Cho nước vào nhóm I
+ Mẫu thử không tan phân lớp chất ban đầu là bezen
+ Mẫu thử tan không phân lớp chất ban đầu là rượu etylic

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *