Nội dung bài giảng Cacbon tìm hiểu Đơn chất cacbon có 3 dạng thù hình chính: Kim cương, than chì và cacbon vô định hình; Cacbon vô định hình (than gỗ, than xương, mồ hóng…) có tính hấp phụ và hoạt động hóa học nhất; Sơ lược tính chất vật lí của 3 dạng thù hình; Cacbon là phi kim hoạt động hóa học yếu: Tác dụng với oxi và một số oxit kim loại, tính chất hóa học đặc biệt của cácbon là tính khử ở nhiệt độ cao; Một số ứng dụng tương ứng với tính chất vật lí và tính chất hóa học của cacbon.
Dạng thù hình là những đơn chất khác nhau do nguyên tố đó tạo nên . Ví dụ: O2 (Oxi) và O3 (Ozon)
| Kim cương | Than chì | Cacbon vô định hình (than gỗ, than xương...) | |
| Cấu trúc | 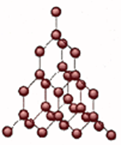 | ||
| Tính chất | Cứng, trong suốt, không dẫn điện | Mềm, dẫn điện | xốp, không dẫn điện. |
Video 1: Khả năng lọc màu của than hoạt tính
Cacbon là phi kim hoạt động hóa học yếu điều kiện xảy ra phản ứng của C với H2 và kim loại rất khó khăn nên ta chỉ xét một số tính chất hóa học có nhiều ứng dụng trong thực tế như sau:
Video 2: Cacbon cháy trong Oxi
Cácbon tác dụng với oxít kim loại: CuO (đen) + C (đen) CO2 (không màu) + Cu (đỏ)
Video 3: Phản ứng giữa Cacbon và Đồng (II) oxit
Ngoài ra ở nhiệt độ cao C còn khử được một số oxít kim loại như ZnO, PbO ...
Hình 1: Ứng dụng của kim cương
Hình 2: Ứng dụng của than chì
Hình 3: Ứng dụng của than muội
Hình 4: Sơ đồ tư duy bài Cacbon
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 27có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Chất dùng làm chất khử một số kim loại ở nhiệt độ cao là:
Để khẳng định một chất bột là cacbon hay oxit sắt , cách làm nào sau đây là đúng?
Dạng thù hình nào của cacbon dẫn điện tốt?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 27.
Bài tập 1 trang 84 SGK Hóa học 9
Bài tập 2 trang 84 SGK Hóa học 9
Bài tập 3 trang 84 SGK Hóa học 9
Bài tập 4 trang 84 SGK Hóa học 9
Bài tập 5 trang 84 SGK Hóa học 9
Bài tập 27.1 trang 33 SBT Hóa học 9
Bài tập 27.2 trang 33 SBT Hóa học 9
Bài tập 27.3 trang 33 SBT Hóa học 9
Bài tập 27.4 trang 33 SBT Hóa học 9
Bài tập 27.5 trang 34 SBT Hóa học 9
Bài tập 27.6 trang 34 SBT Hóa học 9
Bài tập 27.7 trang 34 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Chất dùng làm chất khử một số kim loại ở nhiệt độ cao là:
Để khẳng định một chất bột là cacbon hay oxit sắt , cách làm nào sau đây là đúng?
Dạng thù hình nào của cacbon dẫn điện tốt?
Khí CO2 bị coi là chất làm ô nhiễm môi trường vì nó
Ở điều kiện thích hợp cacbon có thể phản ứng với các chất CuO, PbO, CO2. Vai trò của cacbon trong các phản ứng này là gì?
Chất nào sau đây không phải dạng thủ hình của cacbon ?
Phản ứng nào trong các phản ứng sau đây, cacbon thể hiện tính oxi hóa ?
Vật liệu dưới đây được dùng để chế tạo ruột bút chì ?
Trong những nhận xét dưới đây, nhận xét nào không đúng ?
Đốt cháy hết m gam than (C) trong V lít oxi thu được 2,24 lít hỗn hợp X gồm 2 khí. Tỉ khối của X so với oxi bằng 1,25. Các thể tích đo được (đktc). Giá trị của m là
Dạng thù hình của nguyên tố là gì? Cho hai ví dụ.
Viết phương trình hóa học của cacbon với các oxit sau:
a) CuO.
b) PbO.
c) CO2.
d) FeO.
Hãy cho biết loại phản ứng: vai trò của C trong các phản ứng, ứng dụng của các phản ứng đó trong sản xuất.
Hãy xác định công thức hóa học thích hợp của A, B, C, D trong thí nghiệm ở hình vẽ bên.
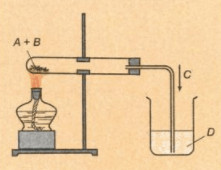
Nêu hiện tượng thí nghiệm và viết phương trình hóa học.
Tại sao sử dụng than để đun nấu, nung gạch ngói, nung vôi gây ô nhiễm môi trường. Hãy nêu biện pháp chống ô nhiễm môi trường và giải thích?
Trong công nghiệp, người ta sử dụng cacbon để làm nhiên liệu. Tính nhiệt lượng tỏa ra khi đốt cháy 5kg than đá chứa 80% cacbon, biết rằng 1 mol cacbon cháy thì tỏa ra 394kJ.
Người ta đã căn cứ vào tính chất vật lí và tính chất hoá học của than để sử dụng than trong thực tế đời sống như thế nào ? Cho thí dụ.
Viết phương trình hoá học của các phản ứng sau và cho biết tính chất hoá học của cacbon (là chất oxi hoá hay chất khử)
C + CO2 to→ CO (1)
C + Fe2O3 to → Fe + CO (2)
C + CaO to→ CaC2 + CO (3)
C + PbO to→ Pb + CO2 (4)
C + CuO to→ Cu + CO2 (5)
Trong quá trình luyện quặng sắt thành gang, người ta dùng CO làm chất khử. Hãy tính thể tích khí CO (đktc) có thể thu được từ 1 tấn than chứa 90% cacbon, nếu hiệu suất của cả quá trình phản ứng là 85%.
Viết phương trình hóa học biểu diễn những chuyển đổi hóa học sau:
a) C → CO2 → CaCO3 → CaO → Ca(OH)2 → Ca(HCO3)2
b) Fe2O3 → Fe → FeCl3 → Fe(OH)3 → Fe2O3
Fe → FeCl2 → Fe(OH)2
Cho hơi nước đi qua than nóng đỏ, người ta thu được hỗn hợp khí CO và H2 (hình 3.3).
a) Viết phương trình hoá học.
b) Tính thể tích hỗn hợp khí (đktc) thu được ở phản ứng trên khi dùng hết 1 tấn than chứa 92%
Cho 268,8 m3 hỗn hợp khí CO và H2 khử sắt(III) oxit ở nhiệt độ cao.
a) Viết phương trình hoá học.
b) Tính khối lượng sắt thu được.
Đem nung hỗn hợp hai oxit CuO và ZnO có tỉ lệ số mol là 1 : 1 với cacbon trong điều kiện thích hợp để oxit kim loại bị khử hết, thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí (ở đktc). Hãy tính khối lượng mỗi oxit kim loại.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
A. than chì, cacbon vô định hình, khí cacbonic.
B. than chì, kim cương, canxi cacbonat.
C. cacbon, cacbon oxit; cacbon ddioxxit.
D. kim cương, than chì, cacbon vô định hình.
Câu trả lời của bạn
Các dạng thù hình của cacbon là kim cương, than chì, cacbon vô định hình.
A. điện cực, chất khử.
B. trắng đường, mặt nạ phòng hơi độc.
C. ruột bút chì, chất bôi trơn.
D. mũi khoan, dao cắt kính.
Câu trả lời của bạn
Do có tính hấp phụ, nên cacbon vô định hình được dùng làm trắng đường, mặt nạ phòng hơi độc.
A. những đơn chất khác nhau do nguyên tố đó tạo nên.
B. những chất khác nhau do từ hai nguyên tố hoá học trở lên tạo nên.
C. những chất khác nhau được tạo nên từ cacbon.
D. những chất khác nhau được tạo nên từ nguyên tố phi kim với oxi.
Câu trả lời của bạn
Dạng thù hình của một nguyên tố là những đơn chất khác nhau do nguyên tố đó tạo nên.
A. Kali.
B. Silic.
C. Cacbon.
D. Natri.
Câu trả lời của bạn
Cacbon khi cháy tạo ra oxit ở thể khí
A. CuO, BaO, Fe2O3.
B. PbO, CuO, FeO.
C. Fe2O3, PbO, Al2O3.
D. K2O, ZnO, Fe3O4.
Câu trả lời của bạn
Đáp án: B
C khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học thành kim loại.
Câu trả lời của bạn
Số mol cacbon: nC = 45 : 12 = 3,75 mol
C + O2 → CO2
3,75 3,75 mol
Thể tích khí O2 cần dùng: VO2 = 3,75.22,4 = 84 lít
→ Thể tích không khí cần dùng: Vkk = 5.84 = 420 lít.
A. 1,12 lít.
B. 11,2 lít.
C. 2,24 lít.
D. 22,4 lít.
Câu trả lời của bạn
Số mol cacbon: nC = 12 : 12 = 1 mol
C + O2 → CO2
1 1 mol
→ Thể tích CO2: V = 1.22,4 = 22,4 lít.
A. 3,6 gam.
B. 1,2 gam.
C. 2,4 gam.
D. 0,6 gam.
Câu trả lời của bạn
Đáp án: D
Số mol CuO: nCuO = 8 : 80 = 0,1 mol
2CuO + C → 2Cu + CO2
0,1 0,05 mol
→ mC pư = 0,05.12 = 0,6 gam.
A. 1717,3 m3
B. 1715,3 m3
C. 1710,3 m3
D. 1708 m3
Câu trả lời của bạn
%C có trong than là 100% - 8% = 92%
Khối lượng C có trong 1 tấn than là: mC = 1.92/100 = 0,92 tấn = 920 kg = 920000 gam
nC = 920000/12 = 76666,67 mol
C + O2 → CO2
→ VCO2 = nCO2.22,4 = nC.22,4 = 76 666,67.22,4 = 1717333,408 lít
≈ 1717,33 m3.
A. dung dịch HCl đặc, nóng.
B. dung dịch NaCl.
C. dung dịch CuSO4.
D. nước nóng.
Câu trả lời của bạn
Sử dụng dung dịch HCl đặc, nóng.
+ chất rắn tan dần, có khí màu vàng lục, mùi xốc thoát ra → mangan đioxit (MnO2)
MnO2 + 4HCl to→ MnCl2 + Cl2 + 2H2O
+ chất rắn tan dần, sau phản ứng thu được dung dịch màu xanh → đồng (II) oxit (CuO)
CuO + 2HCl → CuCl2 (xanh) + H2O
+ không có hiện tượng gì xuất hiện → cacbon.
A. Kim cương
B. Than chì
C. Fuleren
D. Cả A, B, C và cacbon vô định hình
Câu trả lời của bạn
Cacbon tạo thành một số dạng thù hình là: Kim cương, than chì, fuleren và cacbon vô địch hình.
Đáp án D
A. CO, CO3
B. CO2, CO3
C. CO, CO2
D. CO2, C2O4
Câu trả lời của bạn
Cacbon có thể tạo với oxi 2 oxit là CO, CO2
C + O2 \(\xrightarrow{{{t^o}}}\) CO2
C + CO2 \(\xrightarrow{{{t^o}}}\) 2CO
Đáp án C
Câu trả lời của bạn
\({n_{CO}} + {n_{C{O_2}}} = 0,7\) mol (1)
\({n_{CO}} + {n_{C{O_2}}} = 3:4\) (2)
Từ (1) và (2) ⟹ nCO = 0,3 mol; \({n_{C{O_2}}} = 0,4\) mol.
\(2C + {O_2}\xrightarrow{{{t^0}}}2CO\)
\(C + {O_2}\xrightarrow{{{t^0}}}C{O_2}\)
⟹ nC = 0,3 + 0,4 = 0,7 mol.
⟹ m = mC = 0,7.12 = 8,4 gam.
⟹ \({n_{{O_2}}} = \dfrac{{0,3}}{2} + 0,4 = 0,55\) mol.
⟹ V = 0,55.22,4 = 12,32 lít.
A. Một số oxit kim loại như PbO, ZnO, CuO, ...
B. Một số bazơ như NaOH, Ca(OH)2, Cu(OH)2, ...
C. Một số axit như HNO3; H2SO4; H3PO4, ....
D. Một số muối như NaCl, CaCl2, CuCl2,...
Câu trả lời của bạn
Trong luyện kim, người ta sử dụng cacbon và oxit của kim loại để điều chế kim loại
Đáp án A
A. Nước vôi trong; đồng (II) oxit nung nóng.
B. Kali hiđroxit, nhôm oxit
C. Natri hiđroxit, đồng (II) oxit nung nóng.
D. Nước vôi trong; nhôm oxit
Câu trả lời của bạn
Dẫn hỗn hợp khí qua (1) thấy xuất hiện kết tủa trắng => (1) là dung dịch nước vôi trong Ca(OH)2
=> khí CO2 bị hấp thụ, còn lại khí CO thoát ra khỏi bình
PTHH: CO2 + Ca(OH)2 → CaCO3 + H2O
Dẫn CO qua (2) thấy chất rắn màu đỏ xuất hiện => chất rắn đó là Cu
=> (2) là CuO
PTHH: CO + CuO \(\xrightarrow{{{t^o}}}\) Cu + CO2
Đáp án A
Câu trả lời của bạn
Gọi công thức muối X là AlxCy.
\(xAl + yC\xrightarrow{{{t^0}}}A{l_x}{C_y}\)
Theo PTHH ⟹
\(\dfrac{x}{y} = \dfrac{{{n_{Al}}}}{{{n_C}}} = \dfrac{{0,4}}{{0,3}} = \dfrac{4}{3}\).
Câu trả lời của bạn
1 tấn= 1000 kg
Khối lượng cacbon có trong 1 tấn than là: \({m_C} = {{92} \over {100}} \times 1000 = 920(kg)\)
C + H2O \(\xrightarrow{{{t^0}}}\) CO + H2
Theo pư Cứ 12g 22,4 l 22,4l
Hay 12 kg 22,4 m3 22,4 m3
Vậy 920 kg x m3 x m3
\( = > {\rm{ }}{V_{CO(DKTC)}} = {\rm{ }}{V_{{H_2}(DKTC)}} = {{920} \over {12}}\,.\,22,4 = 1717,33({m^3})\)
=>m tổng thể tích 2 khí thu được theo lí thuyết là (H=100%) = 2×1717,33=3434,66(m3)
Vì H= 85% => Tổng thể tích khí thu được là:\({{{V_{{\rm{LT}}}}} \over {100\% }} \times 85\% = {{3434,66} \over {100}} \times 85 = 2919,46({m^3})\)
Câu trả lời của bạn
n khí = V hh khí : 22,4 = 1,568 : 22,4 = 0,07 mol
Gọi x và y lần lượt là số mol của Fe2O3 và CuO
Fe2O3 + 3C → 3CO + 2Fe
CuO + C → CO + Cu
Nhận thấy nC = nCO = 0,07 mol
=> mC =0,84g
m CO = 0,07 . 28 = 1,96g
Áp dụng ĐLBT khối lượng ta có
m hh oxit = mhhKL + mCO - mC =3,68 + 1,96 - 0,84 = 4,8g

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *