Nội dung bài giảng ôn tập lại toàn bộ tính chất hóa học của hai nhóm chất cơ bản của hóa học vô cơ là Oxit và Axit. Vậy giữa oxit và axit liên hệ với nhau như thế nào chúng ta cùng nhau hệ thống lại qua bài hoc sau:
Hình 1: Mối liên hệ giữa oxit axit và oxit bazơ
Các phản ứng minh họa tính chất hóa học của Oxit
(1). CuO + 2HCl → CuCl2 + H2O
(2) .CO2 + Ca(OH)2 → CaCO3 + H2O
(3). CaO + CO2 → CaCO3
(4). Na2O + H2O → 2NaOH
(5). P2O5 + 3H2O → 2H3PO4
Hình 2: Tính chất hóa học của Axit
Các phản ứng minh họa tính chất hóa học của Axit
(1). 2HCl + Mg → MgCl2 + H2 .
(2). 3H2SO4 + Fe2O3 → Fe2(SO4)3 + 3H2O
(3). 3HCl + Fe(OH)3 → FeCl3+ 3H2O
Hình 2: Sơ đồ tư duy bài luyện tập tính chất hóa học của Oxit
Hình 3: Tính chất hóa học của Axit
Cho các chất sau : SO2, Fe2O3, K2O, BaO, P2O5 . Hãy cho biết những chất nào tác dụng được với:
a. Nước
b. Axit clohiđric
c. Kalihđroxit .
a. Những chất tác dung với nước là: SO2, K2O, BaO, P2O5 .
SO2 + H2O → H2SO3
K2O + H2O → 2KOH
BaO + H2O → Ba(OH)2
P2O5 +3H2O → 2H3PO4
b. Những chất tác dụng với HCl là: Fe2O3, K2O, BaO .
6HCl + Fe2O3 → 2FeCl3+ 3H2O
2HCl + K2O → 2KCl+ H2O
2HCl + BaO → BaCl2 + H2O
c. Những chất tác dụng với dd KOH: SO2, P2O5 .
2KOH + SO2 → K2SO3 + H2O
6KOH + P2O5 → 2K3PO4 + 3H2O
Cho 1,12 lít khí CO2(đktc) tác dụng vừa hết với 100ml dung dịch Ba(OH)2, sản phẩm là BaCO3 và H2O.
a. CO2 + Ba(OH)2 → BaCO3 + H2O
b. \({n_{C{O_2}}} = \frac{V}{{22,4}} = \frac{{1,12}}{{22,4}} = 0,05(mol)\)
CO2 + Ba(OH)2 → BaCO3 + H2O
1mol 1mol 1mol
0,05mol 0,05mol 0,05mol
\({C_M} = \frac{n}{V} = \frac{{0,05}}{{0,1}} = 0,5M\)
c. Khối lượng BaCO3 thu được:
\({m_{BaC{O_3}}} = n.M = 0,05.197 = 9,85(g)\)
Bài 3:
Lập công thức hóa học của một oxit kim loại hóa trị II biết rằng cứ 30ml dung dịch HCl nồng độ 14,6% thì hòa tan hết 4,8g oxit đó.
Đặt công thức hóa học của kim loại cần tìm là: RO.
Phương trình hóa học của phản ứng: RO + 2HCl → RCl2 + H2O
Số mol axit HCl: nHCl = 30.14,6100.36,5 = 0,12 mol
Số mol oxit : nRO = 0,12 : 2 = 0,06 mol
Khối lượng mol của oxit là 4,8 : 0,06 = 80g
Phân tử khối của oxit là RO = 80
Nguyên tử khối của R bằng: 80 – 16 = 64 đvc.
Cho 14,5 gam hỗn hợp (Fe, Zn, Mg) tan hết trong H2SO4 loãng , thu được 6,72 lít khí (đktc) và dung dịch A.Cô cạn dung dịch A thu được m (gam) muối.
a) Tính m = ?
b) Tính V lít H2SO4 2M
a. Số mol khí H2 sinh ra là: \(n = \frac{V}{{22,4}} = \frac{{6,72}}{{22,4}} = 0,3(mol)\)
\({n_{{H_2}}} = {n_{{H_2}S{O_4}}} = 0,3(mol)\)
áp dụng định luật bảo toàn điện tích ta có:
mhỗn hợp kim loại + maxit = mmuối + mH2
⇔ 14,5 + 0,3.98 = m + 0,3.2
⇒ m = 43,3 (gam)
b. Thể tích H2SO4 đã dùng là:
\({C_M} = \frac{n}{V} \Rightarrow V = \frac{n}{{{C_M}}} = \frac{{0,3}}{2} = 0,15(lit)\)
Sau bài học cần nắm: tính chất hóa học của hai nhóm chất cơ bản của hóa học vô cơ là Oxit và Axit.
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 5có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho cùng một lượng sắt và kẽm tác dụng hết với axit clohiđric:
Để nhận biết 3 ống nghiệm chứa dung dịch HCl , dung dịch H2SO4 và nước ta dùng:
Cho magiê tác dụng với axit sunfuric đặc nóng xãy ra theo phản ứng sau:
Mg + H2SO4 (đặc,nóng) → MgSO4 + SO2 + H2O. Tổng hệ số trong phương trình hoá học là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 5.
Bài tập 1 trang 21 SGK Hóa học 9
Bài tập 2 trang 21 SGK Hóa học 9
Bài tập 3 trang 21 SGK Hóa học 9
Bài tập 4 trang 21 SGK Hóa học 9
Bài tập 5 trang 21 SGK Hóa học 9
Bài tập 5.1 trang 7 SBT Hóa học 9
Bài tập 5.2 trang 8 SBT Hóa học 9
Bài tập 5.3 trang 8 SBT Hóa học 9
Bài tập 5.4 trang 8 SBT Hóa học 9
Bài tập 5.5 trang 8 SBT Hóa học 9
Bài tập 5.6 trang 8 SBT Hóa học 9
Bài tập 5.7 trang 8 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho cùng một lượng sắt và kẽm tác dụng hết với axit clohiđric:
Để nhận biết 3 ống nghiệm chứa dung dịch HCl , dung dịch H2SO4 và nước ta dùng:
Cho magiê tác dụng với axit sunfuric đặc nóng xãy ra theo phản ứng sau:
Mg + H2SO4 (đặc,nóng) → MgSO4 + SO2 + H2O. Tổng hệ số trong phương trình hoá học là:
Nhỏ từ từ dung dịch axit clohiđric vào cốc đựng một mẩu đá vôi cho đến dư axit. Hiện tượng nào sau đây xảy ra ?
Dãy các kim loại đều tác dụng với dung dịch axit clohiđric:
Trung hòa 200 ml dung dịch H2SO4 1M bằng dung dịch NaOH 20%. Khối lượng dung dịch NaOH cần dùng là:
Hấp thụ hoàn toàn 11,2 lít khí CO2 (đktc) bằng một dung dịch chứa 20 g NaOH. Muối được tạo thành là:
Có thể tinh chế CO ra khỏi hỗn hợp (CO + CO2) bằng cách:
Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Nồng độ phần trăm của dung dịch A là:
Để loại bỏ tạp chất CO2, SO2 ra khỏi khí CO người ta dùng hóa chất nào sau đây?
Có những oxit sau: SO2, CuO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với:
a) Nước.
b) Axit clohidric.
c) Natri hiđroxit?
Viết các phương trình hóa học.
Những oxit nào dưới đây có thể điều chế bằng
a) Phản ứng hóa hợp? Viết phương trình hóa học
b) Phản ứng hóa hợp và phản ứng phân hủy? Viết phương trình hóa học.
(1) H2O;
(2) CuO;
(3) Na2O;
(4) CO2;
(5) P2O5
Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí SO2 và CO2. Làm thế nào có thể loại bỏ được những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất?
Viết các phương trình hóa học?
Cần phải điều chế một lượng muối đồng (II) sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric?
a) Axit sunfuric tác dụng với đồng (II) oxit.
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Giải thích các câu trả lời.
Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình hóa học?
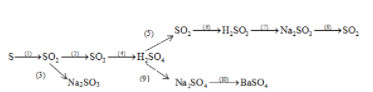
Có những chất sau: Cu, Zn, MgO, NaOH, Na2CO3. Hãy dẫn ra những phản ứng hoá học của dung dịch HCl và dung dịch H2SO4 loãng với những chất đã cho để chứng minh rằng hai axit này có tính chất hoá học giống nhau.
Để phân biệt được hai dung dịch Na2SO4 và Na2CO3 người ta dùng:
A. BaCl2
B. HCl
C. Pb(NO3)2
D. NaOH
Cho những chất sau :
A. CuO
B. MgO
C. H2O
D. SO2
E. CO2.
Hãy chọn những chất thích hợp đã cho để điền vào chỗ trống trong các phương trình hoá học sau :
1. 2HCl + ... → CuCl2 + ...
2. H2SO4 + Na2SO3 → Na2SO4 + ... + ...
3. 2HCl + CaCO3 → CaCl2 +... + ...
4. H2SO4 + ... → MgSO4 + ...
5. ... + ... ⇔ H2SO3
Cho các chất: Cu, Na2SO3, H2SO4.
a) Viết các phương trình hoá học của phản ứng điều chế SO2 từ các chất trên.
b) Cần điều chế n mol SO2, hãy chọn chất nào để tiết kiệm được H2SO4. Giải thích cho sự lựa chọn.
a) Viết các phương trình hoá học của phản ứng điều chế khí hiđro từ những chất sau: Zn, dung dịch HCl, dung dịch H2SO4.
b) So sánh thể tích khí hiđro (cùng điều kiện t° và p) thu được của từng cặp phản ứng trong những thí nghiệm sau :
Thí nghiệm 1:
0,1 mol Zn tác dụng với dung dịch HCl dư.
0,1 mol Zn tác dụng với dung dịch H2SO4 dư.
Thí nghiệm 2:
0,1 mol H2SO4 tác dụng với Zn dư.
0,1 mol HCl tác dụng với Zn dư.
Để tác dụng vừa đủ với 44,8 gam hỗn hợp gồm FeO, Fe2O3, Fe3O4 cần phải dùng 400 ml dung dịch H2SO4 2M. Sau phản ứng thấy tạo ra a gam hỗn hợp muối sunfat. Hãy tính a.
Từ 80 tấn quặng pirit chứa 40% lưu huỳnh, người ta sản xuất được 73,5 tấn axit sunfuric.
a) Tính hiệu suất của quá trình sản xuất axit sunfuric.
b) Tính khối lượng dung dịch H2SO4 50% thu được từ 73,5 tấn H2SO4 đã được sản xuất ở trên.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
1Có 4 dung dịch sau: BaCl2, H2SO4, HCl, Ca(OH)2 đựng trong 4 lọ bị mất nhãn. Bằng phương pháp hóa học hãy nhận biết 4 dung dịch trên?
Câu trả lời của bạn
Dung dịch Ba(OH)2 và dung dịch KOH không có tính chất nào sau đây?
Dãy chất nào sau đây bị nhiệt phân hủy ở nhiệt độ cao:
A. CaCO3, Zn(OH)2, KClO3, KMnO4
B. BaSO3, BaCl2, KOH, Na2SO4
C. Fe(OH)3, Na2SO4, BaSO4, KCl
D.AgNO3, Na2CO3, KCl, BaSO4
23.Tính chất hóa học nào sau đây không phải là của muối:
A. Tác dụng với axit tạo thành muối mới và axit mới.
B.Tác dụng với bazo tạo thành muối mới và bazo mới.
C. Tác dụng với kim loại sinh ra muối mới và khí bay hơi.
D. Bị phân hủy ở nhiệt độ cao.
24. Phân bón nào sau đây có hàm lượng nito cao nhất?
A. NH4NO3
B. NH4Cl
C.(NH4)2SO4
D.(NH2)2CO
Câu trả lời của bạn
Giúp mình với :)
Bài 2: hòa tan 20gam đá vôi CaCO3 bằng dung dịch HCl 2M
a) Viết PTHH
b) Tính thể tích dd HCl cần dùng
c) Tính thể tích khí sinh ra đkc
d) Tính khối lượng muối tạo thành
e) Tính nồng độ mol của dd thu được sau phản ứng
Câu trả lời của bạn
Câu 1 nêu tính chất hóa học của NaOH
Câu 2 hoàn thành chuỗi biến hóa sau:
CuO ->CuCl->Cu(OH)->CuSO4 -> CuCl2
Câu 3 Hòa tan 9,2g hôn hợp gồm: Mg và MgO vào dung dịch HCl 14,6% vừa đủ
Sau phản ứng thu được 1,12 lít khí ở đktc
(cho Mg= 24; Cl = 35,5;H=1;O=16)
Câu trả lời của bạn
để sản xuất đá vôi sống người ta thường để xen kẽ đá than với đá vôi . hãy giải thích vì sao và viết các phản ứng xảy ra
Câu trả lời của bạn
Đểtrung hòa vừa đủ16 gam CuO cần dùng vừa đủ200g dd H2SO4thu được dd A. a.Tính C% của dd H2SO4đã dùng.b.Cho dd A tác dụng vừa đủvới 200 ml dd NaOH tạo ra a gam kết tủa. Tính a vàCMcủa dd NaOH.
Câu trả lời của bạn
CuO + H2SO4 -> CuSO4 + H2O
0,2......>0,2........> 0,2 (mol)
C%dd H2SO4 = (0,2.98/200).100% = 9,8%
m CuSO4 = 0,2.160 = 32(g)
CuSO4 + NaOH -> Cu(OH)2 kết tủa + Na2SO4
0,2...........>0,4.......>0,2. (mol)
Cm dd NaOH = 0,4/0,2 = 2M
m kết tủa Cu(OH)2 = 0,2.98=19,6(g)
Trong quá trình sán xuất công nghiệp sẽ sản sinh ra các chất khí gây ô nhiễm môi trường: Co2, So2.... Hóa chất dùng để hạn chế các chất thải trên là:
Câu trả lời của bạn
Cho 15g hợp kim Nhôm-Magie tác dụng với dd HCl dư. Sau phản ứng thu được 15,68 lít khí(đktc). Tính thành phần % theo khối lượng của mỗi kim loại trong hợp kim ban đầu.
Câu trả lời của bạn
Vôi sống có rất nhiều ứng dụng trong nhiều ngành quan trọng của đời sống. Nó có dạng bột hoặc dạng cục. Trong công nghiệp, người ta sử dụng lò xây bằng gạch chịu lửa và sản xuất theo công nghệ nung liên tục. Lò nung vôi công nghiệp có nhiều ưu điểm là sản xuất vôi liên tục và không gây ô nhiễm không khí. Sau một thời gian nhất định, người ta lại nạp nguyên liệu vào lò, vôi sống được lấy ra qua cửa ở đáy lò; khí carbon dioxide được thu qua cửa lò.
Câu trả lời của bạn
Câu trả lời của bạn
Câu trả lời của bạn
cho 11,2 l CO2 vào 500ml NaOH 25% (D= 1,3 g/ml) . Tính nồng độ mol/lít của dung dịch muối tạo thành :((
Câu trả lời của bạn
Thể Tích nước nguyên chất cần thêm vào 11 dung dịc axit H2SO4 98%(D1,84g/ml) để thu được dd mới có nồng độ 10%
Câu trả lời của bạn
Câu trả lời của bạn
Hợp chất A có công thức hoá học dạng chung la SxOy , trong đó ( x,y là số nguyên dương) (0,5đ)
Khối lượng của hợp chất : mA = 2 + 3 = 5 (gam) (0,5đ)
→ Thành phần phần trăm khối lượng các nguyên tố :
% S = (100.2 / 5).100% = 40% ( 0,5 đ)
% O = ( 3.100 / 5).100% = 60% (0,5 đ)
Ta có tỉ lệ : x / y = (40/32) : (60 / 16) = 1 /3 (0,5đ)
Chọn x = 1 và y = 3 thế vào công thức dạng chung,ta có công thức hoá học là SO3 (0,5đ)
Câu trả lời của bạn
Khi nung nóng đá vôi CaCO3 sẽ phân huỷ thành CaO và khí CO2 thoát ra ngoài nên làm cho khối lượng nhẹ đi . (0,5 đ)
CaCO3 → CaO + CO2
Còn khi nung nóng một que đồng thì khối lượng lại nặng thêm vì đồng hoá hợp với oxi tạo oxit đồng. (0,5 đ)
2Cu + O2 → 2CaO
Câu trả lời của bạn
4480 ml = 4,48 lít (0,25 đ)
Ở đktc,1 mol chất khí có thể tích bằng 22,4 (lít) (0,25 đ)
→ n(O2) = V : 22,4 =4,48 : 22,4 = 0,2 (mol) (0,5 đ)
nNa = mNa : MNa = 9,2 : 23 = 0,4 (mol) (0,5đ)
4Na + O2 → 2Na2O (0,5đ)
4 mol 1 mol
Lập tỉ lệ : 0,4/4 < 0,2/1 sau phản ứng chất dư là oxi (0,5đ)
Ta dựa vào Natri để tính.
Theo PTHH cứ 4 mol Na phản ứng với 1 mol O2 . Vậy 0,4 x mol Na với x mol O2
x = 0,4 . 1 : 4 = 0,1 (mol)
Số mol oxi còn dư là : 0,2 – 0,1 = 0,1 (mol)
Khối lượng oxi còn dư là : m(O2) = n(O2) . M(O2) = 0,1 . 32 = 3,2 (gam)
a. Viết phương trình hóa học của phản ứng.
b. Tính khối lượng mangandioxit tạo thành sau phản ứng ?
c. Tính thể tích chất khí sinh ra sau phản ứng (ở đktc) ?
Câu trả lời của bạn
a.2KMnO4 →t° K2MnO4 + MnO2 + O2 ↑
b. n (KMnO4) = m (KMnO4) : M (KMnO4) = 632: 158 = 4 (mol)
Theo PTHH : cứ 2 mol KMnO4 phân huỷ tạo 1 mol MnO2.Vậy 4 mol KMnO4 phân huỷ tạo x mol MnO2.
x = 4.1 : 2 = 2 (mol)
→ Khối lượng MnO2 tạo thành sau phản ứng là :
m (MnO2) = n (MnO2) . M (MnO2) = 2 . 87 = 174 (gam)
c. Theo PTHH cứ 2 mol KMnO4 phân huỷ tạo thành 1 mol O2.Vậy 4 mol KClO3 phân huỷ tạo thành y mol O2.
→ y = 4 . 1 : 2 = 2 (mol)
Ở đktc 1 mol chất khí có V =22,4 lít nên thể tích khí oxi thu được là:
V (O2) = n(O2) . 22,4 = 2 . 22,4 = 44,8 (lít)
A. 2,44 B. 4,42 C. 24,4 D. 4,24
Câu trả lời của bạn
Ta có:
\({n_{{H_2}}} = 0,03\) → \(n_e^ \uparrow = 0,06\) → \({n_{SO_4^{2 - }}} = 0,03\) → \(m = 1,36 + 0,03.96 = 4,24\)
A. 1,0 B. 0,8 C. 1,2 D. 1,5
Câu trả lời của bạn
Ta có:
\({n_{{H_2}}} = 0,15\) → \({n_e} = 0,3\) → \({n_{O{H^ - }}} = 0,3\) \({→n_{{H^ + }}} = 0,3 = 0,3a\) → a = 1
Câu trả lời của bạn
C + O2 → CO2 (0,25 đ)
12 gam → 44 gam
x gam → 264 gam
→ x = 264 . 12 : 44 = 72 (gam) (0,5 đ)
Khối lượng tạp chất có trong than đá là : mtc = mtđ - mc = 120 – 72 = 48 (gam) (0,25đ)
% tạp chất có trong than đá là : % tc = (48 . 100) / 120 . 100% = 40%

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *