Nội dung bài học nghiên cứu về các vấn đề: Natri hidroxit NaOH và Canxi hidroxit Ca(OH)2 có những tính chất vật lí, tính chất hóa học nào? Những ứng dụng trong đời sống và sản xuất gồm những gì?

Hình 1: Trạng thái tự nhiên của NaOH
NaOH là bazơ tan và có các tính chất hóa học của một bazơ tan:
Dung dịch NaOH làm quì tím chuyển sang màu xanh, phenolphtalein không màu thành màu đỏ.
Video 1: Dung dịch NaOH tác dụng với giấy quỳ và phenolphtalein
Video 2: Phản ứng giữa dung dịch NaOH và HCl
2NaOH + CO2 → Na2CO3 + H2O
NaOH + CO2 → NaHCO3
2NaOH + SO2 → Na2SO3 + H2O
(Sẽ được trình bày cụ thể ở bài 9)
Hình 2: Ứng dụng của NaOH
Hình 3: Điện phân dung dịch NaCl
Tác dụng của màng ngăn xốp: Không cho khí Hiđro và clo tác dụng với nhau (không có màng ngăn xốp không thu được NaOH) H2 + Cl2 → 2HCl
Phương trình phản ứng: 2NaCl + 2H2O (Điện phân dung dịch, có màng ngăn) → 2NaOH + H2 + Cl2
Hình 4: Cách pha chế dung dịch Caxi hidroxit
Phương trình hóa học:
H2SO4 + Ca(OH)2 → CaSO4 + 2H2O
HCl + Ca(OH)2 → CaCl2 + 2H2O
Tuỳ theo tỉ lệ số mol của Ca(OH)2 với số SO2 mà có thể tạo muối trung hoà và nước, muối axit Hoặc cả hai muối.
Phương trình hóa học:
Ca(OH)2 + SO2 → CaSO3 + H2O
Ca(OH)2 + 2SO2 → Ca(HSO3)2
Nếu pH = 7 thì dung dịch là trung tính
Nếu pH > 7 thì dung dịch có tính bazơ ⇒ Nếu pH càng lớn, độ bazơ của dung dịch càng lớn và ngược lại
Nếu pH < 7 thì dung dịch có tính axit ⇒ Nếu pH càng nhỏ, độ axit của dung dịch càng lớn và ngược lại
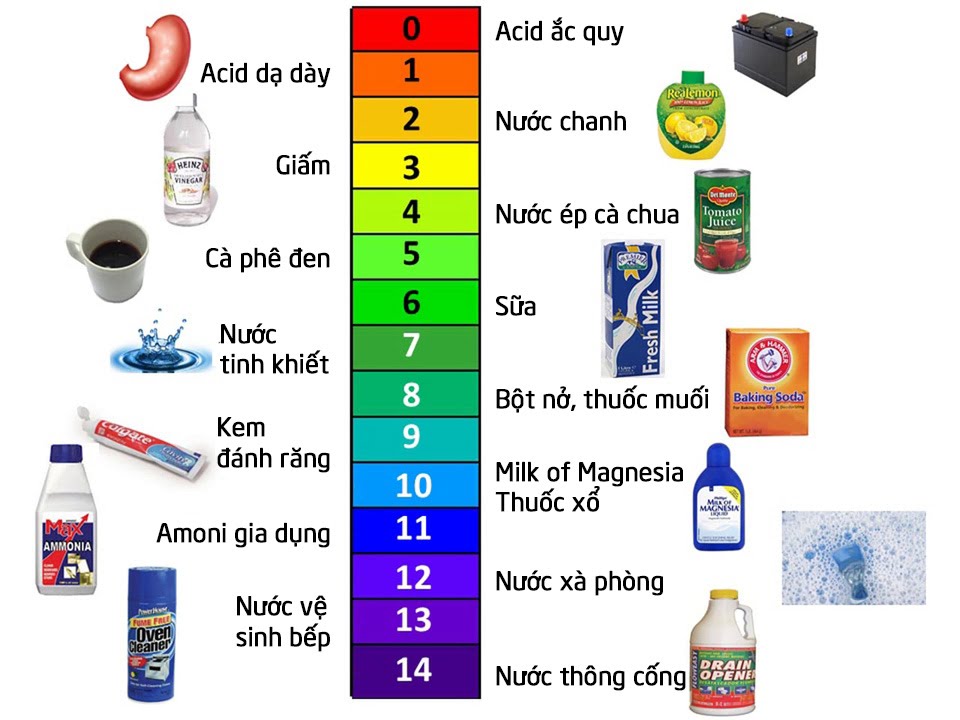
Hình 5: Thang pH
Na2O → NaOH → Na2SO4 → BaSO4
Na2O + H2O → 2NaOH
2NaOH + H2SO4 → Na2SO4 + 2H2O
Hoặc : 2NaOH + SO3 → Na2SO4 + 2H2O
Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Hoặc : Na2SO4 + Ba(NO3)2 → BaSO4 + 2NaNO3
Hoặc : Na2SO4 + Ba(OH)2 → BaSO4 + 2NaOH
Hòa tan 112 g KOH vào nước thì được 2 lit dung dịch. Nồng độ mol của dung dịch thu được là:
Số mol KOH là: \({n_{KOH}} = \frac{m}{M} = \frac{{112}}{{56}} = 2(mol)\)
Nồng độ mol của dung dịch thu được là:
\({C_M} = \frac{n}{V} = \frac{2}{2} = 1M\)
Dẫn V lit CO2 (đktc) vào dung dịch chứa 3,7 gam Ca(OH)2. Sau phản ứng thu được 4 gam kết tủa. Tính V?
Theo bài ra ta có:
Số mol của Ca(OH)2 = \(\frac{{3,7}}{{74}}\) = 0,05 mol
Số mol của CaCO3 = \(\frac{4}{{100}}\) = 0,04 mol
Phương trình hóa học:
CO2 + Ca(OH)2 → CaCO3 + H2O
Nếu CO2 không dư:
Ta có số mol CO2 = số mol CaCO3 = 0,04 mol
Vậy V(đktc) = 0,04 x 22,4 = 0,896 lít
Nếu CO2 dư:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,05 \(\leftarrow\) 0,05 mol → 0,05
CO2 + CaCO3 + H2O → Ca(HCO3)2
0,01 \(\leftarrow\) (0,05 - 0,04) mol
Vậy tổng số mol CO2 đã tham gia phản ứng là: 0,05 + 0,01 = 0,06 mol
V(đktc) = 22,4 x 0,06 = 1,344 lít
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 8có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Thuốc thử để nhận biết dung dịch Ca(OH)2 là:
Nhóm các dung dịch có pH > 7 là:
Để phân biệt hai dung dịch NaOH và Ba(OH)2 đựng trong hai lọ mất nhãn ta dùng thuốc thử:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 8.
Bài tập 1 trang 27 SGK Hóa học 9
Bài tập 2 trang 27 SGK Hóa học 9
Bài tập 3 trang 27 SGK Hóa học 9
Bài tập 1 trang 30 SGK Hóa học 9
Bài tập 2 trang 30 SGK Hóa học 9
Bài tập 3 trang 30 SGK Hóa học 9
Bài tập 4 trang 30 SGK Hóa học 9
Bài tập 8.1 trang 9 SBT Hóa học 9
Bài tập 8.2 trang 9 SBT Hóa học 9
Bài tập 8.3 trang 10 SBT Hóa học 9
Bài tập 8.4 trang 10 SBT Hóa học 9
Bài tập 8.5 trang 10 SBT Hóa học 9
Bài tập 8.6 trang 10 SBT Hóa học 9
Bài tập 8.7 trang 10 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Thuốc thử để nhận biết dung dịch Ca(OH)2 là:
Nhóm các dung dịch có pH > 7 là:
Để phân biệt hai dung dịch NaOH và Ba(OH)2 đựng trong hai lọ mất nhãn ta dùng thuốc thử:
Dãy các bazơ bị phân hủy ở nhiệt độ cao:
Cặp chất đều làm đục nước vôi trong Ca(OH)2 :
Cặp oxit phản ứng với nước ở nhiệt độ thường tạo thành dung dịch bazơ là:
Cho 2,24 lít khí CO2 ( đktc) hấp thụ hoàn toàn bởi 200 ml dung dịch Ca(OH)2 , chỉ thu được muối CaCO3. Nồng độ mol của dung dịch Ca(OH)2 cần dùng là:
Hòa tan 30 g NaOH vào 170 g nước thì thu được dung dịch NaOH có nồng độ là:
Dẫn 22,4 lít khí CO2 ( đktc) vào 200g dung dịch NaOH 20%. Sau phản ứng tạo ra sản phẩm nào trong số các sản phẩm sau:
Xác định chất dư sau phản ứng khi dẫn từ từ 1,568 lít CO2 (đktc) vào dung dịch có hòa tan 6,4g NaOH?
Có 3 lọ không nhãn, mỗi lọ đựng chất rắn sau: NaOH, Ba(OH)2, NaCl. Hãy trình bày cách nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết các phương trình hóa học (nếu có).
Có những chất sau: Zn, Zn(OH)2, NaOH, Fe(OH)3, CuSO4, NaCl, HCl.
Hãy chọn chất thích hợp điền vào mỗi sơ đồ phản ứng sau và lập phương trình học:
a) …..  Fe2O3 + H2O;
Fe2O3 + H2O;
b) H2SO4 + … → Na2SO4 + H2O;
c) H2SO4 + … → ZnSO4 + H2O;
d) NaOH + …. → NaCl + H2O;
e) ….. + CO2 → Na2CO3 + H2O.
Dẫn từ từ 1,568 lít khí CO2 (đktc) vào một dung dịch có hòa tan 6,4 gam NaOH, sản phẩm là muối Na2CO3.
a) Chất nào đã lấy dư và dư là bao nhiêu (lít hoặc gam)?
b) Hãy xác định khối lượng muối thu được sau phản ứng?
Viết các phương trình hóa học thực hiện những chuyển đổi hóa hoặc sau:
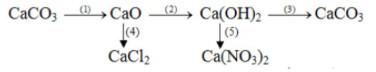
Có ba lọ không nhãn, mỗi lọ đựng một trong ba chất rắn màu trắng sau: CaCO3, CaO, Ca(OH)2. Hãy nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết các phương pháp hóa học?
Hãy viết các phương trình hóa học của phản ứng khi cho dung dịch NaOH tác dụng với dung dịch H2SO4 tạo ra:
a) Muối natri hiđrosunfat.
b) Muối natrisunfat.
Một dung dịch bão hòa khí CO2 trong nước có pH = 4. Hãy giải thích và viết phương trình hóa học của CO2 với nước?
Bằng phương pháp hoá học nào có thể phân biệt được hai dung dịch bazơ: NaOH và Ca(OH)2? Viết phương trình hoá học.
Có 4 lọ không nhãn, mỗi lọ đựng một trong những dung dịch sau: NaOH, Na2SO4, H2SO4, HCl. Hãy nhận biết dung dịch trong mỗi lọ bằng phương pháp hoá học. Viết các phương trình hoá học.
Cho những chất sau: Na2CO3, Ca(OH)2, NaCl.
a) Từ những chất đã cho, hãy viết các phương trình hoá học điều chế NaOH.
b) Nếu những chất đã cho có khối lượng bằng nhau, ta dùng phản ứng nào để có thể điều chế được khối lượng NaOH nhiều hơn ?
Bảng dưới đây cho biết giá trị pH của dung dịch một số chất
A (pH = 13), B (pH = 3); C (pH = 1); D (pH = 7); E (pH = 8)
a) Hãy dự đoán trong các dung dịch ở trên :
Dung dịch nào có thể là axit như HCl, H2SO4
Dung dịch nào có thể là bazơ như NaOH, Ca(OH)2.
Dung dịch nào có thể là đường, muối NaCl, nước cất.
Dung dịch nào có thể là axit axetic (có trong giấm ăn).
Dung dịch nào có tính bazơ yếu, như NaHCO3.
b) Hãy cho biết:
1. Dung dịch nào có phản ứng với Mg, với NaOH.
2. Dung dịch nào có phản ứng với dung dịch HCl.
3. Những dung dịch nào trộn với nhau từng đôi một sẽ xảy ra phản ứng hoá học.
3,04 gam hỗn hợp NaOH và KOH tác dụng vừa đủ với dung dịch HCl, thu được 4,15 gam các muối clorua.
a) Viết các phương trình hoá học.
b) Tính khối lượng của mỗi hiđroxit trong hỗn hợp ban đầu.
Cho 10 gam CaCO3 tác dụng với dung dịch HCl dư.
a) Tính thể tích khí CO2 thu được ở đktc
b) Dẫn khí CO2 thu được ở trên vào lọ đựng 50 gam dung dịch NaOH 40%. Hãy tính khối lượng muối cacbonat thu được.
Cho m gam hỗn hợp gồm Mg(OH)2, Cu(OH)2, NaOH tác dụng vừa đủ với 400 ml dung dịch HCl 1M và tạo thành 24,1 gam muối clorua. Hãy tính m.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Hỗn hợp X gồm CH4và C2H4.Nếu dẫn hỗn hợp X đi qua dung dịch Br2dư thì lượngBr2tham gia phản ứng là 48 gam.Nếu đốt cháy hoàn toàn hỗn hợp X thì sau phản ứng thu được 15,68 lít khí CO2(đktc). Tính thành phần phần trăm theo thểtích mỗi khí trong hỗn hợp X.Cho nguyên tửkhối của: C = 12, O = 16, Br = 80.
Câu trả lời của bạn
Cho 200g dung dịch canxicacbonat CaCO 3 phản ứng vừa đủ với 200g dung dịch axit clohydric HCl tạo
thành 4.48 lít khí ở đktc
a)Viết phương trình hóa học?
b)Tính khối lượng muối tạo thành sau phản ứng ?
d)Tính khối lượng muối tạo thành sau phản ứng?
c)Tính nồng độ phần trăm của dung dịch sau khi phản ứng kết thúc?
Câu trả lời của bạn
Fe --> FeCl2 --> Fe(OH)2 --> FeO --> FeCl2
Câu trả lời của bạn
Fe+ 2HCl--->FeCl2+H2
FeCl2+2NaOH---->Fe(OH)2+2NaCl
Fe(OH)2------> FeO +H2O
FeO + 2HCl---> FeCl2+ H2O
1/Hỗn hợp khí A gồm H2 và 1 hiđrocacbon X mạch hở. Đốt cháy 6 gam A thu được
17,6 gam CO2. Mặt khác, 6 gam A tác dụng vừa đủ với dung dịch chứa 32 gam Br2.
Hỗn hợp khí B gồm H2 và 1 hiđrocacbon Y, mạch hở. Tỉ khối của B so với H2 bằng 3. Đun
nóng B với bột Ni (xt) tới phản ứng hoàn toàn thu được hỗn hợp khí B1 có tỉ khối so với H2
bằng 4,5. Tính % thể tích mỗi khí trong A và B và xác định CTPT của X và Y. Biết chúng là
các chất khí ở đktc.
2/: A là 1 hỗn hợp 2 hiđrocacbon thể khí; B là hỗn hợp O2 và O3. Nếu trộn A và B theo
tỉ lệ 1: 2 về thể tích rồi đốt thì các chất phản ứng vừa vặn hết, tạo ra khí CO2 và nước theo tỉ
lệ 3: 5 về thể tích.
a) Xác định tỉ khối của A đối với H2, biết rằng tỉ khối của B đối với H2 là 17,6.
b) Xác định CTPT và % về thể tích của từng chất trong hỗn hợp A biết rằng nếu dẫn 5 lít
A đi qua dung dịch brom dư thì thể tích khí còn lại là 4 lít.
Các thể tích được đo ở cùng 1 điều kiện.
Câu trả lời của bạn
Fe(So3)3 --> Fecl3 --> fe(OH)3 -->Fe
Câu trả lời của bạn
Câu trả lời của bạn
nCO2 = V/22.4=2.24/22.4=0,1 mol
Có 1 cốc thiếu mg thêm lân lượt vào cốc đó theo thứ tự các chất sau
H2so4 dư, naoh dư, hcl dư, bacl2 dư, naco3 vừa đủ , roiif lóc kết tủa thu đc các chất tan trg dung dịch xác định các chất tan đó
Câu trả lời của bạn
Câu trả lời của bạn
NaOH phản ứng được với Al, CO2, FeSO4, H2SO4.
PTHH:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 (↑)
CO2 + 2NaOH (dư) → Na2CO3 + H2O
FeSO4 + 2NaOH → Fe(OH)2 (↓) + Na2SO4
H2SO4 + 2NaOH → Na2SO4 + 2H2O.
Câu trả lời của bạn
Cu(OH)2 (rắn) + H2SO4 (không màu) → CuSO4 + 2H2O
Hiện tượng: Cu(OH)2 tan dần, sau phản ứng thu được dung dịch có màu xanh lam.
Câu trả lời của bạn
Na2CO3 + Ca(OH)2 → CaCO3 + 2NaOH
→ (a + b) : (c + d) = 2 : 3.
Câu trả lời của bạn
Câu trả lời của bạn
nBa(OH)2 = VBa(OH)2 . CBa(OH)2 = 0,1 . 0,1 = 0,01 mol
nHCl= VHCl. CM HCl = 0,1 . 0,1 = 0,01 mol
PTHH: Ba(OH)2 + 2HCl → BaCl2 + H2O
1 2
0,01 0,01
Từ phương trình ta có tỉ lệ:
0,01/1 > 0,01/2
=> Ba(OH)2 dư => dd có môi trường bazo
=> dd sau phản ứng làm quỳ hóa xanh
Câu trả lời của bạn
n NaOH = 0,2.1 = 0,2 mol
n H2SO4 = 0,1.1 = 0,1 mol
Phương trình hóa học:
2NaOH + H2SO4 → Na2SO4 + 2H2O
0,2 mol 0,1 mol
=>
NaOH và H2SO4 phản ứng vừa đủ với nhau
=> dung dịch thu được có môi trường trung tính => không làm thay đổi màu quỳ tím.
Câu trả lời của bạn
Để điều chế KOH ta cho muối của kali tác dụng với bazo nhưng sau phản ứng phải có kết tủa tạo thành
K2CO3 + Ca(OH)2 → 2KOH + CaCO3↓
Câu trả lời của bạn
Để phân biệt NaOH và Ba(OH)2 ta dùng dung dịch H2SO4
NaOH không có hiện tượng gì còn Ba(OH)2 tạo kết tủa màu trắng
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
Câu trả lời của bạn
Cho 2 dung dịch qua CO2, dd nào xuất hiện kết tủa trắng là Ca(OH)2, còn lại không có hiện tượng là NaOH
CO2 + Ca(OH)2→ CaCO3↓ + H2O
CO2 + NaOH → NaOH + H2O (xảy ra phản ứng nhưng không quan sát được hiện tượng, vì không có gì đặc trưng của phản ứng)
Câu trả lời của bạn
Để phân biệt NaOH và Ba(OH)2 ta dùng dung dịch H2SO4
NaOH không có hiện tượng gì còn Ba(OH)2 tạo kết tủa màu trắng
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
Câu trả lời của bạn
KOH và Ba(OH)2 đều làm đổi màu phenolphtalein và quì tím
KOH và Ba(OH)2 tác dụng với HCl không có hiện tượng
KOH tác dụng với H2SO4 không có hiện tượng; Ba(OH)2 tác dụng với H2SO4 xuất hiện kết tủa trắng
KOH + HCl → KCl + H2O
Ba(OH)2 + 2HCl → BaCl2 + H2O
2KOH + H2SO4 → K2SO4 + H2O
Ba(OH)2 + H2SO4→ BaSO4↓ + H2O
Câu trả lời của bạn
nNaOH = 0,2.1 = 0,2 mol
2NaOH + H2SO4 → Na2SO4 + H2O
0,2 mol 0,1 mol
\({m_{dd{H_2}S{O_4}}} = \frac{{{m_{ct}}.100\% }}{{C\% }} = \frac{{0,1.98.100\% }}{{10\% }}\) = 98g
A. Làm đổi màu quỳ tím và phenophtalein
B. Bị nhiệt phân hủy khi đun nóng tạo thành oxit bazơ và nước
C. Tác dụng với oxit axit tạo thành muối và nước
D. Tác dụng với axit tạo thành muối và nước
Câu trả lời của bạn
Dung dịch NaOH và dung dịch KOH không có tính chất : bị nhiệt phân hủy khi đun nóng tạo thành oxit bazơ và nước.
Vì NaOH và KOH đều là bazơ tan.
Đáp án: B

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *