Benzen là hiđrocacbon khác với metan, etilen, axetilen. Vậy benzen có cấu tạo và tính chất như thế nào, chúng ta hãy cùng nhau tìm hiểu qua bài giảng về Benzen.
Hình 1: Benzen không tan trong nước
Hình 2: Công thức cấu tạo của benzen
Hình 3: Mô hình phân tử Benzen
a) Dạng đặc b) Dạng rỗng
Video 1: Đốt cháy Benzen
Benzen dễ cháy tạo ra CO2 và nước: 2C6H6 + 15O2 → 12CO2 +6H2O
Hình 4: Thí nghiệm Benzen tác dụng với Brom có mặt bột Fe
C6H6 + 3H2 C6H12 (Xiclohexan)
Hình 5: Ứng dụng của benzen
Hình 6: Sơ đồ tư duy bài Benzen
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 39có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Trong phân tử benzen có:
Hợp chất hữu cơ có số nguyên tử hiđro bằng số nguyên tử Cacbon. Hợp chất này tham gia phản ứng thế brôm , không tham gia phản ứng cộng brôm . Hợp chất đó là:
Công thức cấu tạo của benzen có đặc điểm:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 39.
Bài tập 1 trang 125 SGK Hóa học 9
Bài tập 2 trang 125 SGK Hóa học 9
Bài tập 3 trang 125 SGK Hóa học 9
Bài tập 4 trang 125 SGK Hóa học 9
Bài tập 39.1 trang 49 SBT Hóa học 9
Bài tập 39.2 trang 49 SBT Hóa học 9
Bài tập 39.3 trang 49 SBT Hóa học 9
Bài tập 39.4 trang 49 SBT Hóa học 9
Bài tập 39.5 trang 49 SBT Hóa học 9
Bài tập 39.6 trang 49 SBT Hóa học 9
Bài tập 39.7 trang 49 SBT Hóa học 50
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Trong phân tử benzen có:
Hợp chất hữu cơ có số nguyên tử hiđro bằng số nguyên tử Cacbon. Hợp chất này tham gia phản ứng thế brôm , không tham gia phản ứng cộng brôm . Hợp chất đó là:
Công thức cấu tạo của benzen có đặc điểm:
Tính chất vật lí của benzen là:
Đun nóng Brom với 7,8g benzen (có bột sắt), người ta thu được 9,42g Brombenzen. Hiệu suất của phản ứng là:
Cấu tạo đặc biệt của phân tử benzen là:
Công thức hóa học của benzen là:
Chất nào có thể làm mất màu dung dịch brom?
Tính khối lượng benzen cần dùng để điều chế 15,7g brombenzen. Biết hiệu suất phản ứng đạt 80%?
Đốt cháy hoàn toàn ankybenzen X thu được 7,84 lít CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của X là
Cấu tạo đặc biệt của phân tử benzen là:
a) Phân tử có 6 vòng cạnh.
b) Phân tử có ba liên kết đôi.
c) Phân tử có 6 vòng cạnh chứa ba liên kết đôi xen kẽ ba liên kết đơn.
d) Phân tử có 6 vòng cạnh chứa ba liên kết đôi và ba liên kết đơn.
Hãy chọn câu đúng nhất trong các câu trên.
Một số học sinh viết công thức cấu tạo của benzen như sau:
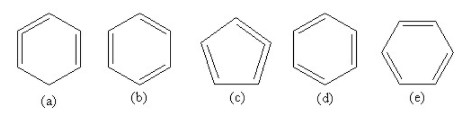
Hãy cho biết công thức nào viết đúng, viết sai, tại sao?
Cho benzen tác dụng với brom tạo ra brombenzen:
a) Viết phương trình hóa học (có ghi rõ điều kiện phản ứng).
b) Tính khối lượng benzen cần dùng để điều chế 15,7g brombenzen. Biết hiệu suất phản ứng đạt 80%.
Hãy cho biết chất nào trong các chất sau đây có thể làm mất màu dung dịch brom. Giải thích và viết phương trình hóa học (nếu có).
a) C6H6.
b) CH2 = CH – CH = CH2.
c) CH3 – C≡ CH.
d) CH3 – CH3.
Benzen không làm mất màu dung dịch brom vì
A. benzen là chất lỏng.
B. phân tử có cấu tạo vòng.
C. phân tử có 3 liên kết đôi.
D. phân tử có cấu tạo vòng, trong đó có 3 liên kết đôi xen kẽ ba liên kết đơn.
Cho benzen vào ống nghiệm đựng dung dịch brom, lắc đều sau đó để yên thấy chất lỏng trong ống nghiệm
A. là đồng nhất và có màu của dung dịch brom.
B. tách thành hai lớp và đều có màu.
C. tách thành hai lớp, lớp ở trên không màu.
D. là đồng nhất và không có màu.
Đốt cháy cùng 1 gam các chất CH4, C2H4, C2H2, C6H6 thu được khí CO2 với khối lượng tương ứng là a, b, c, d gam. Trật tự của a, b, c, d là
A. a < b < c < d
B. b < a < d < c
C. a < b < c = d
D. c = d < b < a
Đốt cháy hiđrocacbon A, người ta thu được CO2 và H2O theo tỉ lệ mCO2 : mH2O = 44 : 9. Biết A không làm mất màu dung dịch brom. Hỏi A là hiđrocacbon nào trong số các hiđrocacbon sau ?
CH ≡CH ; CH3 - CH3 ; CH2 = CH - C = CH ; CH2 = CH2 ;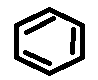
a) Để đốt cháy 0,1 mol benzen cần dùng bao nhiêu lít oxi ở đktc ? Bao nhiêu lít không khí ở đktc ?
b) Từ kết quả trên hãy giải thích tại sao khi benzen cháy trong không khí lại sinh ra nhiều muội than.
Trong những hiđrocacbon sau : CH3-CH2-CH3; CH2=CH2; CH3-CH3; CH≡CH; C6H6 (benzen) những chất nào có phản ứng thế với brom? Có phản ứng cộng với brom? Viết phương trình hoá học minh hoạ và ghi rõ điều kiện phản ứng?
Khi có mặt bột sắt, benzen phản ứng với clo tương tự như phản ứng với brom. Hãy tính lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng với clo dư khi có mặt bột Fe và đun nóng. Biết hiệu suất phản ứng đạt 80%.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Cho mình hỏi benzen có tác dụng được với dung dịch brom không? Cảm ơn các bạn.
Câu trả lời của bạn
Có nha bạn - benzen tác dụng với dung dịch brom tạo thành brombenzen và axit bromhidric .
\(PTHH:C_6H_6Br+Br_2-t^0->C_6H_5Br+HBr\)
biết rằng benzen cũng có phản ứng thế với clo như với brom. cho clo dư tác dụng với 878g benzen( có mặt bột sắt xúc tác) thu được 78g clobenzen. tính hiệu suất của phản ứng
Câu trả lời của bạn
Khi có mặt bột sắt, benzen phản ứng với clo tương tự như phản ứng với brom. Hãy tính lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng với clo dư khi có mặt bột Fe và đun nóng. Biết hiệu suất phản ứng đạt 80%.
Câu trả lời của bạn
Phương trình hoá học của phản ứng giữa benzen và clo
\(C_6H_6+Cl_2\xrightarrow[t^o]{Fe}C_6H_5Cl+HCl\)
Theo phương trình hoá học : số mol C6H6 = số mol C6H5Cl.
Vì hiệu suất 80% và clo dư nên số mol clobenzen thu được là :
\(n_{C6H5Cl}=\dfrac{15,6}{78}.\dfrac{80}{100}=0,16mol\Rightarrow m_{C5H5Cl}=0,16.112,5=18g\)
Lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng hết với Clo (xúc tác Fe), hiệu suất của phản ứng đạt 80% là:
Câu trả lời của bạn
\(C_6H_6+Cl_2\) ( Xúc tác bột Fe ) \(\rightarrow C_6H_5Cl\)
nC6H6 = 0,2 mol.
Suy ra:
nC6H5Cl = 0,2 mol.
mC6H5Cl = 0,2.112,5.0,8 = 18 (g)
Khi có mặt bột sắt, benzen phản ứng với clo tương tự như phản ứng với brom. Hãy tính lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng với clo dư khi có mặt bột Fe và đun nóng. Biết hiệu suất phản ứng đạt 80%.
Câu trả lời của bạn
Phương trình hoá học của phản ứng giữa benzen và clo:
\(C_6H_6+Cl_2\xrightarrow[t^{.0}]{Fe}C_6H_5Cl+HCl\)
Theo phương trình hoá học : số mol C6H6 = số mol C6H5Cl.
Vì hiệu suất 80% và clo dư nên số mol clobenzen thu được là :
\(n_{C_6H_5Cl}=\dfrac{15,6}{78}.\dfrac{8}{100}=0,16\left(mol\right)\Rightarrow m_{C_5H_5Cl}=0,16.112,5=18\left(g\right)\)
Cho 9,75 g benzen phản ứng với brom dư. Hãy tính khối lượng brombenzen thu được sau phản ứng. Biết Hphản ứng = 80%
các bạn giải giúp mình với, sáng mai kiểm tra 15 phút rồi
Câu trả lời của bạn
nC6H6 = 0,125 mol
C6H6 + Br2 → C6H5Br + HBr
0,125..................0,125
⇒ mC6H5Br = 0,125.157.\(\dfrac{80}{100}\) = 15,7 (g)
Tính khối lượng clobenzen thu được khi cho 7,8(g) benzen tác dụng hết với clo với hiệu suất phản ứng là 80%.
Câu trả lời của bạn
n C6H6 = \(\dfrac{7,8}{78}=0,1\) (mol)
n pứ = 0,1 . 80% = 0,08 (mol)
C6H6 + CL2 -> C6H5CL + HCL
0,1 ..............................0,1 (mol)
=> m C6H5Cl = 0,08 . 112,5 = 9(g)
Nêu cách nhận biết 3 chất lỏng đựng riêng biệt
C2H5OH, CH3COOH ,C6H6
Câu trả lời của bạn
Giải thích vì sao axetilen cháy trong không khí với ngọm lửa sáng còn benzen cháy trong không khí với ngọn lửa sáng và nhiều khói đen.
Câu trả lời của bạn
VÌ C2H2 có số nguyên tử C ít hơn số nguyên tử C trong C6H6 nên khi đốt C6H6 sẽ có thể thiếu khoogn khí nên sinh ra muội than còn C2H2 ko sinh ra muội than.
Đốt cháy 10,6g hỗn hợp A gồm CH4 ,benzen , etilen ta thu duoc 26,4g CO2 mặt khác khi cho hỗn hợp A đi qua dung dịch Br2 dư chỉ có 48g br2 sau phản ứng . Tính thành phần phần trăm theo V của mỗi chất khí trong hỗn hợp
Câu trả lời của bạn
Trong hồn hợp A chỉ có etilen tác dụng với dd brom
( Lưu ý: benzen chỉ tác dụng với br2 nguyên chất ko phải ddbrom)
nBr2=0,3 mol
Ta có
C2H4+Br2---->C2H4Br2
0,3<----0,3
m C2H4= 0,3.28=8,4 gam=> m CH4+ m C6H6= m hỗn hợp - mC2H4=10,6-8,4=2,2 (g)
gọi số mol ch4 là x; benzen là y
PT:
CH4+ 2O2--->CO2 +2H2O
x---------------->x
C6H6+ 15/2O2 -----> 6CO2 +3H2O
y----------------------->6y
C2H4+3O2--------> 2CO2+2H2O
0,3------------------->0,6
Ta có hpt:
16x+78.y=2,2
x+ 6y=0 ( bắt đầu chỗ này thấy sai sai) cách giải của mik mik nghĩ là đúng nên có thể đề bài chỗ ta thu được 26,4 gam là số hơi sai
hãy tính lượng brombenzen thu được khi cho 23,4g benzen tác dụng với brom dư khi có mặt bột săt và đun nóng. biết hiệu suất phản ứng là 90%
Câu trả lời của bạn
nC6H6 = 0,3 mol
C6H6 + Br2 → C6H5Br + HBr
0,3........................0,3
⇒ mC6H5Br = 0,3.157.\(\dfrac{90}{100}\) = 42,39 (g)
tính lượng benzen cần dùng để điều chế 31,4g brombenzen. biết hiệu suất đạt 85%
Câu trả lời của bạn
nC6H5Br = 0,2 mol
C6H6 + Br2 → C6H5Br + HBr
0,2 <-----------0,2
⇒ mC6H6 = 0,2.78.\(\dfrac{100}{85}\) = 18,35 (g)
Trình bày phương pháp vật lý và hóa học phân biệt 2 lọ chất lỏng riêng biệt đựng rượu etylic và benzen
Câu trả lời của bạn
- Lấy mẫu thử và đánh dấu
- Cho nước vào các mẫu thử
+ Mẫu thử không tan phân lớp chất ban đầu là bezen
+ Mẫu thử tan không phân lớp chất ban đầu là rượu etylic
Tính khối lượng benzen cần dùng để điều chế được 15.7g brom benzen, biết hiệu suất phản ứng là 65%
Câu trả lời của bạn
nC6H5Br = 0,1 mol
C6H6 + Br2 → C6H5Br + HBr
0,1<-------------0,1
⇒ mC6H6 = 0,1.78.\(\dfrac{100}{65}\) = 12 (g)
tính khối lượng của benzen cần dùng để điều chế được 31,4g brombenzen biết hiệu suất phản ứng là 80%
Câu trả lời của bạn
C6H6 + Br2 \(\rightarrow\) C6H5Br + HBr
n C6H5Br = 31,4 : 157 = 0,2 mol
Theo PTHH : n C6H6 = n C6H5Br = 0,2 mol
\(\Rightarrow\) m C6H6 = 0,2 . 78 = 15,6 g
Vì hiệu suất phản ứng là 80% nên :
m C6H6 cần dùng = 15,6 . 100 : 80 = 19,5 g
Cần bao nhiêu kg oxi để đốt cháy hết 4kg benzen chứa 2,5% tạp chất không cháy?
Câu trả lời của bạn
C6H6+15/2 O2-> 6CO2+3H2O
khối lượng benzen phản ứng (100-2,5)%*4=3,9 (g)
n C6H6= 3,9:( 12*6+1*6)=0,05 ( mol)
n O2=15/2 * 0,05 =0,375 (mol)
mO2= 0,375* 32=12(g)
đốt cháy hoàn toàn 0.78g C6H6 trong không khí thu được CO2 và H2O. Dẫn khí CO2 qua dung dịch Ca(OH)2 dư thu dduocj 1 muối trắng CaCO3. Tính khối lượng CO2, CaCO3 qua thể tích khí O2 thu được ở ĐKTC
Câu trả lời của bạn
nC6H6 = 0,78/78 = 0,01 mol.
C6H6 + 15/2O2 ---> 6CO2 + 3H2O
CO2 + Ca(OH)2 ---> CaCO3 + H2O
nCO2 = 6nC6H6 = 0,06 mol. suy ra: mCO2 = 44.0,06 = 2,64 g.
nCaCO3 = nCO2 = 0,06 mol; mCaCO3 = 6 g.
nO2 = 7,5nC6H6 = 0,075 mol; VO2 = 0,075.22,4 = 1,68 lít.
Tại sao các chất sau làm mất màu dd Brom
a) \(CH_2=CH-CH=CH_2\)
b) \(CH_3-C\equiv CH\)
Câu trả lời của bạn
Vì trong công thức cấu tạo của 2 chất trên có liên kết đôi và liên kết ba, là liên kết kém bền nên dễ đứt ra trong phản ứng hóa học, Br thế chỗ của H.
điều chế benzen trong phòng thí nghiệm
Câu trả lời của bạn
Điều chế benzen(C6H6)
1) Trùng hợp 3 phân tử axetilen(tam hợp)
3C2H2 \(\underrightarrow{xt,600^{0C}}\) C6H6
2) Đóng vòng ankan tương ứng
\(C6H14\underrightarrow{xt,t^{0C}}C6H6+4H2\uparrow\)
(n-hecxan)
câu 4, tính khối lượng benzen cần dùng để điều chế 15,7 gam brombenzen C6H5 Br. biết hiệu suất phản ứng đạt 80%
Câu trả lời của bạn
C6H6 + Br2 \(\rightarrow\) C6H5Br + HBr
n C6H5Br = 15,7 : 157 = 0,1 mol
Theo PTHH : n C6H6 = n C6H5Br = 0,1 mol
\(\Rightarrow\) m C6H6 = 0,1 . 78 = 7,8 g
Vì hiệu suất phản ứng đạt 80% nên :
m C6H6 cần dùng = 7,8 . 100 : 80 = 9,75 g

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *