Nội dung bài học Các oxit của cacbon tìm hiểu về hai hợp chất quan trọng là CO và CO2. Hai oxit này thuộc loại nào? Chúng có những tính chất và ứng dụng gì? để trả lời chúng ta sẽ nghiên cứu về tính chất và ứng dụng của các oxit này.
Công thức phân tử: CO
Phân tử khối: 28
CO là chất khí không màu, không mùi, ít tan trong nước, hơi nhẹ hơn không khí, rất độc.
Ở nhiệt độ thường CO không phản ứng với nước, kiềm và axít.
Ở nhiệt độ cao CO khử được nhiều oxít kim loại
Hình 1: CO khử Cu
Video 1: Phản ứng giữa CO và CuO
Làm nhiên liệu, chất khử, nguyên liệu trong công nghiệp hóa học
Công thức phân tử: CO2
Phân tử khối: 44
CO2 là chất khí không màu, không mùi, nặng hơn không khí, không duy trì sự cháy, CO2 bị nén và làm lạnh thì hoá rắn.
Video 2: Chứng minh CO2 không duy trì sự cháy
Ngọn nến đang cháy, khi rót khí CO2 vào nến tắt
Tác dụng với nước
Hình 2: Khí CO2 phản ứng với nước
Tác dụng với dd bazơ
CO2 + 2NaOH → Na2CO3+H2O
1 mol 2 mol
CO2 + NaOH → NaHCO3(dd)
1 mol 1 mol
2CO2+3NaOH → NaHCO3+Na2CO3
2 mol 3 mol
CO2 chữa cháy, bảo quản thực phẩm, sản xuất nước giải khát có gas, sản xuất xôđa, phân đạm urê.
Khử hoàn toàn 32 gam CuO bằng khí CO dư, thu được m gam kim loại. Giá trị của m là
Phương trình hóa học: CuO + CO Cu + CO2
Số mol Cu = số mol CuO = 0,4 → mCu = 25,6 gam
Cho khí CO dư đi qua ống chứa 0,2 mol MgO và 0,2 mol CuO nung nóng, đến phản ứng hoàn toàn, thu được x gam chất rắn. Giá trị của x là:
Phương trình hóa học: CuO + CO Cu + CO2
0,2 → 0,2
Chất rắn gồm MgO và Cu (vì MgO không phản ứng với CO)
⇒ x = mMgO + mCu = 0,2.(24+16) + 0,2.64 = 20,8g
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 28có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cacbon mono oxit là oxit:
Cacbon đioxit tác dụng được với dãy chất nào sau đây:
Người ta có thể rót khí CO2 từ cốc này sang cốc khác là do tính chất nào sau đây:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 28.
Bài tập 1 trang 87 SGK Hóa học 9
Bài tập 2 trang 87 SGK Hóa học 9
Bài tập 3 trang 87 SGK Hóa học 9
Bài tập 4 trang 87 SGK Hóa học 9
Bài tập 5 trang 87 SGK Hóa học 9
Bài tập 28.1 trang 34 SBT Hóa học 9
Bài tập 28.2 trang 34 SBT Hóa học 9
Bài tập 28.3 trang 34 SBT Hóa học 9
Bài tập 28.4 trang 35 SBT Hóa học 9
Bài tập 28.5 trang 35 SBT Hóa học 9
Bài tập 28.6 trang 35 SBT Hóa học 9
Bài tập 28.7 trang 35 SBT Hóa học 9
Bài tập 28.8 trang 35 SBT Hóa học 9
Bài tập 28.9 trang 36 SBT Hóa học 9
Bài tập 28.10 trang 36 SBT Hóa học 9
Bài tập 28.11 trang 36 SBT Hóa học 9
Bài tập 28.12 trang 36 SBT Hóa học 9
Bài tập 28.13 trang 36 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cacbon mono oxit là oxit:
Cacbon đioxit tác dụng được với dãy chất nào sau đây:
Người ta có thể rót khí CO2 từ cốc này sang cốc khác là do tính chất nào sau đây:
Khi sục khí CO2 vào dung dịch NaOH để vừa tạo thành muối trung hòa vừa tạo thành muối axit thì tỉ lệ số mol của NaOH và CO2 phải là:
Có thể dùng thuốc thử nào sau đây để phân biệt khí CO2 và CO ?
Trong bình chữa cháy chứa khí nào sau đây:
Sục 1,5 mol khí CO2 vào 1,5 mol NaOH thu được muối nào sau đây:
Phản ứng nào sau đây được sử dụng để điều chế CO trong phòng thí nghiệm
Cho hỗn hợp khí gồm CO2 và CO. dùng chất nào sau đây có thể thu được CO2 tinh khiết hơn ?
Một loại đá vôi chứa 80% CaCO3 còn lại là tạp chất trơ. Nung m gam đá này một thời gian thu được 0,78m gam chất rắn. Hiệu suất phân hủy CaCO3 là
Hãy viết phương trình hóa học của CO với:
a) Khí O2
b) CuO.
Cho biết: loại phản ứng, điều kiện phản ứng, vai trò của CO và ứng dụng của mỗi phản ứng đó.
Hãy viết phương trình hóa học của CO2 với dung dịch NaOH, dung dịch Ca(OH)2 trong trường hợp:
a) Tỉ lệ số mol n : n = 1 : 1
b) Tỉ lệ số mol n : n = 2 : 1
Có hỗn hợp hai khí CO và CO2. Nêu phương pháp hóa học để chứng minh sự có mặt của hai khí đó. Viết các phương trình hóa học.
Trên bề mặt hồ nước tôi vôi lâu ngày thường có lớp màng chất rắn. Hãy giải thích hiện tượng này và viết phương trình hóa học.
Hãy xác định thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp CO và CO2, biết các số liệu thực nghiệm sau:
- Dẫn 16 lít hỗn hợp CO và CO2 qua nước vôi trong dư thu được khí A.
- Để đốt cháy A cần 2 lít khí oxi. Các thể tích khí đo được ở cùng điều kiện nhiệt độ và áp suất.
Có 4 lọ đựng 4 khí riêng biệt: oxi, hiđro, clo và cacbon đioxit. Dựa vào tính chất của các chất, làm thế nào để nhận biết được mỗi khí trên ?
So sánh tính chất hoá học của CO và CO2. Cho các thí dụ minh hoạ.
Một em học sinh làm thí nghiệm như sau: Cho một mẩu giấy quỳ tím vào ống nghiệm đựng nước cất, sau đó sục khí CO2 vào ống nghiệm. Màu của giấy quỳ tím có biến đổi không ? Nếu đun nóng nhẹ ống nghiệm thì màu của giấy quỳ tím biến đổi ra sao ? Hãy giải thích và viết các phương trình hoá học, nếu có.
Có những khí sau:
A. Cacbon đioxit
B. Clo
C. Hiđro
D. Cacbon oxit
E. Oxi
Hãy cho biết, khí nào
a) có thể gây nổ khi đốt cháy với oxi.
b) có tính chất tẩy màu khi ẩm.
c) làm đổi màu dung dịch quỳ tím.
d) làm bùng cháy tàn đóm đỏ
Nung nóng 19,15 gam hỗn hợp CuO và PbO với một lượng cacbon vừa đủ trong môi trường không có oxi để oxit kim loại bị khử hết. Toàn bộ lượng khí sinh ra được dẫn vào dung dịch Ca(OH)2 dư, phản ứng xong người ta thu được 7,5 gam chất kết tủa màu trắng.
a) Viết phương trình hoá học của các phản ứng đã xảy ra
b) Xác định thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp ban đầu.
c) Tính khối lượng cacbon cần dùng cho phản ứng khử các oxit
(Cho biết Cu : 64 ; Pb : 207.)
Người ta cần dùng 7,84 lít khí CO (đktc) để khử hoàn toàn 20 gam hỗn hợp CuO và Fe2O3 ở nhiệt độ cao.
a) Viết các phương trình hoá học.
b) Xác định thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp trước và sau phản ứng.
Quá trình nào sau đây không sinh ra khí cacbonic ?
A. Đốt cháy khí đốt tự nhiên.
B. Sản xuất vôi sống.
C. Quá trình hô hấp của người và động vật.
D. Quang hợp của cây xanh.
Hàm lượng khí CO2 trong khí quyển của hành tinh chúng ta gần như là không đổi là vì
A. CO2 không có khả năng tác dụng với các chất khí khác trong không khí.
B. Trong quá trình quang hợp, cây xanh hấp thụ khí CO2, mặt khác một lượng CO2 được sinh ra do đốt cháy nhiên liệu, sự hô hấp của ngưòi và động vật...
C. CO2 hoà tan trong nước mưa.
D. CO2 bị phân hủy bởi nhiệt.
Khí cacbon monooxit (CO) nguy hiểm là do có khả năng kết hợp với hemoglobin trong máu làm mất khả năng vận chuyển oxi của máu. Trong trường hợp nào sau đây, con người có thể bị tử vong do ngộ độc CO ?
A. Dùng bình gas để nấu nướng ở ngoài trời.
B. Đốt bếp lò trong nhà không được thông gió
C. Nổ (chạy) máy ôtô trong nhà xe đóng kín.
D. Cả trường hợp B và C.
Khí CO và CO2 bị coi là chất làm ô nhiễm môi trường vì
A. Nồng độ (%V) CO cho phép trong không khí là 10-20 phần triệu, nếu đến 50 phần triệu sẽ có hại cho não.
B. CO2 tuy không độc nhưng gây hiệu ứng nhà kính làm Trái Đất nóng lên.
C. CO2 cần cho cây xanh quang hợp nên không gây ô nhiễm.
D. Cả hai nguyên nhân A và B.
Cacbon và oxi phản ứng theo phương trình hoá học sau: C + O2 ⟶ CO2
Nếu cho 1,20 gam cacbon phản ứng với 1,68 lít khí oxi (đktc) thì lượng tối đa cacbon đioxit sinh ra là:
A. 1,8 lít
B. 1,68 lít
C. 1,86 lít
D. 2,52 lít
Khí CO sinh ra thường có lẫn một phần khí CO2. Hãy giới thiệu hai phương pháp hoá học có thể thu được khí CO trong phòng thí nghiệm và viết các phương trình hoá học.
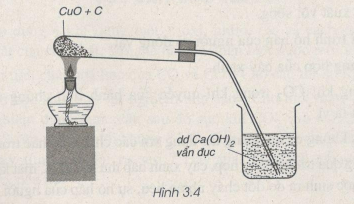
Qua thí nghiệm ở hình vẽ 3.4, em hãy viết phương trình hoá học của phản ứng xảy ra. Phản ứng hoá học này thuộc loại phản ứng nào ?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Hóa 9 Giúp mình với
Cho V lít CO2 đktc tác dụng với dung dịch X có 0,4 mol Ca(OH)2, 0,2 mol NaOH thu được 30 gam CaCO3. Tính V?
Câu trả lời của bạn
Câu trả lời của bạn
Ta có:
nO/hh = nH2O = 1,44/18 = 0,08 mol
⇒ mran = a = mhh - mO/hh = 8,14 - 0,08.16 = 6,86g
Đốt cháy hoàn toàn toàn m gam photpho trong oxi dư thu được chất rắn X. Cho X thu được vào dung dịch KOH sau phản ứng thu được (m+13.45)gam chất rắn. Dung dịch sau phản ứng chứa những chất nào? (các bạn ghi lời giải đầy đủ giúp mình nhé, sáng mai mình phải học rồi)
Câu trả lời của bạn
Câu trả lời của bạn
CO tác dụng với hỗn hợp oxit dư thu được khí X là CO2.
CO2 tác dụng với Ca(OH)2 dư thu được muối duy nhất là kết tủa CaCO3.
⇒ nCO2 = nCaCO3 = 4/100 = 0,04 mol
⇒ nCO = nCO2 = 0,04 mol
⇒ VCO = 0,04.224 = 0,896 lit
Câu trả lời của bạn
CO → CO2
H2 → H2O
⇒ nO/oxit = nCO2+H2 = 0,32/16 = 0,02 mol
Mà khối lượng rắn giảm chính là khối lượng O vào CO và H2.
⇒ nO/oxit = nCO+H2 = 0,32/16 = 0,02 mol
⇒ VCO+H2 = 0,02.22,4 = 0,448 lit
Câu trả lời của bạn
Al2O3 không tác dụng với CO.
Khối lượng chất rắn giảm là khối lượng O trong CuO.
⇒ mO/CuO = moxit - mran = 9,1 - 8,3 = 0,8g
⇒ nO/CuO = nCuO = 0,8/16 = 0,05 mol
⇒ mCuO = 0,05.80 = 4g
Câu trả lời của bạn
H2 khử được các oxit của kim loại đứng sau Al. Suy ra MgO không bị khử.
Hỗn hợp rắn sau phản ứng là: Cu, Fe, Zn, MgO.
2) Cho C tác dụng với khí O2 ở điều kiện nhiệt độ cao;
3) Cho HCl tác dụng với dung dịch muối Na2CO3;
4) Hòa tan kim loại Mg trong dung dịch H2SO4 loãng;
5) Cho khí CO qua bột CuO, nung nóng;
6) Đốt cháy S trong không khí;
Số trường hợp phản ứng tạo chất khí là:
Câu trả lời của bạn
→ Các phản ứng 2, 3, 4, 5, 6 tạo ra chất khí.
Câu trả lời của bạn
nCO2 = 2,24/22,4 = 0,1 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
0,1 0,1
=> mBaCO3 = 0,1.197 = 19,7 gam
Câu trả lời của bạn
nCO2 = 2,24/22,4 = 0,1 mol
CO2 + Ba(OH)2 → BaCO3 + H2O
0,1 0,1
=> CM Ba(OH)2 = 0,1/0,2 = 0,5M
.png)
A. Al2O3, C, CO2 và CaCO3.
B
Câu trả lời của bạn
Đáp án B
A sai do C không phản ứng được với Al2O3.
C sai do O2 không phản ứng với Ca(OH)2
D sai do CO không phản ứng với Ca(OH)2.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O (2)
Các phát biểu sau, phát biểu nào đúng?
A. phương trình (1) chứng tỏ axit H2CO3 là axit không bền. Phương trình (2) chứng tỏ axit H2CO3 có tính axit yếu hơn axit HCl
B. phương trình (1) nói lên axit H2CO3 là axit 2 nấc
C. phương trình (2) nói lên CaCO3 là muối tan được trong nước
D. phương trình (2) có thể xảy ra theo chiều ngược lại
Câu trả lời của bạn
Đáp án A
CO2 + H2O ⇌ H2CO3 (1)
Nghĩa là có sự phân hủy H2CO3.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O (2)
Axit H2CO3 bị axit HCl đẩy ra khỏi muối CaCO3.
Câu trả lời của bạn
nCO2 = 6,72/22,4 = 0,3 mol
nKOH = 0,4 mol => 1 < nKOH/nCO2 < 2
Nên phản ứng tạo ra 2 muối: CO2 + KOH → KHCO3
CO2 + 2KOH → K2CO3 + H2O
Gọi x, y lần lượt là số mol của KHCO3, K2CO3.
Thì nCO2 = x + y = 0,3 và nKOH = x + 2y = 0,4.
Giải ta được y = 0,1 mol, x = 0,2 mol => mK2CO3 = 0,1 x 138 = 13,8 gam.
Câu trả lời của bạn
nCO2 = 6,72/22,4 = 0,3 mol
nKOH = 0,4 mol => 1 < nKOH/nCO2 < 2
Nên phản ứng tạo ra 2 muối: CO2 + KOH → KHCO3
CO2 + 2KOH → K2CO3 + H2O
Gọi x, y lần lượt là số mol của KHCO3, K2CO3.
Thì nCO2 = x + y = 0,3 và nKOH = x + 2y = 0,4.
Giải ta được y = 0,1 mol, x = 0,2 mol => mKHCO3 = 0,2 x 100 = 20 gam.
Câu trả lời của bạn
Phương trình hóa học của sự tôi vôi: CaO + H2O → Ca(OH)2.
Không sinh ra khí CO2.
A. CO2 là chất nặng hơn không khí
B. CO2 là chất khí không màu, không mùi.
C. CO2 không duy trì sự cháy và sự sống.
D. CO2 bị nén và làm lạnh hóa rắn.
Câu trả lời của bạn
Người ta có thể rót khí CO2 từ cốc này sang cốc khác là do tính chất : CO2 là chất nặng hơn không khí
Đáp án: A
A. dung dịch NaCl.
B. dung dịch CuSO4.
C. dung dịch HCl.
D. dung dịch Ca(OH)2 dư.
Câu trả lời của bạn
Để phân biệt khí CO2 và khí CO, ta dùng dung dịch Ca(OH)2 dư vì CO2 tạo kết tủa trắng còn CO không phản ứng
CO2 + Ca(OH)2 → CaCO3 + H2O
Đáp án: D
A. Cl2
B. CO2
C. SO2
D. O2
Câu trả lời của bạn
Trong bình chữa cháy chứa khí CO2
Đáp án: B
Câu trả lời của bạn
Khí CO chỉ khử được các oxit kim loại đứng sau Al => khử được CuO và Fe2O3
Câu trả lời của bạn
Để phòng nhiễm độc CO, là khí không màu, không mùi, rất độc người ta dùng chất hấp thụ là than hoạt tính.
Vì CuO và MnO có phản ứng với CO nhưng ở nhiệt độ cao
MgO không phản ứng với CO

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *