Nội dung bài giảng Cacbon tìm hiểu Đơn chất cacbon có 3 dạng thù hình chính: Kim cương, than chì và cacbon vô định hình; Cacbon vô định hình (than gỗ, than xương, mồ hóng…) có tính hấp phụ và hoạt động hóa học nhất; Sơ lược tính chất vật lí của 3 dạng thù hình; Cacbon là phi kim hoạt động hóa học yếu: Tác dụng với oxi và một số oxit kim loại, tính chất hóa học đặc biệt của cácbon là tính khử ở nhiệt độ cao; Một số ứng dụng tương ứng với tính chất vật lí và tính chất hóa học của cacbon.
Dạng thù hình là những đơn chất khác nhau do nguyên tố đó tạo nên . Ví dụ: O2 (Oxi) và O3 (Ozon)
| Kim cương | Than chì | Cacbon vô định hình (than gỗ, than xương...) | |
| Cấu trúc | 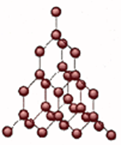 | ||
| Tính chất | Cứng, trong suốt, không dẫn điện | Mềm, dẫn điện | xốp, không dẫn điện. |
Video 1: Khả năng lọc màu của than hoạt tính
Cacbon là phi kim hoạt động hóa học yếu điều kiện xảy ra phản ứng của C với H2 và kim loại rất khó khăn nên ta chỉ xét một số tính chất hóa học có nhiều ứng dụng trong thực tế như sau:
Video 2: Cacbon cháy trong Oxi
Cácbon tác dụng với oxít kim loại: CuO (đen) + C (đen) CO2 (không màu) + Cu (đỏ)
Video 3: Phản ứng giữa Cacbon và Đồng (II) oxit
Ngoài ra ở nhiệt độ cao C còn khử được một số oxít kim loại như ZnO, PbO ...
Hình 1: Ứng dụng của kim cương
Hình 2: Ứng dụng của than chì
Hình 3: Ứng dụng của than muội
Hình 4: Sơ đồ tư duy bài Cacbon
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 27có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Chất dùng làm chất khử một số kim loại ở nhiệt độ cao là:
Để khẳng định một chất bột là cacbon hay oxit sắt , cách làm nào sau đây là đúng?
Dạng thù hình nào của cacbon dẫn điện tốt?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 27.
Bài tập 1 trang 84 SGK Hóa học 9
Bài tập 2 trang 84 SGK Hóa học 9
Bài tập 3 trang 84 SGK Hóa học 9
Bài tập 4 trang 84 SGK Hóa học 9
Bài tập 5 trang 84 SGK Hóa học 9
Bài tập 27.1 trang 33 SBT Hóa học 9
Bài tập 27.2 trang 33 SBT Hóa học 9
Bài tập 27.3 trang 33 SBT Hóa học 9
Bài tập 27.4 trang 33 SBT Hóa học 9
Bài tập 27.5 trang 34 SBT Hóa học 9
Bài tập 27.6 trang 34 SBT Hóa học 9
Bài tập 27.7 trang 34 SBT Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Chất dùng làm chất khử một số kim loại ở nhiệt độ cao là:
Để khẳng định một chất bột là cacbon hay oxit sắt , cách làm nào sau đây là đúng?
Dạng thù hình nào của cacbon dẫn điện tốt?
Khí CO2 bị coi là chất làm ô nhiễm môi trường vì nó
Ở điều kiện thích hợp cacbon có thể phản ứng với các chất CuO, PbO, CO2. Vai trò của cacbon trong các phản ứng này là gì?
Chất nào sau đây không phải dạng thủ hình của cacbon ?
Phản ứng nào trong các phản ứng sau đây, cacbon thể hiện tính oxi hóa ?
Vật liệu dưới đây được dùng để chế tạo ruột bút chì ?
Trong những nhận xét dưới đây, nhận xét nào không đúng ?
Đốt cháy hết m gam than (C) trong V lít oxi thu được 2,24 lít hỗn hợp X gồm 2 khí. Tỉ khối của X so với oxi bằng 1,25. Các thể tích đo được (đktc). Giá trị của m là
Dạng thù hình của nguyên tố là gì? Cho hai ví dụ.
Viết phương trình hóa học của cacbon với các oxit sau:
a) CuO.
b) PbO.
c) CO2.
d) FeO.
Hãy cho biết loại phản ứng: vai trò của C trong các phản ứng, ứng dụng của các phản ứng đó trong sản xuất.
Hãy xác định công thức hóa học thích hợp của A, B, C, D trong thí nghiệm ở hình vẽ bên.
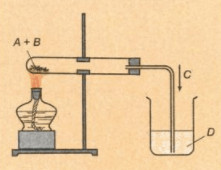
Nêu hiện tượng thí nghiệm và viết phương trình hóa học.
Tại sao sử dụng than để đun nấu, nung gạch ngói, nung vôi gây ô nhiễm môi trường. Hãy nêu biện pháp chống ô nhiễm môi trường và giải thích?
Trong công nghiệp, người ta sử dụng cacbon để làm nhiên liệu. Tính nhiệt lượng tỏa ra khi đốt cháy 5kg than đá chứa 80% cacbon, biết rằng 1 mol cacbon cháy thì tỏa ra 394kJ.
Người ta đã căn cứ vào tính chất vật lí và tính chất hoá học của than để sử dụng than trong thực tế đời sống như thế nào ? Cho thí dụ.
Viết phương trình hoá học của các phản ứng sau và cho biết tính chất hoá học của cacbon (là chất oxi hoá hay chất khử)
C + CO2 to→ CO (1)
C + Fe2O3 to → Fe + CO (2)
C + CaO to→ CaC2 + CO (3)
C + PbO to→ Pb + CO2 (4)
C + CuO to→ Cu + CO2 (5)
Trong quá trình luyện quặng sắt thành gang, người ta dùng CO làm chất khử. Hãy tính thể tích khí CO (đktc) có thể thu được từ 1 tấn than chứa 90% cacbon, nếu hiệu suất của cả quá trình phản ứng là 85%.
Viết phương trình hóa học biểu diễn những chuyển đổi hóa học sau:
a) C → CO2 → CaCO3 → CaO → Ca(OH)2 → Ca(HCO3)2
b) Fe2O3 → Fe → FeCl3 → Fe(OH)3 → Fe2O3
Fe → FeCl2 → Fe(OH)2
Cho hơi nước đi qua than nóng đỏ, người ta thu được hỗn hợp khí CO và H2 (hình 3.3).
a) Viết phương trình hoá học.
b) Tính thể tích hỗn hợp khí (đktc) thu được ở phản ứng trên khi dùng hết 1 tấn than chứa 92%
Cho 268,8 m3 hỗn hợp khí CO và H2 khử sắt(III) oxit ở nhiệt độ cao.
a) Viết phương trình hoá học.
b) Tính khối lượng sắt thu được.
Đem nung hỗn hợp hai oxit CuO và ZnO có tỉ lệ số mol là 1 : 1 với cacbon trong điều kiện thích hợp để oxit kim loại bị khử hết, thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí (ở đktc). Hãy tính khối lượng mỗi oxit kim loại.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
a)Viết phương trình hóa học xảy ra
b)Giá trị của a là bao nhiêu?
c) Xác định thành phần % các muối thu được sau phản ứng
Câu trả lời của bạn
a) Các PTHH xảy ra:
2FeO + C \(\xrightarrow{{{t^0}}}\) 2Fe + CO2 (1)
CO2 + NaOH → NaHCO3 (2)
CO2 + 2NaOH → Na2CO3 + H2O (3)
2NaHCO3 + 2KOH → Na2CO3 + K2CO3 + 2H2O (4)
b) \({n_{FeO}} = \frac{{18}}{{72}} = 0,25\,(mol)\,\,;\,\,{n_{KOH}} = 0,1.1 = 0,1\,(mol)\)
nCO2 = ½ nFeO = 0,25/2 = 0,125 (mol)
Toàn bộ CO2 hấp thụ vào NaOH thu được dd A . Dd A phản ứng được với KOH nên trong dung dich A chắc chắn phải có NaHCO3
Vậy khi CO2 phản ứng với dd NaOH có thể xảy ra các trường hợp sau:
TH1: Chỉ xảy ra phản ứng tạo muối NaHCO3.
NaOH phản ứng hết, CO2 hết hoặc dư, mọi tính toán theo NaHCO3
CO2 + NaOH → NaHCO3 (2)
0,1 ←0,1 ←0,1 (mol)
nCO2(2) = nNaHCO3 = 0,1 (mol) < 0,125 mol => CO2 dư => không phù hợp với bài toán là hấp thụ hết CO2 => loại
TH2: Xảy ra phản ứng tạo muối Na2CO3 và NaHCO3. Cả CO2 và NaOH đều phản ứng hết
CO2+ NaOH → NaHCO3 (2)
0,1 ←0,1 ←0,1
CO2 + 2NaOH → Na2CO3 + H2O (3)
(0,125-0,1) → 0,05→ 0,025 (mol)
∑ nNaOH = 0,1 + 0,05= 0,15 (mol)
=> CM NaOH = nNaOH : VNaOH = 0,15 : 0,1 = 1,5 (M)
c)
Sau phản ứng dd A với KOH thu được dd B có chứa: Na2CO3 và K2CO3
2NaHCO3 + 2KOH → Na2CO3 + K2CO3 + 2H2O (4)
0,1 ←0,1 → 0,05 →0,05 (mol)
nK2CO3(4) = 1/2nKOH = ½. 0,1 = 0,05 (mol) => mK2CO3(4) = 0,05. 138 = 6,9 (g)
∑ nNa2CO3 = nNa2CO3 (3) + nNa2CO3(4) = 0,025 + 0,05 = 0,075 (mol)
=> ∑ mNa2CO3 = 0,075.106 = 7,95 (g)
Tổng khối lượng 2 muối là: m = mK2CO3 + mNa2CO3 = 6,9 + 7,95 = 14,85(g)
\(\begin{gathered}
\% {K_2}C{O_3} = \frac{{{m_{{K_2}C{O_3}}}}}{{m{\,_{hh\,muoi}}}}.100\% = \frac{{6,9}}{{14,85}}.100\% = 46,46\% \hfill \\
\% N{a_2}C{O_3} = 100\% - 46,46\% = 53,54\% \hfill \\
\end{gathered} \)
A. than chì
B. than cốc
C. than nâu
D. than antranxit
Câu trả lời của bạn
Than cốc không có trong thiên nhiên
Câu trả lời của bạn
mC = 10 . 84% = 8,4kg = 8400g
=> nC = mC : MC = 8400 : 12 = 700mol
Lượng nhiệt tỏa ra Q = 700 . 396 = 277200kJ
A. Hidro
C. Kim loại
D. KClO
Câu trả lời của bạn
Cacbon không tác dụng trực tiếp với halogen( Cl
Câu trả lời của bạn
Cacbon có 3 dạng thù hình
A. Kim cương, than chì, cacbon vô định hình
C. Kim cương, than chì, than đá
D. Than đá, than mỡ, than gỗ, than hoa,...
Câu trả lời của bạn
Nguyên tố C có các dạng thù hình là: Kim cương, than chì, Flueren, cacbon vô định hình
A. Đều có cấu tạo mạng tinh thể nguyên tử
C. Có tính chất vật lý tương tự nhau.
D. Cả A và B
Câu trả lời của bạn
Kim cương và than chì là hai dạng thù hình của cacbon vì: Đều do nguyên tử cacbon tạo nên
A. Tinh thể kim cương
B. Tinh thể than chì
C. Cacbon vô định hình
D. Các dạng đều hoạt động mạnh như nhau
Câu trả lời của bạn
Trong các dạng tồn tại của cacbon, Cacbon vô định hình hoạt động hóa học mạnh nhất
A. Cacbon monooxit không tạo muối và là một chất khử mạnh
C. Than gỗ được dùng để chế thuốc súng, thuốc pháo, chất hấp phụ
D. Than muội được dùng để làm chất độn cao su, sản xuất mực in, xi đánh giày
Câu trả lời của bạn
Nhận định sai: Ở nhiệt độ cao, cacbon có thể khử được tất cả các oxit kim loại giải phóng kim loại
A. Chúng có thành phần cấu tạo nguyên tố khác nhau
B. Kim cương là loại kim loại, còn than chì là phi kim
C. Chúng có kiến trúc cấu tạo khác nhau
D. Kim cương cứng còn than chì mềm
Câu trả lời của bạn
Kim cương và than trì là các dạng thù hình của nguyên tố cacbon nhưng lại có nhiều tính chất khác nhau như độ cứng, khả năng dẫn điện. Chúng khác nhau là do chúng có kiến trúc cấu tạo khác nhau
A. Trong mỗi lớp vỏ của tinh thể than chì, mỗi nguyên tử cacbon liên kết theo kiểu cộng hóa trị với ba nguyên tử cacbon lân cận
C. Trong tinh thể than chì, các lớp liên kết với nhau bằng lực Van deVan yếu
D. Than chì được dùng làm điện cực, chế chất bôi trơn,..
Câu trả lời của bạn
Nội dung sai: Trong tinh thể than chì, khoảng cách giữa hai nguyên tử cacbon thuộc hai lớp lân cận ngắn hơn độ dài liên kết C- C
1) Phải đốt bao nhiêu gam cacbon để khi cho khí CO2 tạo ra trong pứ trên tác dụng với 3,4 lít dd NAOH 0,5M ta đc 2 muối với nồng độ mol muối hidrocacbonat bằng 1,4 lần nồng độ mol của muối trung hòa?
2) Nếu thêm một lượng vừa đủ dd CaCl2 1M thì sẽ đc bao nhiêu gam kết tủa? Tính thể tích dd CaCl2 phải dùng
Câu trả lời của bạn
1) CO2+NaOH-->NaHCO3
CO2+2NaOH-->Na2CO3+H2O
nNaOH=1,7mol
tỉ lệ nồng độ mol=tỉ lệ số mol
-->1,4nNaHCO3=nNa2CO3
gọi nNa2CO3=x--->nNaHCO3=1,4x
-->nNaOH(1)=1,4x, nNaOH(2)=2x
hay 1,7=1,4x+2x
-->x=0,5
-->tổng số mol CO2=1,2mol
-->mC=1,2.12=14,4g
2) Khi thêm lượng vừa đủ dung dịch CaCl2 vào dung dịch chứa 2 muối trên chỉ xảy ra p/ư:
CaCl2 + Na2CO3 ---> CaCO3 (rắn)+ 2NaCl (3)
Từ p/ư (3): số mol CaCl2 = số mol Na2CO3 = số mol CaCO3 = 3,4x 5/34 = 0,5 (mol)
=> Khối lượng kết tủa CaCO3 = 0,5 . 100 = 50 (g)
=> Thể tích dung dịch CaCl2 phải dùng: 0,5 : 1 = 0,5 lít.
Đốt một mẫu than đá (chứa tạp chất không cháy) có khối lượng 0,600kg trong oxi dư, thu được 1,06 m3 (đktc) khí cacbonic. Tính thành phần phần trăm khối lượng của cacbon trong mẫu than đá trên.
Câu trả lời của bạn
C + O2 CO2
1,00mol 1,00mol
47,3 mol = 47,3 (mol)
Phần trăm khối lượng của C trong mẫu than đá: = 94,6%
cong thuc cua kim cuong la gi
Câu trả lời của bạn
Công thức của kim cương là C
Cho 2,688 lít hỗn hợp khí A (đktc) gồm 40%V là O2, còn lại là N2. Đốt cháy m gam Cacbon thu được 7,95% O2, còn lại là N2, CO và CO2. Tỉ khối của B so với H2 là 15,67.
a) Tính m.
b) Tính % mỗi khí trong B.
Câu trả lời của bạn
a./ n(A) = 2,688/22,4 = 0,12mol
Số mol các khí trong hh A ban đầu:
n(O2) = 40%.n(A) = 0,12.40% = 0,048mol; n(N2) = n(A) - n(O2) = 0,12 - 0,048 = 0,072mol
Gọi x, y là số mol hai khí CO và CO2
C + 1/2O2 → CO
x x/2 x
C + O2 → CO2
y y y
n(O2 dư) = n(O2) - n(O2 pư) = 0,048 - x/2 - y
n(B) = n(O2 dư) + n(N2) + n(CO) + n(CO2) = 0,048 - x/2 - y + 0,072 + x + y = 0,12 + x/2
O2 chiếm 7,95% thể tích hh B ⇒ n(O2 dư) = 7,95%.n(B)
⇒ 0,048 - x/2 - y = 7,95%.(0,12 + x/2) = 0,00954 + 0,03975x
⇒ 0,5397x + y = 0,03846 [1]
Khối lượng hh khí A: m(A) = m(O2) + m(N2) = 0,048.32 + 0,072.28 = 3,552g
m(B) = m(A) + m(C) = 3,552 + 12.(x+y)
Khối lượng mol trung bình của hh B:
M(B) = m(B)/n(B) = (3,552 + 12x + 12y)/(0,12 + x/2) = 15,67.2 = 31,34 g/mol
⇒ 3,67x - 12y = -0,2088 [2]
Giải hệ PT [1], [2] ta được:x = 0,025mol và y =0,025mol
Khối lượng C đem đốt cháy: m(C) = 12.(x+y) = 12.(0,025+0,025) = 0,6gam
b./ Số mol các khí có trong hh B:
n(CO) = 0,025mol; n(CO2) = 0,025mol; n(N2) = 0,072mol
n(O2 dư) = 0,048 - x/2 - y = 0,048 - 0,025/2 - 0,025 = 0,0105mol
n(B) = 0,12 + x/2 = 0,12 + 0,025/2 = 0,1325mol
% thể tích bằng % số mol nên thành phần % thể tích của hh B là:
%O2 dư = n(O2)/n(B) .100% = 0,0105/0,1325 .100% = 7,92%
%CO = 18,87%; %CO2 = 18,87% và %N2 = 54,34%
Củi than cháy đc trong kk. Nhà e có củi than xếp trong hộc bếp. Tại sao củi than đó lại k cháy
Giúp mình với
Câu trả lời của bạn
củi , than chất đc trong không khí phải có mồi của ngọn lửa dể nâng nhiệt độ cháy. còn than, củi trong hộc bếp có không khí nhưng không cháy vì ở nhiệt độ thấp hơn nhiệt độ cháy
Khí X là hợp chất của cacbon và hiđro có tỉ khối so với khí H2 bằng 14. Tính khối lượng mol phân tử của khí X.
Câu trả lời của bạn
MX=14.2=28 g/mol
tại vùng nông thôn người dân phải lấy nước sông hoặc nước giếng khoan để dùng trong sinh hoạt hàng ngày để nước sinh hoạt được bảo đảm người ta phải lọc nước cấu tạo của bể lọc như sau (hình 14.7)
em hãy cho biết vai trò của lớp than hoạt tính trong bể lọc nước nói trên
Câu trả lời của bạn
Than hoạt tính là một chất có tính hấp phụ cao. Than hoạt tính có thể hấp thụ các kim loại nặng, chất hữu cơ,...từ đó loại bỏ các chất độc hại ra khỏi nước.
ở nhiệt độ cao trong lò điện,cacbon tác dụng với vôi sống tạo ra canxicacbua theo pthh:
3C+CaO--->CaC2+CO
phải dùng bao nhiêu kg cacbon để thu được 128kg đất đèn?
Câu trả lời của bạn
Theo đề: nCaC2 = \(\dfrac{128}{40+12.2}=2\left(Kmol\right)\)
Mặt khác, theo phương trình: nC = 3nCaC2 = 3 . 2 = 6 (Kmol)
\(\Rightarrow\) mC cần dùng = 6.12 = 72(Kg)
Vậy cần dùng 72 (Kg) C đề thu được 128 (Kg) đất đèn
1.viết các phương trình hóa học chuyển đổi sau: C→CO2→CaCO3→CaO→Ca(OH)3.
Câu trả lời của bạn
C + O2 ---to---> CO2
CO2 + CaO → CaCO3
CaCO3 ---to---> CaO + CO2
CaO + H2O → Ca(OH)2

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *