Khoa học tự nhiên 7 Chân trời sáng tạo Bài 2 được DapAnHay biên soạn tóm tắt nội dung bài Nguyên tử chương trình KHTN lớp 7. Nội dung tóm tắt lại các ý chính trong bài, giúp các em học sinh đến nắm chắc nội dung cần học. Đây cũng sẽ là tài liệu hay giúp cho việc dạy và học của quý thầy cô trong việc Khoa học tự nhiên 7 Chân trời sáng tạo Bài 2 và các em học sinh trở nên dễ dàng và hiệu quả hơn.
- Các chất đều được tạo nên từ những hạt vô cùng nhỏ, gọi là nguyên tử.
Ví dụ: Mỗi thanh thép chứa hàng tỉ tỉ nguyên tử iron (sắt)
- Theo Ernest Rutherford, nguyên tử có cấu tạo gồm:
+ Hạt nhân: ở bên trong mang điện tích dương
Ví dụ: Nguyên tử nitrogen có 7p trong hạt nhân, điện tích hạt nhân của nitrogen là +7, số đơn vị diện tích hạt nhân là 7.
+ Vỏ: tạo bởi một hay nhiều electron (kí hiệu là e) mang điện tích âm. Mỗi electron mang một đơn vị điện tích âm, quy ước là -1.
+ Trong nguyên tử: số hạt proton = số hạt electron
Hình 2.4. Mô hình nguyên tử của Rutherford
- Dựa trên mô hình của Rutherford, Niels Bohr đã phát triển một mô hình hoàn chỉnh hơn để mô tả về nguyên tử.
+ Nguyên tử gồm các electron được sắp xếp thành từng lớp và chuyển động xung quanh hạt nhân theo quỹ đạo tương tự như hành tinh trong hệ Mặt Trời.
+ Các electron chuyển động rất nhanh xung quanh hạt nhân và phân bố theo từng lớp với số lượng electron nhất định trên mỗi lớp ở vỏ nguyên tử.
+ Lớp đầu tiên gần sát hạt nhân chứa tối đa 2 electron, lớp thứ hai chứa tối đa 8 electron,...Các electron được sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
Hình 2.5. Mô hình cấu tạo của một số nguyên tử (Mô hình của Rutherford – Bohr)
- Năm 1932, khi nghiên cứu sâu hơn về nguyên tử, James Chadwick phát hiện bên trong hạt nhân còn có một loại hạt không mang điện. Ông gọi chúng là neutron.
Hình 2.6. Mô hình nguyên tử oxygen (O)
- Khối lượng nguyên tử bằng tổng khối lượng của các hạt proton, neutron, electron có trong nguyên tử.
- Khối lượng nguyên tử rất nhỏ, để biểu thị khối lượng nguyên tử, người ta sử dụng đơn vị khối lượng nguyên tử, viết tắt là amu (atomic mass unit).
1 amu = 1,6605.10-24 gam
- Proton và neutron có khối lượng xấp xỉ bằng nhau (gần bằng 1 amu). Electron có khối lượng rất bé (khoảng 0,00055 amu). Khối lượng hạt nhân được xem là khối lượng của nguyên tử.
Ví dụ:
- Nguyên tử hydrogen có 1 p trong hạt nhân nên khối lượng nguyên tử xấp xỉ là 1 amu.
- Nguyên tử carbon có 6 p và 6 n trong hạt nhân nên khối lượng nguyên tử xấp xỉ là 12 amu.
|
Bài 1: Mọi vật thể tự nhiên hay nhân tạo đều được tạo thành từ một số loại hạt vô cùng nhỏ bé gọi là nguyên tử. Vậy nguyên tử có cấu tạo như thế nào?
Hướng dẫn giải
- Cấu tạo của nguyên tử gồm: hạt nhân và vỏ
- Hạt nhân: mang điện tích dương
- Vỏ: tạo bởi các electron (kí hiệu e) mang điện tích âm
Bài 2: Quan sát mô hình nguyên tử carbon và cho biết:
a) Số proton và số electron
b) Điện tích hạt nhân và số đơn vị điện tích hạt nhân
c) Số lớp electron và số electron trên mỗi lớp?
d) Xác định khối lượng nguyên tử carbon (biết số neutron bằng 6)
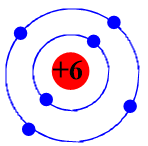
Mô hình nguyên tử carbon (C)
Hướng dẫn giải
a) Số p = số e = 6
b) Điện tích hạt nhân bằng +6. Số đơn vị điện tích hạt nhân bằng 6.
c) Có 2 lớp electron. Lớp 1 có 2 electron, lớp 2 có 4 electron.
d) Khối lượng hạt nhân được xem là khối lượng của nguyên tử.
Khối lượng của nguyên tử carbon: 6 + 6 = 12 (do khố lượng 1 p ≈ 1n ≈ 1 amu)
Bài 3: Nhôm (aluminium) là kim loại có nhiều ứng dụng trong thực tiễn, được dùng làm dây dẫn điện, chế tạo các thiết bị, máy móc trong công nghiệp và nhiều đồ dùng sinh hoạt. Cho biết tổng số hạt trong hạt nhân nguyên tử nhôm là 27, số đơn vị điện tích hạt nhân là 13. Tính số hạt mỗi loại trong nguyên tử nhôm và cho biết điện tích hạt nhân của nhôm?
Hướng dẫn giải
- Vì hạt nhân gồm có proton và neutron
→ Tổng số hạt trong hạt nhân = số proton + số neutron
→ 27 = số proton + số neutron
- Mà số đơn vị điện tích hạt nhân = số proton = 13 = số electron
→ Số neutron = 27 – 13 = 14
Vậy trong nguyên tử nhôm có: 13 hạt electron, 13 hạt proton, 14 hạt neutron
Học xong bài học này, em có thể:
- Trình bày được mô hình nguyên tử của Rutherford - Bohr (mô hình sắp xếp electron trong các lớp electron ở Vỏ nguyên tử).
- Nêu được khối lượng của một nguyên tử theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử).
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Khoa học tự nhiên 7 Chân trời sáng tạo Bài 2 cực hay có đáp án và lời giải chi tiết.
Nguyên tử được cấu tạo bởi các loại hạt nào?
Hạt nhân được cấu tạo bởi:
Trong nguyên tử, hạt mang điện là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Khoa học tự nhiên 7 Chân trời sáng tạo Bài 2để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Mở đầu trang 14 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Thảo luận 1 trang 14 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Thảo luận 2 trang 14 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Thảo luận 3 trang 15 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Thảo luận 4 trang 15 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Thảo luận 5 trang 16 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Thảo luận 6 trang 17 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Luyện tập trang 16 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Luyện tập trang 17 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 1 trang 17 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Giải bài 2 trang 17 SGK Khoa học tự nhiên 7 Chân trời sáng tạo - CTST
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Khoa học tự nhiên DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Nguyên tử được cấu tạo bởi các loại hạt nào?
Hạt nhân được cấu tạo bởi:
Trong nguyên tử, hạt mang điện là:
Chọn đáp án sai:
Cho các phát biểu sau:
1). Khối lượng nguyên tử tập trung phần lớn ở lớp vỏ
(2). Trong nguyên tử, số electron bằng số proton
(3). Trong hạt nhân nguyên tử, hạt mang điện là proton và electron
(4). Trong nguyên tử, hạt electron có khối lượng không đáng kể so với các hạt còn lại
Số phát biểu đúng là:
Điều nào sau đây mô tả đầy đủ thông tin nhất về proton?
Một đơn vị khối lượng nguyên tử (1 amu) theo định nghĩa có giá trị bằng
Trong các nguyên tử sau, nguyên tử nào có khối lượng nguyên tử lớn nhất?
Tổng số hạt trong hạt nhân của nguyên tử A là 24 hạt, trong đó số hạt không mang điện là 12. Tính số electron của nguyên tử A?
Quan sát mô hình nguyên tử sodium dưới đây:
Mô hình nguyên tử sodium (Na)
Chọn phát biểu không đúng:
Từ những vật thể đơn giản như cây bút, quyển vở, chai nước cho đến những công trình nổi tiếng như tháp Eiffel,… đều được tạo nên từ chất. Mỗi chất lại được tạo nên từ những hạt vô cùng nhỏ. Những hạt đó là gì?
Những đối tượng nào trong Hình 2.1 ta có thể quan sát bằng mắt thường? Bằng kính lúp? Bằng kính hiển vi?
Hình 2.1. Kích thước của một số vật thể
Quan sát Hình 2.2, em hãy cho biết khí oxygen, sắt, than chì có đặc điểm chung gì về cấu tạo.
Hình 2.2. Mô phỏng cấu tạo của một số chất
Theo Rutherford – Bohr, nguyên tử có cấu tạo như thế nào?
Quan sát Hình 2.5, hãy cho biết nguyên tử nitrogen và potassium có bao nhiêu
a) điện tích hạt nhân nguyên tử?
b) lớp electron?
c) electron trên mỗi lớp?
Hình 2.5. Mô hình cấu tạo của một số nguyên tử
Tại sao nguyên tử trung hòa về điện?
Vì sao người ta thường sử dụng amu làm đơn vị khối lượng nguyên tử?
Cho biết các thành phần cấu tạo nên nguyên tử trong hình minh họa sau:
Quan sát Hình 2.6, hãy hoàn thành bảng sau:
| Số đơn vị điện tích hạt nhân | Số proton | Số electron trong nguyên tử | Số electron ở lớp ngoài cùng |
| ? | ? | ? | ? |
Để lớp electron ngoài cùng của nguyên tử oxygen có đủ số electron tối đa thì cần thêm bao nhiêu electron nữa?
Hình 2.6. Mô hình nguyên tử oxygen (O)
Quan sát mô hình dưới đây, cho biết số proton, số electron và xác định khối lượng nguyên tử magnesium (biết số neutron = 12)
Mô hình nguyên tử magnesium (Mg)
Em hãy điền vào chỗ trống các từ, cụm từ thích hợp sau để được câu hoàn chỉnh:
| chuyển động | các electron | hạt nhân | điện tích dương | trung hòa về điện |
| vỏ nguyên tử | điện tích âm | vô cùng nhỏ | sắp xếp |
|
Nguyên tử là hạt...(1) và (2)...Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm 2 phần là (3)...(mang (4)...) và (5)... tạo bởi (6)... (mang (7)...).
Trong nguyên tử, các electron (8)... xung quanh hạt nhân và (9)... thành từng lớp.
Vì sao nói khối lượng hạt nhân được coi là khối lượng nguyên tử?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Hãy chọn từ/ cụm từ thích hợp cho sẵn dưới đây để điền vào chỗ …. trong mỗi câu sau: proton, neutron, electron, hạt nhân nguyên tử, vỏ nguyên tử, nguyên tử.
a) Trong nguyên tử, số proton bằng số …..
b) Hạt nhân nguyên tử gồm ….. và …..
c) Phần lớn khối lượng nguyên tử tập trung ở …..
d) Trong hạt nhân nguyên tử, hạt ….. không mang điện.
Câu trả lời của bạn
a) Trong nguyên tử, số proton bằng số electron.
b) Hạt nhân nguyên tử gồm proton và neutron.
c) Phần lớn khối lượng nguyên tử tập trung ở hạt nhân nguyên tử.
d) Trong hạt nhân nguyên tử, hạt neutron không mang điện.
Mỗi phát biểu sau là đúng hay sai?
a) Các hạt electron được tìm thấy ở hạt nhân của nguyên tử.
b) Các hạt neutron và electron hút nhau.
c) Trong nguyên tử, số electron tối đa ở lớp electron thứ hai là 8.
d) Phần lớn khối lượng của nguyên tử tập trung ở hạt nhân nên kích thước của hạt nhân gần bằng kích thước của nguyên tử.
Câu trả lời của bạn
- Phát biểu a) sai vì các hạt electron được tìm thấy ở vỏ nguyên tử.
- Phát biểu b) sai vì hạt neutron không mang điện nên không hút được electron.
- Phát biểu c) đúng.
- Phát biểu d) sai vì phần lớn khối lượng của nguyên tử tập trung ở hạt nhân nên khối lượng của hạt nhân gần bằng khối lượng của nguyên tử.
Hãy chọn từ/ cụm từ thích hợp cho sẵn dưới đây để điền vào chỗ …. trong mỗi câu sau: proton, neutron, electron, hạt nhân nguyên tử, vỏ nguyên tử, nguyên tử.
a) Trong nguyên tử, số proton bằng số …..
b) Hạt nhân nguyên tử gồm ….. và …..
c) Phần lớn khối lượng nguyên tử tập trung ở …..
d) Trong hạt nhân nguyên tử, hạt ….. không mang điện.
Câu trả lời của bạn
a) Trong nguyên tử, số proton bằng số electron.
b) Hạt nhân nguyên tử gồm proton và neutron.
c) Phần lớn khối lượng nguyên tử tập trung ở hạt nhân nguyên tử.
d) Trong hạt nhân nguyên tử, hạt neutron không mang điện.
Nguyên tử tạo thành từ ba loại hạt nhỏ hơn nữa (gọi là hạt dưới nguyên tử), đó là những hạt nào ?
Câu trả lời của bạn
Nguyên tử được tạo thành từ ba loại hạt dưới nguyên tử đó là: electron, proton và nơtron.
a) Các hạt electron được tìm thấy ở hạt nhân của nguyên tử.
b) Các hạt neutron và electron hút nhau.
c) Trong nguyên tử, số electron tối đa ở lớp electron thứ hai là 8.
d) Phần lớn khối lượng của nguyên tử tập trung ở hạt nhân nên kích thước của hạt nhân gần bằng kích thước của nguyên tử.
Câu trả lời của bạn
- Phát biểu a) sai vì các hạt electron được tìm thấy ở vỏ nguyên tử.
- Phát biểu b) sai vì hạt neutron không mang điện nên không hút được electron.
- Phát biểu c) đúng.
- Phát biểu d) sai vì phần lớn khối lượng của nguyên tử tập trung ở hạt nhân nên khối lượng của hạt nhân gần bằng khối lượng của nguyên tử.
A. Một electron có khối lượng lớn hơn một proton và mang điện tích âm.
B. Một electron có khối lượng nhỏ hơn một proton và mang điện tích âm.
C. Một electron có khối lượng nhỏ hơn một neutron và không mang điện tích.
D. Một electron mang điện tích dương và có khối lượng lớn hơn một neutron.
Câu trả lời của bạn
Đáp án đúng là: B
Một electron có khối lượng nhỏ hơn một proton và mang điện tích âm.
Nitơ (nitrogen) là nguyên tố hoá học phổ biến trong không khí. Trong hạt nhân nguyên tử nitơ có 7 proton. Số electron trong các lớp của vỏ nguyên tử nitơ, viết từ lớp trong ra lớp ngoài, lần lượt là
A.7.
B. 2, 5.
C. 2, 2, 3.
D. 2,4, 1.
Câu trả lời của bạn
Đáp án B
=> Nguyên tử nitơ có số proton = 7
=> Số electron = 7.
Lớp electron bên trong gần hạt nhân có 2 electron, lớp bên ngoài có 7 - 2 = 5 electron.
Tổng số proton, neutron và electron của nguyên tử X là 46. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a) Tính số proton, số neutron, số electron của nguyên tử X.
b) Tính khối lượng nguyên tử X.
c) Cho biết nguyên tử X có bao nhiêu lớp electron và chỉ ra số electron trên mỗi lớp.
Câu trả lời của bạn
a) Gọi số hạt proton, neutron và electron trong nguyên tử X lần lượt là P, N và E.
Nguyên tử trung hòa về điện nên E = P (1)
Tổng số proton, neutron và electron của nguyên tử X là 46 nên:
P + N + E = 46 (2)
Thay E = P vào (2) ta được 2P + N = 46 hay N = 46 – 2P (3)
Trong X số hạt mang điện nhiều hơn số hạt không mang điện là 14 nên:
(P + E) – N = 14 (4)
Thay E = P; N = 46 – 2P vào (4) ta được:
2P – (46 – 2P) = 14 ⇒ P = 15 (= E)
Vậy N = 46 – 2.15 = 16.
Số hạt proton, electron và neutron của X lần lượt là 15, 15, 16.
b) Khối lượng nguyên tử X là: 15 . 1 + 16 . 1 = 31 (amu)
c) Nguyên tử X có 15 electron được sắp xếp vào 3 lớp.
- Lớp thứ nhất (gần hạt nhân nhất) có 2 electron.
- Lớp thứ hai có 8 electron.
- Lớp thứ ba (lớp ngoài cùng) có 5 electron.
A.2.
B. 8.
C.10.
D. 18.
Câu trả lời của bạn
A
Số electron ở lớp trong cùng của nguyên tử nhôm là 2
A.2, 10, 6.
B. 2, 6, 8.
C.2,8, 6.
D.2,9, 5.
Câu trả lời của bạn
số electron = số proton = 16.
Lớp electron trong cùng, gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 16 – 8 – 2 = 6 electron.
=> Đáp án C. 2,8, 6.
Nguyên tử có mang điện không? Vì sao?
Câu trả lời của bạn
Nguyên tử không mang điện. Trong nguyên tử, số proton mang điện dương luôn bằng với số electron mang điện âm nên nguyên tử trung hoà điện, do đó nguyên tử không mang điện.
Nguyên tử B có tổng số hạt là 28. Số hạt không mang điện chiếm 35,7%. Tính số p, n, e.
Câu trả lời của bạn
Nguyên tử B chứa các loại hạt: hạt p, hạt e, hạt n. Trong đó, số hạt p = số hạt e
p + n + e = 28
=> 2p + n = 28 (1)
Số hạt không mang điện chiếm 35,7%.
=>n = 35,7%.28 ≈ 10(hạt)
Thay n = 10 vào (1):
=>2p = 18 => p = 9
Vậy số p = số e = 9 (hạt)
số n = 10 (hạt)
Một nguyên tử có điện tích hạt nhân bằng +9, cấu tạo của nguyên tử đó có bao nhiêu lớp electron?
Câu trả lời của bạn
Nguyên tử có điện tích hạt nhân bằng +9, suy ra số p = số e = 9. Các lớp electron sẽ phân bố vào các lớp như sau:
+ Lớp 1: 2e
+ Lớp 2: 7e
(Lớp 1 chứa tối đa 2e, lớp 2 chứa tối đa 8e)
Vậy nguyên tử có 2 lớp electron
Một nguyên tử có tổng các hạt là 93. Số hạt không mang điện bằng 0,6034 số hạt mang điện. Tìm số hạt proton, notron, electron?
Câu trả lời của bạn

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *