Nội dung bài học Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học; Số electron lớp ngoài cùng quyết định tính chất hóa học của các nguyên tố thuộc nhóm A. Mối quan hệ giữa cấu hình electron nguyên tử của các nguyên tố với vị trí của chúng trong bảng tuần hoàn.
Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng (số electron hóa trị)
nsanpb ( 1 ≤ a ≤ 2 ; 0 ≤ b ≤ 6)
Số electron hóa trị = a + b
Electron hóa trị của các nguyên tố nhóm IA và IIA thuộc phân lớp s nên là các nguyên tố s
Electron hóa trị của các nguyên tố nhóm IIIA và VIIIA thuộc phân lớp p nên là các nguyên tố p
Nhóm VIIIA (Nhóm khí hiếm)
Nhóm IA là nhóm kim loại kiềm
4Na + O2 → 2Na2O
2Na + 2H2O → NaOH + H2
2Na + Cl2 → 2NaCl
Nhóm VIIA (Nhóm halogen)
2Al + 3Cl2 → 2AlCl3
2K + Br2 → KBr
Cl2 + H2 → 2HCl
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 8có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho một nguyên tố X có cấu hình electron là: 1s2 2s2 2p6 3s2 3p5. X thuộc chu kỳ nào, nhóm nào?
Nguyên tố Photpho thuộc chu kỳ 3, nhóm VA. Cấu hình electron của Photpho là:
Tính chất nào sau đây biến đổi tuần hoàn?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 10 Bài 8.
Bài tập 1 trang 41 SGK Hóa học 10
Bài tập 2 trang 41 SGK Hóa học 10
Bài tập 3 trang 41 SGK Hóa học 10
Bài tập 4 trang 41 SGK Hóa học 10
Bài tập 5 trang 41 SGK Hóa học 10
Bài tập 6 trang 41 SGK Hóa học 10
Bài tập 7 trang 41 SGK Hóa học 10
Bài tập 8.1 trang 19 SBT Hóa học 10
Bài tập 8.2 trang 19 SBT Hóa học 10
Bài tập 8.3 trang 19 SBT Hóa học 10
Bài tập 8.4 trang 20 SBT Hóa học 10
Bài tập 8.5 trang 20 SBT Hóa học 10
Bài tập 8.6 trang 20 SBT Hóa học 10
Bài tập 8.7 trang 20 SBT Hóa học 10
Bài tập 8.8 trang 20 SBT Hóa học 10
Bài tập 8.9 trang 20 SBT Hóa học 10
Bài tập 8.10 trang 20 SBT Hóa học 10
Bài tập 8.11 trang 21 SBT Hóa học 10
Bài tập 8.12 trang 21 SBT Hóa học 10
Bài tập 8.13 trang 21 SBT Hóa học 10
Bài tập 8.14 trang 21 SBT Hóa học 10
Bài tập 8.15 trang 21 SBT Hóa học 10
Bài tập 8.16 trang 21 SBT Hóa học 10
Bài tập 8.17 trang 21 SBT Hóa học 10
Bài tập 1 trang 44 SGK Hóa học 10 nâng cao
Bài tập 2 trang 44 SGK Hóa học 10 nâng cao
Bài tập 3 trang 44 SGK Hóa học 10 nâng cao
Bài tập 4 trang 44 SGK Hóa học 10 nâng cao
Bài tập 5 trang 44 SGK Hóa học 10 nâng cao
Bài tập 6 trang 44 SGK Hóa học 10 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho một nguyên tố X có cấu hình electron là: 1s2 2s2 2p6 3s2 3p5. X thuộc chu kỳ nào, nhóm nào?
Nguyên tố Photpho thuộc chu kỳ 3, nhóm VA. Cấu hình electron của Photpho là:
Tính chất nào sau đây biến đổi tuần hoàn?
Cho các nguyên tử: M (z = 16); N (z = 12); P (z = 19); Q(z = 18). Nguyên tử nào thuộc nhóm kim loại kiềm?
Cho các nguyên tử: M (z = 9); N (z = 12); P (z = 16); Q(z = 15). Nguyên tử nào thuộc nhóm halogen?
Cho nguyên tử các nguyên tố X1, X2, X3, X4, X5, X6 lần lượt có cấu hình electron như sau:
X1: 1s22s22p63s2
X2: 1s22s22p63s23p64s1
X3: 1s22s22p63s23p64s2
X4: 1s22s22p63s23p5
X5: 1s22s22p63s23p63d64s2
X6: 1s22s22p63s23p4
Các nguyên tố cùng một chu kì là:
X1, X3, X6
X2, X3, X5
X1, X2, X6
Nguyên tử nguyên tố X có tổng electron ở phân lớp d bằng 6. Vị trí của X trong tuần hoàn các nguyên tố hóa học là:
Nguyên tố X có tổng số proton, nơtron, electron là 13. Vậy X thuộc :
Cho các dãy nguyên tố mà mỗi nguyên tố được biểu diễn bằng số hiệu nguyên tử tương ứng. Dãy nào sau đây gồm các nguyên tố thuộc cùng một chu kì trong bảng tuần hoàn?
Nguyên tố có cấu hình electron hóa trị 4d25s2 ở vị trí nào trong bảng tuần hoàn?
Viết cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố thuộc . nhóm VIIA: flo (F), clo (Cl), brom (Br), iot (I), atatin (At).
Hãy cho biết đặc điểm về cấu hình electron lớp ngoài cùng của các nguyên tử trên và từ đó cho biết đặc điểm về tính chất của các nguyên tố tương ứng.
Hãy cho biết nguyên nhân sự biến đổi tuần hoàn tính chất của các nguyên tố.
Nguyên tử của nguyên tố X có cấu hình electron: 1s22s22p6
Hãy cho biết số thứ tự của nguyên tố X. Trong bảng tuần hoàn, X thuộc chu kì thứ mấy và thuộc nhóm nào ? Các nguyên tố thuộc nhóm này có tên chung là gì ?
Một nguyên tố có số thứ tự z = 11.
Hãy viết cấu hình electron nguyên tử của nguyên tố đó và từ cấu hình electron hãy cho biết nguyên tố đó thuộc chu kì thứ mấy và thuộc nhóm nào ? Các nguyên tố thuộc nhóm này có tên chung là gì ?
Sự biến thiên tính chất của các nguyên tố thuộc chu kì sau lại được lặp lại giống như chu kì trước là do:
A. sự lặp lại tính kim loại của các nguyên tố ở chu kì sau so với chu kì trước.
B. sự lặp lại tính phi kim của các nguyên tố ở chu kì sau so với chu kì trước.
C. sự lặp lại cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố ở chu kì sau so với chu kì trước.
D. sự lặp lại tính chất hóa học của các nguyên tố ở chu kì sau so với chu kì trước.
Hãy chọn đáp án đúng.
Dựa vào bảng 2.1, hãy cho biết số electron lớp ngoài cùng của nguyên tử các nguyên tố sau đây: H, He, Li, Na, K, Ga, O, S, Cl, Br.
Cho nguyên tử các nguyên tố có: Z = 8, Z = 9, Z = 17, Z = 19. Hãy xác định số electron lớp ngoài cùng của nguyên tử các nguyên tố đó, số thứ tự nhóm và chu kì chứa các nguyên tố đó.
Viết cấu hình electron nguyên tử của các nguyên tố có Z = 18 và Z = 19. Tại sao nguyên tố có Z = 18 ở chu kì 3, còn nguyên tố có Z = 19 lại ở chu kì 4?
Viết cấu hình electron nguyên tử của các nguyên tố có Z = 20; 21; 24; 29; 30. Cấu hình electron của chúng có đặc điểm gì? Tại sao Cu ở nhóm IB, Zn ở nhóm IIB?
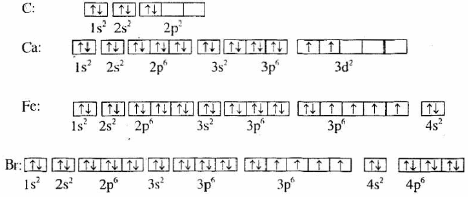
Sự phân bố electron vào các AO của nguyên tử các nguyên tố C, Ca, Fe và Br sau đây đúng hay sai? Nếu sai hãy sửa lại cho đúng.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *