Nội dung bài học Lưu huỳnh tìm hiểu về Cấu tạo phân tử và tính chất vật lí của lưu huỳnh biến đổi như thế nào theo nhiệt độ. Tính chất hóa học của lưu huỳnh có gì đặc biệt? Lưu huỳnh có những ứng dụng quan trọng nào?
Dạng thù hình là những đơn chất khác nhau của 1 nguyên tố hóa học. Ví dụ: O2 và O3.
Các dạng thù hình của S không tan trong nước nhưng tan nhiều trong benzen, dầu hỏa.
Hình 1: 2 dạng thù hình của lưu huỳnh
| Cấu tạo tinh thể và tính chất vật lí | Lưu huỳnh tà phương (Sα) | Lưu huỳnh đơn tà (Sβ) | Kết luận |
| Cấu tạo tinh thể | Cấu tạo khác nhau | ||
| Khối lượng riêng | 2,07g/cm3 | 1,96g/cm3 | Sα > Sβ |
| Nhiệt độ nóng chảy | 1130C | 1190C | Sα < Sβ |
| Nhiệt độ bền | < 95,50C | 95,50C → 1190C | Sα < Sβ |
| Nhiệt độ | Trạng thái | Màu | Cấu tạo phân tử | |
| <1130 | Rắn | Vàng | S8, mạch vòng tinh thể Sβ - Sα | |
| 1190 | Lỏng | Vàng | S8, mạch vòng linh hoạt | |
| >1870 | Quánh | Nâu đỏ | S8 vòng → chuỗi S8 → Sn | |
| >4450 14000 17000 | Hơi Hơi Hơi | Da cam | S6, S4 S2 S |
⇒ Ở nhiệt độ cao, lưu huỳnh tác dụng với nhiều kim loại tạo ra muối sunfua và với hiđro tạo ra khí hiđrosunfua, S thể hiện tính oxi hóa.
Hình 1: Khi nhiệt kế vỡ, có thể sử dụng bột lưu huỳnh để tạo muối với thủy ngân,
tránh hơi thủy ngân gây độc.
⇒ Ở nhiệt độ thích hợp, lưu huỳnh tác dụng với một số phi kim mạnh hơn, S thể hiện tính khử.
Video 1: Phản ứng giữa lưu huỳnh và axit nitric đặc nóng
(chứng minh phản ứng có xảy ra bằng cách nhỏ vài giọt dd BaCl2 thấy kết tủa màu trắng của BaSO4
⇒ Lưu huỳnh tác dụng được với các axit có tính oxi hóa, S thể hiện tính khử.
Phương trình phản ứng: S + 3C + 2KNO3 → K2S + 3CO2 + N2
Hình 2: Ứng dụng của lưu huỳnh
Trạng thái tự nhiên của S:
Khai thác lưu huỳnh từ các mỏ lưu huỳnh: người ta dùng thiết bị đặc biệt để nén nước siêu nóng (1700C) vào mỏ làm lưu huỳnh nóng chảy và đẩy lên mặt đất. Sau đó lưu huỳnh được tách ra khỏi các tạp chất.
2 H2S + O2(thiếu) 2 H2O + 2 S
2 H2S + SO2 → 2 H2O + 3 S
Hình 3: Thiết bi khai thác lưu huỳnh (phương pháp Frasch)
Hình 4: Sơ đồ tư duy bài lưu huỳnh
Vì sao nên hạn chế sử dụng măng khô, đũa dùng một lần, tăm tre?
Măng khô, đũa dùng 1 lần, tăm tre thường được xông lưu huỳnh để diệt mốc, ngăn chặn mốc phát triển. Lưu huỳnh gây bệnh đường hô hấp. Quá trình xông thường sinh khí SO2 có mùi khó chịu – đó chính là khí độc, có ảnh hưởng tới môi trường, sức khỏe của người chế biến và người sống xung quanh.
Đun nóng hỗn hợp gồm 11,2g bột sắt và 3,2g bột lưu huỳnh, cho sản phẩm tạo thành vào 500ml dung dịch HCl thu đc hỗn hợp khí và dd A. Để trung hòa HCl còn dư trong dd A phải dùng 250ml dung dịch NaOH 0,1M. Tính nồng độ mol/l của dd HCl đã dùng.
Phương trình phản ứng:
Fe + S → FeS (1)
FeS + 2HCl → FeCl2 + H2S (2)
Fe + 2HCl → FeCl2 + H2 (3)
HCl + NaOH →NaCl + H2O (4)
Số mol của sắt và lưu huỳnh là:
nFe=0,2 mol, nS =0,1 mol.
Phản ứng xảy ra thu được 0,1mol FeS và 0,1mol Fe dư .
Phương trình (4) nNaOH = nHCl .
Vậy nHCl đã dùng là = 2nFeS + 2nFe dư + nNaOH = 0,2 + 0,2 + 0,025 = 0,425 mol
Vậy CM (HCl) = n/ v = 0,425/0,5 = 0,85M
Cho sản phẩm tạo thành khi đun nóng hỗn hợp gồm 5,6g bột Fe và 1,6g bột S vào 500ml dd HCl thì thu được hỗn hợp khí bay ra và 1 dd B. Hiệu suất phản ứng là 100%.
a) Tính thành phần phần trăm về thể tích mỗi khí trong hh khí
b) Để trung hoà HCl còn thừa trong dd A phải dùng 125ml dd NaOH 0,1M. Tính CM HCl đã dùng.
Tính số mol từng chất
nFe = 0,1 mol
nS = 0,05 mol
Fe + S FeS
⇒ S hết, Fe dư
nFe(dư) = 0,05mol
Fe + 2HCl → FeCl2 + H2
0,05....0,1 ..............0,05
FeS + 2HCl → FeCl2 + H2S
0,05......0,1.................0,05
⇒ Vhh khí =22,4 . 0,1 = 2,24 lit
⇒ Thành phần phần trăn từng khí là 50% H2S và 50% H2
b)
nNaOH = 0,0125mol
NaOH + HCl → NaCl + H2O
0,0125 0,0125
Ta có số mol HCl là =0,1+0,1+0,0125=0,2125,ol
⇒ CMHCl = 0,2125/0,5 = 0,425M
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 30có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Đơn chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
Phát biểu nào sau đây chưa đúng:
Nhận định nào sau đây phản ánh đúng tính chất hóa học của lưu huỳnh ?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 10 Bài 30.
Bài tập 1 trang 132 SGK Hóa học 10
Bài tập 2 trang 132 SGK Hóa học 10
Bài tập 3 trang 132 SGK Hóa học 10
Bài tập 4 trang 132 SGK Hóa học 10
Bài tập 5 trang 132 SGK Hóa học 10
Bài tập 30.1 trang 66 SBT Hóa học 10
Bài tập 30.2 trang 66 SBT Hóa học 10
Bài tập 30.3 trang 66 SBT Hóa học 10
Bài tập 30.4 trang 66 SBT Hóa học 10
Bài tập 30.5 trang 67 SBT Hóa học 10
Bài tập 30.6 trang 67 SBT Hóa học 10
Bài tập 30.7 trang 67 SBT Hóa học 10
Bài tập 30.8 trang 67 SBT Hóa học 10
Bài tập 30.9 trang 67 SBT Hóa học 10
Bài tập 30.10 trang 68 SBT Hóa học 10
Bài tập 30.11 trang 68 SBT Hóa học 10
Bài tập 1 trang 172 SGK Hóa học 10 nâng cao
Bài tập 2 trang 172 SGK Hóa học 10 nâng cao
Bài tập 3 trang 172 SGK Hóa học 10 nâng cao
Bài tập 4 trang 172 SGK Hóa học 10 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Đơn chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
Phát biểu nào sau đây chưa đúng:
Nhận định nào sau đây phản ánh đúng tính chất hóa học của lưu huỳnh ?
Tổng số electron ở phân lớp p của nguyên tử nguyên tố X bằng 10. Nguyên tố X là
Khi làm vỡ nhiệt kế thủy ngân, ta dùng biện pháp nào sau đây để thu gom thủy ngân có hiệu quả nhất ?
Lưu huỳnh tác dụng với axit sunfuric đặc, nóng: S + 2H2SO4 → 3SO2 + 2H2O
Trong phản ứng này, tỉ lệ nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hoá là:
1 : 2.
1 : 3.
3 : 1.
Lưu huỳnh có thể tồn tại ở những trạng thái số oxi hoá nào ?
-2; +4; +5; +6
-3; +2; +4; +6.
-2; 0; +4; +6
Tính chất vật lí nào sau đây không phải của lưu huỳnh
chất rắn màu vàng, giòn
không tan trong nước
có tnc thấp hơn ts của nước
Đun nóng 4,8 gam bột Mg với 9,6 gam bột lưu huỳnh (trong điều kiện không có không khí), thu được chất rắn X. Cho toàn bộ X vào lượng dư dung dịch HCl, thu được V lít khí (đktc). Giá trị của V là
2,24
3,36
4,48
6,72
Cho 11 gam hỗn hợp bột sắt và bột nhôm tác dụng với bột lưu huỳnh trong điều kiện không có không khí) thấy có 12,8 gam lưu huỳnh tham gia phản ứng. Khối lượng sắt có trong 11 gam hỗn hợp đầu là
5,6 gam.
11,2 gam.
2,8 gam.
8,4 gam.
Lưu huỳnh tác dụng với aixt sunfuric đặc, nóng:
S + 2H2SO4 → 3SO2 + 2H2O
Trong phản ứng này, tỉ lệ số nguyên tử lưu huỳnh bị khử: số nguyên tử lưu huỳnh bị oxi hóa là:
A. 1 : 2.
B. 1 : 3.
C. 3 : 1.
D. 2 : 1.
Chọn đáp án đúng.
Đơn chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
A. Cl2, O3, S.
B. S, Cl2, Br2.
C. Na, F2, S.
D. Br2, O2, Ca.
Có thể dự đoán sự thay đổi như thế nào về khối lượng riêng, về nhiệt độ nóng chảy khi giữ lưu huỳnh đơn tà (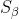 ) dài ngày ở nhiệt độ phòng?
) dài ngày ở nhiệt độ phòng?
Đun nóng một hỗn hợp gồm có 0,65g bột kẽm và 0,224 g bột lưu huỳnh trong ống nghiệm đậy kín không có không khí. Sau phản ứng, người ta thu được chất nào trong ống nghiệm? Khối lượng là bao nhiêu?
1,10g hỗn hợp bột sắt và bột nhôm tác dụng vừa đủ với 1,28g bột lưu huỳnh.
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tính tỉ lệ phần trăm của sắt và nhôm trong hỗn hợp ban đầu, theo:
Câu nào sau đây diễn tả đúng tính chất hoá học của lưu huỳnh ?
A. Lưu huỳnh chỉ có tính oxi hoá.
B. Lưu huỳnh chỉ có tính khử.
C. Lưu huỳnh vừa có tính oxi hoá, vừa có tính khử.
D. Lưu huỳnh không cố tính oxi hoá và không có tính khử.
Liên kết hoá học giữa nguyên tử của nguyên tố nào với nguyên tử natri trong hợp chất sau thuộc loại liên kết cộng hoá trị có cực ?
A. Na2S
B. Na2O
C. NaCl
D. NaF
Cho PTHH: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
Cần đốt cháy bao nhiêu mol FeS2 để thu được 64 gam SO2 theo PTHH trên ?
A. 0,4 mol.
B. 0,5 mol.
C. 0,8 mol.
D. 1,2 mol.
Câu nào sau đây đúng
A. Lưu huỳnh ở ô 32 trong bảng HTTH
B. Lưu huỳnh ở thể khí trong điều kiện thường
C. Lưu huỳnh vừa có tính oxi hóa, vừa có tính khử
D. Lưu huỳnh luôn có số oxi hóa -2 trong mọi hợp chất
Lưu huỳnh có các số oxi hóa nào sau đây
A. -2; -4; +6; +8
B. -1; 0; +2; +4
C. -2; +6; +4: 0
D. -2; -4; -6; 0
Đốt nóng một hỗn hợp gồm 5,6 gam bột sắt và 1,6 gam bột lưu huỳnh trong môi trường không có không khí, thu được hỗn hợp rắn X. Cho hỗn hợp X phản ứng hoàn toàn với 500 ml dung dịch HCl, thu được hỗn hợp khí A và dung dịch B (hiệu suất của các phản ứng là 100%).
a) Tính thành phần phần trăm theo thể tích của hỗn hợp khí A.
b) Biết rằng cần dùng 125 ml dung dịch NaOH 0,1M để trung hoà HCl còn dư trong dung dịch B, hãy tính nồng độ mol của dung dịch HCl đã dùng.
Viết phương trình hoá học của các phản ứng hoàn thành chuỗi phản ứng sau :
Cho sơ đồ chuỗi phản ứng:
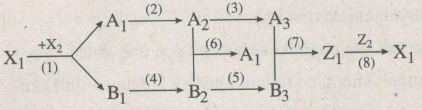
Biết rằng : X1 là hợp chất của 1 kim loại và 1 phi kim.
A1, A2, A3, Z1 là các hợp chất của lưu huỳnh
B1, B3, B5, Z1 là hợp chất của đồng hoặc đồng kim loại.
Hãy viết PTHH của chuỗi phản ứng (có ghi điều kiện) xảy ra theo sơ đồ trên.
Cho 1,10 gam hỗn hợp bột sắt và bột nhôm tác dụng vừa đủ với 1,28 gam bột lưu huỳnh.
a) Viết PTHH của các phản ứng đã xảy ra.
b) Tính tỉ lệ % của sắt và nhôm trong hỗn hợp ban đầu theo :
+ Lượng chất (số mol).
+ Khối lượng chất (số gam).
Đun nóng một hỗn hợp gồm có 0,650 gam bột kẽm và 0,224 gam bột lưu huỳnh trong ống nghiệm đậy kín không có không khí. Sau phản ứng người ta thu được chất nào trong ống nghiệm ? Khối lượng là bao nhiêu ?
Đốt cháy lưu huỳnh trong bình đựng không khí, lưu huỳnh cháy hết. Tính tỉ khối đối với He của hỗn hợp khí thu được sau phản ứng, nếu oxi trong bình vừa đủ đốt cháy hết S.
Cấu hình electron nguyên tử nào là của lưu huỳnh ở trạng thái kích thích?
A. 1s22s22p63s23p4
B. 1s22s22p4
C. 1s22s22p63s23p33d1
D. 1s22s22p63s23p6
Hãy chọn câu trả lời đúng.
Ta có thể dự đoán sự thay đổi về khối lượng riêng, về thể tích diễn ra như thế nào khi giữ lưu huỳnh đơn tà (Sβ) vài ngày ở nhiệt độ phòng?
Hãy viết các phương trình hóa học biểu diễn sự biến đổi số oxi hóa của nguyến tố lưu huỳnh theo sơ đồ sau:
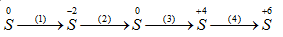
Đun nóng một hỗn hợp bột gồm 2,97g Al và 4,08g S trong môi trường kín không có không khí, được sản phẩm là hỗn hợp rắn A. Ngâm A trong dung dịch HCl dư, thu được hỗn hợp khí B.
a) Hãy viết phương trình hóa học của các phản ứng.
b) Xác định thành phần định tính và khối lượng các chất trong hỗn hợp A.
c) Xác định thành phần định tính và thể tích các chất trong hỗn hợp khí B ở điều kiện tiêu chuẩn.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *