Nội dung bài giảng Sơ lược về hợp chất có oxi của clo tìm hiểu nước Javen và Clorua vôi có thành phần, tính chất, cấu tạo như thế nào? Chúng được dùng làm gì và được điều chế bằng cách nào?
| Nước Javel | Clorua vôi | |
| Thành phần | Dung dịch: NaCl và NaClO. NaClO ⇔ HClO natri hipoclorit axit hipoclorơ | - CTPT: CaOCl2 - CTCT: → muối hỗn tạp. |
| Tính chất | - Tính tẩy màu, sát trùng. - NaClO là muối của axit yếu: NaClO + CO2 + H2O → HClO + NaHCO3 - NaClO, HClO: có tính oxi hóa rất mạnh. | - Chất bột, màu trắng, xốp. - Tính oxi hóa mạnh: CaOCl2 + 2HCl →CaCl2 + Cl2+ H2O - Tác dụng với CO2 trong không khí ẩm: 2CaOCl2 + CO2 + H2O → 2HClO + CaCO3 + CaCl2 |
| Ứng dụng | - Tẩy trắng vải, sợi, giấy, ... - Tẩy uế chuồng trại chăn nuôi, nhà vệ sinh | - Tẩy trắng, tẩy uế. - Tinh chế dầu mỏ. - Xử lí các chất độc, bảo vệ môi trường. |
⇒ nước Javel không để được lâu trong không khí.
CaOCl2 + 2HCl → CaCl2 + Cl2 + H2O
Cho khí clo tác dụng với NaOH loãng ở nhiệt độ thường:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Hình 1: Sơ đồ điều chế nước Javel trong phòng thí nghiệm
Điện phân dung dịch NaCl nồng độ 15 – 20% trong thùng điện phân không có màng ngăn.
\(2NaCl + 2{H_2}O \to 2NaOH + {H_2} \uparrow + C{l_2} \uparrow \)
\(C{l_2} + 2NaOH \to NaCl + NaClO + H{}_2O\)
Hình 2: Điều chế nước Javel trong công nghiệp
Cho clo tác dụng với vôi tôi (sữa vôi) ở 30oC thu được clorua vôi:
Cl2 + Ca(OH)2 → CaOCl2 + H2O (to = 30OC)

Hình 3: Clorua vôi
Viết phương trình phản ứng biểu diễn sơ đồ chuyển hóa sau:
(1) \(2KMn{O_4} + 16HCl \to 2KCl + 2MnC{l_2} + 5C{l_2} \uparrow + 8{H_2}O\)
(2) \(C{l_2} + 2NaOH \to NaCl + NaClO + {H_2}O\)
(3) \(Mn{O_2} + 4HCl \to MnC{l_2} + C{l_2} \uparrow + 2{H_2}O\)
(4) \(C{l_2} + Ca{(OH)_2} \to CaOC{l_2} + {H_2}O\) ĐK: Ở 30oC
(5) \(CaOC{l_2} + 2HCl \to CaC{l_2} + C{l_2} + {H_2}O\)
Hoặc \(CaOC{l_2} \to CaC{l_2} + \frac{1}{2}{O_2}\) ĐK: toc
Viết các phương trình phản ứng điều chế nước Javel từ các chất có trong phòng thí nghiệm: NaCl, MnO2, H2SO4 đặc, NaOH
NaCl (r) + H2SO4 (đặc) → NaHSO4 + HCl ĐK: tOC
MnO2 + 4HCl (đặc) → MnCl2 + Cl2 + 2H2O ĐK: tOC
Cl2+ 2NaOH → NaCl + NaClO + H2O
Chỉ dùng một thuốc thử, hãy nhận biết các dung dịch mất nhãn sau: HCl, HClO, NaCl, NaClO
Sử dụng quỳ tím:
Sau bài học cần nắm: Thành phần hóa học, ứng dụng, nguyên tắc sản xuất cũng như tính oxi hóa mạnh của một số hợp chất có oxi của clo (nước Gia-ven, clorua vôi).
Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 24có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Nước Gia- ven và clorua vôi có tính tẩy màu giấy, vải, sát trùng, tẩy uế môi trường vì:
Clorua vôi được sử dụng nhiều hơn nước Gia - ven vì
Chọn câu đúng trong các câu sau:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 10 Bài 24.
Bài tập 1 trang 108 SGK Hóa học 10
Bài tập 2 trang 108 SGK Hóa học 10
Bài tập 3 trang 108 SGK Hóa học 10
Bài tập 4 trang 108 SGK Hóa học 10
Bài tập 5 trang 108 SGK Hóa học 10
Bài tập 24.1 trang 56 SBT Hóa học 10
Bài tập 24.2 trang 57 SBT Hóa học 10
Bài tập 24.3 trang 57 SBT Hóa học 10
Bài tập 24.4 trang 57 SBT Hóa học 10
Bài tập 24.5 trang 57 SBT Hóa học 10
Bài tập 24.6 trang 57 SBT Hóa học 10
Bài tập 24.7 trang 57 SBT Hóa học 10
Bài tập 24.8 trang 58 SBT Hóa học 10
Bài tập 24.9 trang 58 SBT Hóa học 10
Bài tập 24.10 trang 58 SBT Hóa học 10
Bài tập 1 trang 134 SGK Hóa học 10 nâng cao
Bài tập 2 trang 134 SGK Hóa học 10 nâng cao
Bài tập 3 trang 134 SGK Hóa học 10 nâng cao
Bài tập 4 trang 134 SGK Hóa học 10 nâng cao
Bài tập 5 trang 134 SGK Hóa học 10 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Nước Gia- ven và clorua vôi có tính tẩy màu giấy, vải, sát trùng, tẩy uế môi trường vì:
Clorua vôi được sử dụng nhiều hơn nước Gia - ven vì
Chọn câu đúng trong các câu sau:
Nước Gia-ven là hỗn hợp các chất nào sau đây?
Tính chất sát trùng và tẩy màu của nước Gia-ven là do nguyên nhân nào sau đây?
Clorua vôi là muối của kim loại canxi với 2 loại gốc axit là clorua Cl- và hipoclorit ClO-. Vậy clorua vôi gọi là muối gì ?
Muối trung hoà.
Muối kép.
Phát biểu nào sau đây sai?
Nước Gia-ven là dung dịch hỗn hợp muối NaCl và NaClO.
Clorua vôi là chất bột màu trắng, xốp, có tính oxi hóa mạnh.
Nước Gia-ven dung để tẩy trắng vải, sợi và tẩy uế chuồng trại chăn nuôi, nhà vệ sinh.
Trong công nghiệp, nước Gia-ven được điều chế bằng cách
điện phân dung dịch NaCl có màng ngăn.
điện phân dung dịch NaCl không có màng ngăn.
cho khí clo tác dụng với dung dịch NaOH.
Cho các phản ứng sau:
Cl2 + NaOH → NaCl + NaClO + H2O
NaClO + CO2 + H2O → NaHCO3 + HClO
Cl2 + Ca(OH)2 → CaOCl2 + H2O
CaOCl2 + CO2 + H2O → CaCO3 + CaCl2 + HClO
Trong các phản ứng trên, số phản ứng thuộc loại phản ứng oxi hóa – khử là
Trong một loại nước clo ở 25℃, người ta xác định được nồng độ của clo là 0,06M, còn nồng độ của HCl và HClO đều là 0,03M. Thể tích khí clo (đktc) cần dùng để điều chế 5 lít nước clo trên là
Chọn câu đúng trong các câu sau:
A. Clorua vôi là muối tạo bởi một kim loại liên kết với một loại gốc axit.
B. Clorua vôi là muối tạo bởi một kim loại liên kết với hai loại gốc axit.
C. Clorua vôi là muối tạo bởi hai kim loại liên kết với một loại gốc axit.
D. Clorua vôi không phải là muối.
Nêu tính chất hóa học chính và ứng dụng của nước Gia-ven, clorua vôi.
Trong phòng thí nghiệm có các hóa chất NaCl, MnO2, NaOH và H2SO4 đặc, ta có thể điều chế nước Gia – ven không? Viết các phương trình phản ứng.
Có những sơ đồ phản ứng hóa học sau:
a) Cl2 + H2O → HCl + HClO
b) CaOCl2 + HCl → CaCl2 + Cl2 + H2O
c) Cl2 + KOH → KCl + KClO3 + H2O
d) HCl + KClO3 → KCl + Cl2 + H2O
e) NaClO + CO2 + H2O → NaHCO3 + HClO
f) CaOCl2 → CaCl2 + O2
Cho biết những phản ứng nào là phản ứng oxi hóa – khử? Vai trò các chất tham gia phản ứng oxi hóa – khử. Hoàn thành phương trình hóa học của các phản ứng.
Trong phòng thí nghiệm có canxi oxit, nước, MnO2, axit H2SO4 70% (D = 1,61g/cm3) và NaCl. Hỏi cần phải dùng những chất gì và với lượng chất là bao nhiêu để điều chế 254 g clorua vôi?
Nước Gia-ven là hỗn hợp các chất nào sau đây ?
A. HCl, HClO, H2O
B. NaCl, NaClO, H2O
C. NaCl, NaClO3, H2O
D. NaCl, NaClO4, H2O
Tính chất sát trùng và tẩy màu của nước Gia-ven là do nguyên nhân nàc sau đây ?
A. Do chất NaClO phân huỷ ra oxi nguyên tử có tính oxi hoá mạnh.
B. Do chất NaClO phân huỷ ra Cl2 là chất oxi hoá mạnh.
C. Do trong chất NaClO, nguyên tử Cl có số oxi hoá là +1, thể hiện tính oxi hoá mạnh.
D. Do chất NaCl trong nước Gia-ven có tính tẩy màu và sát trùng.
Hãy chọn nửa sơ đồ phản ứng ở cột II để ghép với nửa sơ đồ phản ứng II cột I cho phù hợp.
| Cột I | Cột II |
| a) Cl2 + H2O → b) Cl2 + NaOH (dd) → c) Cl2 + NaOH (dd) to→ d) KClO3 MnO2→ e) KClO3 to→ | 1) KCl + O2 2) NaCl + NaClO3 + H2O 3) NaCl + NaClO + H2O 4) HCl + HClO 5) KClO4 + KCl 6) HCl + H2O 7) K + Cl2 + O2 |
Viết PTHH của các phản ứng trong sơ đồ biến đổi sau (ghi đầy đủ điều kiện phản ứng):
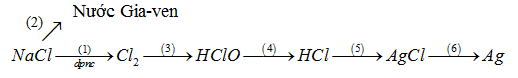
Viết PTHH của các phản ứng xảy ra trong quá trình sản xuất clorua vôi từ đá vôi và muối ăn.
Tại sao có thể dùng bình thép đựng khí clo khô mà không được dùng bình thép đựng khí clo ẩm ?
Đưa một bình cầu đựng 250 gam nước clo ra ngoài ánh sáng mặt trời thì có 0,112 lít (đktc) khí được giải phóng. Hỏi khí nào được giải phóng? Tính nồng độ % của clo trong dung dịch đầu, cho rằng tất cả clo tan trong nước, đã phản ứng với nước.
Cho 17,4 gam MnO2 tác dụng hết với dung dịch HCl. Toàn bộ khí cu sinh ra được hấp thụ hết vào 145,8 gam dung dịch NaOH 20% ở nhiệt độ thường tạo ra dung dịch A. Hỏi dung dịch A có chứa những chất tan nào ? Tính nồng độ % của từng chất tan đó.
Trong phòng thí nghiệm có các hoá chất : NaCl, KMnO4, NaOH, H2O, dung dịch H2SO4 đặc. Viết PTHH của các phản ứng dùng để điều chế nước Gia-ven từ các chất trên.
Chất KClO4 có tên là gì?
A. Kali clorat.
B. Kali clorit.
C. Kali hipoclorit.
D. Kali peclorat.
Đọc tên các hợp chất sau đây và cho biết số oxi hóa của clo trong từng hợp chất:
Cl2O, KClO3, HClO, Cl2O3, CaCl2, HClO2, Cl2O7, Ca(ClO)2, HClO3, CaOCl2, Ca(ClO3)2.
Hãy cho biết tính chất hóa học quan trọng nhất của nước Gia - ven, clorua vôi và ứng dụng của chúng. Vì sao clorua vôi được sử dụng nhiều hơn nước Gia - ven?
Cho các hóa chất NaCl (r), MnO2 (r), NaOH (dd), KOH (dd), H2SO4 (dd đặc), Ca(OH)2 (r). Từ các hóa chất đó, có thể điều chế được các chất sau đây hay không?
a) Nước Gia-ven.
b) Kali clorat.
c) Clorua vôi.
d) Oxi.
e) Lưu huỳnh đioxit.
Viết phương trình hóa học của các phản ứng xảy ra.
Để điều chế kali clorat với giá thành hạ, người ta thường làm như sau: Cho khí clo đi qua nước vôi đun nóng, lấy dung dịch thu được trộn với KCl và làm lạnh. Khi đó kali clorat sẽ kết tinh. Hãy viết phương trình hóa học của các phản ứng xảy ra và giải thích vì sao kali clorat kết tinh?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *