Nội dung bài giảng Luyện tập: Liên kết hóa học củng cố lại kiến thức về các loại liên kết hóa học chính để vận dụng, giải thích sự hình thành một số loại phân tử. Đặc điểm cấu trúc và đặc điểm liên kết của ba loại tinh thể. Rèn kĩ năng xác định hóa trị và số oxi hóa của nguyên tố trong đơn chất và hợp chất.
| Loại liên kết | Liên kết ion | Liên kết cộng hoá trị | |
| Không cực | Có cực | ||
| Định nghĩa | Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu. | Liên kết cộng hoá trị là liên kết được tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung. | |
| Bản chất của liên kết | Cho và nhận electron | Đôi electron chung không lệch về nguyên tử nào. | Đôi e chung lệch về nguyên tử nào có độ âm điện lớn hơn. |
| Hiệu độ âm điện | ≥ 1,7 | 0 → 0,4 | 0,4 → < 1,7 |
| Tinh thể ion | Tinh thể nguyên tử | Tinh thể phân tử | |
| Khái niệm | Các cation và anion được phân bố luân phiên đều đặn ở các điểm nút của mạng tinh thể ion | Ở các điểm nút mạng tinh thể nguyên tử là những nguyên tử | Ở các điểm nút của mạng tinh thể phân tử là các phân tử |
| Lực liên kết | Các ion mang điện tích trái dấu hút nhau bằng lực hút tĩnh điện, lực này lớn. | Các nguyên tử liên kết với nhau bằng lực liên kết cộng hóa trị. Lực này rất lớn. | Các phân tử liên kết với nhau bằng lực hút giữa các phân tử, yếu hơn nhiều lực hút tĩnh điện giữa các ion và lực liên kết cộng hóa trị |
| Đặc tính | Bền, khá rắn, khó bay hơi, khó nóng chảy | Bền, khá cứng, khó nóng chảy, khó bay hơi | Không bền, dễ nóng chảy, dễ bay hơi |
Dựa vào giá trị hiệu độ âm điện của 2 nguyên tử, hãy xác định loại liên kết trong các phân tử sau:
| Phân tử | Hiệu độ âm điện | Loại liên kết |
| H2S | ||
| NH3 | ||
| CaS | ||
| H2O | ||
| BaF2 | ||
| Cl2 |
Cho biết giá trị độ âm điện của các nguyên tố như sau:
| Ca | Ba | H | S | N | Cl | O | F |
| 1,0 | 0,89 | 2,2 | 2,58 | 3,04 | 3,16 | 3,44 | 3,98 |
| Phân tử | Hiệu độ âm điện | Loại liên kết |
| H2S | 2,58 – 2,2 = 0,38 <0,4 | Liên kết cộng hóa trị không cực |
| NH3 | 3,04 - 2,2 = 0,84 > 0,4 | Liên kết cộng hóa trị có cực |
| CaS | 2,58 – 1,0 = 1,58 >0,4 | Liên kết cộng hóa trị có cực |
| H2O | 3,44 – 2,2 = 1,24 >0,4 | Liên kết cộng hóa trị có cực |
| BaF2 | 3,98 –0,89 =3,09 >1,7 | Liên kết ion |
| Cl2 | 0 | Liên kết cộng hóa trị không cực |
Xác định số oxi hóa của nguyên tố trung tâm trong các hợp chất sau: HNO3, H2S, NaNO3, K2SO4, KMnO4, K2Cr2O7
HNO3: N có số oxi hóa là +5
H2S: S có số oxi hóa là -2
NaNO3: N có số oxi hóa là +5
K2SO4: S có số oxi hóa là +6
KMnO4: Mn có số oxi hóa là +7
K2Cr2O7: Cr có số oxi hóa là +6
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 16có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Số oxi hoá của Clo trong hợp chất HCl, HClO, HClO3, NaClO, NaClO4
Phân tử HF có công thức electron phù hợp nhất là:
Cho biết độ âm điện của O là 3,44 và của Si là 1,90. Liên kết trong phân tử SiO2 là liên kết
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 10 Bài 16.
Bài tập 1 trang 76 SGK Hóa học 10
Bài tập 2 trang 76 SGK Hóa học 10
Bài tập 3 trang 76 SGK Hóa học 10
Bài tập 4 trang 76 SGK Hóa học 10
Bài tập 5 trang 76 SGK Hóa học 10
Bài tập 6 trang 76 SGK Hóa học 10
Bài tập 8 trang 76 SGK Hóa học 10
Bài tập 9 trang 76 SGK Hóa học 10
Bài tập 7 trang 76 SGK Hóa học 10
Bài tập 16.1 trang 37 SBT Hóa học 10
Bài tập 16.2 trang 37 SBT Hóa học 10
Bài tập 16.3 trang 37 SBT Hóa học 10
Bài tập 16.4 trang 37 SBT Hóa học 10
Bài tập 16.5 trang 37 SBT Hóa học 10
Bài tập 16.6 trang 38 SBT Hóa học 10
Bài tập 16.7 trang 38 SBT Hóa học 10
Bài tập 16.8 trang 38 SBT Hóa học 10
Bài tập 16.9 trang 38 SBT Hóa học 10
Bài tập 16.10 trang 38 SBT Hóa học 10
Bài tập 16.11 trang 39 SBT Hóa học 10
Bài tập 16.12 trang 39 SBT Hóa học 10
Bài tập 16.13 trang 39 SBT Hóa học 10
Bài tập 16.14 trang 39 SBT Hóa học 10
Bài tập 16.15 trang 39 SBT Hóa học 10
Bài tập 16.16 trang 39 SBT Hóa học 10
Bài tập 16.17 trang 39 SBT Hóa học 10
Bài tập 16.18 trang 39 SBT Hóa học 10
Bài tập 16.19 trang 39 SBT Hóa học 10
Bài tập 16.20 trang 39 SBT Hóa học 10
Bài tập 1 trang 87 SGK Hóa học 10 nâng cao
Bài tập 2 trang 87 SGK Hóa học 10 nâng cao
Bài tập 3 trang 87 SGK Hóa học 10 nâng cao
Bài tập 4 trang 87 SGK Hóa học 10 nâng cao
Bài tập 5 trang 87 SGK Hóa học 10 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Số oxi hoá của Clo trong hợp chất HCl, HClO, HClO3, NaClO, NaClO4
Phân tử HF có công thức electron phù hợp nhất là:
.PNG)
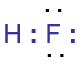

.PNG)
Cho biết độ âm điện của O là 3,44 và của Si là 1,90. Liên kết trong phân tử SiO2 là liên kết
Dãy gồm các phân tử có cùng một kiểu liên kết :
Cấu hình electron lớp ngoài cùng của nguyên tử Cl (Z=17), Ca (Z=20) và liên kết giữa canxi và clo trong hợp chất CaCl2 lần lượt là
3s23p5, 4s1 và liên kết cộng hóa trị
3s23p3, 4s2 và liên kết ion
3s23p5, 4s2 và liên kết ion
Cho các chất: HBr, HI, HCl. Mức độ phân cực của liên kết hóa học trong phân tử các chất này được sắp xếp theo thứ tự giảm dần từ trái sang phải là
HBr, HI, HCl
HI, HBr, HCl
HCl, HBr, HI
Hợp chất tạo bởi các nguyên tử có cấu hình electron ở trạng thái cơ bản là 1s22s1 và 1s22s22p5 có liên kết thuộc loại
cộng hóa trị có cực
cộng hóa trị không cực
ion
Dãy nào trong các chất sau đây gồm các chất được xếp theo chiều giảm dần độ phân cực của liên kết trong phân tử?
MgO, NaBr, CaO, AlCl3, CH4
CaO, MgO, NaBr, AlCl3, CH4
NaBr, CaO, AlCl3, MgO, CH4
Hạt nhân của nguyên tố X có 20 proton, hạt nhân của nguyên tố Y có 9 proton. Công thức hóa học và liên kết trong phân tử của hợp chất tạo bởi hai nguyên tố này là
X2Y và liên kết cộng hóa trị
XY2 và liên kết ion
XY và liên kết ion
Cho một số hợp chất: H2S, H2SO3, H2SO4, NaHS, Na2SO3, SO3, K2S, SO2. Dãy các chất trong đó lưu huỳnh có cùng só oxi hóa là
K2S, NaHS, Na2SO3
K2SO3, H2S, CaS
K2S, H2SO4, NaHS
Hãy cho biết sự khác nhau về liên kết hoá học trong các tinh thể ion, tinh thể nguyên tử và tinh thể phân tử.
Hãy cho biết sự khác nhau về các cấu tử (các hạt tạo nên tinh thể) trong tinh thể ion, tinh thể nguyên tử, tinh thể phân tử.
Hãy cho biết sự khác nhau về tính chất giữa tinh thể nguyên tử và tinh thể phân tử.
Hãy viết công thức cấu tạo của các phân tử: N2, CH4, NH3, H2O.
Dựa vào quy tắc biến thiên độ âm điện của các nguyên tố trong một chu kì, hãy cho biết trong các phân tử nói trên, phân tử nào có liên kết không phân cực, phân tử nào có liên kết phân cực mạnh nhất.
Cho dãy oxit sau đây: Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
Biết rằng độ âm điện của các nguyên tố: Na, Mg, Al, Si, P, S, Cl, O Lần lượt bằng: 0,93; 1,31; 1,61; 1,90; 2,19; 2,58; 3,16; 3,44.
Hãy dự đoán trong các oxit đó thì liên kết trong các oxit nào là liên kết ion, liên kết cộng hoá trị có cực, liên kết cộng hoá trị không cực ?
Hãy cho biết số oxi hoá của các kim loại trong các hợp chất sau đây: LiBr, NaCl, KI, MgCl2, CaO, BaF2.
a) Hãy cho biết số oxi hoá của O trong các hợp chất: Na2O, CaO, Al2O3, H2O2, F2O
b) Hãy cho biết trong trường hợp nào thì oxi có số oxi hoá bằng -2, bằng -1, bằng +2.
Các cation R+,Y 2+ và anion X − đều có cấu hình electron lớp ngoài cùng là 3s23p 6. Xác định vị trí của R, Y, X trong bảng tuần hoàn.
Hợp chất MX có tổng số các hạt trong phân tử là 84. Trong nguyên tử M cũng như X, số hạt proton bằng số hạt nơtron. Tổng số electron trong M2+ nhiều hơn trong X2- là 8 hạt. Xác định chất MX.
Chọn câu đúng trong các câu sau:
A. Trong liên kết cộng hóa trị, cặp electron chung lệch về phía nguyên tử có độ âm điện nhỏ hơn.
B. Liên kết cộng hóa trị có cực được tạo thành giữa hai nguyên tử có hiệu độ âm điện trong khoảng từ 0,4 đến nhỏ hơn 1,7.
C. Liên kết cộng hóa trị không cực được tạo nên từ các nguyên tử khác hẳn nhau về tính chất hóa học.
D. Hiệu độ âm điện giữa 2 nguyên tử lớn thì phân tử phân cực yếu.
Hãy cho biết thế nào là liên kết cộng hóa trị không cực? Cho ba ví dụ về liên kết cộng hóa trị không cực.
Hãy cho biết công thức electron của phân tử F2, phân tử HF, phân tử N2. Hãy cho biết, trong các phân tử đó thì phân tử nào có liên kết cộng hóa trị có cực và không cực.
Xét các phân tử sau đây: NaCl, MgCl2, AlCl3, HCl. Hãy cho biết liên kết trong phân tử nào là liên kết cộng hóa trị và liên kết trong phân tử nào là liên kết ion.
Xét phân tử sau đây HBr, O2, H2, NH3. Hãy cho biết liên kết trong phân tử nào có cực, liên kết phân tử nào không cực.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *