Mẫu nguyên tử Bolà sự phối hợp giữa mẫu nguyên tử Rutherford cùng với 2 tiên đề Bo về các trạng thái dừng, các quỹ đạo dừng và về sự hấp thụ và bức xạ năng lượng của nguyên tử. Thông qua những nội dung được đề cập tới trong bài học, mời các bạn cùng nghiên cứu bài 33- Mẫu nguyên tử Bo.
Năm 1911, Rutherford mạnh dạn đề sướng mẫu hành tinh nguyên tử: Theo Rutherford nguyên tử được cấu tạo bởi hạt nhân mang tích điện dương nằm ở chính giữa, xung quanh có các electron mang điện tích âm chuyển động trên các quỹ đạo tròn hay elíp giống như hệ Mặt Trời nên gọi là mẫu hành tinh nguyên tử.
Mẫu hành tinh nguyên tử của Rơ-dơ-pho gặp phải khó khăn là không giải thích được tính bền vững của các nguyên tử và sự tao thành quang phổ vạch của các nguyên tử.
Mẫu nguyên tử của Bo bao gồm mô hình hành tinh nguyên tử và hai tiên đề của Bo.
Nguyên tử chỉ tồn tại trong một số trạng thái có năng lượng xác định En, gọi là các trạng thái dừng. Khi ở trạng thái dừng, nguyên tử không bức xạ.
Trong các trạng thái dừng của nguyên tử, electron chuyển động quanh hạt nhân trên những quỹ đạo có bán kính hoàn toàn xác định gọi là quỹ đạo dừng.
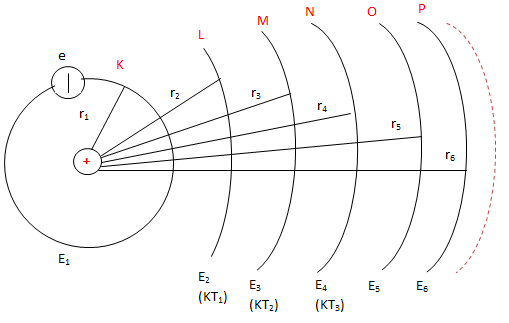
Bán kính quỹ đạo dừng của electron trong nguyên tử hyđrô:
\(r_n=n^2.r_0\), với n là số nguyên và \(r_0=5,3.10^{-11}(m)\), là bán kính Bo.
Bình thường, nguyên tử ở trạng thái dừng có năng lượng thấp nhất gọi là trạng thái cơ bản. Khi hấp thụ năng lượng thì nguyên tử chuyển lên trạng thái dừng có năng lượng cao hơn, gọi là trạng thái kích thích. Thời gian nguyên tử ở trạng thái kích thích rất ngắn (chỉ cỡ 10-8s). Sau đó nguyên tử chuyển về trạng thái dừng có năng lượng thấp hơn và cuối cùng về trạng thái cơ bản.
Khi nguyên tử chuyển từ trạng thái dừng có năng lượng \(E_n\) sang trạng thái dừng có năng lượng \(E_m\) nhỏ hơn thì nó phát ra một phôtôn có năng lượng:
\(\varepsilon _{nm}=h.f{nm}=E_n-E_m\).

Ngược lại, nếu nguyên tử đang ở trạng thái dừng có năng lượng \(E_m\) mà hấp thụ được một phôtôn có năng lượng \(h.f\) đúng bằng hiệu \(E_n-E_m\) thì nó chuyển sang trạng thái dừng có năng lượng \(E_n\) lớn hơn.
Mẫu nguyên tử Bo giải thích được các quy luật của quang phổ nguyên tử Hyđrô.
Khi electron chuyển từ mức năng lương cao (\(E_{cao}\)) xuống mức năng lượng thấp hơn (\(E_\) thấp) thì nó phát ra một phôtôn có năng lượng hoàn toàn xác định: \(h.f\) = \(E_{cao}\) – \(E_\) thấp.
Mỗi phôtôn có tần số f ứng với một sóng ánh sáng đơn sắc có bước sóng \(\lambda =\frac{c}{f}\) , tức là ứng với một vạch quang phổ có một màu nhất định.
Ngược lại, nếu một nguyên tử hyđrô đang ở một mức năng lương \(E_\) thấp nào đó mà nằm trong một chùm ánh sáng trắng, trong đó có tất cả các phôtôn có năng lượng từ lớn đến nhỏ khác nhau, thì lập tức nguyên tử đó sẽ hấp thụ ngay một phôtôn có năng lượng phù hợp \(\varepsilon =h.f\) = \(E_{cao}\) – \(E_\) thấp để chuyển lên mức năng lượng \(E_{cao}\). Như vậy một sóng ánh sáng đơn sắc đã bị hấp thụ làm cho trên nền quang phổ liên tục xuất hiện một vạch tối.
Khi nguyên tử hidro ở trạng thái n thì năng lượng và bán kính được xác định \(E_n=-\frac{13,6}{n^2}\) và \(r_n=n^2.r_0\), với \(n_0=5,3.10^{-11}(m)\). Khi bán kính của electron bằng 2,12.10-10 (m) thì năng lượng của nó bằng bao nhiêu?
Ta có
\(r_n=n^2.r_0\)
\(\Rightarrow 2,12.10^{-10}=n^2.5,3.10^{-11}\Rightarrow n^2=4\)
⇒ Năng lượng \(E_n=\frac{13,6}{n^2}=-\frac{13,6}{4}=-3,4 \ eV\)
Khi nguyên tử hidro chuyển từ trạng thái E4 về E2 thì phát ra photon có bước sóng \(\lambda _{42}\). Khi nguyên tử hidro chuyển từ trạng thái E5 về E3 thì phát ra photon có bước sóng \(\lambda _{53}\). Tìm \(\frac{\lambda _{53}}{\lambda _{42}}\) = ?
Ta có
\(\left.\begin{matrix} \varepsilon _{42}=\frac{hc}{\lambda _{42}}=E_4-E_2\\ \varepsilon _{53}=\frac{hc}{\lambda _{53}}=E_5-E_3 \end{matrix}\right\} \ \Rightarrow \frac{\varepsilon _{42}}{\varepsilon _{53}}=\frac{\lambda _{53}} {\lambda _{42}}=\frac{E_4-E_2}{E_5-E_3}\)
\(\Rightarrow \frac{\lambda _{53}}{\lambda _{42}}=\frac{-\frac{13,6}{4^2} -(-\frac{13,6}{2^2})}{-\frac{13,6}{5^2}-(-\frac{13,6}{3^2})}\)
\(\Rightarrow \frac{\lambda _{53}}{\lambda _{42}}=\frac{-\frac{1}{4^2}+\frac{1}{2^2}} {-\frac{1}{5^2}+\frac{1}{3^2}}=\frac{675}{256}\)
\(\Rightarrow \frac{\lambda _{53}}{\lambda _{42}}=\frac{675}{256}\)
Qua bài giảng Mẫu nguyên tử Bo này, các em cần hoàn thành 1 số mục tiêu mà bài đưa ra như :
Trình bày được mẫu nguyên tử Bo.
Phát biểu được hai tiên đề của Bo về cấu tạo nguyên tử.
Giải thích được tại sao quang phổ phát xạ và hấp thụ của nguyên tử hiđrô lại là quang phổ vạch.
Vận dụng công thức cơ bản vào giải quyết một số bài tập dạng trắc nghiệm
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Vật lý 12 Bài 33 cực hay có đáp án và lời giải chi tiết.
Trong quang phổ của nguyên tử hiđro, ba vạch đầu tiên trong dãy Lai man có bước sóng \(\lambda _{12}=121,6 nm\) ; \(\lambda _{13}=102,6 nm\) ; \(\lambda _{14}=97,3 nm\). Bước sóng của vạch đầu tiên trong dãy Banme và vạch đầu tiên trong dãy Pasen là
Electron đang ở quỹ đạo n chưa rõ thì chuyển về quỹ đạo L và thấy rẳng bán kính quỹ đạo đã giảm đi 4 lần. Hỏi ban đầu electron đang ở quỹ đạo nào?
Khi nguyên tử hidro ở trạng thái n thì năng lượng và bán kính được xác định \(E_n=-\frac{13,6}{n^2}\) và \(r_n=n^2.r_0\), với \(n_0=5,3.10^{-11}(m)\). Khi bán kính của electron bằng 2,12.10-10 (m) thì năng lượng của nó bằng bao nhiêu?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Vật lý 12 Bài 33để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Bài tập 1 trang 169 SGK Vật lý 12
Bài tập 2 trang 169 SGK Vật lý 12
Bài tập 3 trang 169 SGK Vật lý 12
Bài tập 4 trang 169 SGK Vật lý 12
Bài tập 5 trang 169 SGK Vật lý 12
Bài tập 6 trang 169 SGK Vật lý 12
Bài tập 7 trang 169 SGK Vật lý 12
Bài tập 33.1 trang 94 SBT Vật lý 12
Bài tập 33.2 trang 94 SBT Vật lý 12
Bài tập 33.3 trang 94 SBT Vật lý 12
Bài tập 33.4 trang 94 SBT Vật lý 12
Bài tập 33.5 trang 95 SBT Vật lý 12
Bài tập 33.6 trang 95 SBT Vật lý 12
Bài tập 33.7 trang 95 SBT Vật lý 12
Bài tập 33.8 trang 95 SBT Vật lý 12
Bài tập 33.9 trang 96 SBT Vật lý 12
Bài tập 33.10 trang 96 SBT Vật lý 12
Bài tập 33.11 trang 96 SBT Vật lý 12
Bài tập 33.12 trang 96 SBT Vật lý 12
Bài tập 33.13 trang 97 SBT Vật lý 12
Bài tập 33.14 trang 97 SBT Vật lý 12
Bài tập 33.15 trang 97 SBT Vật lý 12
Bài tập 33.16 trang 97 SBT Vật lý 12
Bài tập 33.17 trang 97 SBT Vật lý 12
Bài tập 33.18 trang 97 SBT Vật lý 12
Bài tập 33.19 trang 98 SBT Vật lý 12
Bài tập 33.20 trang 98 SBT Vật lý 12
Bài tập 1 trang 241 SGK Vật lý 12 nâng cao
Bài tập 2 trang 241 SGK Vật lý 12 nâng cao
Bài tập 3 trang 241 SGK Vật lý 12 nâng cao
Bài tập 4 trang 241 SGK Vật lý 12 nâng cao
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Vật lý DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
-- Mod Vật Lý 12 DapAnHay
Trong quang phổ của nguyên tử hiđro, ba vạch đầu tiên trong dãy Lai man có bước sóng \(\lambda _{12}=121,6 nm\) ; \(\lambda _{13}=102,6 nm\) ; \(\lambda _{14}=97,3 nm\). Bước sóng của vạch đầu tiên trong dãy Banme và vạch đầu tiên trong dãy Pasen là
Electron đang ở quỹ đạo n chưa rõ thì chuyển về quỹ đạo L và thấy rẳng bán kính quỹ đạo đã giảm đi 4 lần. Hỏi ban đầu electron đang ở quỹ đạo nào?
Khi nguyên tử hidro ở trạng thái n thì năng lượng và bán kính được xác định \(E_n=-\frac{13,6}{n^2}\) và \(r_n=n^2.r_0\), với \(n_0=5,3.10^{-11}(m)\). Khi bán kính của electron bằng 2,12.10-10 (m) thì năng lượng của nó bằng bao nhiêu?
Khi nguyên tử hidro chuyển từ trạng thái E4 về E2 thì phát ra photon có bước sóng \(\lambda _{42}\). Khi nguyên tử hidro chuyển từ trạng thái E5 về E3 thì phát ra photon có bước sóng \(\lambda _{53}\). Xác định tỉ số \(\frac{\lambda _{53}}{\lambda _{42}}\) = ?
Mẫu nguyên tử Bo khác mẫu nguyên tử Rơ-dơ-pho ở điểm nào?
Nguyên tử hiđrô ở trạng tháy cơ bản được kích thích và chuyển lên trạng thái có bán kính quỹ đạo tăng lên 16 lần. Số bức xạ mà nguyên tử có thể phát ra là
Ở nguyên tử hidro, quỹ đạo nào sau đây có bán kính lớn nhất so với bán kính các quỹ đạo còn lại?
Đối với nguyên tử hiđrô, bán kính Bo là ro=5,3.10-11 m. Nguyên tử hiđrô có thể có bán kính nào sau đây?
Electron đang ở quỹ đạo n chưa rõ thì chuyển về quỹ đạo L và thấy rẳng bán kính quỹ đạo đã giảm đi 4 lần. Hỏi ban đầu electron đang ở quỹ đạo nào?
Năng lượng của êlectron trong nguyên tử hiđrô được tính theo công thức: En = -13,6 / n2; n = 1, 2, 3, … Xác định năng lượng ở quỹ đạo dừng L.
Mẫu nguyên tử Bo khác mẫu nguyên tử Rơ-đơ-pho ở điểm nào?
Trình bày tiên đề Bo về các trạng thái dừng.
Trình bày tiên đề Bo về sự bức xạ và hấp thụ năng lượng của nguyên tử.
Chọn câu đúng.
Trạng thái dừng là
A. Trạng thái êlectron không chuyển động quanh hạt nhân.
B. Trạng thái hạt nhân không dao động.
C. Trạng thái đứng yên của nguyên tử.
D. Trạng thái ổn định của hệ thống nguyên tử.
Xét ba mức năng lượng EK, EL và EM của nguyên tử hiđrô (H.33.2). Một phôtôn có năng lượng bằng EM - EK bay đến gặp nguyên tử này.

Nguyên tử sẽ hấp thụ phôtôn và chuyển trạng thái như thế nào?
A. Không hấp thụ.
B. Hấp thụ nhưng không chuyển trạng thái.
C. Hấp thụ rồi chuyển dần từ K lên L rồi lên M.
D. Hấp thụ rồi chuyển thẳng từ K lên M.
Có một đám nguyên tử của một nguyên tố mà mỗi nguyên tử có ba mức năng lượng EK, EL và EM của nguyên tử hiđrô (H.33.2). Chiếu vào đám nguyên tử này một chùm sáng đơn sắc mà mỗi phô tôn trỏng chùm có năng lượng là ε = EM - EK. Sau đó nghiên cứu quang phổ vạch phát xạ của đám nguyên tử trên. Ta sẽ thu được bao nhiêu vạch quang phổ?

A. Một vạch.
B. Hai vạch.
C. Ba vạch.
D. Bốn vạch.
Ion crôm trong hồng ngọc phát ra ánh sáng đỏ bước sóng \(0,694 \mu m\). Tính hiệu giữa hai mức năng lượng mà khi chuyển hai mức đó, ion crôm phát ra ánh sáng nói trên.
Mẫu nguyên tử Bo khác mẫu nguyên tử Rơ-dơ-pho ở điếm nào ?
A. Mô hình nguyên tử có hạt nhân.
B. Hình dạng quỹ đạo của các êlectron.
C. Biểu thức của lực hút giữa hạt nhân và êlectron.
D. Trạng thái có năng lượng ổn định.
Hãy chỉ ra câu nói lên nội dung chính xác của tiên đề về các trạng thái dừng. Trạng thái dừng là
A. trạng thái có năng lượng xác định.
B. trạng thái mà ta có thể tính toán được chính xác năng lượng của nó.
C. trạng thái mà năng lượng của nguyên tử không thể thay đổi được.
D. trạng thái trong đó nguyên tử có thể tồn tại một thời gian xác định mà không bức xạ năng lượng.
Câu nào dưới đây nói lên nội dung chính-xác của khái niệm về quỹ đạo dừng ?
A. Quỹ đạo có bán kính tỉ lệ với bình phương của các số nguyên liên tiếp.
B. Bán kính quỹ đạo có thể tính toán được một cách chính xác.
C. Quỹ đạo mà êlectron bắt buộc phải chuyển động trên đó.
D. Quỹ đạo ứng với năng lượng của các trạng thái dừng.
Nội dung của tiên đề về sự bức xạ và hấp thụ năng lượng của nguyên được phản ánh trong câu nào dưới đây ?
A. Nguyên tử phát ra một phôtôn mỗi lần bức xạ ánh sáng.
B. Nguyên tử thu nhận một phôtôn mỗi lần hấp thụ ánh sáng.
C. Nguyên tử phát ra ánh sáng nào thì có thể hấp thụ ánh sáng đó.
D. Nguyên tử chỉ có thể chuyển giữa các trạng thái dừng. Mỗi lần chuyển, nó bức xạ hay hấp thụ một phôtôn có năng lượng đúng bằng độ chên lệch năng lượng giữa hai trạng thái đó.
Xét ba mức năng lượng EK < EL < EM của nguyên tử hiđrô. Cho biết EL - EK > EM - EL. Xét ba vạch quang phổ (ba ánh sáng đơn sắc) ứng với ba sự chuyển mức năng lượng như sau :
Vạch λLK ứng với sự chuyển EL → EK.
Vạch λML ứng với sự chuyển EL → EK.
Vạch λMK ứng với sự chuyển EM → EK.
Hãy chọn cách sắp xếp đúng.
A. λLK < λML < λMK.
B. λLK > λML > λMK.
C. λMK < λLK < λML.
D. λMK > λLK > λML.
Bước sóng ứng với bốn vạch quang phổ của hiđrô là vạch tím : 0,4102 μm; vạch chàm : 0,4340 μm; vạch lam 0,4861 μm và vạch đỏ : 0,6563 μm. Bốn vạch này ứng với sự chuyến của êlectron trong nguyên tử hiđrô từ các quỹ đạo M, N, o và p về quỹ đạo L. Hỏi vạch lam ứng với sự chuyển nào ?
A. Sự chuyển M → L.
B. Sự chuyển N → L.
C. Sự chuyển O → L.
D. Sự chuyển P → L.
Hãy xác định trạng thái kích thích cao nhất của các nguyên tử hiđr trong trường hợp người ta chỉ thu được 6 vạch quang phổ phát xạ của nguyên tử hiđrô.
A. Trạng thái L.
B. Trạng thái M.
C. Trạng thái N.
D. Trạng thái O.
Ta thu được quang phổ vạch phát xạ của một đám khí hiđrô trong hai trường hợp sau :
Trường hợp I : Kích thích đám khí hiđrô bằng ánh sáng đơn sắc mà các phôtôn có năng lượng ε1 = EM - EK.
Trường hợp 2 : Kích thích đám khí hiđrô bằng ánh sáng đơn sắc mà các phôtôn có năng lượng ε2 = EM - EL.
Hỏi trong trường hợp nào ta sẽ thu được vạch quang phổ ứng với sự chuyển EM → EL của các nguyên tử hiđrô ?
A. Trong cả hai trường hợp, ta đều thu được vạch quang phổ nói trên.
B. Trong cả hai trường hợp, ta đều không thu được vạch quang phổ nói trên.
C. Trong trường hợp 1, ta thu được vạch quang phổ nói trên ; trong trường hợp 2 thì không.
D. Trong trường hợp 1 thì không ; trong trường hợp 2, ta sẽ thu được vạch quang phổ nói trên.
Trong nguyên tử hiđrô, bán kính Bo là r0 = 5,3.10 -11 m. Bán kính quỹ đạo dừng N là
A. 47,7.10 -11 m.
B. 84,8.10 -11 m.
C. 21,2.10 -11 m.
D. 132,5.10 -11 m.
Một đám nguyên tử hiđrô đang ở trạng thái kích thích mà êlectron chuyển động trên quỹ đạo dừng N. Khi êlectron chuyển về các quỹ đạo dừng bên trong thì quang phổ vạch phát xạ của đám nguyên tử đó có bao nhiêu vạch ?
A. 3. B. 6.
C. 1. D. 4.
Theo mẫu nguyên tử Bo, bán kính quỹ đạo K của êlectron trong nguyên tử hiđrô là r0. Khi êlectron chuyển từ quỹ đạo N về quỹ đạo L thì bán kính quỹ đạo giảm bớt
A. 12r0. B. 4r0.
C. 9r0. D. 16r0.
Theo tiên đề Bo, khi êlectron trong nguyên tử hiđrô chuyển từ quỹ đạo L sang quỹ đạo K thì nguyên tử hiđrô phát ra phôtôn có bước sóng λ21, khi êlectron chuyển từ quỹ đạo M sang quỹ đạo L thì nguyên tử phát ra phôtôn. có bước sóng λ32 và khi êlectron chuyển từ quỹ đạo M sang quỹ đạo K thì nguyên tử phát ra phôtôn có bước sóng λ31. Biểu thức xác định λ31 là :
\(\begin{array}{l} A.\,\,{\lambda _{31}} = \frac{{{\lambda _{31}}.{\lambda _{21}}}}{{{\lambda _{21}} - {\lambda _{31}}}}\\ B.\,\,{\lambda _{31}} = {\lambda _{32}} - {\lambda _{21}}\\ C.\,\,{\lambda _{31}} = {\lambda _{32}} + {\lambda _{21}}\\ D.\,\,{\lambda _{31}} = \frac{{{\lambda _{32}}.{\lambda _{21}}}}{{{\lambda _{21}} + {\lambda _{32}}}} \end{array}\)
Khi êlectron ở quỹ đạo dừng thứ n thì năng lượng của nguyên tử hiđrô được xác định bởi công thức En = -13,6/n2(eV) (với n = 1, 2, 3,...). Khi êlectrôn chuyển từ quỹ đạo dừng n = 3 về quỹ đạo dừng n = 1 thì nguyên tử phát ra phôtôn có bước sóng λ1. Khi êlectron chuyển từ quỹ đạo dừng n = 5 về quỹ đạo dừng n = 2 thì nguyên tử phát ra phôtôn có bước sóng λ2. Mốì liên hệ giữa hai bước sóng λ1 và λ2 là
A. λ2 = 5λ1.
B. λ2 = 4λ1.
C. 27λ2 = 128λ1.
D. 189λ2 = 800λ1.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Vạch thứ hai của dãy Lyman trong quang phổ của nguyên tử hiđrô ℓà \(\lambda _1=102,6(nm)\)
\(E_{31}=E_3-E_1=\frac{hc}{\lambda _1}=12,1(eV)\)
Năng ℓượng tối thiểu cần thiết để bứt êℓectron ra khỏi nguyên tử từ trạng thái cơ bản
\(E_{\infty 1}=E_\infty -E_1=13,6(eV)\)
Bước sóng ngắn nhất của vạch quang phổ trong dãy Pasen ℓà
\(E_{\infty 3}=E_\infty -E_3=E_{\infty 1}-E_{31}=1,49(eV)\)
\(E_{\infty 3}=\frac{hc}{\lambda }\Rightarrow \lambda =\frac{hc}{E_{\infty 3}}=8,33.10^{-7}(m)\)
Câu trả lời của bạn
Nguyên tử Hyđrô đang ở trạng thái cơ bản sẽ hấp thụ phôtôn
\(E=E_n-E_1=-13,6\left ( \frac{1}{n^2}- 1 \right )\)
Nguyên tử Hyđrô đang ở trạng thái cơ bản sẽ hấp thụ phôtôn có n là số nguyên
\(n=2 \Rightarrow E=13,6\left ( 1-\frac{1}{2^2} \right ) =10,2(eV)\)
\(n=3 \Rightarrow E=13,6\left ( 1-\frac{1}{3^2} \right ) \approx 12,09(eV)\)
\(n=4 \Rightarrow E=13,6\left ( 1-\frac{1}{4^2} \right ) \approx 12,75(eV)\)
Vậy nguyên tử Hyđrô đang ở trạng thái cơ bản sẽ không hấp thụ phôtôn có năng ℓượng bằng 11,12 (eV)
Nguyên tử Hyđrô đang ở trạng thái cơ bản sẽ hấp thụ phôtôn
\(E=E_n-E_1=-13,6\left ( \frac{1}{n^2}- 1 \right )\)
Ta thế đáp án vào nếu đáp án nào cho n là số nguyên chính là đáp án
\(E=12,75(eV)\Rightarrow n=4\)
Câu trả lời của bạn
Khi êℓectron chuyển về các quỹ đạo dừng bên trong thì quang phổ vạch phát xạ của đám nguyên tử đó phát ra
\(C_{2}^{4}=\frac{4.(4-1)}{2}=6\) (bức xạ)
Câu trả lời của bạn
Vạch quang phổ trong dãy Pasen với tần số ℓớn nhất ℓà
\(E_{Pmax}=E_\infty -E_3=-\frac{13,6}{\infty ^2}-\left (-\frac{13,6}{3^2} \right )=1,51(eV)\)
\(E_{Pmax}=hf\Rightarrow f=\frac{E_{Pmax}}{h}=3,65.10^{14}(Hz)\)
Câu trả lời của bạn
Bước sóng dài nhất trong dãy Banme thì
\(E_{32}=E_3-E_2\)
Bước sóng dài nhất trong dãy Pasen thì
\(E_{43}=E_4-E_3\)
Bước sóng của vạch \(H_\beta\) ℓà
\(E_{42}=E_4-E_2=E_{32}+E_{43}\Rightarrow \frac{hc}{\lambda _{H\beta} }=\frac{hc}{\lambda _B}+\frac{hc}{\lambda _P}\)
\(\Rightarrow \frac{1}{\lambda _{H\beta} }=\frac{1}{\lambda _B}+\frac{1}{\lambda _P} \Rightarrow \lambda _{H\beta}=\frac{\lambda _B.\lambda _P}{\lambda _B+\lambda _P}=0,4866(\mu m)\)
Câu trả lời của bạn
Bước sóng dài nhất trong dãy Banme thì
\(E_{32}=E_3-E_2\)
Bước sóng dài nhất trong dãy Laiman thì
\(E_{21}=E_2-E_1\)
Bước sóng dài thứ hai của dãy Laiman
\(E_{31}=E_3-E_1=E_{32}+E_{21}\Rightarrow \frac{hc}{\lambda }=\frac{hc}{\lambda _B}+\frac{hc}{\lambda _L}\)
\(\Rightarrow \frac{1}{\lambda }=\frac{1}{\lambda _B}+\frac{1}{\lambda _L} \Rightarrow \lambda =\frac{\lambda _B.\lambda _L}{\lambda _B+\lambda _L}=0,10286(\mu m)\)
Câu trả lời của bạn
Bước sóng của vạch quang phổ thứ nhất trong dãy Laiman
\(E_{21}=E_2-E_1\)
Bước sóng của vạch quang phổ thứ nhất và thứ hai của dãy Banme
\(E_{32}=E_3-E_2;E_{42}=E_4-E_2\)
Bước sóng của vạch thứ ba trong dãy Laiman
\(E_{41}=E_4-E_1=E_{42}+E_{21}\Rightarrow \frac{hc}{\lambda }=\frac{hc}{\lambda _{42}}+\frac{hc}{\lambda _{21}}\)
\(\Rightarrow \frac{1}{\lambda _{41}}=\frac{1}{\lambda _{42}}+\frac{1}{\lambda _{21}} \Rightarrow \lambda _{41}=\frac{\lambda _{42}.\lambda _{21}}{\lambda _{42}+\lambda _{21}}=0,0975(\mu m)\)
Câu trả lời của bạn
Bước sóng của vạch quang phổ thứ nhất trong dãy Laiman
\(E_{21}=E_2-E_1\)
Bước sóng của vạch quang phổ thứ nhất và thứ hai của dãy Banme
\(E_{32}=E_3-E_2;E_{42}=E_4-E_2\)
Bước sóng của vạch thứ ba trong dãy Laiman
\(E_{43}=E_4-E_3=E_{42}+E_{32}\Rightarrow \frac{hc}{\lambda _{43}}=\frac{hc}{\lambda _{42}} – \frac{hc}{\lambda _{32}}\)
\(\Rightarrow \frac{1}{\lambda _{43}} = \frac{1}{\lambda _{42}} – \frac{1}{\lambda _{32}} \Rightarrow \lambda _{43}=\frac{\lambda _{42} .\lambda _{32}}{\lambda _{32} – \lambda _{42}}=1,8754(\mu m)\)
Câu trả lời của bạn
Quỹ đạo M ứng với n = 3
\(\Rightarrow E_M=- \frac{13,6}{3^2}= – 1,51(eV)\)
Câu trả lời của bạn
Trong nguyên tử hiđrô, êℓectrôn từ quỹ đạo L chuyển về quỹ đạo K
\(E_{LK}=E_L-E_K=\frac{hc}{\lambda }\Rightarrow E_L=\frac{hc}{\lambda }+E_K= – 3,4(eV)\)
Câu trả lời của bạn
Năng lượng ion hóa nguyên tử Hyđrô mà 13,6 eV => Năng lượng lớn nhất của bức xạ mà nguyên tử Hidro có thể phát ra là 13,6(eV)
Bước sóng ngắn nhất mà nguyên tử có thể bức ra là \(E_{max}=\frac{hc}{\lambda _{min}}=13,6(eV)\Rightarrow \lambda _{min}=\frac{hc}{E_{max}}=9,14.10^{-8}(m)\)
Câu trả lời của bạn
Nguyên tử phát bức xạ điện từ có bước sóng
\(E_{mn}=E_m-E_n=12,75(eV)\)
\(E_{mn}=\frac{hc}{\lambda }\Rightarrow \lambda = \frac{hc}{E_{mn} }=9,74.10^{-8}(m)\)
Câu trả lời của bạn
Nguyên tử phát ra bức xạ có tần số
\(E_{mn}=E_m-E_n=-1,514-(-3,407)=1,893(eV)\)
\(E_{mn}=hf \Rightarrow f = \frac{E_{mn}}{h }=4,57.10^{14}(Hz)\)
Câu trả lời của bạn
Ta có:\(E_n – E_m = -\frac{13,6}{n^2} + \frac{13,6}{m^2} = \Delta E\)
+ Thay \(\Delta E = 2,55 \Rightarrow 2,55 = -\frac{13,6}{n^2} + \frac{13,6}{m^2}\)
\(\Rightarrow \frac{3}{16}= -\frac{1}{n^2} + \frac{1}{m^2}\) \(\Rightarrow \left\{\begin{matrix} m = 2\\ n = 4 \end{matrix}\right.\)
+ Thay \(\Delta E = 8,36 \Rightarrow 8,36 = -\frac{13,6}{n^2} + \frac{13,6}{m^2}\)
\(\Rightarrow \frac{209}{240}= -\frac{1}{n^2} + \frac{1}{m^2}\) ⇒ Vô nghiệm
+ Thay \(\Delta E = 10,2 \Rightarrow 10,2 = -\frac{13,6}{n^2} + \frac{13,6}{m^2}\)
\(\Rightarrow \frac{3}{4}= -\frac{1}{n^2} + \frac{1}{m^2}\) \(\Rightarrow \left\{\begin{matrix} m = 1\\ n = 2 \end{matrix}\right.\)
+ Thay \(\Delta E = 12,75 \Rightarrow 12,75 = -\frac{13,6}{n^2} + \frac{13,6}{m^2}\)
\(\Rightarrow \frac{15}{16}= -\frac{1}{n^2} + \frac{1}{m^2}\) \(\Rightarrow \left\{\begin{matrix} m = 1\\ n = 4 \end{matrix}\right.\)
Câu trả lời của bạn
Theo mẫu nguyên tử Bo, lực Cu_lông đóng vai trò là lực hướng tâm gây ra chuyển động của electron \(k \frac{e^2}{r^2} = m_e\frac{v_n^2}{r_n}\rightarrow v_n = e \sqrt{\frac{k}{r_n}}; v_1 = 4v_2 \rightarrow r_2 = 16 r_1 \rightarrow n_2 = 4n_1\)
=> Chuyển từ quỹ đạoN vè K
Câu trả lời của bạn
\(R \sim n^2 \Rightarrow\) Tăng 4 lần thì n tăng 2 lần.
\(L \Rightarrow n = 2 \Rightarrow\) n tăng từ 2 lên 4.
\(\varepsilon = h.f = E_4 – E_2 = (- \frac{13,6}{4^2} + \frac{13,6}{2^2}).1,6.10^{-19} = 4,08.10^{19} \rightarrow f = \varepsilon /h =6,16.10^{14}Hz\)
Câu trả lời của bạn
Hai vạch có bước sóng dài nhất trong dãy Laiman ứng với sự chuyển mức năng lượng \(E_2 \rightarrow E_1\) và \(E_3 \rightarrow E_1\) nên
\(E_2 – E_1 = \frac{hc}{\lambda _{21}} (1)\)
\(E_3 – E_1 = \frac{hc}{\lambda _{31}} (2)\)
Từ (1) và (2) suy ra: \(E_3 – E_2 = hc(\frac{1}{\lambda _{31}} – \frac{1}{\lambda _{21}}) = \frac{hc}{\lambda }\Rightarrow \frac{1}{\lambda }= \frac{1}{\lambda _{31}} – \frac{1}{\lambda _{21}} \Rightarrow \lambda = \frac{\lambda _{31}. \lambda _{21}}{\lambda _{21} – \lambda _{31}} = 0,6458.10^{-6} (m)\)
Câu trả lời của bạn
Bán kính của electron ở quỹ đạo L là:
\(r_L = n_L^2.r_o = 4ro\)
Bán kính của electron ở quỹ đạo O là:
\(r_0 = n_0^2.r_o = 25ro\)
=> Khi electron chuyển từ quỹ đạo L lên quỹ đạo O thì bán kính quỹ đạo tăng thêm
\(\Delta r= 25ro-4ro = 21 ro\)
Câu trả lời của bạn
Công thức bán kính Borh cho ta: \(r = n^2r_0\)
Ban đầu hidro đang ở trạng thái kích thích thứ nhất: \(r_1 = 2^2r_0\). Lúc sau ở trạng thái kích thích khác, bán kính tăng lên 9 lần: \(r’ = 9r_1 = 9.2^2r_0 = x^2r_0 \rightarrow x = 6\). Vậy Hidro đang ở quỹ đạo lượng từ P. Bức sóng hồng ngoại lớn nhất là bước sóng phát ra khi hidro từ mức 6 về mức 5, bước sóng nhìn thấy nhỏ nhất khi hidro từ mức 6 về mức 2. Ta có:
\(\frac{\lambda _{65}}{\lambda _{62}} = \frac{E_6 – E_2}{E_6 – E_5} = \frac{\frac{1}{2^2} – \frac{1}{6^2}}{\frac{1}{5^2} – \frac{2}{6^2}} = \frac{200}{11}\approx 18,2\)
Câu trả lời của bạn
Bước sóng dài nhất của vạch quang phổ trong dãy Laiman thì
\(\frac{hc}{\lambda _1}=E_2-E_1\)
Bước sóng của vạch kề với nó trong dãy này ℓà \(\lambda\)2 thì
\(\frac{hc}{\lambda _2}=E_3-E_1\)
Bước sóng \(\lambda\)a của vạch quang phổ H\(\alpha\) trong dãy Banme ℓà
\(\frac{hc}{\lambda _\alpha }=E_3-E_2=\frac{hc}{\lambda _2 }-\frac{hc}{\lambda _1 } \Rightarrow \frac{1}{\lambda _\alpha }=\frac{1}{\lambda _2 }-\frac{1}{\lambda _1 } \Rightarrow \lambda _\alpha =\frac{\lambda _1\lambda _2}{\lambda _1-\lambda _2}\)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *