Nội dung bài luyện tập Tính chất của Tính chất của kim loại kiềm, kim loại kiềm thổ là bài tổng ôn, củng cố các kiến thức đã học về Tính chất của kim loại kiềm, kim loại kiềm thổ. Ngoài ra còn rèn luyện cho các em học sinh kĩ năng giải các bài tập và các dạng toán quan trọng.
| Vị trí trong Bảng tuần hoàn | Cấu hình electron lớp ngoài cùng | Tính chất hóa học đặc trưng | Điều chế | |
| Kim loại kiềm | Nhóm IA | ns1 | Có tính khử mạnh nhất trong các kim loại \(M\rightarrow M^{+} + e\) | Điện phân muối halogen nóng chảy \(2MX\overset{dpnc}{\rightarrow}2M+X_{2}\) |
| Kim loại kiềm thổ | Nhóm IIA | ns2 | Có tính khử mạnh chỉ sau kim loại kiềm \(M\rightarrow M^{2+}+2e\) | \(MX_{2}\overset{dpnc}{\rightarrow}M+X_{2}\) |
Hỗn hợp rắn A gồm Ca(HCO3); CaCO3; NaHCO3; Na2CO3. Nung A đến khối lượng không đổi được chất rắn B gồm:
Các muối hidrocacbonat của kim loại kiềm và kiềm thổ đều bị phân hủy tạo muối cacbonat khi ở nhiệt độ không quá cao, tuy nhiên chỉ có muối cacbonat của kim loại kiềm thổ mới bị thủy phân ở nhiệt độ cao tạo oxit kim loại.
⇒ Nhiệt phân hỗn hợp ban đầu sẽ thu được: CaO; Na2CO3.
Cho các chất: Na2CO3; NaHCO3; NaHSO4; HCl; BaCl2; CuO; Fe. Số cặp chất có thể tác dụng trực tiếp với nhau ở nhiệt độ thường là:
Các cặp chất: (Na2CO3 + NaHSO4); (Na2CO3 + HCl); (Na2CO3 + BaCl2); (NaHCO3 + NaHSO4); (NaHCO3 + HCl); (NaHSO4 + BaCl2); (NaHSO4 + CuO); (NaHSO4 + Fe); (HCl + CuO); (HCl + Fe).
Hoà tan hoàn toàn 14,52 gam hỗn hợp X gồm NaHCO3, KHCO3 và MgCO3 bằng dd HCl dư, thu được 3,36 lít khí CO2 (đktc) và dd chứa m gam muối KCl. Giá trị của m là:
Coi hỗn hợp gồm KHCO3 và MgCO3 có số mol lần lượt là x và y (vì \(M_{NaHCO_{3}}= M_{MgCO_{3}}\))
\(\\ n_{CO_{2}}= 0,15 \ mol \Rightarrow x + y = 0,15 \\ 100x + 84y = 14,52 \\ \Rightarrow x = 0,12 ; \ y = 0,03 \\ \Rightarrow m = 0,12 . (39 + 35,5) = 8,94 \ g\)
Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2, thu được m gam kết tủa. Giá trị của m là:
Dạng toán CO2 tác dụng với hỗn hợp bazơ của kim loại nhóm kiềm – kiềm thổ.
\(\begin{array}{l} {n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15(mol)\\ {n_{O{H^ - }}} = {n_{NaOH}} + 2.{n_{Ba{{(OH)}_2}}} = 0,15 + 2.0,1 = 0,25(mol) \end{array}\)
Vì:\({n_{C{O_2}}} < {n_{O{H^ - }}} < 2{n_{C{O_2}}} \Rightarrow {n_{C{O_3}^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}}\)
\({n_{HC{O_3}^ - }} = {n_{C{O_2}}} - {n_{C{O_3}^{2 - }}}\)
\(\Rightarrow {n_{C{O_3}^{2 - }}} = 0,15mol\); có \({n_{Ba{{\left( {OH} \right)}_2}}} = 0,1mol\)
\({n_{BaC{{\rm{O}}_3}}} = 0,1mol\)
Vậy \({m_{BaC{O_3}}} = 19,700g\)
Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 131,4 gam X vào nước, thu được 6,72 lít khí H2 (đktc) và dung dịch Y, trong đó có 123,12 gam Ba(OH)2. Hấp thụ hoàn toàn 40,32 lít khí CO2 (đktc) vào Y, thu được m gam kết tủa. Giá trị của m là:
Quy hỗn hợp X về Ba, Na và O.
\({{\rm{n}}_{{\rm{Ba}}}}{\rm{ = }}{{\rm{n}}_{{\rm{Ba(OH}}{{\rm{)}}_{\rm{2}}}}}{\rm{ = 0,72 mol; }}{{\rm{n}}_{{{\rm{H}}_{\rm{2}}}}}{\rm{ = 0,3 mol}}\)
Đặt nNa = x (mol) , nO = y (mol)
BTKL: mNa + mO = mX - mBa ⇔ 23x + 16y = 32,76 (1)
BT electron: ne nhường = ne nhận
(ở đây Na, Ba nhường e, O nhận e về O2-, H+ nhận e thành H2 bay lên)
⇔ x + 2 .0,72 = 2y + 0,3. 2 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ \begin{array}{l} 23x{\rm{ }} + {\rm{ }}16y{\rm{ }} = {\rm{ }}32,76\;\;\\ x{\rm{ - 2y }} = - 0,84 \end{array} \right. \Leftrightarrow \left\{ \begin{array}{l} x = 0,84\\ y = 0,84 \end{array} \right.\)
⇒ nOH- = nNa + 2nBa = 2,28 mol
\(n_{CO_2}=1,8\ mol\)
\(\Rightarrow n_{{CO_3}^{2-}}=0,48\ mol,\ n_{{HCO_3}^-}=1,32\ mol\)
\(\Rightarrow n_{BaCO_3}=0,48\ mol \Rightarrow m_{BaCO_3}=94,56\ g\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 28có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
Dung dịch nào dưới đây dùng để phân biệt dung dịch KCl với dung dịch K2SO4?
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
Cho các chất: (1) NaCl; (2) Na2CO3; (3) BaCl2; (4) Ca(OH)2; (5) Na3PO4; (6) Na2SO4. Những chất có thể làm mềm nước cứng tạm thời là:
Phát biểu nào sau đây không đúng?
Để phân biệt dung dịch CaCl2 với dung dịch NaCl, người ta dùng dung dịch:
Cho các phản ứng xảy ra theo sơ đồ sau:
X1 + H2O 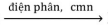 X2 + X3 + H2↑
X2 + X3 + H2↑
X2 + X4 → BaCO3↓ + K2CO3 + H2O
Chất X1, X4 lần lượt là:
Câu 8-20: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 28.
Bài tập 1 trang 132 SGK Hóa học 12
Bài tập 2 trang 132 SGK Hóa học 12
Bài tập 3 trang 132 SGK Hóa học 12
Bài tập 4 trang 132 SGK Hóa học 12
Bài tập 5 trang 132 SGK Hóa học 12
Bài tập 6 trang 132 SGK Hóa học 12
Bài tập 1 trang 170 SGK Hóa 12 Nâng cao
Bài tập 2 trang 170 SGK Hóa 12 Nâng cao
Bài tập 3 trang 170 SGK Hóa 12 Nâng cao
Bài tập 28.1 trang 65 SBT Hóa học 12
Bài tập 28.2 trang 65 SBT Hóa học 12
Bài tập 28.3 trang 66 SBT Hóa học 12
Bài tập 28.4 trang 66 SBT Hóa học 12
Bài tập 28.5 trang 66 SBT Hóa học 12
Bài tập 28.6 trang 66 SBT Hóa học 12
Bài tập 28.7 trang 66 SBT Hóa học 12
Bài tập 28.8 trang 66 SBT Hóa học 12
Bài tập 28.9 trang 67SBT Hóa học 12
Bài tập 28.10 trang 67 SBT Hóa học 12
Bài tập 28.11 trang 67 SBT Hóa học 12
Bài tập 28.12 trang 67 SBT Hóa học 12
Bài tập 28.13 trang 67 SBT Hóa học 12
Bài tập 28.14 trang 67 SBT Hóa học 12
Bài tập 28.15 trang 67 SBT Hóa học 12
Bài tập 28.16 trang 68 SBT Hóa học 12
Bài tập 28.17 trang 68 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
Dung dịch nào dưới đây dùng để phân biệt dung dịch KCl với dung dịch K2SO4?
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
Cho các chất: (1) NaCl; (2) Na2CO3; (3) BaCl2; (4) Ca(OH)2; (5) Na3PO4; (6) Na2SO4. Những chất có thể làm mềm nước cứng tạm thời là:
Phát biểu nào sau đây không đúng?
Để phân biệt dung dịch CaCl2 với dung dịch NaCl, người ta dùng dung dịch:
Cho các phản ứng xảy ra theo sơ đồ sau:
X1 + H2O 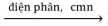 X2 + X3 + H2↑
X2 + X3 + H2↑
X2 + X4 → BaCO3↓ + K2CO3 + H2O
Chất X1, X4 lần lượt là:
Cho dãy kim loại: Na, Ba, Al, K, Mg. Số kim loại trong dãy phản ứng với lượng dư dung dịch FeCl3 có tạo kết tủa là:
Kim loại nào sau đây khi cho vào dung dịch CuSO4 bị hòa tan hết và phản ứng tạo thành kết tủa gồm 2 chất:
Cho 26 gam hỗn hợp chất rắn A gồm Ca, MgO, Na2O tác dụng hết với dung dịch HCl 1M (vừa đủ) thu được dung dịch A trong đó có 23,4 gam NaCl. Giá trị của V là:
Hấp thu hoàn toàn 4,48 lít khí CO2 (ở đkc) vào 500ml dung dịch hỗn hợp gồm NaOH 0,1M và Ba(OH)2 0,25M, sinh ra m gam kết tủa. Giá trị m là
Cho một mẫu hợp kim Na-Ca-K tác dụng với nước (dư), thu được dung dịch X và 7,84 lít H2 (ở đktc). Thể tích dung dịch axit H2SO4 1,4M cần dùng để trung hoà dung dịch X là:
Hòa tan hoàn toàn hỗn hợp gồm một kim loại hóa trị 1 và oxit kim loại hóa trị 2 vào nước dư. Sau khi phản ứng xong được 500 ml dd X chỉ chứa một chất tan duy nhất và 4,48 lít khí H2 (đktc). Nồng độ mol/l của dung dịch X là:
Hấp thụ hoàn toàn 3,36 lít khí CO2 (điều kiện tiêu chuẩn) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2 thu được m gam kết tủa. Giá trị của m là:
Cho 7,1 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng với lượng dư dung dịch HCl loãng thu được 5,6 lít khí. Hai kim loại X, Y có thể là:
Hòa tan hoàn toàn 8,94 gam hỗn hợp gồm Na, K và Ba vào nước thu được dung dịch X và 2,688 lit khí H2 (đktc) . Dung dịch Y gồm HCl và H2SO4 có tỉ lệ mol tương ứng: 4 : 1. Trung hòa dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
13,7
12,78
18,46
14,62
Hòa tan hỗn hợp Na2CO3, KHCO3, Ba(HCO3)2 (trong đó số mol Na2CO3 và KHCO3 bằng nhau) vào nước lọc thu được dung dịch X và m gam kết tủa Y. Biết X tác dụng vừa đủ 0,16mol NaOH hoặc 0,24mol HCl thì hết khí bay ra. Giá trị m là:
Hấp thụ hoàn toàn 1,568 lít CO2 (đktc) vào 500ml dung dịch NaOH 0,16M thu được dung dịch X. Thêm 250 ml dung dich Y gồm BaCl2 0,16M và Ba(OH)2 a mol/l vào dung dịch X thu được 3,94 gam kết tủa và dung dịch Z. Tính a?
0,02M
0,04M
Cho 2,22 gam hỗn hợp kim loại gồm K, Na và Ba vào nước được 500ml dung dịch X có pH = 13. Cô cạn dung dịch X được m gam chất rắn. m là:
4,02
3,42
Hoà tan 46 gam một hỗn hợp Ba và hai kim loại kiềm A, B thuộc hai chu kì kế tiếp nhau vào nước thu được dung dịch C và 11,2 lít khí (đktc). Nếu thêm 0,18 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng vẫn chưa kết tủa hết Ba. Nếu thêm 0,21 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng còn dư Na2SO4. A và B là:
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng với dung dịch axit HCl thu được 4,15 gam hỗn hợp muối clorua. Khối lượng của mỗi hiđrôxit trong hỗn hợp lần lượt là:
A. 1,17 gam và 2,98 gam.
B. 1,12 gam và 1,6 gam.
C. 1,12 gam và 1,92 gam.
D. 0,8 gam và 2,24 gam.
Sục 6,72 lít khí CO2 (đktc) vào dung dịch có chứa 0,25 mol Ca(OH)2. Khối lượng kết tủa thu được là:
A.10 gam.
B. 15 gam.
C. 20 gam.
D. 25 gam.
Chất nào sau đây có thể dùng để làm mềm nước cứng có tính cứng vĩnh cửu?
A. NaCl
B. H2SO4
C. Na2CO3
D. HCl
Có 28,1 gam hỗn hợp MgCO3 và BaCO3 trong đó MgCO3 chiếm a% khối lượng. Cho hỗn hợp trên tác dụng hết dụng với dung dịch axit HCl để lấy khí CO2 rồi đem sục vào dung dịch có chứa 0,2 mol Ca(OH)2 được kết tủa b. Tính a để kết B thu được là lớn nhất?
Cách nào sau đây thường được dùng để điều chế kim loại Ca?
A. Điện phân dung dịch CaCl2 có màng ngăn
B. Điện phân CaCl2 nóng chảy
C. Dùng Al để khử CaO ở nhiệt độ cao
D. Dùng kim loại Ba để đẩy Ca ra khỏi dung dịch CaCl2
Sục a mol khí CO2 vào dung dịch Ca(OH)2 thu được 3 gam kết tủa. Lọc tách kết tủa, dung dịch còn lại mang đun nóng thu thêm được 2 gam kết tủa nữa. Giá trị của a là:
A. 0,05 mol.
B. 0,06 mol.
C. 0,07 mol.
D. 0,08 mol.
Khi điện phân MgCl2 nóng chảy
A. Ở cực dương, ion Mg2+ bị oxi hóa
B. Ở cực âm, ion Mg2+ bị khử.
C. Ở cực dương, nguyên tử Mg bị oxi hóa.
D. Ở cực âm, nguyên tử Mg bị khử.
Điện phân một muối kim loại M nóng chảy với cường độ dòng là 10A trong thời gian 2 giờ, người ta thu được ở catot 0,373 mol kim loại M. Số oxi hóa kim loại M trong muối là:
A. +1
B. +2
C. +3
D. +4
1,24 gam Na2O tác dụng với nước, được 100 ml dung dịch. Nồng độ mol của chất trong dung dịch là:
A. 0,04M
B. 0,02M
C. 0,4M
D. 0,2M
Có 3 lọ, mỗi lọ đựng một dung dịch sau: BaCl2, Ba(NO3)2, Ba(HCO3)2. Chỉ dùng thuốc thử nào sau đây có thể nhận biết được các dung dịch trên
A. Quỳ tím
B. Phenolphtalein
C. Na2CO3
D. AgNO3
Điện phân nóng chảy 4,25 g muối clorua của một kim loại kiềm thu được 1,568 lít khí tại anot (đo ở 109,2°c và 1 atm). Kim loại kiềm đó là
A. Li.
B. Na.
C. K.
D. Rb.
Cho 21,6 g một kim loại chưa biết hoá trị tác dụng hết với dung dịch HNO3 loãng thu được 6,72 lít N2O duy nhất (đktc). Kim loại đó là
A. Na.
B. Zn.
C. Mg.
D. Al.
Sục 11,2 lít khí SO2 (đktc) vào dung dịch NaOH dư, dung dịch thu được cho tác dụng với BaCl2 dư thì khối lượng kết tủa thu được là
A. 107,5 g.
B. 108,5g
C. 106,5 g.
D. 105,5g.
Sục V lít khí SO2 (đktc) vào dung dịch brom dư thu được dung dịch X. Cho BaCl2 dư vào dung dịch X thu được 23,3 g kết tủa. V có giá trị là
A. 1,12
B. 2,24.
C. 3,36.
D. 6,72.
Cho 5,75 g hỗn hợp Mg, Al và Cu tác dụng với dung dịch HNO3 loãng, dư thu được 1,12 lít (đktc) hỗn hợp khí X gồm NO và N2O (đktc). Tỉ khối của X đối với khí H2 là 20,6. Khối lượng muối nitrat sinh ra trong dung dịch là
A. 27,45 g.
B. 13,13 g.
C. 58,91 g
D. 17,45 g.
Xác định các chất trong chuỗi phản ứng sau :
A + B → C + H2O
B → C + H2O + D
D+ A → B hoặc C
Biết D là hợp chất của cacbon. A, B, C là hợp chất của một kim loại, khi đốt nóng cho ngọn lửa màu vàng.
Cho các chất: MgCO3, MgO, Mg(OH)2, MgCl2, MgSO4. Hãy viết PTHH của các chuỗi phản ứng có thể xảy ra theo sơ đồ:
A ⟶ B ⟶ C ⟶ D ⟶ E
Ion Ca2+ có cấu hình electron giống với cấu hình electron của nguyên tử khí hiếm và ion halogen nào ? Viết cấu hình electron của chúng.
Bằng những phản ứng hoá học nào có thể phân biệt được các chất trong mỗi dãy sau ?
a) Các kim loại: Al, Mg, Ba, Na.
b) Các dung dịch muối: NaCl, Ba(NO3)2, Al2(SO4)3.
c) Các oxit: CaO, FeO, Al2O3.
d) Các dung dịch: NaNO3, Ca(NO3)2, Al(NO3)3.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Hòa tan hoàn toàn 16,3g hỗn hợp Na và K vào 1500ml nước, thấy thoát ra 5,6 lít H2(dktc). % khoi lượng K là??? Mong anh chị bạn bè giúp đỡ ạ...
Câu trả lời của bạn
\(n_{H_2}=\dfrac{v}{22,4}=\dfrac{5,6}{22,4}=0,25mol\)
2Na+2H2O\(\rightarrow\)2NaOH+H2
2K+2H2O\(\rightarrow\)2KOH+H2
-Gọi số mol Na là x, số mol K là y. Ta có hệ:
\(\left\{{}\begin{matrix}m_{hh}=23x+39y=16,3\\n_{H_2}=\dfrac{x}{2}+\dfrac{y}{2}=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
mNa=0,2.23=4,6 gam
mK=0,3.39=11,7 gam
%K=\(\dfrac{11,7.100}{16,3}\approx71,8\%\)
%Na=100%=71,8%=28,2%
Hoàn thành sơ đồ chuyển hóa sau :
Ca - > CaO - > Ca(OH)2 - > CaCO3 - > Ca(HCO3)2 - > CaCl2 - > CaCO3
Câu trả lời của bạn
1) 2Ca + O2 \(\rightarrow\) 2CaO
2) CaO + H2O \(\rightarrow\)Ca(OH)2
3) Ca(OH)2 + CO2 \(\rightarrow\) CaCO3 + H2O
4) CaCO3 + CO2 + H2O \(\rightarrow\) Ca(HCO3)2
5) Ca(HCO3)2 + 2HCl \(\rightarrow\) CaCl2 + 2CO2 + 2H2O
6)CaCl2 + K2CO3 \(\rightarrow\) CaCO3 + KCl
1) Tìm 2 chất vô cơ thỏa mãn chất R trong sơ đồ sau :
Câu trả lời của bạn
2 chất vô cơ thỏa mãn R là BaCO3 hoặc caCO3 và NaCl hoặc KCl
Mình sẽ làm ví dụ 1 trong 2 chất trên nha !
Mình chọn R là BaCO3 hoặc R là naCl ( 2 TH kia thì tương tự )
Trường hợp R là BaCO3
Xác định :
A : \(BaO\)
X: CO2
B : Ba(OH)2
Y : NaHCO3
C BaCl2
Z : Na2CO3
PTHH theo sơ đồ của đề ra :
\(BaCO3-^{t0}->BaO+CO2\)
\(BaO+CO2->BaCO3\downarrow\)
\(BaO+H2O->Ba\left(OH\right)2\)
\(CO2+Na2CO3+H2O->2NaHCO3\)
\(NaHCo3+ba\left(OH\right)2->Na2CO3+BaCO3\downarrow+H2O\)
Ba(OH)2 + 2HCl - > BaCl2 + 2H2O
NaHCO3 -t0- > Na2CO3 + CO2 + H2O
\(Bacl2+Na2CO3->BaCO3\downarrow+2NaCl\)
Trường hợp R là NaCl
Xác định :
A: Na
X : Cl2
B : NaOH
Y : HCl
C: Na2CO3 (hoặc Na2SO4)
z : Cacl2 hoặc Bacl2
PTHH :
\(2NaCl-^{đpnc}->2Na+Cl2\uparrow\)
\(2Na+Cl2-^{t0}->2NaCl\)
\(2Na+2H2O->2NaOH+H2\)
\(Cl2+H2-^{t0}->2HCl\)
NaOH + HCl - > Nacl + H2O
NaOH + CO2 - > Na2CO3
2HCl + caO - > cacl2 + H2O
Na2CO3 + cacl2 - > 2NaCl + CaCO3
Cần hòa tan bao nhiêu gam KOH vào 68,8 gam nước để được đ KOH 14 phần trăm
Các bạn ơi giúp mk với chiều mk cần rồi TKS mấy bạn nhiều
Câu trả lời của bạn
Gọi số g KOH thêm vào là x(g)
Ta có:
\(\dfrac{x}{68,8+x}.100\%=14\%\)
\(\dfrac{x}{68,8+x}=0,14\)
x=0,14(68,8+x)
x=9,632+0,14x
0,86x=9,632
x=11,2
Vậy..................
Hấp thụ hoàn toàn 2,24 lít khí co2(dktc) vào dung dịch nước vôi trong có chứa 0,075 mol ca(oh)2. Muối thu đc sau phản ứng là
bài2: hấp thụ hoàn toàn 11,2lít khí co2 ( dktc) bằng 1 dung dịch chưa 20g naoh . Muối thu đc tạo thành là
Câu trả lời của bạn
bài 1
nCO2=2,24/22,4=0,1mol
nCa(OH)2<nCO2<2nCa(OH)2
muối thu được là CaCO3,Ca(HCO3)2
Cho khí CO2(đktc) phản ứng với 80g dung dịch NaOH 25% tạo thành hỗn hợp muối và muối trung hòa theo tỉ lệ số mol là 2:3. Vậy thể tích CO2 cần dùng là bao nhiêu?
Câu trả lời của bạn
\(n_{NaOH}=\dfrac{80.25}{100.40}=0,5mol\)
\(Na^++HCO_3^-\rightarrow NaHCO_3\)
x--------->x----------->x
\(2Na^++CO_3^{2-}\rightarrow Na_2CO_3\)
(0,5-x)-->(0,5-x)-->(0,5-x)
Theo đề: \(\dfrac{x}{0,5-x}=\dfrac{2}{3}\Rightarrow x=0,2\) mol
\(CO_2+OH^-\rightarrow HCO_3^-\)
0,2<-----0,2<-------0,2
\(HCO_3^-+OH^-\rightarrow CO_3^{2-}+H_2O\)
0,3<------0,3<--------0,3
\(\Rightarrow\sum n_{HCO_3^-}=0,2+0,3=0,5mol\)
\(\Rightarrow n_{CO_2}=n_{HCO_3^-}=0,5mol\)
\(\Rightarrow V_{CO_2}=22,4.0,5=11,2\left(\text{lít}\right)\)
Cho 22.2g hh metylaxetat và axit propionic tác dụng với V lít dd hỗn hợp NaOH 1M và Ba(OH)2 0.25M. Giá trị tối thiểu của V cần dùng là??
A.400
B.300
C.100
D.200
Câu trả lời của bạn
\(\left\{{}\begin{matrix}CH_3C\text{OO}CH_3\\C_2H_5C\text{OO}H\end{matrix}\right.\) đều có CT là C3H6O2 suy ra nhh = 0,3 (mol)
Cả hai chất đều tác dụng với Ba(OH)2 theo tỉ lệ 2:1
2CH3COOCH3 + Ba(OH)2 \(\rightarrow\) (CH3COO)2Ba + 2CH3OH
2C2H5COOH + Ba(OH)2 \(\rightarrow\) (C2H5COO)2Ba + 2H2O
VBa(OH)2 = 0,6 (l)
Thổi khí Co2 vào dd chứa 0.02 mol Ba(oh)2. Giá trị khối lượng kết tủa biến thiên trong khoảng nào khi Co2 biến thien trong khoảng từ 0.005 mol đến 0.024mol?
Câu trả lời của bạn
Xét \(T=\dfrac{n_{CO2}}{n_{Ba\left(OH\right)2}}\)
TH1. \(T\le1\Rightarrow n_{CO2}\le0,02mol\): sp là muối BaCO3.
TH2. \(1< T< 2\Rightarrow0,02< n_{CO2}< 0,04\): sp tạo thành gồm BaCO3 và Ba(HCO3)2.
TH3. \(T\ge2\Rightarrow n_{CO2}\ge0,04mol\): sp là muối Ba(HCO3)2.
Vì nCO2 biến thiên trong khoảng 0,005mol đến 0,024mol.
=> Xảy ra TH1 và TH2.
- Nếu nCO2 biến thiên từ 0,05mol đến 0,2mol
nBaCO3=nCO2 (Em viết PTHH sẽ thấy rõ).
- Nếu nCO2 biến thiên từ 0,2mol đến 0,024mol
nBaCO3 =nCO3= nOH-nCO2=2nBa(OH)2-nCO2 (Công thức giải nhanh áp dụng cho TH sản phẩm tạo thành chứa 2 muối nCO3= nOH-nCO2 )
Bảng giá trị.
| nCO2 | 0,005 | 0,02 | 0,024 | |
| nBaCO3 | 0,005 | 0,02 | 0,016 | |
| mBaCO3 | 0,985 | 3,94 | 3,152 |
1. Cho 1,36 gam hỗn hợp 2 kim loại kiềm kế tiếp nhau trong nhóm IA tác dụng hết với nước thu được 0,56 lít khí H2 (đktc). Đó là 2 kim loại nào sau đây ?
A. Na, K. B. Rb, Cs. C. K, Rb. D. Li, Na.
2. Cho a mol CO2 vào dung dịch chứa b mol NaOH, thu được dung dịch X. Dung dịch X vừa tác dụng được với HC1 vừa tác dụng được với KOH. Quan hệ giữa a và b là
A. a > b. B. b > 2a
C. a = b. D. b < 2a.
3. Cho từ từ dung dịch chứa a mol HCl vào dung dịch chứa b mol Na2CO3 đồng thời khuấy đều, thu được khí X và dung dịch Y. Khi cho dư nước vôi trong vào dung dịch Y thấy xuất hiện m gam kết tủa. Biểu thức liên hộ giữa m với a và b là
A. m = 100(2b - a) B. m = 56(2a - b).
C. m = 100(a - b). D. m = 197(a + b).
Câu trả lời của bạn
| 6.8 | 6.9 | 6.10 |
| A | D | A |
6.8. Chọn A
Gọi công thức của 2 kim loại là
Ta có:
2¯¯¯¯¯¯M+2H2O→2MOH+H2⇒n¯¯¯¯¯¯M=2.nH2=0,05(mol)⇒¯¯¯¯¯¯M=1,360,05=27,1(g/mol)
nghiên cứu cà giải thích các hiện tượng hóa học:
1. tại sao người ta phải quét vôi lên tường nhà mới xây?
2.tại sao khi sản xuất vôi người ta phải đập nhỏ vôi đến một kích thước nhất định tùy theo từng loại lò?
3.giải thích sự hình thành thạch nhũ trong các hang đá vôi? liên hệ thực tế?
4.tìm hiểu câu tục ngữ nước chảy đá mòn.
5.nghiên cứu tại sao chỉ dùng thạch cao nung để nặn tượng , đúc khuôn, bó bột khi gãy xương mà không dùng thạch cao sống hoặc thạch cao khan?
Câu trả lời của bạn
4. Thành phần chủ yếu của đá là CaCO3. Trong không khí có khí CO2 nên nước hòa tan một phần tạo thành axit H2CO3.
Do đó xảy ra phản ứng học : CaCO3 + CO2 + H2O ⇔ Ca(HCO3)2 (*)
Khi nước chảy cuốn theo Ca(HCO3)2, theo nguyên lí dịch chuyển cân bằng thì cân bằng (*) sẽ chuyển dịch theo phía phải. Kết quả là sau một thời gian nước đã làm cho đá bị bào mòn dần.
hấp thụ hoàn toàn 4.48 l khí CO2 (đktc) vào 500ml hỗn hợp gồm NAOH 0,1M và BA(OH)2 0,2 M sinh ra M (g) kết tủa . tính M
Câu trả lời của bạn
Lời giải
nCO2 = 0,2 mol. nOH- = 0,25 mol, nBa2+ = 0,1 mol
CO2 + 2OH- → CO32- + H2O
0,1250,25 → 0,125
CO2 + CO32- + H2O → 2HCO3-
0,075 →0,075 → 1,5
nCO32- = 0,05mol
Ba2+ + CO32- → BaCO3
0,05 0,05
=> m↓ = 0,05 . 197 = 9,85g
Một hợp chất phân tử gồm một nguyên tử nguyên tố X Liên kết với hai nguyên tử O và có tỉ khối hơi với Heli là 11,5. cho biết nguyên tử khối, tên và kí hiệu hóa học của nguyên tố X.
Câu trả lời của bạn
XO2
\(M_{XO_2}\)=11,5.4=46\(\rightarrow\)X+16.2=46\(\rightarrow\)X=14(Nitơ: N)
bài 1 :người ta dùng 200 ml dung dịch NaOH 0,25M để hấp thụ hoàn toàn 2,25 gam CO2 muối nào được tạo thành kl là bn
bài 2 :cho 2,24 lít khí CO2 ( đktc )tác dụng với 200 ml dung dịch BA(OH) 1M tính nồng độ mol của dung dịch các chất sau phản ứng . Biết V không thay đổi
!_ove![]()
Câu trả lời của bạn
\(n_{NaOH}=0,2.0,25=0,05\left(mol\right)\)
\(n_{CO_2}=\dfrac{2,25}{44}=0,05\left(mol\right)\)
\(T=\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,05}{0,05}=1\)
T = 1 sp tạo thành là NaHCO3
Pt: \(NaOH+CO_2\rightarrow NaHCO_3\)
0,05 ----------------> 0,05
\(m_{NaHCO_3}=0,05.84=4,2\left(g\right)\)
2. \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
\(T=\dfrac{n_{CO_2}}{n_{Ba\left(OH\right)_2}}=\dfrac{0,1}{0,2}=0,5\)
T < 1, sp tạo thành là BaCO3
Pt: \(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
0,1mol 0,2mol ---->0,1mol
Lập tỉ số -> CO2 dư, Ba(OH)2 hết
\(C_{M_{BaCO_3}}=\dfrac{0,1}{0,2}=0,5M\)
cho 4,6g Na vào 500g nước. Tính thể tích khí thoát ra ở DKC và nồng độ phần trăm các chất trong dung dịch thu được
Câu trả lời của bạn
Dung dịch X có chứa a mol \(CA\left(OH\right)_2\).Cho X hấp thụ 0,06 mol \(CO_2\) thì được 2b mol kết tủa. Nếu dùng 0,08 mol \(CO_2\)thì được b mol kết tủa.Tìm a và b
Câu trả lời của bạn
search trc khi hỏi : X chứa a mol Ca(OH)2.cho X hấp thụ qua CO2 0.06 mol thu được 2b mol kết tủa? | Yahoo Hỏi & Đáp
Cho hỗn hợp gồm các chất sau:N2,CO2,O2,CO,hơi nước làm thế nào để tách riêng N2,CO2 ở dạng tinh khiết?
Câu trả lời của bạn
cho qua CuO nóng dư để chuyển Co về CO2
CO + CuO --to--> Cu + CO2
sục vào kiềm dư để hấp thụ CO2 (có cả CO đã chuyển về CO2) và hoi nước tốt nhất nên chọn NạOH vì nó là dd kiềm ko bay hơi
CO2 + 2NaOH -> Na2CO3 + H2O
Cho hh khí còn lại đi qua Cu nóng đỏ dư thu dc ở bước làm đầu tiên (tiết kiệm nguyên liệu)
2Cu + O2 --> 2CuO
khí thoát ra là N2 tinh khiết
5 . Hãy giải thích tại sao các kim loại K ,Na,Ca...khi tác dụng với dd muối không đẩy các kim loại đứng sau chúng ra khỏi dd muối ?
Câu trả lời của bạn
Các kim loại K ,Na,Ca...khi tác dụng với dd muối không đẩy các kim loại đứng sau chúng ra khỏi dd muối vì:
Các kim loại Li, K ,Na,Ca, Ba có tính kiềm rất háo nước nên khi tác dụng với dung dịch muối ( dung dịch muối gồm : dung môi (nước) và chất tan (muối) ) nên khi cho các kim loại này p/ứ với muối thì các kim loại này sẽ p/ứ với dung môi : nước tạo thành dd kiềm và khí. Sau đó dd kiềm này mới t/dụng với muối tạo ra muối mới và bazơ mới=> Không đúng theo tính chất phản ứng với muối của kim loại là tạo ra muối mới và kim loại mới nên p/ứ không thể xảy ra.
Minh dang can gap. Cam ban gioi hoa lam giup minh nhe. Cam on cac ban nhieu.
Trong phong thi nghiem, nguoi ta dieu Che CO2 bang cach cho muoi Na2CO3 tac dung voi dung dich HCl. Cho khi Sinh ra suc vao 2 l dung Dịch NaOH 0,5 M(D=1,05g/mol) thu duoc dung Dịch chua 2 muoi moi co tong nong do la 3,2%. Tinh m Na2CO3 da dung.
Câu trả lời của bạn
Na2CO3 + 2HCl -> 2NaCl + CO2 + H2O (1)
2NaOH + CO2 -> Na2CO3 + H2O (2)
NaOH + CO2 -> NaHCO3 (3)
nNaOH=1(mol)
mdd NaOH=2000.1,05=2100(g)
Đặt nNa2CO3=a
nNaHCO3=b
Ta có:
\(\left(\dfrac{106a}{2100}+\dfrac{84b}{2100}\right).100\%=3,2\%\)
Từ 1 và 2:
nNaOH(1)=2nNa2CO3=2a(mol)
nNaOH(2)=nNaHCO3=b(mol)
=>2a+b=1
Ta có hệ:
\(\left\{{}\begin{matrix}\dfrac{106a}{2100}+\dfrac{84b}{2100}=0,032\\2a+b=1\end{matrix}\right.\)
Giải hệ tìm kết quả rồi mà tính nhé bạn
hấp thụ hết V (l) CO2 (đktc) vào 200 ml dung dịch hỗn hợp NaOH 1M và Ba(OH)2 0.5M thu được 11.82 gam kết tủa . Xác định giái trị của V?
Câu trả lời của bạn
nNaOH = 0,2.1 = 0,2 mol
nBa(OH)2 = 0,2.0,5 = 0,1 mol
\(\Rightarrow\) \(n_{OH^-}=0,2+\left(0,1.2\right)=0,4mol\)
nBaCO3 = 0,06 mol
Ta có
\(n_{BaCO3}< n_{OH^-}\)
\(\Rightarrow\) Tạo 2 muối
CO2 + 2OH- \(\rightarrow\) CO32- + 2H2O (1)
CO2 + OH- \(\rightarrow\) HCO32- (2)
Từ (1)(2)
\(\Rightarrow\) nCO2 = 0,06 + 0,28 = 0,34 mol
\(\Rightarrow\) VCO2 = 0,34.22,4 = 7,616 (l)
cho 100ml dung dịch chưa ZnSO4 0,1 M và MgSO4 0,2 M tác dụng với lượng dư Ba(OH)2. Xác định khối lượng kết tủa tạo thành sau phản ứng.
Câu trả lời của bạn
nZnSO4 = 0,01 mol
- Bảo toàn SO4- : => nBaSO4 = 0,01 mol
nMgSO4 = 0,02 mol
- Bảo toàn SO4- => nBaSO4 = 0,02 mol
=> \(\Sigma nBaSO4=0,01+0,02=0,03\left(mol\right)\)
=> mBaSO4 = 6,99 gam

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *