Bài Thực hành: Tính chất hóa học của sắt, đồng và hợp chất của sắt, crom củng cố kiến thức đã học về Crom, Sắt, Đồng và hợp chất của chúng. Đồng thời bài học cũng rèn luyện kĩ năng quan sát, ghi chép và giải thích các hiện tượng hóa học diễn ra.
Fe + 2HCl → FeCl2 + H2 ↑
FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl
Trắng xanh
6FeSO4+K2Cr2O7+7H2SO4 → 3Fe2(SO4)3+K2SO4 +Cr2(SO4)3 +7H2O
Cu + 2H2SO4 → CuSO4 + SO2↑+ 2H2O
Không dùng tay cầm trực tiếp hoá chất.
Không đổ hoá chất này vào hoá chất khác ngoài chỉ dẫn.
Không đổ lại hoá chất thừa lại lọ đựng ban đầu.
Không dùng hoá chất nếu không biết hoá chất gì.
Không nếm hoặc ngửi trực tiếp hoá chất.
Khi mở lọ hoá chất và lấy hoá chất không để dây ra bàn, dùng xong đậy nắp lại ngay.
Các em chú ý quan sát các thao tác tiến hành thí nghiệm cũng như hiện tượng diễn ra trong đoạn video sau:
Khi gần kết thúc phản ứng, màu của dung dịch chuyển sang màu vàng do một phần Fe2+ bị oxi hoá trong không khí thành Fe3+
Cách bảo quản muối sắt(II) không bị oxi hoá là cho vào dung dịch muối sắt(II) một ít bột sắt: Fe + 2Fe3+ → 3Fe2+
Các em chú ý quan sát các thao tác tiến hành thí nghiệm cũng như hiện tượng diễn ra trong đoạn video sau:
Trắng xanh
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
Trắng xanh Nâu đỏ
Các em chú ý quan sát các thao tác tiến hành thí nghiệm cũng như hiện tượng diễn ra trong đoạn video sau:
Các em chú ý quan sát các thao tác tiến hành thí nghiệm cũng như hiện tượng diễn ra trong đoạn video sau:
CuSO4 + 2NaOH → Cu(OH)2 (kết tủa xanh)+ Na2SO4
2NaOH + H2SO4 →Na2SO4 + 2H2O ⇒ Phản ứng xảy ra chậm do nồng độ axit giảm
Sau bài học cần nắm: Tính chất hóa học của sắt, đồng và hợp chất của sắt, crom
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 39có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho đinh sắt đã đánh thật sạch vào ống nghiệm. Rót vào ống nghiệm 3-5 ml dung dịch HCl 2M. Đun nóng nhẹ. Quan sát hiện tượng ta thấy :
Đun sôi 4 - 6 ml dung dịch NaOH trong ống nghiệm. Rót nhanh dung dịch FeCl2 mới điều chế vào dung dịch NaOH. Quan sát hiện tượng ta thấy xuất hiện kết tủa có màu
Cho đinh sắt đã đánh thật sạch vào ống nghiệm chứa 4-5 ml dung dịch H2SO4 2M. Đun nóng nhẹ. Quan sát hiện tượng ta thấy :
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 39.
Đang cập nhật câu hỏi và gợi ý làm bài.
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho đinh sắt đã đánh thật sạch vào ống nghiệm. Rót vào ống nghiệm 3-5 ml dung dịch HCl 2M. Đun nóng nhẹ. Quan sát hiện tượng ta thấy :
Đun sôi 4 - 6 ml dung dịch NaOH trong ống nghiệm. Rót nhanh dung dịch FeCl2 mới điều chế vào dung dịch NaOH. Quan sát hiện tượng ta thấy xuất hiện kết tủa có màu
Cho đinh sắt đã đánh thật sạch vào ống nghiệm chứa 4-5 ml dung dịch H2SO4 2M. Đun nóng nhẹ. Quan sát hiện tượng ta thấy :
Nhỏ dần từng giọt dung dịch K2Cr2O7 vào dung dịch FeSO4 mới điều chế, lắc ống nghiệm, ta thấy :
Ngâm đinh sắt trong dung dịch đồng II sunfat (CuSO4). Hiện tượng gì xảy ra.
Để bảo quản dung dịch muối sắt (II) trong phòng thí nghiệm, người ta thường ngâm vào dung dịch đó
Thí nghiệm nào sau đây thu được muối sắt (II).
Thực hiện các thí nghiệm sau ở điều kiện thường:
Cho đòng kim loại vào dung dịch sắt (III) clorua
Cho dung dịch bạc nitrat vào dung dịch sắt (III) clorua
Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
Nhúng lá nhôm vào dung dịch H2SO4 đặc nguội.
Cho dung dịch HCl vào dung dịch Fe(NO3)2.
Số thí nghiệm xảy ra phản ứng là:
Khi clo tác dụng với kiềm đặc nóng, tạo muối clorat thì có một phần clo bị khử, đồng thời một phần clo bị oxi hóa. Tỉ lệ số nguyên tử clo bị khử và số nguyên tử clo bị oxi hóa là:
Thực hiện các thí nghiệm sau:
1. Đốt cháy dây sắt trong khí clo
2. Đốt nóng hỗn hợp bột Fe và S (trong điều kiện không có oxi)
3. Cho FeO vào dung dịch HNO3 loãng, dư
4. Cho Fe vào dung dịch Fe2(SO4)3
5. Cho Fe vào dung dịch H2SO4 loãng, dư
Có bao nhiêu thí nghiệm tạo muối sắt (II)?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
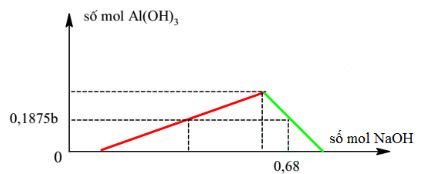
Cho a mol Al phản ứng với dung dịch hỗn hợp chứa 0,15b mol FeCl3 và 0,2b mol CuCl2. Sau khi phản ứng kết thúc thu được x gam chất rắn. Giá trị của x là:
Câu trả lời của bạn
Dung dịch Y chứa nAlCl3 = nHCl dư = a mol
Bảo toàn nguyên tố Cl ta có: nCl- = 3a + a = 4a = b mol (1)
Khi nNaOH = 0,68 mol: kết tủa bị hòa tan một phần:
Do đó: nOH- = nH+ + 4.nAl3+ - nAl(OH)3 ⟹ 0,68 = a + 4a - 0,1875b (2)
Giải hệ (1) và (2) ta có: a = 0,16 và b = 0,64
Vậy nFeCl3 = 0,15b = 0,096 mol; nCuCl2 = 0,2b = 0,128 mol
Sau phản ứng dung dịch thu được chứa Cl- 0,544 mol; Al3+ 0,16 mol;
Bảo toàn điện tích ta suy ra nFe2+ = 0,032 mol
Vậy chất rắn gồm Fe (0,096 - 0,032 = 0,064 mol) và Cu: 0,128 mol
→ mchất rắn = 0,128.64 + 0,064.56 =11,776 gam.
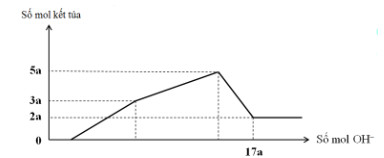
Câu trả lời của bạn
Đặt 5x và x là số mol của HCl và H2SO4
Dựa vào đồ thị ta thấy nMg(OH)2 = 2a mol và n ↓ max = 5a mol → nAl(OH)3 = 3a mol
Vậy ban đầu nMg = 2a mol; nAl2O3 = 1,5a mol → 24.2a + 102.1,5a = 12,06 gam
→ a = 0,06 mol
Dung dịch X chứa 0,12 mol Mg2+, 0,18 mol Al3+, 5x mol Cl-, x mol SO42- → nH+ = 7x - 0,78 mol
→ nOH- = 17.0,06 = 7x - 0,78 + 0,12.2+ 0,18.4 → x = 0,12 mol
Vậy dung dịch X chứa 0,12 mol Mg2+, 0,18 mol Al3+, 0,6 mol Cl-, 0,12 mol SO42-; 0,06 mol H+
Đặt nNaOH = 3y mol và nBa(OH)2 = y mol → nBa2+ = y mol; nOH- = 3y + 2y = 5y mol
Khi BaSO4 đạt cực đại tại y = 0,12 mol:
Khi đó nOH- = 0,6 mol < nH+ + 2.nMg2+ + 3.nAl3+ = 0,84 mol → Kết tủa hiđroxit chưa đạt cực đại
→ Khi nOH- = 0,84 mol thì các kết tủa đều cực đại, bao gồm 0,12 mol BaSO4, 0,12 mol Mg(OH)2; 0,18 mol Al(OH)3.
Khi nung thu được 0,12 mol BaSO4, 0,12 mol MgO; 0,09 mol Al2O3 → m = 41,94 gam.
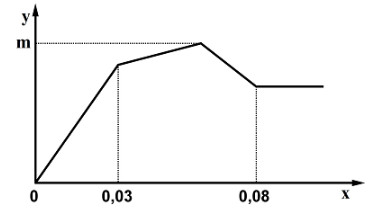
Câu trả lời của bạn
3 Ba(OH)2+ Al2(SO4)3 → 2 Al(OH)3+ 3BaSO4
0,03 → 0,01 0,02 0,03 mol
Khi thêm Ba(OH)2 mà kết tủa không thay đổi thì chứng tỏ Al(OH)3 bị hòa tan hết
→ nOH- = 0,08.2 = 4.nAl3+ → nAl3+ = 0,04 mol → nAl(OH)3 max = 0,04 mol
Vậy khối lượng kết tủa cực đại là m = mBaSO4 + mAl(OH)3 max = 0,03.233 + 0,04.78 = 10,11 gam.
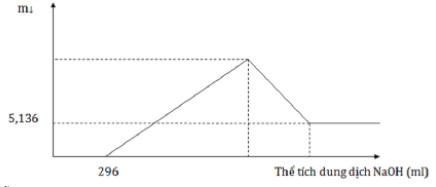
Câu trả lời của bạn
Phần 1: nSO2 = 0,09 mol
Áp dụng bảo toàn electron ta có nAl = 0,06 mol
Phần 2: nHNO3 = 0,4.2 = 0,8 mol; nH+ dư = nNaOH = 0,296 mol
Áp dụng bảo toàn electron ta có: nNO = 0,06 mol
Vậy nH+ pứ = 0,8 - 0,296 = 4.nNO + 2.nO → nO = 0,132 mol
Khi cho dung dịch NaOH dư vào Y thì Al(OH)3 và Cr(OH)3 bị hòa tan hoàn toàn. Khi đó còn lại 5,136 gam Fe(OH)3 → nFe(OH)3 = 0,048 mol → nFe2O3 = 0,024 mol
Bảo toàn nguyên tố O ta có: nO = 3.nFe2O3 + 3.nCr2O3 = 0,132 mol → nCr2O3 = 0,02 mol
Vậy khối lượng Cr2O3 ban đầu là 0,02.152.2 = 6,08 gam.
Câu trả lời của bạn
Đặt nAlCl3 = a mol và nFeCl3 = b mol
→ Số mol cực đại của Al(OH)3 là a mol; số mol cực đại của Fe(OH)3 là b mol
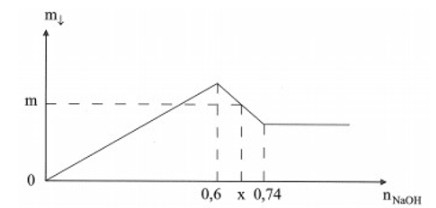
Khi Al(OH)3 và Fe(OH)3 đạt cực đại thì: nOH- = 3a + 3b = 0,6 mol
Khi nNaOH = 0,74 mol thì số mol kết tủa không đổi → Tại đó Al(OH)3 tan hết tạo NaAlO2
Suy ra nNaOH = 4a + 3b = 0,74 mol
Giải hệ trên ta được a = 0,14 mol và b = 0,06 mol
Khi nNaOH = x mol thì Fe(OH)3 đạt cực đại và Al(OH)3 bắt đầu tan ra
→ nNaOH = 3.nFe(OH)3 + 4.nAl3+ - nAl(OH)3
Với x = 0,66 mol suy ra 0,66 = 3.b + 4.a - nAl(OH)3 → nAl(OH)3 = 0,08 mol
Vậy khối lượng kết tủa là m = mFe(OH)3+ mAl(OH)3 = 0,06.107 + 0,08.78 =12,66 gam.
Câu trả lời của bạn
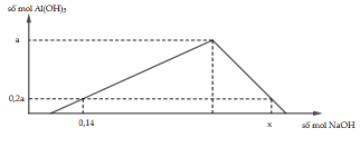
Đặt số mol AlCl3 và HCl trong mỗi phần là a, b mol
- Phần 1: Bảo toàn nguyên tố Cl ta có: nAgCl = 3a + b = 71,75/143,5 = 0,5 mol (1)
- Phần 2:
Khi nNaOH = 0,14 mol thì kết tủa chưa đạt cực đại: nOH- = 0,14 = nH++ 3.nAl(OH)3
→ 0,14 = b+ 3. 0,2a = b+ 0,6a (2)
Giải hệ (1) và (2) ta có a = 0,15 và b = 0,05
Khi nNaOH = x mol thì kết tủa bị tan một phần:
nOH- = nH++ 4.nAl3+ - nkết tủa = b + 4a - 0,2a = b + 3,8a = 0,05 + 3,8.0,15 = 0,62 mol → x = 0,62 mol.
Câu trả lời của bạn

Câu trả lời của bạn
Câu trả lời của bạn
A. 0,03
B. 0,045
C. 0,06
D. 0,09
Câu trả lời của bạn
C
C
Hòa tan hoàn toàn hỗn hợp gồm 0,12 mol FeS2 và x mol Cu2S vào dung dịch HNO3 vừa đủ, thu được dung dịch X chỉ chứa 2 muối sunfat của các kim loại và giải phóng khí NO duy nhất. Giá trị của x là:
A. 0,03
B. 0,045
C. 0,06
D. 0,09
Dung dịch X chỉ chứa 2 muối là: Fe2(SO4)3 và CuSO4
nFeS2 = ½ nFe2(SO4)3 = 0,06mol
nCuSO4 = 2nCu2S = 2x mol
Bảo toàn nguyên tố S: 0,12.2 + x = 0,06.3 + 2x
⇒ x = 0,06
⇒ Đáp án C

Câu trả lời của bạn
dùng 6.72 lít đktc khí CO để khử m gam hỗn hợp các oxit sau CuO Fe2O3 Fe3O4 Zno .Sau phản ứng thu được khối lượng chất rắn chỉ bằng 84% khối lượng chất rắn bau đầu. Hãy tính khối lượng m gam hỗn hợp ban đầu
Câu trả lời của bạn
Gọi hỗn hợp oxit;kim loại là X;Y
PTTQ:
X + CO -> Y + CO2
nCO=0,3(mol)
Ta có:
nO bị khử =nCO=0,3(mol)
mO bị khử=0,3.16=4,8(g)
4,8g ứng với 16% khối lượng chất rắn ban đầu
=>mX=4,8:16%=30(g)
Mọi người cho mình hỏi chút được không?
Dụng cụ nào sau đây được gọi là ống đong để lấy chính xác một thể tích chất lỏng?
Câu trả lời của bạn
A
a
Cảm ơn bạn nhiều nhé.
Hình A là ống đong, dùng để định lượng chất lỏng ak bạn. Có vạch chia ml dùng để đong chính xác lượng chất lỏng cần lấy.
Hình B là ống nhỏ giọt nó chỉ dùng với các thí nghiệm không cần nhiều độ chính xác. Mỗi lần hút chất lỏng vào ống tùy vào độ mạnh của tay người cầm mà nó hút được bao nhiêu ml. Ống nhỏ giọt thường lấy là 1 - 2ml. Và tác dụng rất hay của ống nhỏ giọt là cho từ từ dung dịch được dễ dàng hơn pipet.
Hình C là ống nghiệm thủy tinh dùng để tiến hành các thí nghiệm với chất lỏng.
Hình D là ống nghiệm có nhánh, chức năng giống ống nghiệm thủy tinh nhưng có thêm nhánh để thu khí.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *