Nôi dung bài học giúp các em hiểu về nguyên tắc điều chế kim loại cũng như các phương pháp để điều chế như phương pháp nhiệt luyện, thủy luyện, điện phân.
- Là sự khử ion kim loại thành kim loại: \({M^{n + }} + ne \to M\)
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Sục khí Cl2 vào dung dịch FeCl2
(c) Dẫn khí H2 dư qua bột CuO nung nóng
(d) Cho Na vào dung dịch CuSO4 dư
(e) Nhiệt phân AgNO3
(f) Điện phân nóng chảy Al2O3
Sau khi kết thúc các phản ứng, những thí nghiệm thu được kim loại?
(a) Cho Mg vào dung dịch Fe3+(dư) tạo Fe2+
(b) \(C{l_2} + 2FeC{l_2} \overset{t^{0}}{\rightarrow} 2FeC{l_3}\)
(c) \({H_2} + CuO\overset{t^{0}}{\rightarrow}Cu + {H_2}O\)
(d) \(2Na + 2{H_2}O \to 2NaOH + {H_2};2NaOH + CuS{O_4} \to Cu{\left( {OH} \right)_2} + N{a_2}S{O_4}\)
(e) \(2AgN{O_3}\overset{t^{0}}{\rightarrow}2Ag + 2N{O_2} + {O_2}\)
(f) \(2A{l_2}{O_3}\overset{dpnc}{\rightarrow}4Al + 3{O_2}\)
Vậy có 3 thí nghiệm thu được kim loại là: (c); (e); (f)
Trong các kim loại Cu; Ag; Na; K và Ba, số kim loại điều chế được bằng phương pháp thủy luyện là:
Phương pháp thủy luyện dùng để điều chế nững kim loại yếu, đứng sau H trong dãy hoạt động hóa học. Như vậy ta có các kim loại: Cu; Ag
Bốn kim loại K, Al, Fe và Ag được ấn định không theo thứ tự là X, Y, Z, và T. Biết rằng X và Y được điều chế bằng phương pháp điện phân nóng chảy; X đẩy được kim loại T ra khỏi dung dịch muối; và Z tác dụng được với dung dịch H2SO4 đặc nóng nhưng không tác dụng được với dung dịch H2SO4 đặc nguội. Các kim loại X, Y, Z và T theo thứ tự là:
Do X và Y điều chế bằng cách điện phân nóng chảy ⇒ đó là Al và K
Mà X đẩy được T ra khỏi muối ⇒ X là Al ⇒ Y là K
Z tác dụng được với dung dịch H2SO4 đặc nóng nhưng không tác dụng được với dung dịch H2SO4 đặc nguội ⇒ Z bị thụ động hóa trong H2SO4 đặc nguội.
⇒ Z là Fe ⇒ T là Ag.
Cho khí CO dư đi qua ống chứa 0,2 mol MgO và 0,2 mol CuO nung nóng, đến phản ứng hoàn toàn, thu được x gam chất rắn. Giá trị của x là:
Chất rắn gồm MgO và Cu (vì MgO không phản ứng với CO)
⇒ x = 20,8g
Thổi rất chậm 2,24 lít (đktc) một hỗn hợp khí gồm CO và H2 qua một ống sứ đựng hỗn hợp Al2O3, CuO, Fe3O4, Fe2O3 có khối lượng là 24 gam dư đang được đun nóng. Sau khi kết thúc phản ứng khối lượng chất rắn còn lại trong ống sứ là:
\(n_{hh \ (CO + H_{2})} = \frac{2,24}{22,4} = 0,1 \ mol\)
Thực chất phản ứng khử các oxit là:
CO + O → CO2
H2 + O → H2O
Vậy: \(n_{O}=n_{CO}+n_{H_{2}} = 0,1 \ mol\)
Khối lượng chất rắn còn lại trong ống sứ là: 24 - 1,6 = 22,4 gam.
Điện phân 10 ml dung dịch AgNO3 0,4M ( điện cực trơ ) trong thời gian 10 phút 30 giây với dòng điện có cường độ I = 2A, thu được m gam Ag. Giả sử hiệu suất phản ứng điện phân đạt 100%.
| Tại catot | Tại anot |
| Ag+ + e → Ag 0,004 → 0,004 → 0,004 2H2O + 2e → H2 + 2OH- | 2H2O → 4H+ + O2 + 4e
|
Ta có: \({n_{e{\rm{ trao doi}}}} = \frac{{It}}{{96500}} = 0,013\,mol\)
Lớn hơn ne Ag nhường = 0,004 mol
\(\Rightarrow {m_{Ag}} = 0,004.108 = 0,432gam\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 12 Bài 21có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Dãy gồm các kim loại được điều chế trong công nghiệp bằng phương pháp điện phân hợp chất nóng chảy của chúng là:
Điện phân dung dịch NaCl không có màng ngăn giữa hai điện cực, thu được:
Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 12 Bài 21.
Bài tập 1 trang 98 SGK Hóa học 12
Bài tập 2 trang 98 SGK Hóa học 12
Bài tập 3 trang 98 SGK Hóa học 12
Bài tập 4 trang 98 SGK Hóa học 12
Bài tập 5 trang 98 SGK Hóa học 12
Bài tập 1 trang 140 SGK Hóa 12 Nâng cao
Bài tập 2 trang 140 SGK Hóa 12 Nâng cao
Bài tập 3 trang 140 SGK Hóa học 12 nâng cao
Bài tập 4 trang 140 SGK Hóa 12 Nâng cao
Bài tập 5 trang 140 SGK Hóa 12 Nâng cao
Bài tập 6 trang 140 SGK Hóa 12 Nâng cao
Bài tập 7 trang 140 SGK Hóa 12 Nâng cao
Bài tập 8 trang 140 SGK Hóa 12 Nâng cao
Bài tập 21.1 trang 46 SBT Hóa học 12
Bài tập 21.2 trang 46 SBT Hóa học 12
Bài tập 21.3 trang 46 SBT Hóa học 12
Bài tập 21.4 trang 46 SBT Hóa học 12
Bài tập 21.5 trang 46 SBT Hóa học 12
Bài tập 21.6 trang 47 SBT Hóa học 12
Bài tập 21.7 trang 47 SBT Hóa học 12
Bài tập 21.8 trang 47 SBT Hóa học 12
Bài tập 21.9 trang 47 SBT Hóa học 12
Bài tập 21.10 trang 47 SBT Hóa học 12
Bài tập 21.11 trang 47 SBT Hóa học 12
Bài tập 21.12 trang 47 SBT Hóa học 12
Bài tập 21.13 trang 48 SBT Hóa học 12
Bài tập 21.14 trang 48 SBT Hóa học 12
Bài tập 21.15 trang 48 SBT Hóa học 12
Bài tập 21.16 trang 48 SBT Hóa học 12
Bài tập 21.17 trang 48 SBT Hóa học 12
Bài tập 21.18 trang 48 SBT Hóa học 12
Bài tập 21.19 trang 48 SBT Hóa học 12
Bài tập 21.20 trang 49 SBT Hóa học 12
Bài tập 21.21 trang 49 SBT Hóa học 12
Bài tập 21.22 trang 49 SBT Hóa học 12
Bài tập 21.23 trang 49 SBT Hóa học 12
Bài tập 21.24 trang 49 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Dãy gồm các kim loại được điều chế trong công nghiệp bằng phương pháp điện phân hợp chất nóng chảy của chúng là:
Điện phân dung dịch NaCl không có màng ngăn giữa hai điện cực, thu được:
Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh nhôm ra cân lại thấy nặng 46,38 gam. Khối lượng Cu thoát ra là:
Điện phân 400 ml dung dịch CuSO4 0,5M điện cực trơ cho đến khí ở catot xuất hiện 6,4 g kim loại thì thể tích khí thu được (dktc) là:
Để điều chế Ca từ CaCO3 cần thực hiện ít nhất mấy phản ứng ?
Điện phân (với cực điện trơ, mồng ngăn xốp) dung dịch gồm 0,2 mol Fe2(SO)4, 0,2 mol CuSO4 và 0,4 mol NaCl. Biết rằng hiệu suất điện phân đạt 100%. Điều khẳng định nào sau đây là đúng ?
Khi khối lượng catot tăng 12,8 gam thì dung dịch hoàn toàn chỉ có màu nâu vàng.
Khi khối lượng calot tăng lên 6,4 gam thì đã có 19300 culong chạy qua bình diện phân.
Khi có 4,48 lít khi (đktc) thoát ra ở anot thì khối lượng catot không thay đổi.
Điện phân 1 lit dung dịch có chứa 18,8 gam Cu(NO3)2 và 29,8 gam KCl bằng điện cực trơ, có màng ngăn xốp. Sau 1 thời gian thấy khối lượng dung dịch giảm 34,3 gam so với ban đầu. Coi thẻ tích dung dịch không đổi trong quá trình điện phân, Nồng độ các chất trong dung dịch sau khi điện phân là
KCl 0,1M; KNO3 0,2M ; KOH 0,1M,
KNO3 0,1 M ; KCl 0,2 M
KCl 0,05M ; KNO3 0,2M ; KOH 0,15M.
Một nhóm học sinh đã đề xuất các cách điều chế Ag từ AgNO3 như sau :
(1) Cho kẽm tác dụng với dung dịch AgNO3.
(2) Điện phân dung dịch AgNO3.
(3) Cho dung dịch AgNO3 tác dụng với dung dịch NaOH sau đó thu lấy kết tủa đem nhiệt phân.
(4) Nhiệt phân AgNO3.
Trong các cách điều chế trên, có bao nhiêu cách có thể áp dụng để điều chế Ag từ AgNO3 ?
Cho các chất sau đây : NaOH, Na2CO3, NaCl, NaNO3 và Na2SO4. Có bao nhiêu chất điều chế được Na chỉ băng 1 phản ứng ?
Cho hơi nước qua than nóng đỏ thu được 2,24 lít hồn hợp khí X gồm CO2, CO và 112 (đo ở đktc). Dẫn X qua hổn hợp gồm CuO và Al2O3 dư nung nóng thu dược m gam chất rắn và hỗn hợp khí và hơi Y. Dẫn Y qua dung dịch Ca(OH)2 dư, lọc bỏ kết tủa thấy khối lượng dung dịch giảm 1,16 gam. Khối lượng kim loại có trong m là
Trình bày cách để:
– Điều chế Ca từ CaCO3
– Điều chế Cu từ CuSO4
Viết phương trình hoá học của các phản ứng?
Từ Cu(OH)2, MgO, Fe2O3 hãy điều chế các kim loại tương ứng bằng một phương pháp thích hợp. Viết phương trình hóa học của phản ứng?
Một loại quặng sắt chứa 80% Fe2O3, 10% SiO2 và một số tạp chất khác không chứa Fe và Si. Hàm lượng các nguyên tố Fe và Si trong quặng này là:
A. 56% Fe và 4,7% Si.
B. 54% Fe và 3,7% Si.
C. 53% Fe và 2,7% Si.
D. 52% Fe và 4,7% Si.
Để khử hoàn toàn 30 gam hỗn hợp gồm CuO, FeO, Fe3O4, Fe2O3, Fe, MgO cần dùng 5,6 lít khí CO (đktc). Khối lượng chất rắn thu được sau phản ứng là:
A. 28 gam.
B. 26 gam.
C. 24 gam.
D. 22 gam.
Điện phân (điện cực trơ) dung dịch muối sunfat của một kim loại hoá trị II với dòng điện cường độ 3A. Sau 1930 giây điện phân thấy khối lượng catot tăng 1,92 gam.
a) Viết phương trình hoá học của phản ứng xảy ra tại mỗi điện cực và phương trình hoá học của sự ⇒điện phân.
b) Xác định tên kim loại.
Dãy các ion kim loại nào sau đây bị Zn khử thành kim loại?
A. Cu2+, Mg2+, Pb2+
B. Cu2+, Ag+, Na+
C. Sn2+, Pb2+, Cu2+
D. Pb2+, Ag+, Al3+
Phản ứng hóa học nào sau đây chỉ được thực hiện bằng phương pháp điện phân?
A. Fe + CuSO4 → FeSO4 + Cu
B. CuSO4 + H2O → Cu + O2 + H2SO4
C. CuSO4 + NaOH → Cu(OH)2 + Na2SO4
D. Cu + AgNO3 → Ag + Cu(NO3)2
Từ mỗi hợp chất sau: Cu(OH)2, NaCl, Fe2S2. Hãy lựa chọn những phương pháp thích hợp để điều chế kim loại tương ứng. Trình bày các phương pháp đó.
Điều chế Cu bằng cách điện phân dung dịch Cu(NO3)2
a. Trình bày sơ đồ điện phân.
b. Viết phương trình điện phân.
c. Cho biết vai trò của nước trong quá trình điện phân.
d. Có nhận xét gì về nồng độ ion trong dung dịch trước và sau khi điện phân?
Có hỗn hợp các bột kim loại Ag, Cu. Bằng những phương pháp hóa học nào ta có thể thu được Ag từ hỗn hợp? Giải thích và viết phương trình hóa học.
Điện phân 200ml một dung dịch có chứa hai muối là Cu(NO3)2 và AgNO3 với cường độ dòng điện là 0,804 A, đến khi bọt khí bắt đầu thoát ra ở cực âm thì thời gian điện phân là 2 giờ. Hãy xác định tên của muối clorua kim loại.
Điện phân hoàn toàn 3,33 gam muối clorua của một kim loại nhóm IIA, người ta thu được 6,72 lit khí clo (đktc). Hãy xác định tên của muối clorua kim loại.
Điện phân một dung dịch AgNO3 trong thời gian 15 phút với cường độ dòng điện là 5 ampe. Để làm kết tủa hết ion Ag⁺ còn lại trong dung dịch sau điện phân, cần dùng 25 ml dd NaCl 0,4M.
a. Viết phương trình điện phân và phương trình hóa học của phản ứng xảy ra.
b. Tính khối lượng Ag thu được ở catot.
c. Tính khối lượng AgNO₃ có trong dung dịch ban đầu.
Khi điện phân có màng ngăn dung dịch muối ăn bão hoà trong nước thì xảy ra hiện tượng nào trong số các hiện tượng cho dưới đây ?
A. Khí oxi thoát ra ở catot và khí clo thoát ra ở anot.
B. Khí hiđro thoát ra ở catot và khí clo thoát ra ở anot.
C. Kim loại natri thoát ra ở catot và khí clo thoát ra ở anot.
D. Nước Gia-ven được tạo thành trong bình điện phân.
Phương pháp điều chế kim loại bằng cách dùng đơn chất kim loại có tính khử mạnh hơn để khử ion kim loại khác trong dung dịch muối được gọi là
A. phương pháp nhiệt luyện.
B. phương pháp thuỷ luyện.
C. phương pháp điện phân.
D. phương pháp thuỷ phân.
Điện phân bằng điện cực trơ dung dịch muối sunfat của kim loại hoá trị II với dòng điện có cường độ 6A. Sau 29 phút điện phân thấy khối lượng catot tăng 3,45 g. Kim loại đó là
A. Zn.
B. Cu
C. Ni.
D. Sn.
Điện phân 200 ml dung dịch KOH 2M (D = 1,1 g/cm3) với điện cực trơ. Khi ở catot thoát ra 2,24 lít khí (đktc) thì ngừng điện phân. Biết rằng nước bay hơi không đáng kể. Dung dịch sau điện phân có nồng độ phần trăm là
A. 10,27%.
B. 10,18%.
C. 10,9%.
D. 38,09%.
Trong số những công việc sau, công việc nào không được thực hiện trong công nghiệp bằng phương pháp điện phân ?
A. Điều chế kim loại Zn.
B. Điều chế kim loại Cu.
C. Điều chế kim loại Fe.
D. Mạ niken.
Có thể thu được kim loại nào trong số các kim loại sau: Cu, Na, Ca, Al bằng cả 3 phương pháp điều chế kim loại phổ biến (nhiệt luyện, thuỷ luyện, điện phân) ?
A. Na.
B. Ca.
C. Cu
D. Al
Dãy gồm các kim loại được điều chế trong công nghiệp bằng phương pháp điện phân hợp chất nóng chảy của chúng là
A. Na, Ca, Al.
B. Na, Ca, Zn.
C. Na, Cu, Al.
D. Fe, Ca, Al.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Cho hai bình điện phân, bình (I) đựng 20 ml dung dịch NaOH 1,73 M; bình (2) đựng dung dịch gồm 0,225 mol Cu(NO3)2 và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M. Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất của N+5 .Giá trị m là:
A. 9,8. B. 9,4. C. 10,4. D. 8,3.
giúp em vs ạ. em cảm ơn anh chị
Câu trả lời của bạn
Ở đây có dùng một kiến thức vật lí: mắc nối tiếp nên hai bình điện phân cùng I.
• bình (1): giải điện phân NaOH → có thể coi là quá trình điện phân H2O
từ CM (NaOH) → nH2O bị điện phân = 0,15 mol ⇄ ne trao đổi = 0,3 mol.
• dùng giả thiết ne trao đổi trên: có điện phân bình (2) ra: 0,1 mol CuCl2 + 0,05 mol CuO.
||→ bảo toàn gốc NO3 đọc ra dd sau điện phân gồm 0,075 mol Cu(NO3)2 và 0,3 mol HNO3.
Quy về giải 0,25 mol Fe + 0,075 mol Cu(NO3)2 + 0,3 mol HNO3 → ? gam chất rắn không tan.!
Giải: m gam chất rắn gồm 0,075 mol Cu và 0,0625 mol Fe ⇄ m = 8,3 gam.
Mọi người ơi, bài này giải như nào ạ? Help me...
Điện phân với điện cực trơ dung dịch chứa 0,45 mol AgNO3 bằng cường độ dòng điện 2,68 ampe, trong thời gian t (giờ) thu được dung dịch X. Cho 33,6 gam bột Fe vào dung dịch X thấy thoát ra khí NO (sản phẩm khử duy nhất) thu được 51,42 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của t là?
Câu trả lời của bạn
Mình xin lỗi, chen vô hỏi ké câu điện phân nhé. Chỉ mình cách làm với ạ. Cảm ơn.
Điện phân 100 ml dung dịch A chứa AgNO3 0,2M, Cu(NO3)2 0,1M và Zn(NO3)2 0,15M với cường độ dòng điện I = 1,34 A trong 72 phút. Số gam kim loại thu được ở catot sau điện phân là:
A. 3,775 gam.
B. 2,80 gam.
C. 2,48 gam.
D. 3,45 gam.
Bài này cũng tàm tạm thôi bạn. Bạn giải như này nè.
\(n_{Ag^+}=0,02 \ mol; \ n_{Cu^{2+}}= 0,01 mol; \ n_{Zn^{2+}}=0,015 \ mol\)
\(n_{e}=\frac{It}{96500}=0,06 \ mol\)
\(\Rightarrow n_{Zn}= \frac{0,06 - 0,02 - 0,01.2}{2}=0,01 \ mol\)
\(\Rightarrow m_{Kl}=0,02.108+0,01.64+0,01.65=3,45 \ (g)\)
Mình phải lấy dữ kiện để xét trước như này nhé.
nAg+(X) < 0,45 mol ⇒ mAg tạo ra < 48,6g < 51,42g
⇒ Chứng tỏ Fe dư ⇒ chỉ tạo muối Fe2+
Điện phân:
Catot: Ag+ + 1e → Ag
(mol) x → x
Anot: 2H2O → 4H+ + O2 + 4e
(mol) x \(^{\overset{ \ }{\leftarrow}}\) x
X + Fe:
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
3x/8 \(^{\overset{ \ }{\leftarrow}}\) x
Fe + 2Ag+ → Fe2+ + 2Ag
(0,225 – 0,5x) \(^{\overset{ \ }{\leftarrow}}\) (0,45 – x)
⇒ mrắn sau = mFe dư + mAg = [33,6 – 56.(0,225 – 0,125x)] + 108.(0,45 – x) = 51,42
⇒ x = 0,18 mol
Có ne = It/F ⇒ t = 1,80 h
Bài tập điện phân này làm như thế nào đây mọi người. Giúp mình với.
Điện phân dung dịch hỗn hợp CuSO4 và KCl với điện cực trơ, có màng ngăn xốp. Khi ở cả hai điện cực đều có bọt khí thì dừng lại. Kết quả ở anot có 448ml khí thoát ra (đktc), khối lượng dung dịch sau điện phân giảm m gam và dung dịch sau điện phân có thể hòa tan tối đa 0,8 gam MgO. Giá trị của m là:
Câu trả lời của bạn
Gíup mình câu này với bạn. Cảm ơn nhiều nhiều.
Tiến hành điện phân V lít dung dịch NaCl 1M và CuSO4 1,8M bằng điện cực trơ tới khi nước bắt đầu điện phân ở cả 2 cực thì dừng điện phân, thấy khối lượng dung dịch giảm m gam. Dung dịch sau phản ứng hoà tan tối đa 8,84 gam Al2O3. Giá trị của m là?
Tương tự như bài trên thôi cậu. Gốc axit có chứa oxi và kim loại kiềm không bị điện phân. Rồi cứ vậy viết phương trình điện phân ra và làm như sau nhé.
Catot: Cu2+ + 2e → Cu
1,8V 3,6V 1,8V mol
Anot : 2Cl- → Cl2 + 2e
V 0,5V V mol
2H2O → 4H+ + O2 + 4e
2,6V 0,65V 2,6V mol
(Vì cả 2 điện cực đều thoát khí thì dừng ⇒ điện cực Catot không có điện phân nước)
Có: \(n_{H^+} = 6n_{Al_{2}O_{3}} \Rightarrow V = 0,2 \ lit\)
\(m = m_{Cu}+ m_{Cl_{2}} + m_{O_{2}} = 64.1,8V + 71.0,5V + 32.0,65V = 34,3 \ g\)
Hi, Ly. Gốc axit có chứa oxi và kim loại kiềm không bị điện phân đâu, nhớ nhé. Bài này giải như này nè.
Dung dịch sau điện phân có thể hòa tan MgO ⇒ Còn H+
Catot: \(C{u^{2 + }} + 2e \to Cu\)
Anot: \(2C{l^ - } \to C{l_2} + 2e\)
\(2{H_2}O \to 4{H^ + } + {O_2} + 4e\)
\(MgO + 2{H^ + } \to M{g^{2 + }} + {H_2}O\)
\(\Rightarrow {n_{{H^ + }}} = 0,04mol \Rightarrow {n_{{O_2}}} = 0,01mol\)
Có: \({n_{Kh\'i }} - {n_{C{l_2}}} + {n_{{O_2}}} \Rightarrow {n_{C{l_2}}} = 0,01mol\)
Bảo toàn e: \(2{n_{Cu}} = {n_{{H^ + }}} + 2{n_{C{l_2}}} \Rightarrow {n_{Cu}} = 0,03mol\)
\(\Rightarrow m = {m_{Cu}} + {m_{{O_2}}} + {m_{C{l_2}}} = 2,95g\)
Bài tập này lạ quá mọi người. Cho dữ kiện ở dạng đồ thị, khó hiểu quá ạ. Mọi người hướng dẫn mình chút nhé. Cảm ơn ạ.
Điện phân dung dịch chứa HCl, NaCl, FeCl3 (điện cực trơ, có màng ngăn). Đồ thị nào sau đây biểu diễn đúng sự biến thiên pH của dung dịch theo thời gian (bỏ qua sự thuỷ phân của muối)?
A. 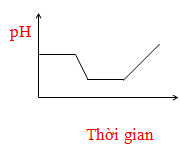
B. .png)
C. .png)
D. 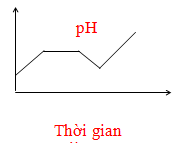
Câu trả lời của bạn
Câu này hỏi chất tan sau điện phân thì làm sao đây mọi người ơi. Giúp với ạ. Em cảm ơn mọi người nhiều.
Điện phân dung dịch gồm 7,45 gam KCl và 28,2 gam Cu(NO3)2 (điện cực trơ, màng ngăn xốp) đến khí khối lượng dung dịch giảm đi 10,75 gam thì ngừng điện phân (giả thiết lượng nước bay hơi không đáng kể). Tất cả các chất tan trong dung dịch sau điện phân là:
A. KNO3 và KOH.
B. KNO3, KCl và KOH.
C. KNO3 và Cu(NO3)2.
D. KNO3, HNO3 và Cu(NO3)2.
Mình làm như này bạn ạ. Haizz. Điện phân có ra năm nay không nhỉ?
\(n_{ KCl }= 0,1 \ mol ; \ n_{ Cu(NO_{3})_{2}} = 0,15 \ mol\)
Nếu đp hết Cl – thì ngừng lại:
Anot Catot
Cl – → Cl2 + 2e Cu2+ + 2e → Cu
0,1 0,05 0,1 mol 0,1 0,05
⇒ \(_{\sum }\) mdd giảm = 0,05.71 + 0,05.64 = 6,75 gam (1)
Nếu đp hết Cu2+ thì ngừng lại:
Catot Anot
Cu2+ + 2e → Cu Cl- → Cl2 + 2e
0,15 0,3 0,15 0,1 0,05 0,1
2H2O → 4H+ + O2 + 4e
0,05 0,3 – 0,1 = 0,2
⇒ \(_{\sum }\) mdd giảm = 0,05. 71 + 0,15. 64 + 0,05. 32 = 14,75 gam (2)
Dễ thế m dd giảm (1) < m dd giảm thực tế < m dd giảm (2)
⇒ quá trình đp diễn ra như sau:
Anot:
Cl – → Cl2 + 2e
0,1 0,05 0,1
2H2O → 4H+ + O2 + 4e
x 2x 0,5x
Catot:
Cu2+ + 2e → Cu
0,1 + 2x (0,5+ x)
⇒ 0,5 + x < 0,15 ⇔ x < 0,1
m dd giảm = 0,05. 71 + 0,5. 32 + (0,5+x)64 = 10,75 ⇒ x = 0,05 (TM)
⇒ dd sau phản ứng K+; H+; Cu2+ và NO3-
Mình xét thứ tự như này nhé:
Fe3+ + 1e → Fe2+ (pH không đổi)
H+ + 1e → ½ H2 (pH tăng vì H+ bị điện phân)
Fe2+ + 2e → Fe (pH không đổi)
2H2O +2e → 2OH- + H2 (pH tăng vì tạo OH-)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *