Nội dung bài học trình bày cụ thể, tỉ mỉ về các hợp chất của Sắt. Thông qua bài học các em học sinh biết được tính chất vật lí - hóa học của hợp chất Sắt (II), Sắt (III) và phương pháp điều chế. Biết được tính chất và ứng dụng của một số hợp chất quan trọng của hợp chất của Sắt.
Tính chất hoá học cơ bản của hợp chất sắt (II) là tính khử.
Fe2+ → Fe3+ + 1e
| Đặc điểm | Sắt (II) oxit | Sắt (II) hidroxit | Muối Sắt (II) |
| Tính chất vật lí | FeO là chất rắn, màu đen. | Fe(OH)2 nguyên chất là chất rắn, màu trắng hơi xanh, không tan trong nước | Tan trong nước, đa số kết tinh thường ở dạng ngậm nước. Ví dụ: FeSO4.7H2O; FeCl2.4H2O |
| Tính chất hóa học | \(3FeO+10HNO_{3}\overset{t^{0}}{\rightarrow}\) \(3Fe(NO_{3})_{3}+NO+5H_{2}O\) | \(\begin{array}{*{20}{c}} {FeC{l_2} + {\rm{ }}2NaOH{\rm{ }} \to {\rm{ }}Fe{{\left( {OH} \right)}_2} \downarrow + {\rm{ }}2NaCl}\\ {4Fe{{\left( {OH} \right)}_2} + {\rm{ }}{O_2} + {\rm{ }}2{H_2}O{\rm{ }} \to {\rm{ }}4Fe{{\left( {OH} \right)}_3} \downarrow } \end{array}\) | \(FeCl_{2} +2Cl_{2}\overset{t^{0}}{\rightarrow}2FeCl_{3}\) |
| Điều chế | \(Fe_{2}O_{3}+CO\overset{t^{0}}{\rightarrow}2FeO+CO_{2}\uparrow\) | Điều chế trong điều kiện không có không khí \({FeC{l_2} + {\rm{ }}2NaOH{\rm{ }} \to {\rm{ }}Fe{{\left( {OH} \right)}_2} \downarrow + {\rm{ }}2NaCl}\) | Cho Fe (hoặc FeO; Fe(OH)2) tác dụng với HCl hoặc H2SO4 loãng. \(\begin{array}{*{20}{c}} {Fe{\rm{ }} + {\rm{ }}2HCl{\rm{ }} \to {\rm{ }}FeC{l_2} + {\rm{ }}{H_2} \uparrow }\\ {FeO{\rm{ }} + {\rm{ }}{H_2}S{O_4} \to {\rm{ }}FeS{O_4} + {\rm{ }}{H_2}O} \end{array}\) *Dung dịch muối sắt (II) điều chế được phải dùng ngay vì trong không khí sẽ chuyển dần thành muối sắt (III). |
Tính chất hoá học đặc trưng của hợp chất sắt (III) là tính oxi hoá.
Fe3+ + 1e → Fe2+
Fe3+ + 2e → Fe
| Đặc điểm | Sắt (III) oxit | Sắt (III) hidroxit | Muối Sắt (III) |
| Tính chất vật lí | Fe2O3 là chất rắn màu đỏ nâu, không tan trong nước | Fe(OH)3 là chất rắn, màu nâu đỏ, không tan trong nước | Đa số các muối sắt (III) tan trong nước, khi kết tinh thường ở dạng ngậm nước. Ví dụ: FeCl3.6H2O; Fe2(SO4)3.9H2O |
| Tính chất hóa học | \(F{e_2}{O_3} + {\rm{ }}6HCl{\rm{ }} \to {\rm{ }}2FeC{l_3} + {\rm{ }}3{H_2}O\) \(Fe_{2}O_{3}+CO\overset{t^{0}}{\rightarrow}2FeO+CO_{2}\uparrow\) | \(2Fe{\left( {OH} \right)_3} + {\rm{ }}3{H_2}S{O_4} \to {\rm{ }}F{e_2}{\left( {S{O_4}} \right)_3} + {\rm{ }}6{H_2}O\) | \(Fe+2FeCl_{3}\rightarrow 3FeCl_{2}\) \(Cu+2FeCl_{3}\rightarrow CuCl_{2}+2FeCl_{2}\) |
| Điều chế | \(Fe(OH)_{3}\overset{t^{0}}{\rightarrow}Fe_{2}O_{3}+3H_{2}O\) | Dung dịch kiềm + dung dịch muối sắt (III) \(FeC{l_3} + {\rm{ }}3NaOH{\rm{ }} \to {\rm{ }}Fe{\left( {OH} \right)_3} \downarrow + {\rm{ }}3NaCl\) |
Muối Fe2+ làm mất màu dung dịch KMnO4 trong môi trường axít tạo ra ion Fe3+. Còn ion Fe3+ tác dụng với I- tạo ra I2 và Fe2+. Sắp xếp các chất oxi hoá Fe3+, I2 và MnO4- theo thứ tự mạnh dần:
Muối Fe2+ làm mất màu dung dịch KMnO4 trong môi trường axít tạo ra ion Fe3+.
⇒ tính oxi hóa của Fe3+ < MnO4-
Còn ion Fe3+ tác dụng với I- tạo ra I2 và Fe2+.
⇒ Tính oxi hóa của I2 < Fe3+
Vậy thứ tự chất oxi hóa mạnh dần là: I2 < Fe3+ < MnO4 -.
Nhúng một lá sắt nhỏ vào dd chứa một trong những chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HNO3 (loãng, dư), H2SO4 (đặc, nóng, dư), NH4NO3, AgNO3 thiếu. Số trường hợp phản ứng tạo muối Fe(II) là?
+) Fe + AlCl3, NaCl, NH4NO3 không phản ứng
+) Fe + HNO3 (loãng, dư), H2SO4 (đặc, nóng, dư) sắt đều bị đưa về hóa trị cao nhất tức Fe (III)
+) Fe + FeCl3 tạo FeCl2
+) Fe + CuSO4 tạo FeSO4
+) Fe + Pb(NO3)2 tạo Fe(NO3)2
+) Fe + AgNO3 ( thiếu) tạo Fe(NO3)2
Lưu ý: nếu AgNO3 dư thì tạo Fe (III) do:
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
⇒ Các dung dịch tạo được muối sắt II là: FeCl3, CuSO4, Pb(NO3)2, AgNO3.
Để hòa tan hoàn toàn m gam bột Fe2O3 cần dùng vừa đủ 300ml dung dịch HCl 1M. Sau phản ứng thu được dung dịch Y. Tính giá trị của m?
nHCl = 0,3 mol
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
0,05 0,3
⇒ \(m_{Fe_{2}O_{3}}\) = 0,05.160 = 8 gam
Cho 100ml dung dịch FeCl2 1,2M tác dụng với 200ml dung dịch AgNO3 2M thu được m gam kết tủa. Giá trị của m là?
3 AgNO3 + FeCl2 → Fe(NO3)3 + 2 AgCl↓ + Ag↓
Mà n\(\tiny AgNO_3\) = 0,4 mol; n \(\tiny FeCl_2\) = 0,12 mol => AgNO3 dư
⇒ nAg = 0,12 mol; nAgCl = 0,24 mol
⇒ m = mAg + mAgCl = 47,4 g
Hòa tan m gam hỗn hợp A gồm FeO vào Fe2O3 bằng lượng vừa đủ dung dịch HCl, sau phản ứng thu được dung dịch B. Cho một nửa dung dịch B tác dụng với dung dịch NaOH dư, kết tủa thu được đem nung trong không khí đến khối lượng không đổi được 40 gam chất rắn. Cho một nửa dung dịch B còn lại tác dụng với lượng dư dung dịch AgNO3, thu được 208,15 gam chất rắn. Giá trị của m là:
Dung dịch B sau phản ứng sẽ gồm: Fe2+, Fe3+, Cl-.
40 g chất rắn chính là Fe2O3 ⇒ nFe = 0,5 mol.
Gọi a, b lần lượt là số mol của Fe2+, Fe3+
Ta có: a + b = 0,5 (1)
Bảo toàn điện tích dd B có nCl- = 2nFe2+ + 3nFe3+ = 2a + 3b
Cho 1 nửa dd B tác dụng với AgNO3 dư thu được kết tủa gồm AgCl và Ag
Ag+ + Cl- → AgCl Fe2+ + Ag+ → Fe3+ + Ag
2a+3b 2a+3b a a
Ta có 143,5(2a + 3b) + 108a = 208,15 (2)
Từ 1 và 2 ⇒ a = 0,2 và b = 0,3
⇒ m = 2.(0,2.72 + 0,3.160) = 124,8g
Cho 8,16 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 phản ứng hết với 250 ml dung dịch HNO3 x mol/lit (loãng), thu được 1,344 lít NO (đktc) và dung dịch Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, sinh ra khí NO. Biết trong các phản ứng, NO là sản phẩm khử duy nhất của N+5. Giá trị của x là:
Vì Z + Fe → khí NO ⇒ HNO3 dư và Fe → Fe3+
⇒ X phản ứng hết qui về: a mol Fe và b mol O
⇒ mX = 56a + 16b = 8,16g và Bảo toàn e: 3nFe = 3nNO + 2nO
⇒ 3a – 2b = 0,18 mol
⇒ a = 0,12; b = 0,09
Fe + 2Fe3+ → 3Fe2+
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O (vì hòa tan tối đa)
⇒ nFe sau = ½ nFe3+ + \(\frac{3}{8}\) nH+ dư ⇒ nH+ dư = 0,08 mol
⇒ \(n_{HNO_{3}}\) bđ = 0,08 + 4nNO + 2nO = 0,5 mol
⇒ x = 2 M
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 32có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Một oxit của sắt khi tan vào dung dịch H2SO4 loãng dư thu được dung dịch A làm mất màu thuốc tím và có khả năng hòa tan Cu. Công thức oxit là:
Cho các chất sau: FeCO3; FeS; Fe3O4; Fe(OH)2. Nếu hòa tan cùng số mol mỗi chất vào dung dịch H2SO4 đặc nóng dư thì chất tạo ra số mol khí lớn nhất là:
Nhiệt phân Fe(NO3)2 trong môi trường khí trơ. Sau khi các phản ứng xảy ra hoàn toàn, thu được sản phẩm gồm:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 32.
Bài tập 1 trang 145 SGK Hóa học 12
Bài tập 2 trang 145 SGK Hóa học 12
Bài tập 3 trang 145 SGK Hóa học 12
Bài tập 4 trang 145 SGK Hóa học 12
Bài tập 5 trang 145 SGK Hóa học 12
Bài tập 1 trang 202 SGK Hóa học 12 nâng cao
Bài tập 2 trang 202 SGK Hóa học 12 nâng cao
Bài tập 3 trang 202 SGK Hóa 12 Nâng cao
Bài tập 4 trang 202 SGK Hóa 12 Nâng cao
Bài tập 32.1 trang 74 SBT Hóa học 12
Bài tập 32.2 trang 74 SBT Hóa học 12
Bài tập 32.3 trang 75 SBT Hóa học 12
Bài tập 32.4 trang 75 SBT Hóa học 12
Bài tập 32.5 trang 75 SBT Hóa học 12
Bài tập 32.6 trang 75 SBT Hóa học 12
Bài tập 32.7 trang 75 SBT Hóa học 12
Bài tập 32.8 trang 76 SBT Hóa học 12
Bài tập 32.9 trang 76 SBT Hóa học 12
Bài tập 32.10 trang 76 SBT Hóa học 12
Bài tập 32.11 trang 76 SBT Hóa học 12
Bài tập 32.12 trang 76 SBT Hóa học 12
Bài tập 32.13 trang 76 SBT Hóa học 12
Bài tập 32.14 trang 77 SBT Hóa học 12
Bài tập 32.15 trang 77 SBT Hóa học 12
Bài tập 32.16 trang 77 SBT Hóa học 12
Bài tập 32.17 trang 77 SBT Hóa học 12
Bài tập 32.18 trang 77 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Một oxit của sắt khi tan vào dung dịch H2SO4 loãng dư thu được dung dịch A làm mất màu thuốc tím và có khả năng hòa tan Cu. Công thức oxit là:
Cho các chất sau: FeCO3; FeS; Fe3O4; Fe(OH)2. Nếu hòa tan cùng số mol mỗi chất vào dung dịch H2SO4 đặc nóng dư thì chất tạo ra số mol khí lớn nhất là:
Nhiệt phân Fe(NO3)2 trong môi trường khí trơ. Sau khi các phản ứng xảy ra hoàn toàn, thu được sản phẩm gồm:
Cho sơ đồ chuyển hoá: Fe \(\xrightarrow{x}\) FeCl3 \(\xrightarrow{y}\) Fe(OH)3 (mỗi mũi tên ứng với một phản ứng). Hai chất X, Y lần lượt là?
Cho dãy các chất Fe, Cu, KI, Ag, AgNO3, KBr, H2S, NaOH. Số chất trong dãy khử được FeCl3 trong dung dịch là?
Cho dung dịch Fe(NO3)2 lần lượt tác dụng với các dung dịch Na2S, H2SO4 loãng, H2S, H2SO4 đặc, NH3, AgNO3, Na2CO3, Br2. Số trường hợp xảy ra phản ứng là:
Khử hoàn toàn một lượng Fe3O4 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,008 lít khí H2 (đktc). Giá trị của m là
Cho m gam kim loại Fe tác dụng với dung dịch HNO3 dư, sau phản ứng thu được 3,36 lít khí NO đo ở đktc (sản phẩm khử duy nhất). Giá trị m là:
Hòa tan hết m gam Fe bằng 400ml dung dịch HNO3 1M. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 26,44 gam chất tan và khí NO (sản phẩm khử duy nhất). Giá trị của m là:
Hoà tan hoàn toàn m (g) FexOy bằng dd H2SO4 đặc nóng thu được 2,24lit SO2 (đktc). Phần dd chứa 120(g) một loại muối sắt duy nhất. Công thức oxit sắt và khối lượng m là:
Fe3O4; m = 23,2(g).
FeO, m = 32(g).
FeO; m = 7,2(g).
Viết phương trình hóa học của các phản ứng trong quá trình chuyển đổi sau:
FeS2 → Fe2O3 → FeCl3 → Fe(OH)3 → Fe2O3 → FeO → FeSO4 → Fe
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi thu được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2(đktc) được giải phóng là:
A. 8,19 lít.
B. 7,33 lít.
C. 4,48 lít.
D. 6,23 lít.
Ngâm một đinh sắt nặng 4 gam trong dung dịch CuSO4, sau một thời gian lấy đinh sắt ra, sấy khô, cân nặng 4,2857 gam. Khối lượng sắt tham gia phản ứng là:
A. 1,9990 gam
B. 1,9999 gam.
C. 0,3999 gam
D. 2,1000 gam.
Hỗn hợp A gồm FeO, Fe3O4, Fe2O3. Trong hỗn hợp A, mỗi oxit đều có 0,5 mol. Khối lượng của hỗn hợp A là:
A. 231 gam.
B. 232 gam.
C. 233 gam.
D. 234 gam.
Khử hoàn toàn 16 gam Fe2O3 bằng khí CO ở nhiệt độ cao. Khí đi ra sau phản ứng được dẫn vào dung dịch Ca(OH)2 dư. Khối lượng kết tủa thu được là:
A. 15 gam.
B. 20 gam.
C. 25 gam.
D. 30 gam.
a. Tính chất hóa học chung của hợp chất sắt (II) là gì? Dẫn ra những phản ứng hóa học để chứng minh những điều đã khẳng định( viết phương trình hóa học)
b. Tính chất hóa học chung cho hợp chất sắt (III) là gì? Dẫn ra những phản ứng hóa học để chứng minh những điều khẳng định (viết phương trình hóa học)
Hãy dẫn ra những phản ứng hóa học để chứng minh rằng các oxit sắt (II) là oxit bazo, các hidroxit sắt (II) là bazo (Viết các phương trình phản ứng hóa học)
Viết các phương trình hóa học biểu diễn những chuyển đổi hóa học sau:
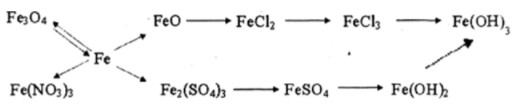
Hoà tan 10 gam FeSO4 có lẫn tạp chất là Fe2(SO4)3 trong nước, được 200 cm3 dung dịch. Biết 20 cm3 dung dịch này được axit hoá bằng H2SO4 loãng làm mất màu tím của 25 cm3 dung dịch KMnO4 0,03 M.
a) Viết phương trình hoá học dạng ion rút gọn. Cho biết vai trò của ion Fe2+ và ion MnO4-.
b) Có bao nhiêu mol ion Fe2+ tác dụng với 1 mol ion MnO4-?
c) Có bao nhiêu mol ion Fe2+ tác dụng với 25 cm3 dung dịch KMnO4 0,03M?
d) Có bao nhiêu gam Fe2+ trong 200 cm3 dung dịch ban đầu.
e) Tính phần trăm theo khối lượng của FeSO4.
Nhận định nào sau đây sai ?
A. Sắt tác dụng được với dung dịch CuSO4
B. Sắt tác dụng được với dung dịch FeCl3.
C. Sắt tác dụng được với dung dịch FeCl2.
D. Đồng tác dụng được với dung dịch FeCl3.
Hợp chất nào sau đây của sắt vừa có tính oxi hoá, vừa có tính khử?
A. FeO
B. Fe2O3
C. Fe(OH)3
D. Fe(NO3)3
Khử hoàn toàn 0,3 mol một oxit sắt FexOy bằng Al thu được 0,4 mol Al2O3 theo sơ đồ phản ứng sau :
FexOy + Al → Fe + Al2O3
Công thức của oxit sắt là
A. FeO
B. Fe2O3
C. Fe3O4
D. không xác định được
Khử hoàn toàn hỗn hợp Fe2O3 và CuO bằng CO thu được số mol CO2 tạo ra từ các oxit có tỉ lệ tương ứng là 3 : 2. Phần trăm khối lượng của Fe2O3 và CuO trong hỗn hợp lần lượt là
A. 50% và 50%.
B. 75% và 25%.
C.75,5% và 24,5%.
D. 25% và 75%.
Khi nung hỗn hợp các chất Fe(NO3)2, Fe(OH)3 và FeCO3 trong không khí đến khối lượng không đổi, thu được một chất rắn là
A. Fe3O4.
B. FeO.
C. Fe.
D. Fe2O3.
Cho các chất : Fe, FeO, Fe(OH)2, Fe(OH)3, Fe3O4, Fe2O3, Fe(NO3)2, Fe(NO3)3, FeSO4, Fe2(SO4)3, FeCO3. Cho từng chất trên lần lượt tác dụng với dung dịch HNO3 đặc, nóng thì số phản ứng thuộc loại phản ứng oxi hoá - khử là
A. 8.
B. 5.
C. 7.
D. 6.
Cho 0,01 mol một hợp chất của sắt tác dụng hết với H2SO4 đặc, nóng (dư) thoát ra 0,112 lít khí SO2 (đktc) (là sản phẩm khử duy nhất). Công thức hợp chất của sắt là
A. FeS.
B. FeS2.
C. FeO.
D. FeCO3.
Có hiện tượng gì xảy ra khi cho dung dịch Na2CO3 từ từ đến dư vào dung dịch FeCl3
A. Không có hiện tượng gì
B. Có kết tủa nâu đỏ
C. Có sủi bọt khí
D. Có kết tủa nâu đỏ và sủi bọt khí
Hãy thay A1, A2 . . . A8 bằng những chất vô cơ thích hợp và hoàn thành các PTHH theo sơ đồ các chuỗi phản ứng sau :
(1) A1 + A2 → A3
(2) A3 + A4 → FeCl3
(3) A5 + FeCl3 → A3 + I2 + A2
(4) A2 + A6 → MnCl2 + A7 + A4
(5) A4 + A8 → CaOCl2 + A7
Cho A là oxit, B là muối, C và D là kim loại. Hãy viết PTHH của các phản ứng sau:
a) A + HCl → 2 muối + H2O
b) B + NaOH → 2 muối + H2O
c) C + muối → 1 muối
d) D + muối → 2 muối
Cho biết các phản ứng xảy ra khi cho hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 vào :
a) Dung dịch H2SO4 loãng.
b) Dung dịch HNO3 loãng.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
A. Hematit đỏ
B. Hematit nâu
C. Manhetit
D. xiderit
Câu trả lời của bạn
Quặng Manhetit có hàm lượng sắt lớn nhất
Câu trả lời của bạn
Các quá trình khi cho kim loại phản ứng với HNO3:
+/ Cho e : Al → Al+3 + 3e
Cu → Cu+2 + 2e
+/ Nhận e: N+5 + 1e → N+4
Đặt số mol Cu và Al lần lượt là x và y
→ mX = 64x + 27y = 1,23
Và ne trao đổi = 2x + 3y = nNO2 = 0,06
→x = 0,015 ; y = 0,01
→%mCu(X) = 78,05%
Khi phản ứng với NH3 thì Cu(OH)2 bị hòa tan tạo phức , kết tủa chỉ còn Al(OH)3
→ m = mAl(OH)3 = 0,78g
Câu trả lời của bạn
Gọi hóa trị của M là n và số mol 2 chất Fe và M lần lượt là x và y
+/ TN1: nH2 = 0,055 mol → Bảo toàn e: 2x + ny = 0,11
+/ TN2 : Bảo toàn e có 2nCl2 = 5nKMnO4 = 3nFe + n.nM
→ 3x + ny = 0,12 mol
→ x = 0,01 mol ; ny = 0,09
→ mX = mFe + mM → 1,37 = 56.0,01 + M.y
→ M = 9n. Chọn cặp n = 3 và M = 27 (Al) phù hợp nhất
A. 20 g
B. 35,6 g
C. 26,95 g
D. 15,138 g
Câu trả lời của bạn
3FeCO3 + 10HNO3 → 3Fe(NO3)3 + NO + 3CO2 + 5H2O
Đặt nFeCO3 =x mol
→ nkhí = 4x/3 = 0,2 → x = 0,15 mol
→ mquặng = 0,15.116/ 0,87 = 20g
Câu trả lời của bạn
Do nAl : nFe = 2 : 1 và 27nAl + 56nFe = 7,15g
→ nAl = 0,13 mol ; nFe = 0,065 mol
nAgNO3 = 0,39 mol. Phản ứng xảy ra :
+/ Al + 3Ag+ → Al3+ + 3Ag
→sau phản ứng có 0,39 mol Ag và 0,065 mol Fe
→ m = 45,76g
A. 5.
B. 6.
C. 7.
D. 4.
Câu trả lời của bạn
Các chất thỏa mãn là : CuSO4 ; Pb(NO3)2 ; HCl ; Fe(NO3)3
→ có 4 TH thỏa mãn
A. 240 ml.
B. 80 ml.
C. 160 ml.
D. 400 ml.
Câu trả lời của bạn
Trong X có : nFe3O4 = 0,03 mol ; nCuO = 0,02 mol
Khi phản ứng với HCl vừa đủ thì trong dung dịch có :
0,02 mol Cu2+ ; 0,03 mol Fe2+ ; 0,06 mol Fe3+ ; 0,28 mol Cl-.
Khi điện phân :
+/ Anot : 2Cl- → Cl2 + 2e
+/ Catot : Fe3+ + 1e → Fe2+ (1)
Cu2+ + 2e → Cu (2)
Fe2+ + 2e → Fe (3)
Nếu dung dịch chỉ giảm khối lượng vì Cl2 bay ra , chỉ xảy ra (1) ở Catot
→ ne trao đổi = 0,06 mol → mCl2 = 2.13g < 11,18g →Loại
Nếu (10 và (20 xảy ra vừa đủ → ne trao đổi = 0,1 mol
→ mgiảm = mCl2 + mCu = 4,83g < 11,18 →Loại
Vậy xảy ra cả (1) ; (2) ; (3)
Đặt nFe2+ phản ứng = a mol
→ ne trao đổi = (0,1 + 2a) mol → nCl2 = (0,05 + a) mol
→mGiảm = 0,02.64 + 56a + 71.(0,05 + a) = 11,18
→nFe2+ dư = 0,03 + 0,06 – 0,05 = 0,04 mol
Khi phản ứng với KMnO4 tạo MnSO4 ; Fe2+ bị OXH thành Fe3+
Bảo toàn e : nFe2+ = 5nKMnO4 → 0,04 = 5.0,1V
→ a = 0,05 mol
→V = 0,08 l = 80 ml
A. 37,44 gam.
B. 31,20 gam.
C. 28,08 gam.
D. 24,96 gam.
Câu trả lời của bạn
Qui hỗn hợp về dạng : x mol Fe ; y mol FeO ; z mol Fe2O3
→ mhh = 56x + 72y + 160z = 26 (1)
Có nHCl = 2x + 2y + 6z = 0,91 mol (2)
Và nH2 = nFe = x = 0,195 mol (3)
Từ (1) ; (2) ; (3) → y = z = 0,065 mol
→ Khi nung kết tủa thì sản phẩm chỉ còn Fe2O3
Bảo toàn Fe : nFe2O3 = ½ nFe(hh đầu) = ½ . ( x + y + 2z) = 0,195 mol
→m = 31,2g
A. 8,96.
B. 3,36.
C. 4,48.
D. 3,92.
Câu trả lời của bạn
Ta có : mKL + mO = mY
→ nO (Y) = 0,2 mol
Qui hỗn hợp về dạng : Fe;Al;Zn;O
→ Bảo toàn e : ne Kl trao đổi = 2nO + 2nSO2 (1)
Lại có mmuối = mKL + mSO4
→ nSO4 = 0,4 mol
→Bỏa toàn điện tích : 2nSO42- = nđiện tíchKL = n e KL trao đổi = 0,8 mol
Từ (1) → nSO2 = 0,2 mol
→V = 4,48l
A. 0,56.
B. 0,448.
C. 1,39.
D. 1,12.
Câu trả lời của bạn
Qui hỗn hợp đầu về : Fe;Mg;Cu;O
→ nO = 0,2 mol
Lại có : nHNO3 dùng = ne KL trao đổi + nN ( N2 ; N2O )
Đặt nN2 = x → nN2O = 1,5x
→ 0,804 / 1,2 = ne KL trao đổi + 5x (1)
Bảo toàn e : ne KL trao đổi = 2nO + 10nN2 + 8nN2O = 0,4 + 22x (2)
Từ (1) và (2) → x = 0,01 mol
→V = 22,4 . 2,5.0,01 = 0,56 l
A. 3.
B. 2.
C. 4.
D. 5.
Câu trả lời của bạn
Phản ứng với H2SO4 không tạo SO2 khi không có phản ứng OXH-K ; không phải là muối của SO3 ; HSO3 ; S2O3
→ các chất thỏa mãn là : Fe2O3 ; Fe(OH)3
→ 2 chất
A. Nhúng thanh sắt (dư) vào dung dịch AgNO3 thấy thanh sắt dần có màu trắng bạc và dung dịch xuất hiện màu vàng nâu.
B. Nhúng thanh sắt (dư) vào dung dịch Cu(NO3)2 thấy thanh sắt chuyển qua màu đỏ và dung dịch nhạt màu xanh.
C. Nhúng thanh đồng (dư) vào dung dịch FeCl3 thấy màu vàng nâu của dung dịch nhạt dần và thay thế bằng màu xanh.
D. Nhúng thanh sắt (dư) vào dung dịch Fe(NO3)3 thấy màu vàng nâu của dung dịch nhạt dần đến màu xanh nhạt.
Câu trả lời của bạn
Do khi nhúng thanh sắt dư vào AgNO3 xảy ra phản ứng:
+/ Fe + 2AgNO3 → Fe(NO3)2 + Ag
Do Fe dư nên không thể xảy ra phản ứng:
+/ Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
→Dung dịch chỉ có màu xanh nhạt của Fe2+
A. 16,3296
B. 14,7744
C. 11.6640
D. 15,5520
Câu trả lời của bạn
Qui hỗn hợp X và Y về: x mol Al ; y mol Fe ; z mol O
Khi phản ứng với HCl :
+/ M + nHCl → MCln + 0,5nH2
+/ O + 2HCl → H2O + 2Cl-
→ Số mol HCl phản ứng = nCl trong muối = 2nH2 + 2nO = 2.0,804 + 2z
Bảo toàn khối lượng : mKL + mCl trong muối = mmuối
→ 27x + 56y + 35,5(1,608 + 2z) = 103,2635 (1)
Khi cho X + HNO3 → 0,593 mol NO
→ + Cho e: Fe → Fe+3 + 3e
Al→ Al+3 + 3e
+ Nhận e : N+5 + 3e → N+2
O + 2e → O-2
→Bảo toàn e : 3x + 3y = 2z + 0,593.3 (2)
Lại có trong X : m = 27x = 56y + 16x (3)
Tử 1;2;3 → x = 0,576 mol
→ m = mAl = 15,5520 g
A. FeS2
B. FeO
C. Fe2O3
D. FeS
Câu trả lời của bạn
Hàm lượng sắt trong các chất : FeS (63,6%) ; FeS2(46,7%) ; Fe2O3(70%) ; FeO(77,8%) →FeO có hàm lượng sắt cao nhất
A. 5
B. 6
C. 4
D. 7
Câu trả lời của bạn
Các chất phản ứng với FeCl3 sinh ra kết tủa là : Na2CO3 ( Fe(OH)3 ) ; AgNO3 ( AgCl) ; H2S (S) ; Na2S ( S và FeS) ; NH3 ( Fe(OH)3 ) ; NaOH ( Fe(OH)3 )
→Có 6 chất
A. 106
B. 103
C. 105
D. 107
Câu trả lời của bạn
Có nO(X) = 0,32 mol và mKL = 20,2 g
Coi X gồm Al ; Fe; Mg ;O
Khi phản ứng với HNO3 giả thiết xảy ra các quá trình :
+/ Cho e : Al → Al+3 + 3e
Mg → Mg+2 + 2e
Fe → Fe+3 + 3e
+/ Nhận e : N+5 + 3e → N+2
2N+5 + 8e → 2N+1
O + 2e → O-2
Có n khí = 0,16 mol và M = 31,75 g
Áp dụng qui tắc đường chéo → nNO : nN2O = 7 : 1
→ nNO = 0,14 mol ; nN2O = 0,02 mol
→ ne trao đổi = 3nNO + 8nN2O + 2nO = 1,22 mol
Khi muối Y nhiệt phân tạo các oxit MgO ; Al2O3 ; Fe2O3
Ta có mrắn = mKL + mO
→ nO = 0,67 mol
Bảo toàn điện tích : nđiện tích cation = 2nO2- → nO = 1,34 mol
→ nđiện tích cation = nNO3- trong muối = ne cation trao đổi = 1,34 mol > 1,22
→sản phẩm khử có NH4NO3
→ 8nNH4NO3 = 1,34 – 1,22 = 0,12
→ nNH4NO3 = 0,015 mol
→mmuối = mKL + mNO3 trong muối + mNH4NO3 = 104,48 g
A. 11523
B. 10684
C. 12124
D. 14024
Câu trả lời của bạn
Đặt số mol mỗi chất trong X là a mol
Dung dịch axit có CHCl = 2CH2SO4
→ nCl = 2nSO4
→Khi phản ứng tạo muối trung hòa nên trong dung dịch có : Cu2+ ; Na+; Cl-; SO42-
→ Bảo toàn điện tích : 2a + a = nCl + 2nSO4 = 4nSO4
→ nSO4 = 0,75a ; nCl = 1,5a
→ m = 64a + 23a + 96.0,75a + 35,5.1,5a
= 212,25a (*)
Khi cho Fe vào Z tạo hỗn hợp kim loại và khối lượng giảm so với ban đầu
→ Fe bị hòa tan 1 phần bởi H+ và Cu2+ dư
Khi điện phân : +/ Catot : Cu2+ + 2e → Cu
+/ Anot : 2Cl- → Cl2 + 2e
2H2O → 4H+ + O2 + 4e
Đặt nO2 = b mol
Bảo toàn e → nCu2+ phản ứng = 0,75a + 2b → nCu2+ dư = 0,25a – 2b mol
→ mgiảm = mO2 + mCl2 + mCu = 32b + 71.0,75a + 64(0,75a + 2b) = 20,225 g
→ 101,25a + 160b = 20,225 (1)
Khi Cho Fe vào : Fe + 2H+ → Fe2+ + H2
Fe + Cu2+ → Fe2+ + Cu
→ mgiảm = mFe phản ứng – mCu tạo ra
→ m – 0,9675m = 56.(2b + 0,25a – 2b ) – 64(0,25a – 2b)
→ 0,0325m = 128b – 2a (**)
Tử (*) và (**) → b = 14,39a (2)
Từ (1) và (2) → a = 0,18 mol ; b = 0,0125 mol
→ ne trao đổi = 2nCu2+ bị điện phân = 0,32 mol
→ t = 11523 s
A. 1,75.
B. 2,25.
C. 2,00.
D. 1,50.
Câu trả lời của bạn
Áp dụng định luật bảo toàn điện tích:
Chuyển hết về cuối là 0,02 mol Zn(NO3)2
Áp dụng bảo toàn khối lượng:
→ m = 0,02.6,5 + 5,82 - 5,2 + 4,16 - 0,04.108= 1,76 gam
A. 6,64.
B. 5,68.
C. 4,72.
D. 5,2.
Câu trả lời của bạn
Phản ứng Kim loại + HNO3 → = 0,18 mol
Nhiệt phân: trong oxit
cân bằng điện → có 0,09 mol O
→ m = 3,76 + 0,09.16 = 5,20 gam
→ Đáp án D
A. 23,33.
B. 15,25.
C. 61,00.
D. 18,30.
Câu trả lời của bạn
Số mol mỗi chất = 0,8x2:(15 + 3 + 8 + 6) = 0,05 mol
→ m = 0,05 x (56 x 2 + 32 x 4 + 65) = 15,25 gam
→ Đáp án B

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *