Nội dung bài học trình bày cụ thể, tỉ mỉ về Nhôm và hợp chất quan trọng của nhôm, giúp các em học sinh biết được vị trí của nhôm trong Bảng hệ thống tuần hoàn các nguyên tố hóa học; cấu tạo nguyên tử, tính chất vật lí - hóa học và phương pháp sản xuất Nhôm. Biết được tính chất và ứng dụng của một số hợp chất quan trọng của Nhôm như: Al2O3 (Nhôm oxit), Al(OH)3 (Nhôm hidroxit), Al2(SO4)3 (Nhôm sunfat)...
Nhôm dể nhường 3 e hoá trị, nên có số oxi hoá +3.
Là kim loại nhẹ ,màu trắng bạc, nóng chảy ở nhiệt độ không cao lắm.
Rất dẻo, có thể dát được lá nhôm mõng 0,01 mm dùng để gói thực phẩm.
Có cấu tạo mạng lập phương tâm diện ,có mật độ electron tự do tượng đối lớn. Do vậy nhôm có khả năng dẩn điện và nhiệt tốt.
Nhôm là kim loại có tính khử mạnh, nên nó bị oxi hoá dể dàng thành ion nhôm Al3+ . Ta có: Al → Al3+ + 3e
Thí nghiệm Nhôm tác dụng với khí Clo: 2Al + 3Cl2 → 2AlCl3 .
Thí nghiệm của Nhôm và Oxi: 4Al + 3 O2 → 2Al2O3
Thí nghiệm của Nhôm vào Sắt (III) oxit: 2Al + Fe2O3 \(\overset{t^{0}}{\rightarrow}\) Al2O3 + 2Fe
Al2O3 + 2 NaOH → 2NaAlO2 + H2O
2Al + 6H2O → 2Al(OH)3 + 3H2 (2)
Al(OH)3 + NaOH → NaAlO2 + 2H2O (3)
Phản ứng (2), (3) xảy ra xen kẽ nhau mãi cho đến khi nhôm bị tan hết .
2Al + 2NaOH + 2H2O → NaAlO2 + 3 H2
Dùng chế tạo máy bay, ô tô, tên lửa …
Trang trí nội thất, xây dựng nhà cửa.
Dẫn điện, dẩn nhiệt tốt nên dùng làm dây cáp dẩn điện.
Nhôm là kim loại hoạt động mạnh nên trong tự nhiên chỉ tồn tại ở dạng hợp chất như: đất sét, mica, criolit …
Khử ion Al3+ thành Al.
Quá trình điện phân:
Cực (-) : Al3+ + 3e → Al
Cực ( +) :Xảy ra sự oxi hoá 2O2- → O2 + 4e
Tính bền ⇒ Al2O3 khó bị khử à Al bằng C, H2, CO.
Tính chất lưỡng tính:
Al2O3+6HCl → 2AlCl3 + 3 H2O
Al2O3+2NaOH → 2NaAlO2+H2O
Dạng oxit ngậm nước là thành phần chủ yếu quặng boxit là nguyên liệu sản xuất nhôm.
Dạng oxit khan có cấu tạo tinh thể giống đá quý: Tinh thể corindon trong suốt, không màu, rất rắn, chế tạo đá mài, giấy nhám…
Bột nhôm oxit xúc tác cho tổng hợp hữu cơ.
Là chất kết tủa keo, màu trắng
Không tan trong nước, trong dd CO2, NH3 nhưng tan được trong môi trường H+ và OH- mạnh.
Al(OH)3+ 3HCl → AlCl3 + 3H2O
Al(OH)3+NaOH → NaAlO2+ 2H2O
Muối nhôm sunfat khan tan trong nước → tỏa nhiệt do bị hiđrat hóa.
Dùng trong ngành thuộc da, công nghiệp giấy, chất cầm màu trong ngành dệt vải, làm trong nước…
2AlCl3 + 3Na2CO3 + 3H2O → 2Al(OH)3 + 6NaCl + 3CO2
Cho sơ đồ phản ứng sau:
\(Al_{4}C_{3} \xrightarrow[]{\ \ \ \ } X \xrightarrow[]{\ +O_{2}\ } Y \xrightarrow[]{\ \ \ \ }C_{2}H_{4}O_{2} \xrightarrow[]{\ +KHCO_{3} \ }Z\)
Các chất X, Y, Z, T lần lượt là:
Sơ đồ hoàn chỉnh: Al4C3 → CH4 → CH3OH → CH3COOH → CH3COOK
Cho hỗn hợp 2 kim loại Al và Cu vào dung dịch hỗn hợp 2 muối AgNO3 và Ni(NO3)2. Kết thúc phản ứng được rắn X (tan một phần trong dung dịch HCl dư) và thu được dung dịch Y (phản ứng vừa đủ với dung dịch NaOH được tủa gồm 2 hydroxit kim loại). Chất rắn X gồm những chất nào?
Đầu tiên Al phản ứng với AgNO3 trước
(1) Nếu Al còn dư thì phản ứng với Ni(NO3)2; Cu không phản ứng
(2) Nếu Al hết và AgNO3 dư thì Cu phản ứng với AgNO3, Ni(NO3)2 giữ nguyên.
X tan 1 phần trong HCl ⇒ Chứng tỏ giả thuyết (1) đúng
⇒ Y gồm Al3+; Ni2+ (có thể)
Mà Y phản ứng với NaOH vừa đủ tạo 2 hydroxit ⇒ Y phải có Ni2+
⇒ Rắn X gồm Ag, Cu, Ni
Khi nhỏ từ từ dung dịch AlCl3 cho tới dư vào dung dịch NaOH và lắc đều thì xảy ra hiện tượng gì?
Đầu tiên do OH- dư nên kết tủa tạo thành sẽ tan ngay:
Al3+ + 3OH- → Al(OH)3
Al(OH)3 + OH- → AlO2- + 2H2O
Khi OH- hết thì xảy ra phản ứng tạo kết tủa:
Al3+ + 3AlO2- + 6H2O → 4Al(OH)3
Bài 4:
Dùng 200 ml dung dịch NaOH 1M để hòa tan hết tối đa m gam Al2O3. Giá trị của m là:
Hướng dẫn:
2NaOH +Al2O3 → 2NaAlO2 +H2O
0,2 0,1
\(\Rightarrow m_{Al_{2}O_{3}} = 0,1. 102 = 10,2 \ g\)
Hoà tan hoàn toàn m gam bột Al vào 150 ml dung dịch HCl 2M thu được dung dịch X. Cho dung dịch X tác dụng với 320 ml dung dịch NaOH 1M thu được 4,68 gam kết tủa. Giá trị của m là:
nHCl = 0,3 mol; nNaOH = 0,32 mol; \(n_{{Al(OH)_{{3}}}}\) = 0,06 mol
Vì nNaOH > nHCl ⇒ dư OH- sau khi phản ứng hết với AlCl3
⇒ có hiện tượng hòa tan kết tủa
⇒ nOH tan kết tủa = nNaOH – nHCl = 0,02 mol
⇒ \(n_{{Al(OH)_{{3}}}}\) max = 0,06 + 0,02 = 0,08 mol = nAl bđ
⇒ mAl = 2,16g
Cho 12,6 gam hỗn hợp X gồm Al và Al4C3 vào dung dịch KOH dư, sau khi các phản ứng xảy ra hoàn toàn thu được a mol hỗn hợp khí Y và dung dịch Z. Sục khí CO2 dư vào dung dịch Z thu được 31,2 gam kết tủa. Giá trị của a là:
Đặt số mol Al: Al4C3: y (mol) ta có: 27x + 144y = 12,6 (1)
Kết tủa thu được là Al(OH)3. Số mol Al(OH)3 = 0,4 mol → x + 4y = 0,4 (BTNT Al) (2)
Giải (1) và (2) ta được: x = 0,2 mol; y = 0,05 mol
Khí thu được gồm H2 và CH4; số mol H2 = 1,5x; số mol CH4 = 3y
⇒ Tổng số mol khí = 1,5x + 3y = 0,45 mol
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 27có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Để thu được Al2O3 từ hỗn hợp Al2O3 và Fe2O3, người ta lần lượt:
Nguyên liệu chính dùng để sản xuất nhôm là:
Để phân biệt dung dịch AlCl3 và dung dịch KCl ta dùng dung dịch:
Cho bột Al và dung dịch KOH dư thấy hiện tượng:
Phát biểu nào sau đây là sai?
Có ba chất rắn riêng biệt: Al, Mg, Al2O3. Dung dịch có thể phân biệt được 3 chất rắn trên là:
Hỗn hợp bột kim loại X và bột oxit Y khi xảy ra phản ứng sẽ tự toả nhiệt với hiệu ứng nhiệt của phản ứng rất lớn, nâng nhiệt độ của hệ đến nhiệt độ nóng chảy của kim loại X vào khoảng 35000C. Phần oxit kim loại X nổi thành xỉ trên bề mặt kim loại Y lỏng. Lợi dụng phản ứng này để thực hiện quá trình hàn kim loại, nhất là đầu nối của các thanh ray trên đường xe lửa.

Kim loại X và oxit Y lần lượt là:
Nung hỗn hợp bột gồm 15,2g Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi phản ứng hoàn toàn thu được 23,3g hỗn hợp rắn X. Cho toàn bộ hỗn hợp X phản ứng với axit HCl dư thấy thoát ra V lit khí H2(dktc). Giá trị của V là :
Cho m gam Al phản ứng hoàn toàn với dung dịch loãng (dư), thu được 4,48 lít khí NO (đktc, sản phẩm khử duy nhất). Giá trị của m là
Hoà tan hoàn toàn 1,02 gam Al2O3 trong dung dịch H2SO4 loãng dư, thu được khối lượng muối là:
Câu 11-30: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 27.
Bài tập 1 trang 128 SGK Hóa học 12
Bài tập 2 trang 128 SGK Hóa học 12
Bài tập 3 trang 128 SGK Hóa học 12
Bài tập 4 trang 129 SGK Hóa học 12
Bài tập 5 trang 129 SGK Hóa học 12
Bài tập 6 trang 129 SGK Hóa học 12
Bài tập 7 trang 129 SGK Hóa học 12
Bài tập 8 trang 129 SGK Hóa học 12
Bài tập 1 trang 176 SGK Hóa 12 Nâng cao
Bài tập 2 trang 167 SGK Hóa học 12 nâng cao
Bài tập 3 trang 176 SGK Hóa học 12 nâng cao
Bài tập 4 trang 176 SGK Hóa 12 Nâng cao
Bài tập 5 trang 176 SGK Hóa 12 Nâng cao
Bài tập 6 trang 176 SGK Hóa 12 Nâng cao
Bài tập 1 trang 180 SGK Hóa 12 Nâng cao
Bài tập 2 trang 180 SGK Hóa 12 Nâng cao
Bài tập 3 trang 180 SGK Hóa 12 Nâng cao
Bài tập 4 trang 181 SGK Hóa 12 Nâng cao
Bài tập 5 trang 181 SGK Hóa 12 Nâng cao
Bài tập 6 trang 181 SGK Hóa 12 Nâng cao
Bài tập 7 trang 181 SGK Hóa 12 Nâng cao
Bài tập 27.1 trang 62 SBT Hóa học 12
Bài tập 27.2 trang 62 SBT Hóa học 12
Bài tập 27.3 trang 62 SBT Hóa học 12
Bài tập 27.4 trang 62 SBT Hóa học 12
Bài tập 27.5 trang 62 SBT Hóa học 12
Bài tập 27.6 trang 63 SBT Hóa học 12
Bài tập 27.7 trang 63 SBT Hóa học 12
Bài tập 27.8 trang 63 SBT Hóa học 12
Bài tập 27.9 trang 63 SBT Hóa học 12
Bài tập 27.10 trang 63 SBT Hóa học 12
Bài tập 27.11 trang 63 SBT Hóa học 12
Bài tập 27.12 trang 63 SBT Hóa học 12
Bài tập 27.13 trang 64 SBT Hóa học 12
Bài tập 27.18 trang 64 SBT Hóa học 12
Bài tập 27.19 trang 64 SBT Hóa học 12
Bài tập 27.20 trang 65 SBT Hóa học 12
Bài tập 27.21 trang 65 SBT Hóa học 12
Bài tập 27.22 trang 65 SBT Hóa học 12
Bài tập 27.23 trang 65 SBT Hóa học 12
Bài tập 27.24 trang 65 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Để thu được Al2O3 từ hỗn hợp Al2O3 và Fe2O3, người ta lần lượt:
Nguyên liệu chính dùng để sản xuất nhôm là:
Để phân biệt dung dịch AlCl3 và dung dịch KCl ta dùng dung dịch:
Cho bột Al và dung dịch KOH dư thấy hiện tượng:
Phát biểu nào sau đây là sai?
Có ba chất rắn riêng biệt: Al, Mg, Al2O3. Dung dịch có thể phân biệt được 3 chất rắn trên là:
Hỗn hợp bột kim loại X và bột oxit Y khi xảy ra phản ứng sẽ tự toả nhiệt với hiệu ứng nhiệt của phản ứng rất lớn, nâng nhiệt độ của hệ đến nhiệt độ nóng chảy của kim loại X vào khoảng 35000C. Phần oxit kim loại X nổi thành xỉ trên bề mặt kim loại Y lỏng. Lợi dụng phản ứng này để thực hiện quá trình hàn kim loại, nhất là đầu nối của các thanh ray trên đường xe lửa.

Kim loại X và oxit Y lần lượt là:
Nung hỗn hợp bột gồm 15,2g Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi phản ứng hoàn toàn thu được 23,3g hỗn hợp rắn X. Cho toàn bộ hỗn hợp X phản ứng với axit HCl dư thấy thoát ra V lit khí H2(dktc). Giá trị của V là :
Cho m gam Al phản ứng hoàn toàn với dung dịch loãng (dư), thu được 4,48 lít khí NO (đktc, sản phẩm khử duy nhất). Giá trị của m là
Hoà tan hoàn toàn 1,02 gam Al2O3 trong dung dịch H2SO4 loãng dư, thu được khối lượng muối là:
Cho 300 ml dung dịch NaOH 0,1M phản ứng với 100 ml dung dịch Al2(SO4)3 0,1M. Sau khi phản ứng xảy ra hoàn toàn, thu được a gam kết tủa. Giá trị của a là:
Hòa tan hết m gam bột nhôm kim loại bằng dung dịch HNO3 thu được dung dịch A không chứa muối amoni và 1,12 lit hỗn hợp khí gồm N2 và N2O có tỉ khối so với He bằng 10,2. Khối lượng ban đầu m có giá trị:
Hiện tượng nào xảy ra khi cho từ từ đến dư dung dịch NaOH vào dung dịch AlCl3 ?
Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện
Xuất hiện kết tủa keo trắng ngay lập tức, sau đó kết tủa tan dần
Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện, rồi tan dần.
Phát biểu nào sau đây là sai ?
Dung dịch AlCl3 và Al2(SO3)3 làm quỳ tím hóa hồng
Al(OH)3, Al2O3, Al đều là các chất lưỡng, tính,
Nhôm là kim loai nhẹ và có khả năng dẫn điện Iot
Chất nào sau đây không có tính lưỡng tính?
Cho 3,82 gam hợp kim Ba, Al vào nước dư chỉ thu được dung dịch chưa duy nhất một muối. Khối lượng Ba là:
3.425 gam.
1,644 gam.
Cho m gam hỗn hợp X gồm 2 kim loại kiềm thuộc 2 chu kì liên tiếp tác dụng với 180 ml dung dịch Al2(SO4)3 1M thu được 15,6 gam kết tủa; khí H2 và dung dịch A. Nếu cho m gam hỗn hợp X tác dụng với 240 gam dung dịch HCI 18,25% thu được dung dịch B và H2. Cô cạn dung dịch B thu được 83,704 gam chất rắn khan. Biết rằng m < 45 gam. Phần trăm khối lượng của kim loại kiềm có nguyên tử khối nhỏ hơn trong X là:
Cho các quặng sau: pirit, thạch cao, mica, apatit, criolit, boxit, dolomit. Số quặng chứa nhôm là:
Cho một lá nhôm vào ống nghiệm chứa dung dịch Hg(NO3)2, thấy có một lớp thủy ngân bám trên bề mặt nhôm. Hiện tượng tiếp theo quan sát được là:
khí hiđro thoát ra mạnh.
khí hiđro thoát ra sau đó dừng lại ngay.
lá nhôm bốc cháy.
Thực hiện các thí nghiệm sau :
(a) Cho từ từ NaOH đến dư vào dung dịch Al2(SO4)3,
(b) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaOH,
(c) Cho từ từ NH3 đến dư vào dung dịch Al2(SO4)3,
(d) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NH3.
(e) Cho từ từ HCl đến dư vào dung dịch NaAlO2 .
(f) Cho từ từ NaAlO2 đến dư vào dung dịch HCl
(g) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaAlO2
Trong các thí nghiệm trên, số thí nghiệm xuất hiện kết tủa là
Hỗn hợp bột X gồm Al và Fe2O3. Nếu cho m gam hỗn hợp X tác dụng hết với dung dịch NaOH loãng thu được 5,376 lít H2 (đktc). Nếu nung nóng m gam hỗn hợp X để thực hiện hoàn toàn phản ứng nhiệt nhôm, thu được chắt rắn y. Cho Y phản ứng vừa du với V mi dung dịch hỗn hợp HCl 1M và H2SO4 0,5M tạo 4,4352 lít H2 (đklc) Giá trị cua V là :
Trong các cặp chất sau đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
AlCl3 và Na2CO3
HNO3 và NaHCO3
NaAlO2 và KOH
Dùng hóa chất nào sau đây để phân biệt Zn(NO3)2 và Al(NO3)3 ?
Dung dịch NaOH
Dung dịch Ba(OH)2
Dung dịch NH3
Hỗn hợp X gồm Al và Fe3O4. Nung hỗn hợp X ở nhiệt độ cao thu được hỗn hợp Y. Chia Y làm 2 phần bằng nhau:
• Phần 1 cho vào dung dịch NaOH lấy dư, sau phản ứng thu được 1,344 lít khí (đktc).
• Phần 2 hòa tan hết trong 310 ml dung dịch H2SO4 1M (loãng) thu được 3,36 lít khí (đktc).
Hiệu suất của phản ứng nhiệt nhôm là ?( Giả sử Fe3O4 chỉ bị khử về Fe)
60%.
66,67%.
Khử hoàn toàn 16 gam bột Fe2O3 bằng bột nhôm. Khối lượng bột nhôm cần dùng là?
Sản xuất nhôm bằng phương pháp điện phân nhôm oxit nóng chảy. Hãy tính khối lượng Al2O3 và than chì (C) cần dùng để sản xuất được 5,4 tấn nhôm.
Một pin điện hóa được cấu tạo bởi các cặp oxi hóa - khử Al3+/Al và Cu2+/Cu. Phản ứng hóa học xảy ra khi pin hoạt động là:
2Al + 3Cu → 2Al3+ + 2Cu2+
2Al3+ + 2Cu → 2Al + 3Cu2+
2Al + 3Cu2+ → 2Al3+ + 3Cu
Cho Al + HNO3 → Al(NO3)3 + NO + H2O, số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat là bao nhiêu?
Phương trình hóa học nào sau đây cân bằng sai:
Al + 6HNO3 → Al(NO3)3 + 3NO2 + 3H2O
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
10Al + 38HNO3 → 10Al(NO3)3 + 3N2 + 18H2O
Để phân biệt Al và Fe người ta dùng dung dịch nào sau đây?
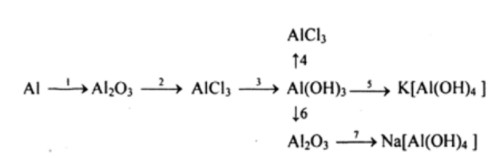
Viết phương trình hóa học của các phản ứng thực hiện dãy chuyển đổi sau:
\(Al \xrightarrow[ \ ]{ \ (1) \ } AlCl_{3}\xrightarrow[ \ ]{ \ (2) \ } Al(OH)_3\xrightarrow[ \ ]{ \ (3) \ } NaAlO_{2} \xrightarrow[ \ ]{ \ (4) \ } Al(OH)_{3} \xrightarrow[ \ ]{ \ (5) \ }\)\(Al_{2}O_{3} \xrightarrow[ \ ]{ \ (6) \ } Al\)
Có 2 lọ không ghi nhãn đựng dung dịch AlCl3 và dung dịch NaOH. Không dùng thêm chất nào khác, làm thế nào để nhận biết mỗi chất?
Phát biểu nào sau đây là đúng?
A. Nhôm là 1 kim loại lưỡng tính.
B. Al(OH)3 là một bazơ lưỡng tính.
C. Al2O3 là một oxit trung tính.
D. Al(OH)3 là một hiđroxxit lưỡng tính.
Trong những chất sau, chất nào không có tính lưỡng tính?
A. Al(OH)3
B. Al2O3
C. ZnSO4
D. NaHCO3
Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc. Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng?
Cho 100 ml dung dịch AlCl3 1M tác dụng với 200 ml dung dịch NaOH. Kết tủa tạo thành được làm khô và nung đến khối lượng không đổi cân nặng 2,55 gam. Tính nồng độ mol của dung dịch NaOH ban đầu.
Có 4 mẫu kim loại là Na, Al, Ca, Fe. Chỉ dùng nước làm thuốc thử thì số kim loại có thể phân biệt được tối đa là bao nhiêu?
A. 1.
B. 2.
C. 3.
D. 4.
Điện phân Al2O3 nóng chảy với dòng điện cường độ 9,65 A trong khoảng thời gian 3000 giây, thu được 2,16 gam Al. Hiệu suất của quá trình điện phân là:
A. 60%.
B. 70%.
C. 80%.
D. 90%.
Cho Al + HNO3 → Al(NO3)3 + NO + H2O, số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat trong phản ứng là:
A. 1 và 3
B. 3 và 2
C. 4 và 3
D. 3 và 4
Một pin điện hóa được cấu tạo bởi các cặp oxi hóa - khử Al3+/Al và Cu2+/Cu. Phản ứng hóa học xảy ra khi pin hoạt động là:
A. 2Al + 3Cu → 2Al3+ + 2Cu2+
B. 2Al3+ + 2Cu → 2Al + 3Cu2+
C. 2Al + 3Cu2+ → 2Al3+ + 3Cu
D. 2Al3+ + 3Cu2+ → 2Al3+ + 3Cu2+
Tùy thuộc nồng độ của dung dịch HNO3 kim loại nhôm có thể khử HNO3 thành NO2, NO, N2 hoặc NH4NO3. Hãy viết phương trình hóa học của các phản ứng trên.
Có 4 kim loại là: Ca, Na, Fe và Al. Hãy nhận biết mỗi kim loại bằng phương pháp hóa học và dẫn ra những phản ứng hóa học đã dùng.
Khử hoàn toàn 16 gam bột Fe2O3 bằng bột nhôm. Hãy cho biết:
a. Khối lượng bột nhôm cần dùng.
b. Khối lượng của những chất sau phản ứng.
Sản xuất nhôm bằng phương pháp điện phân nhôm oxit nóng chảy. Hãy tính khối lượng Al2O3 và than chì (C) cần dùng để sản xuất được 5,4 tấn nhôm. Cho rằng toàn bộ lượng khí oxi sinh ra ở cực dương đã đốt cháy than chì thành cacbon đioxit.
Hợp chất nào của nhôm tác dụng với dung dịch NaOH (theo tỉ lệ mol 1:1) có sản phẩm là Na[Al(OH)4]?
A. Al2(SO4)3
B. AlCl3
C. Al(NO3)3
D. Al(OH)3
Dãy nào dưới đây gồm các chất vừa tác dụng được với dung dịch axit và dung dịch kiềm?
A. AlCl3 và Al2(SO4)3
B. Al(NO3)3 và Al(OH)3
C. Al2(SO4)3 và Al2O3
D. Al(OH)3 và Al2O3
Có 3 chất rắn là: Mg, Al2O3, Al. Hãy nhận biết mỗi chất đã cho bằng phương pháp hóa học. Viết các phương trình hóa học.
Viết các phương trình hóa học biểu diễn những chuyển đổi hóa học sau, ghi rõ các điều kiện của phản ứng và cho biết phản ứng nào thuộc loại phản ứng oxi hóa khử:
Có các dung dịch AlCl3, HCl, NaOH, H2O và những dụng cụ cần thiết. Hãy điều chế và chứng minh tính lưỡng tính của Al2O3 và Al(OH)3. Viết các phương trình hóa học.
Cho 31,2 gam hỗn hợp bột Al và Al2O3 tác dụng với dung dịch NaOH dư, phản ứng xong thu được 13,44 lít H2 (đktc). Hãy cho biết:
a. Các phương trình hóa học của các phản ứng đã xảy ra?
b. Khối lượng mỗi chất có trong hỗn hợp ban đầu?
c. Thể tích dung dịch NaOH 4M đã dùng (biết rằng trong thí nghiệm này người ta đã dùng dư 10 cm3 so với thể tích cần dùng).
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
.png)
Giá trị của V gần nhất với giá trị nào sau đây?
A. 1,7
B. 2,1
C. 2,4
D. 2,5
Câu trả lời của bạn
Đáp án B
Câu trả lời của bạn
Câu trả lời của bạn
Al → Al2(SO4)3 → AlCl3 → Al(OH)3 → Al2O3
Câu trả lời của bạn
(1) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
(2) Al2(SO4)3 + 3BaCl2 → 2AlCl3 + 3BaSO4
(3) AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
(4) 2Al(OH)3 → Al2O3 + 3H2O
Câu trả lời của bạn
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Al2(SO4)3 + 6NaOH → 2Al(OH)3 + 3 Na2SO4
2Al(OH)3 → Al2O3 + 3H2O
Al2O3 + 6HCl → 2AlCl3 + 3H2O

Câu trả lời của bạn
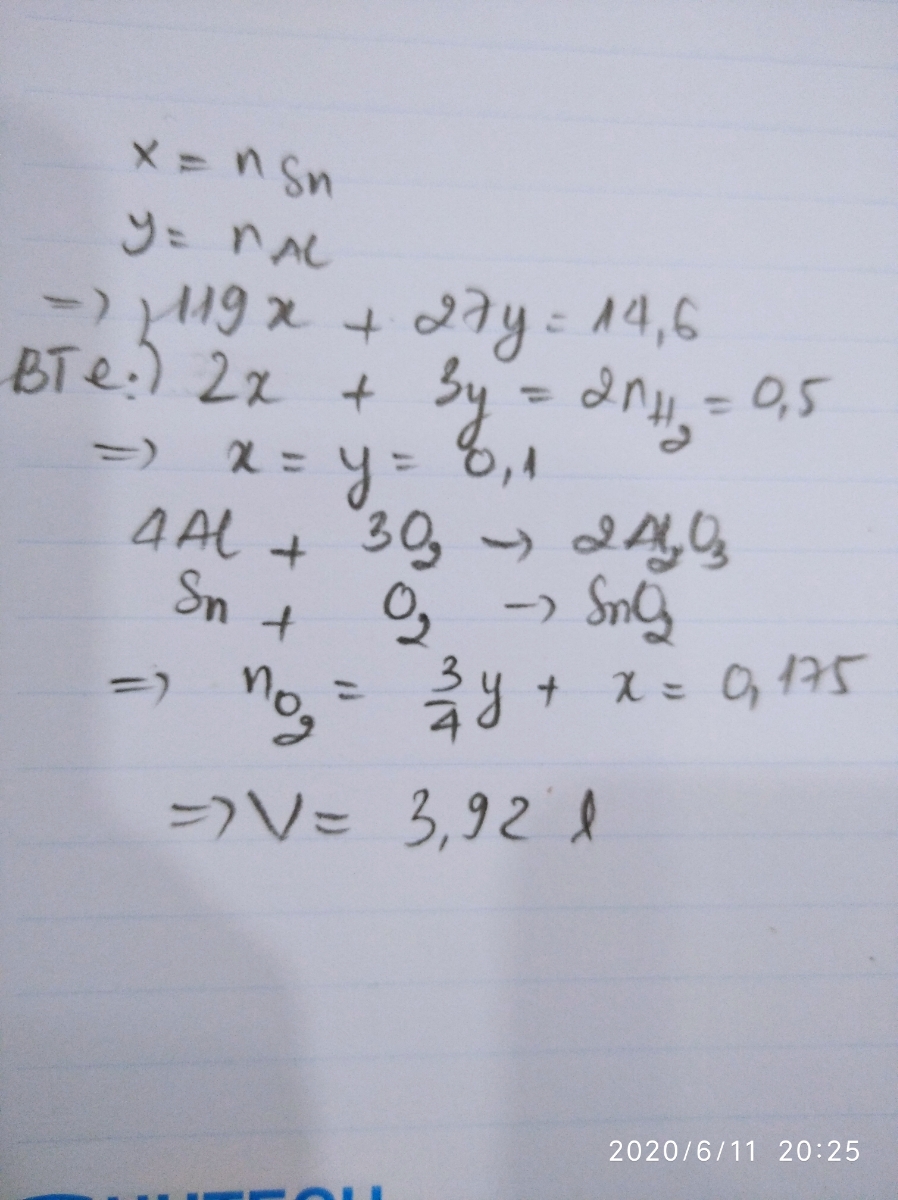
Câu trả lời của bạn
Số mol Al3+ = 0,12 mol.
Số mol Al(OH)2 = 0,02 mol < số mol Al3+ nên có 2 trường hợp xảy ra.
+ TH1: Al3+ dư → Chỉ tạo Al(OH)3 nên số mol OH- = 3 . 0,02 = 0,06 mol.
→ CM(NaOH) = 0,12M
+ TH2: Al3+ hết → tạo
Al(OH)3 : 0,02 mol và [Al(OH)4]- : 0,12 - 0,02 = 0,1 mol
→ Số mol OH- = 3 . 0,02 + 4 . 0,1 = 0,46 mol
→ CM(NaOH) = 0,92M
Câu trả lời của bạn
Tổng nOH- = 0,6 + 0,9 + 1,2 = 2,7 mol
nAl(OH)3 = 0,5
Số mol OH- trong kết tủa là 1,5 mol < 2,7 mol → có tạo [Al(OH)4]-
n[Al(OH)4]- =[nOH- - 3nAl(OH)3] : 4 = 0,3 mol
nAl3+ = nAl(OH)3 + n[Al(OH)4]- = 0,8 mol
Câu trả lời của bạn
Vì lượng OH- ở 2 thí nghiệm khác nhau mà lượng kết tủa không thay đổi nên:
TN1: Al3+ dư, OH- hết.
Số mol OH- = 0,6 mol → nAl(OH)3 = nOH-/3 = 0,2 mol → m = 15,6 g
TN2: Al3+ và OH- đều hết và có hiện tượng hoà tan kết tủa.
Số mol OH- = 0,9 mol → Tạo Al(OH)3 = 0,2 mol và [Al(OH)4]- = 0,075 mol
→ Tổng nAl3+ = 0,2 + 0,075 = 0,275 mol
Số mol Al2(SO4)3 = 0,1375 mol = a.
A. 2,65 lít
B. 2,24 lít
C. 1,12 lít
D. 3,2 lít
Câu trả lời của bạn
Đáp án A
Số mol Al3+ = 0,34 mol.
Số mol Al(OH)3 = 0,3 mol < số mol Al3+ nên có 2 trường hợp xảy ra.
+ TH1: Al3+ dư → Chỉ tạo Al(OH)3 nên số mol OH- = 3 . 0,3 = 0,9 mol.
→ V(dd NaOH) = 2,25 lít = Vmin
+ TH2: Al3+ hết → tạo Al(OH)3 = 0,3 mol và [Al(OH)4]- = 0,34 - 0,3 = 0,04 mol
→ Số mol OH- = 3 . 0,3 + 4 . 0,04 = 1,06 mol
→ V(dd NaOH) = 2,65 lít = Vmax.
A. 0,8M
B. 1,2M
C. 1M
D. 0,75M
Câu trả lời của bạn
Đáp án C
Ta có: nNaOH = 7.0,15 = 1,05 mol; nAl2(SO4)3 = 1.0,1 = 0,1 mol
Al2(SO4)3 + 6NaOH → 2Al(OH)3 + 3Na2SO4
0,1 0,6 0,2 0,3
Vì NaOH dư nên:
Al(OH)3 + NaOH → Na[Al(OH)4]
Sau phản ứng có 0,2 mol Na[Al(OH)4] và 0,25 mol NaOH dư.
Nồng độ mol của Na[Al(OH)4] = 0,2/(0,15 + 0,1) = 0,8M
[NaOH] = 0,25 : (0,15 + 0,1) = 1M
A. 0,2
B. 0,15
C. 0,1
D. 0,05
Câu trả lời của bạn
D. 0,05
Đáp án: C
Ta có: nOH- = nNaOH = 0,7 mol
nAl3+ = 2.0,1 = 0,2 mol
Al3+ + 3OH- → Al(OH)3
0,2 0,6 0,2
→ nOH- dư = 0,7 - 0,6 = 0,1 mol
Al(OH)3 + OH- → AlO2- + 2H2O
0,1 0,1
→ nAl(OH)3 còn = 0,2 - 0,1 = 0,1 mol
A. 0,75 M
B. 1,75M
C. 1M
D. 1,25M
Câu trả lời của bạn
B. 1,75M
Đáp án B
Số mol AlCl3 là nAlCl3 = 0,1.1 = 0,1 (mol)
Số mol Al2O3 là nAl2O3 = 2,55/102 = 0,025 (mol)
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl (1)
0,1 0,3 0,1
Al(OH)3 + NaOH → Na[Al(OH)4] + 2H2O
0,05 0,05
2Al(OH)3 → Al2O3 + H2O
0,05 0,025
Theo pt (3) ta thấy số mol Al(OH)3 còn lại là 0,05 mol
Như vậy đã có: 0,1 - 0,05 = 0,05 mol Al(OH)3 đã bị hòa tan.
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
Nồng độ mol/l CM(NaOH) = 0,35/0,2 = 1,75M
A. 0,3 và 0,6
B. 0,3 và 0,7
C. 0,4 và 0,8
D. 0,3 và 0,5
Câu trả lời của bạn
C. 0,4 và 0,8
Đáp án D
nBa(OH)2 = 0,5V → nOH- = 1V (mol)
nAl3+ = nAl(NO3)3 = 0,75.0,2 = 0,15 (mol)
nAl(OH)3 = 7,8/78 = 0,1 mol
Trường hợp 1: lượng OH- chỉ đủ tạo 0,1 mol kết tủa:
nOH- = 3.nAl(OH)3 = 0,3 mol
V = 0,3 (l)
Trường hợp 2: lượng OH- dư, hòa tan một phần kết tủa
Al3+ + 3OH- → Al(OH)3
0,15 0,45 0,15
Al(OH)3 + OH- → AlO2- + 2H2O
0,05 0,05
Tổng nOH- = 0,45 + 0,05 = 0,5 mol → V = 0,5 lít
* Cách khác áp dụng nhanh công thức cho 2 trường hợp:
nOH- = 3n kết tủa và nOH- = 4.nAl3+ - n kết tủa
→ nOH- = 3.0,1 = 0,3 mol và nOH- = 4.0,15 - 0,1 = 0,5 mol
→ V = 0,3 lít và V = 0,56 lít
A. 0,22 lít
B. 0.2 lít
C. 0,15 lít
D. 0,12 lít
Câu trả lời của bạn
A. 0,22 lít
Đáp án A
Số mol Al = 0,81/27 = 0,03 (mol); số mol HCl = 0,55.0,2 = 0,11 (mol)
2Al + 6HCl → 2AlCl3 + 3H2
0,03 0,09 0,03 0,045
Dung dịch A thu được gồm AlCl3 = 0,03 mol; HCl = 0,11 - 0,09 = 0,02 mol.
Để có lượng kết tủa lớn nhất:
HCl + NaOH → NaCl + H2O
0,02 0,02
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
0,03 0,09 0,03
Thể tích dung dịch NaOH cần dùng = (0,02+0,09)/0,5 = 0,22 (lít)
A. 1,2
B. 1,8
C. 2,4
D. 2
Câu trả lời của bạn
C. 2,4
Đáp án D
Ta có: nAlCl3 = 1,5.0,2 = 0,3 mol; nAl(OH)3 = 15,6/78 = 0,2 mol
Thể tích NaOH lớn nhất khi kết tủa sinh ra cực đại, bị NaOH hòa tan 1 phần còn 15,6 (g).
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
0,3 0,9 0,3
Al(OH)3 + NaOH → NaAlO2 + 2H2O
(0,3-0,2) 0,1
Theo phương trình phản ứng, ta có: nNaOH = 0,9 + 0,1 = 1 mol
→ VNaOH = 1/0,5 = 2 lít
A. 10,8
B. 5,4
C. 7,8
D. 43,2
Câu trả lời của bạn
B. 5,4
Đáp án B
Ta có: nH2 = 0,896/22,4 = 0,04 mol
Gọi: nAl = x mol → nAl = 2x mol
Phản ứng:
2Na + 2H2O → 2NaOH + H2 (1)
x x x/2
Al + NaOH + H2O → NaAlO2 + 3/2H2 (2)
x x 3x/2
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1), (2)
Tổng nH2 = x/2 + 3x/2 = 0,4 → x = 0,2 mol
→ mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol → nAl dư = 0,4 - 0,2 = 0,2 mol
→ mAl = 0,2.27 = 5,4 (g)
A. 0,224 lít
B. 2,24 lít
C. 6,72 lít
D. 0,672 lít
Câu trả lời của bạn
C
c
C. 6,72 lít
Ta có: nAl = 0,03 (mol)
Các phương trình phản ứng:
2Al + Fe2O3 → Al2O3 + 2Fe (1)
2Al + 3CuO → Al2O3 + 3Cu (2)
Gọi số mol Al tham gia phản ứng (1) là x, tham gia phản ứng (2) là y.
Theo (1): nFe = nAl = x (mol)
Theo (2): nCu = 3/2 nAl = 3/2.y (mol)
Fe + 4HNO3 loãng → Fe(NO3)2 + NO + 2H2O (3)
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO + 4H2O (4)
Theo (3): nNO/(3) = nFe = x (mol).
Theo (4): nNO/(4) = 2/3 .nCu = 2/3 .x. 3/2 .x .y = y(mol)
⇒ nNO = x + y = 0,03 (mol) ⇒ VNO = 0,03 x 22,4 = 0,672 (lit).
A. 1,08g
B. 1,62g
C. 2,1g
D. 5,1g
Câu trả lời của bạn
Đáp án: D. 5,1g
8Al + 3Fe3O4 tº→ 9Fe + 4Al2O3
Khối lượng nhôm tăng chính là khối lượng của nguyên tố oxi.
nO (trong Al2O3) = 0,96/16 = 0,06 mol
nAl2O3 = 1/3 n O= 0,06/3 = 0,02 mol
Theo phản ứng: nFe = 9/4 .nAl2O3 = 9/4.0,02 = 0,045 mol
Hỗn hợp A sau phản ứng tác dụng với NaOH dư tạo ra khí H2. Chứng tỏ sau phản ứng nhiệt nhôm, nhôm còn dư:
Ta có: nH2 = 0,672/22,4 = 0,03 mol
Al + NaOH + H2O → NaAlO2 + 3/2H2
0,02 0,03
Vậy: mA = mAl dư + mAl2O3 = 0,02.27 + 0,045.56 + 0,02.102 = 5,1 (g)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *