Nội dung bài học đem đến phần kiến thức mới và thú vị trong mảng Thí nghiệm hóa học, đó chính là nguyên tắc chung và phương pháp nhận biết một số chất khí như khí CO2, SO2, H2S, NH3.
Để nhận biết một chất khí người ta dựa vào tính chất vật lí và tính chất hóa học đặc trưng của nó
| Khí | Thuốc thử | Hiện tượng | Giải thích |
| CO2 không màu, không mùi | Ba(OH)2 dư | Kết tủa trắng | tạo kết tủa BaCO3 |
| SO2 không màu, mùi hắc | Nước Brom | Làm mất màu nước Brom | SO2 + Br2+ H2O → HCl + H2SO4 |
| H2S mùi trứng thối | Cu2+ hoặc Pb2+ | Kết tủa màu đen | CuS, PbS |
| NH3 mùi khai | Giấy quỳ ẩm | Giấy quỳ tím chuyển thành màu xanh | dung dịch có tính bazơ |
Thuốc thử nào sau đây dùng để phân biệt 2 khí H2S và SO2?
Nước Brom là thuốc thử để nhận biết hai khí.
Phản ứng làm mất màu nước Brom: SO2 + Br2+ H2O → HCl + H2SO4 ⇒ Ta nhận biết được Khí SO2
Chất còn lại là khí H2S
Cho biết các pư sau có xảy ra không?Nếu có hãy trình bày hiện tượng ?
Hướng dẫn:
TN1: FeS tan, có khí không màu mùi trứng thối thoát ra FeS + 2H+ → Fe2+ + H2S
TN2: Không hiện tượng vì CuS, PbS, Ag2S không tan trong dd axit HCl, H2SO4 loãng
TN3: Đều xuất hiện kết tủa đen
Pb2+ + H2S → PbS + 2H+
Cu2+ + H2S → CuS + 2H+
2Ag+ + H2S → Ag2S + 2H+
TN4: Dd Br2 bị nhạt màu
H2S + 4Br2 + 4H2O → H2SO4 + 8HBr
Sau bài học cần nắm: phương pháp nhận biết một số chất khí như khí CO2, SO2, H2S, NH3.
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 41có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Nhận biết khí SO2 ta dùng dung dịch nước Br2 dư hiện tượng xảy ra là:
Khí H2S là khí :
Cách nhận biết khí Amoniac là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 41.
Bài tập 1 trang 177 SGK Hóa học 12
Bài tập 2 trang 177 SGK Hóa học 12
Bài tập 3 trang 177 SGK Hóa học 12
Bài tập 1 trang 239 SGK Hóa 12 Nâng cao
Bài tập 2 trang 239 SGK Hóa học 12 nâng cao
Bài tập 3 trang 239 SGK Hóa học 12 nâng cao
Bài tập 4 trang 239 SGK Hóa 12 Nâng cao
Bài tập 41.1 trang 96 SBT Hóa học 12
Bài tập 41.2 trang 96 SBT Hóa học 12
Bài tập 41.3 trang 96 SBT Hóa học 12
Bài tập 41.4 trang 96 SBT Hóa học 12
Bài tập 41.5 trang 96 SBT Hóa học 12
Bài tập 41.6 trang 96 SBT Hóa học 12
Bài tập 41.7 trang 97 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Nhận biết khí SO2 ta dùng dung dịch nước Br2 dư hiện tượng xảy ra là:
Khí H2S là khí :
Cách nhận biết khí Amoniac là:
Khi nhận biết CO2 bằng dung dịch Ba(OH)2 ta quan sát thấy hiện tượng gì?
Kết tủa CuS, PbS có màu gì?
Khí CO2 có lẫn tạp chất là khí HCl. Để loại tạp chất HCl đó nên cho khí CO2 đi qua dung dịch nào sau đây là tốt nhất?
Dung dịch NaOH dư
Dung dịch Na2CO3 dư
Dung dịch NaHCO3 dư
Có 3 khí SO2; CO2; H2S. Chỉ dùng một hóa chất nào sau đây để phân biệt được cả 3 khí trên?
Dung dịch Ca(OH)2
Dung dịch Ba(OH)2
Dung dịch Br2
Khí CO2 có lần tạp chất là khí HCl. Để loại trừ tạp chất HCl đó nên cho khí CO2 đi qua dung dịch nào sau đây tốt nhất?
Dung dịch NaOH dư.
Dung dịch NaHCO3 bão hòa dư.
Dung dịch Na2CO3 dư.
Thuốc thử dùng để phân biệt FeS và FeCO3 là:
Thuốc thử dùng để phân biệt Na2SO4 và Na2SO3 là:
Có thể dùng nước vôi trong để phân biệt 2 khí CO2 và SO2 được không? Tại sao?
Cho 2 bình riêng biệt đựng các khí CO2 và SO2. Hãy trình bày cách nhận biết từng chất. Viết phương trình hóa học.
Có các lọ hóa chất không nhãn, mỗi lọ đựng một trong các dung dịch không màu sau: Na2SO4, Na2S,Na2CO3, Na3PO4, Na2SO3. Chỉ dùng thuốc thử là dung dịch H2SO4 loãng nhỏ trực tiếp vào từng dung dịch thì có thể nhận biết được các dung dịch:
A. Na2CO3, Na2S, Na2SO3.
B. Na2CO3, Na2S
C. Na2S, Na2CO3, Na3PO4
D. Na2SO4, Na2S, Na2CO3, Na3PO4, Na2SO3
Khí CO2 có lẫn tạp chất là khí HCl. Để loại trừ tạp chất HCl đó nên cho khí CO2 đi qua dung dịch nào sau đây là tốt nhất?
A. Dung dịch NaOH dư.
B. Dung dịch NaHCO3 bão hoà dư.
C. Dung dịch Na2CO3 dư.
D. Dung dịch AgNO3 dư.
Có thể dùng dung dịch nước vôi trong để phân biệt hai khí CO2 và SO2 được không? Tại sao?
Cho hỗn hợp 2 khí CO2 và SO2. Hãy trình bày cách tách đồng thời nhận biết sự có mặt từng khí trong hỗn hợp đó. Viết các phương trình hóa học.
Chọn thuốc thử thích hợp để phân biệt các cặp chất sau đây.
a) FeS và FeCO3.
b) Na2SO4 và Na2SO3.
Không thể nhận biết các khí CO2, SO2 và O2 đựng trong các bình riêng biệt nếu chỉ dùng
A. nước brom và tàn đóm cháy dở.
B. nước brom và dung dịch Ba(OH)2.
C. nước vôi trong và nước brom.
D. tàn đóm cháy dở và nước vôi trong.
Để phân biệt các khí CO, CO2, O2 và SO2 có thể dùng
A. tàn đóm cháy dở, nước vôi trong và nước brom.
B. tàn đóm cháy dở, nước vôi trong và dung dịch K2CO3.
C. dung dịch Na2CO3 và nước brom.
D. tàn đóm cháy dở và nước brom.
Phòng thí nghiệm bị ô nhiễm bởi khí clo. Dùng chất nào sau đây có thể khử được clo một cách tương đối an toàn ?
A. Dung dịch NaOH loãng
B. Dùng khí NH3 hoặc dung dịch NH3
C. Dùng khí H2S
D. Dùng khí CO2
Trình bày phương pháp hoá học phân biệt các khí: O2, O3, NH3, HCl và H2S đựng trong các bình riêng biệt.
Để khử khí H2S trong phòng thí nghiệm có thể dùng chất nào ?
Khí X điều chế từ H2 và Cl2; khí Y điều chế bằng cách nung nóng KMnO4; khí Z sinh ra do phản ứng của Na2SO3 với axit HCl; khí A sinh ra khi nung đá vôi; khí B thu được khi cho Fe tác dụng với dung dịch H2SO4 loãng. Trình bày phương pháp hoá học phân biệt các khí đựng trong các bình riêng biệt.
Trong quá trình sản xuất NH3 thu được hỗn hợp gồm ba khí: H2, N2 và NH3. Trình bày phương pháp hoá học để chứng tỏ sự có mặt của mỗi khí trong hỗn hợp.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
NH3: quỳ tím hóa xanh
HCl: quỳ tím hóa đỏ
Cl2: quỳ tím hóa đỏ sau mất màu
N2 quỳ tím không đổi màu.
Câu trả lời của bạn
Khi cho Ba(OH)2 vào 4 dung dịch: NH4Cl: ↑ mùi khai NH3;
NH4HCO3: có ↓CaCO3 và ↑ mùi khai NH3;
NaNO3: không hiện tượng;
MgCl2: ↓ trắng Mg(OH)2
Câu trả lời của bạn
Khi cho Ca(OH)2 vào 4 dung dịch:
NH4Cl: ↑ mùi khai NH3
NaCl: không hiện tượng
Mg(NO3)2: ↓ trắng Mg(OH)2
Al(NO3)3: ↓ trắng Al(OH)3 sau kết tủa tan Ba(AlO2)2
(NH4)2CO3: có ↓BaCO3 và ↑ mùi khai NH3
Câu trả lời của bạn
T = 2,75 tạo 2 muối: Na2HPO4 (x mol) và Na3PO4 (y mol)
2x + 3y = 1,1 (1)
và x + y = 0,4 (2)
→ x = 0,1 và y = 0,3.
Câu trả lời của bạn
SO2 (nâu) + Br2 + 2H2O → 2HBr (không màu) + H2SO4
H2S + Br2 → 2HBr + S↑ (vàng)
Câu trả lời của bạn
Các chất đó là: 1, 3, 4, 6, 7
Câu trả lời của bạn
Vì NaHCO3 vừa loại được HCl lại tạo ra được một lượng CO2 mới.
NaHCO3 + HCl → NaCl + CO2↑ + H2O
Câu trả lời của bạn
SO2 và SO3 làm quỳ tím ẩm hóa đỏ.
CH3NH2 và NH3 làm quỳ tím hóa xanh.
N2 không làm đổi màu quỳ tím.
Câu trả lời của bạn
H2S tạo kết tủa đen với CuCl2.
H2S + CuCl2 → CuS + 2HCl
Câu trả lời của bạn
H2S tạo kết tủa đen với CuCl2.
H2S + CuCl2 → CuS + 2HCl
Câu trả lời của bạn
Cho hỗn hợp đi qua dung dịch Br2, các chất C2H2, C2H4, but-1,3-đien do có phản ứng với dung dịch Br2
Còn lại CH3NH2 và C2H6 đi ra khỏi dung dịch, dẫn hỗn hợp này qua dung dịch HCl. CH3NH2 bị giữ lại do phản ứng với HCl, còn lại ta thu được C2H6 tinh khiết
Câu trả lời của bạn
H2S tạo kết tủa đen với CuCl2.
H2S + CuCl2 → CuS + 2HCl
Câu trả lời của bạn
Dùng BaCl2 có hiện tượng:
+ Xuất hiện kết tủa trắng gồm các khí: CO2; SO3; SO2
+ Không hiện tượng: N2
Dùng dung dịch Br2 để nhận biết các khí: CO2; SO3; SO2
+ SO2 làm mất màu dung dịch brom
+ CO2; SO3 không hiện tượng
Dùng Ca(OH)2 để nhận biết CO2; SO3
+ Xuất hiện kết tủa trắng: CO2
+ Không hiện tượng: SO3
Câu trả lời của bạn
F2 phản ứng với nước tạo O2 → bốc cháy
Câu trả lời của bạn
SO2, SO3: làm quỳ tím ẩm chuyển màu đỏ
CH3NH2 và NH3: làm quỳ tím hóa xanh
N2: không hiện tượng
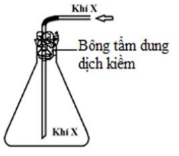
Trong các khí: N2, Cl2, SO2, NO2, số chất thoả mãn điều kiện bài toán?
Câu trả lời của bạn
Khí X thu bằng cách dời không khí, ngửa bình nên khí X có M > 29
→ Khí X là Cl2, SO2, NO2.
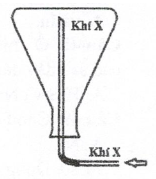
Khí X được tạo ra từ phản ứng hóa học nào sau đây?
Câu trả lời của bạn
- Với khí nhẹ hơn không khí → thu khí bằng cách đặt ngược bình.
- Với khí nặng hơn không khí → thu khí bằng cách đặt xuôi bình.
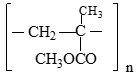
Trong thí nghiệm, xẩy ra phản ứng hóa học nào sau đây?
Câu trả lời của bạn
heo sơ đồ thí nghiệm thì phản ứng tạo ra Y phải đun nóng, chất Y sinh ra ở dạng hơi, được làm lạnh trong ống sinh hàn, Phản ứng phù hợp:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O.
Câu trả lời của bạn
Fe, Al tan trong dung dịch HCl, Au không tan trong dung dịch HCl sục khí O2 dư Cu thỏa mãn.
- Ytác dụng với Z thì có tủa xuất hiện
- X tác dụng với Z thì có khí thoát ra .
X, Y, Z, lần lượt là
Câu trả lời của bạn
X tác dụng với Y thì có kết tủa xuất hiện
→ loại D vì: NaHCO3 + NaHSO4 không có kết tủa. X tác dụng với Z thì có khí thoát ra
→ loại A và B vì không tạo khí.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *