Nội dung bài luyện tập Tính chất của Tính chất của kim loại kiềm, kim loại kiềm thổ là bài tổng ôn, củng cố các kiến thức đã học về Tính chất của kim loại kiềm, kim loại kiềm thổ. Ngoài ra còn rèn luyện cho các em học sinh kĩ năng giải các bài tập và các dạng toán quan trọng.
| Vị trí trong Bảng tuần hoàn | Cấu hình electron lớp ngoài cùng | Tính chất hóa học đặc trưng | Điều chế | |
| Kim loại kiềm | Nhóm IA | ns1 | Có tính khử mạnh nhất trong các kim loại \(M\rightarrow M^{+} + e\) | Điện phân muối halogen nóng chảy \(2MX\overset{dpnc}{\rightarrow}2M+X_{2}\) |
| Kim loại kiềm thổ | Nhóm IIA | ns2 | Có tính khử mạnh chỉ sau kim loại kiềm \(M\rightarrow M^{2+}+2e\) | \(MX_{2}\overset{dpnc}{\rightarrow}M+X_{2}\) |
Hỗn hợp rắn A gồm Ca(HCO3); CaCO3; NaHCO3; Na2CO3. Nung A đến khối lượng không đổi được chất rắn B gồm:
Các muối hidrocacbonat của kim loại kiềm và kiềm thổ đều bị phân hủy tạo muối cacbonat khi ở nhiệt độ không quá cao, tuy nhiên chỉ có muối cacbonat của kim loại kiềm thổ mới bị thủy phân ở nhiệt độ cao tạo oxit kim loại.
⇒ Nhiệt phân hỗn hợp ban đầu sẽ thu được: CaO; Na2CO3.
Cho các chất: Na2CO3; NaHCO3; NaHSO4; HCl; BaCl2; CuO; Fe. Số cặp chất có thể tác dụng trực tiếp với nhau ở nhiệt độ thường là:
Các cặp chất: (Na2CO3 + NaHSO4); (Na2CO3 + HCl); (Na2CO3 + BaCl2); (NaHCO3 + NaHSO4); (NaHCO3 + HCl); (NaHSO4 + BaCl2); (NaHSO4 + CuO); (NaHSO4 + Fe); (HCl + CuO); (HCl + Fe).
Hoà tan hoàn toàn 14,52 gam hỗn hợp X gồm NaHCO3, KHCO3 và MgCO3 bằng dd HCl dư, thu được 3,36 lít khí CO2 (đktc) và dd chứa m gam muối KCl. Giá trị của m là:
Coi hỗn hợp gồm KHCO3 và MgCO3 có số mol lần lượt là x và y (vì \(M_{NaHCO_{3}}= M_{MgCO_{3}}\))
\(\\ n_{CO_{2}}= 0,15 \ mol \Rightarrow x + y = 0,15 \\ 100x + 84y = 14,52 \\ \Rightarrow x = 0,12 ; \ y = 0,03 \\ \Rightarrow m = 0,12 . (39 + 35,5) = 8,94 \ g\)
Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2, thu được m gam kết tủa. Giá trị của m là:
Dạng toán CO2 tác dụng với hỗn hợp bazơ của kim loại nhóm kiềm – kiềm thổ.
\(\begin{array}{l} {n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15(mol)\\ {n_{O{H^ - }}} = {n_{NaOH}} + 2.{n_{Ba{{(OH)}_2}}} = 0,15 + 2.0,1 = 0,25(mol) \end{array}\)
Vì:\({n_{C{O_2}}} < {n_{O{H^ - }}} < 2{n_{C{O_2}}} \Rightarrow {n_{C{O_3}^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}}\)
\({n_{HC{O_3}^ - }} = {n_{C{O_2}}} - {n_{C{O_3}^{2 - }}}\)
\(\Rightarrow {n_{C{O_3}^{2 - }}} = 0,15mol\); có \({n_{Ba{{\left( {OH} \right)}_2}}} = 0,1mol\)
\({n_{BaC{{\rm{O}}_3}}} = 0,1mol\)
Vậy \({m_{BaC{O_3}}} = 19,700g\)
Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 131,4 gam X vào nước, thu được 6,72 lít khí H2 (đktc) và dung dịch Y, trong đó có 123,12 gam Ba(OH)2. Hấp thụ hoàn toàn 40,32 lít khí CO2 (đktc) vào Y, thu được m gam kết tủa. Giá trị của m là:
Quy hỗn hợp X về Ba, Na và O.
\({{\rm{n}}_{{\rm{Ba}}}}{\rm{ = }}{{\rm{n}}_{{\rm{Ba(OH}}{{\rm{)}}_{\rm{2}}}}}{\rm{ = 0,72 mol; }}{{\rm{n}}_{{{\rm{H}}_{\rm{2}}}}}{\rm{ = 0,3 mol}}\)
Đặt nNa = x (mol) , nO = y (mol)
BTKL: mNa + mO = mX - mBa ⇔ 23x + 16y = 32,76 (1)
BT electron: ne nhường = ne nhận
(ở đây Na, Ba nhường e, O nhận e về O2-, H+ nhận e thành H2 bay lên)
⇔ x + 2 .0,72 = 2y + 0,3. 2 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ \begin{array}{l} 23x{\rm{ }} + {\rm{ }}16y{\rm{ }} = {\rm{ }}32,76\;\;\\ x{\rm{ - 2y }} = - 0,84 \end{array} \right. \Leftrightarrow \left\{ \begin{array}{l} x = 0,84\\ y = 0,84 \end{array} \right.\)
⇒ nOH- = nNa + 2nBa = 2,28 mol
\(n_{CO_2}=1,8\ mol\)
\(\Rightarrow n_{{CO_3}^{2-}}=0,48\ mol,\ n_{{HCO_3}^-}=1,32\ mol\)
\(\Rightarrow n_{BaCO_3}=0,48\ mol \Rightarrow m_{BaCO_3}=94,56\ g\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 28có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
Dung dịch nào dưới đây dùng để phân biệt dung dịch KCl với dung dịch K2SO4?
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
Cho các chất: (1) NaCl; (2) Na2CO3; (3) BaCl2; (4) Ca(OH)2; (5) Na3PO4; (6) Na2SO4. Những chất có thể làm mềm nước cứng tạm thời là:
Phát biểu nào sau đây không đúng?
Để phân biệt dung dịch CaCl2 với dung dịch NaCl, người ta dùng dung dịch:
Cho các phản ứng xảy ra theo sơ đồ sau:
X1 + H2O 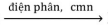 X2 + X3 + H2↑
X2 + X3 + H2↑
X2 + X4 → BaCO3↓ + K2CO3 + H2O
Chất X1, X4 lần lượt là:
Câu 8-20: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 28.
Bài tập 1 trang 132 SGK Hóa học 12
Bài tập 2 trang 132 SGK Hóa học 12
Bài tập 3 trang 132 SGK Hóa học 12
Bài tập 4 trang 132 SGK Hóa học 12
Bài tập 5 trang 132 SGK Hóa học 12
Bài tập 6 trang 132 SGK Hóa học 12
Bài tập 1 trang 170 SGK Hóa 12 Nâng cao
Bài tập 2 trang 170 SGK Hóa 12 Nâng cao
Bài tập 3 trang 170 SGK Hóa 12 Nâng cao
Bài tập 28.1 trang 65 SBT Hóa học 12
Bài tập 28.2 trang 65 SBT Hóa học 12
Bài tập 28.3 trang 66 SBT Hóa học 12
Bài tập 28.4 trang 66 SBT Hóa học 12
Bài tập 28.5 trang 66 SBT Hóa học 12
Bài tập 28.6 trang 66 SBT Hóa học 12
Bài tập 28.7 trang 66 SBT Hóa học 12
Bài tập 28.8 trang 66 SBT Hóa học 12
Bài tập 28.9 trang 67SBT Hóa học 12
Bài tập 28.10 trang 67 SBT Hóa học 12
Bài tập 28.11 trang 67 SBT Hóa học 12
Bài tập 28.12 trang 67 SBT Hóa học 12
Bài tập 28.13 trang 67 SBT Hóa học 12
Bài tập 28.14 trang 67 SBT Hóa học 12
Bài tập 28.15 trang 67 SBT Hóa học 12
Bài tập 28.16 trang 68 SBT Hóa học 12
Bài tập 28.17 trang 68 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
Dung dịch nào dưới đây dùng để phân biệt dung dịch KCl với dung dịch K2SO4?
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
Cho các chất: (1) NaCl; (2) Na2CO3; (3) BaCl2; (4) Ca(OH)2; (5) Na3PO4; (6) Na2SO4. Những chất có thể làm mềm nước cứng tạm thời là:
Phát biểu nào sau đây không đúng?
Để phân biệt dung dịch CaCl2 với dung dịch NaCl, người ta dùng dung dịch:
Cho các phản ứng xảy ra theo sơ đồ sau:
X1 + H2O 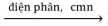 X2 + X3 + H2↑
X2 + X3 + H2↑
X2 + X4 → BaCO3↓ + K2CO3 + H2O
Chất X1, X4 lần lượt là:
Cho dãy kim loại: Na, Ba, Al, K, Mg. Số kim loại trong dãy phản ứng với lượng dư dung dịch FeCl3 có tạo kết tủa là:
Kim loại nào sau đây khi cho vào dung dịch CuSO4 bị hòa tan hết và phản ứng tạo thành kết tủa gồm 2 chất:
Cho 26 gam hỗn hợp chất rắn A gồm Ca, MgO, Na2O tác dụng hết với dung dịch HCl 1M (vừa đủ) thu được dung dịch A trong đó có 23,4 gam NaCl. Giá trị của V là:
Hấp thu hoàn toàn 4,48 lít khí CO2 (ở đkc) vào 500ml dung dịch hỗn hợp gồm NaOH 0,1M và Ba(OH)2 0,25M, sinh ra m gam kết tủa. Giá trị m là
Cho một mẫu hợp kim Na-Ca-K tác dụng với nước (dư), thu được dung dịch X và 7,84 lít H2 (ở đktc). Thể tích dung dịch axit H2SO4 1,4M cần dùng để trung hoà dung dịch X là:
Hòa tan hoàn toàn hỗn hợp gồm một kim loại hóa trị 1 và oxit kim loại hóa trị 2 vào nước dư. Sau khi phản ứng xong được 500 ml dd X chỉ chứa một chất tan duy nhất và 4,48 lít khí H2 (đktc). Nồng độ mol/l của dung dịch X là:
Hấp thụ hoàn toàn 3,36 lít khí CO2 (điều kiện tiêu chuẩn) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2 thu được m gam kết tủa. Giá trị của m là:
Cho 7,1 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng với lượng dư dung dịch HCl loãng thu được 5,6 lít khí. Hai kim loại X, Y có thể là:
Hòa tan hoàn toàn 8,94 gam hỗn hợp gồm Na, K và Ba vào nước thu được dung dịch X và 2,688 lit khí H2 (đktc) . Dung dịch Y gồm HCl và H2SO4 có tỉ lệ mol tương ứng: 4 : 1. Trung hòa dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
13,7
12,78
18,46
14,62
Hòa tan hỗn hợp Na2CO3, KHCO3, Ba(HCO3)2 (trong đó số mol Na2CO3 và KHCO3 bằng nhau) vào nước lọc thu được dung dịch X và m gam kết tủa Y. Biết X tác dụng vừa đủ 0,16mol NaOH hoặc 0,24mol HCl thì hết khí bay ra. Giá trị m là:
Hấp thụ hoàn toàn 1,568 lít CO2 (đktc) vào 500ml dung dịch NaOH 0,16M thu được dung dịch X. Thêm 250 ml dung dich Y gồm BaCl2 0,16M và Ba(OH)2 a mol/l vào dung dịch X thu được 3,94 gam kết tủa và dung dịch Z. Tính a?
0,02M
0,04M
Cho 2,22 gam hỗn hợp kim loại gồm K, Na và Ba vào nước được 500ml dung dịch X có pH = 13. Cô cạn dung dịch X được m gam chất rắn. m là:
4,02
3,42
Hoà tan 46 gam một hỗn hợp Ba và hai kim loại kiềm A, B thuộc hai chu kì kế tiếp nhau vào nước thu được dung dịch C và 11,2 lít khí (đktc). Nếu thêm 0,18 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng vẫn chưa kết tủa hết Ba. Nếu thêm 0,21 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng còn dư Na2SO4. A và B là:
Trình bày phương pháp điều chế từng kim loại riêng biệt từ hỗn hợp những chất NaCl, Al2O3, MgCO3. Viết các phương trình hoá học.
Một hỗn hợp rắn gồm Ca và CaC2 tác dụng với nước (dư) thu được hỗn hợp khí có tỉ khối đối với H2 là 5. Đế trung hoà dung dịch sau phản ứng, cần dùng 600 ml dung dịch HCl 0,5M. Tính :
a) Khối lượng của hỗn hợp rắn đã dùng ban đầu.
b) Thành phần phần trăm thể tích của hỗn hợp khí
Một bình kín có dung tích 5 lít chứa khí ở áp suất 1,4 atm và 27°c. Đốt cháy 12 g kim loại kiềm thổ trong bình kín trên. Sau phản ứng, nhiệt độ và áp suất trong bình là 136,5°C và 0,903 atm. Biết thể tích bình không đổi, thể tích chất rắn không đáng kể. Xác định kim loại kiềm thổ đem đốt.
Hoà tan 1,04 g muối clorua của kim loại kiềm thổ trong nước thu được dung dịch A. Thêm Na2CO3 dư vào dung dịch A được một kết tủa. Hoà tan kết tủa này trong dung dịch HNO3 được dung dịch B. Thêm H2SO4 dư vào dung dịch B được kết tủa mới có khối lượng 1,165 g. Xác định công thức hoá học của muối clorua kim loại kiềm.
Cho 10,6 g hỗn hợp A gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với 300 ml dung dịch HCl 1M (loãng), thu được dung dịch B và 5,6 lít khí (đktc).Dẫn từ từ khí CO2 vào dung dịch B. Số gam kết tủa cực đại thu được là bao nhiêu.
Hoà tan 0,1 mol phèn nhôm - amoni (NH4)2SO4.Al2(SO4)3.24H2O vào nước được dung dịch X. Cho đến dư dung dịch Ba(OH)2 vào dung dịch X (đun nóng) thì thu được kết tủa Y và khí Z. Xác định khối lượng kết tủa Y và thể tích (đktc) khí Z.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Kim loại Cu và dung dịch \(H_{2}SO_{4}\) loãng
Câu trả lời của bạn
Li và Na
Câu trả lời của bạn
\(\left\{\begin{matrix} Ba\\ Na \end{matrix}\right.\xrightarrow{\left\{\begin{matrix} HCl:0,02\ mol\\ CuCl_2:0,02\ mol \end{matrix}\right.}\left\{\begin{matrix} H_2:\ 0,02\ mol\\ CU(OH)_2:m\ gam \end{matrix}\right.\)
\(\left\{\begin{matrix} 2H^++2e\ \ \ \ \ \ \ \ \longrightarrow H_2\\ mol: 0,02 \ \ \ \ \ \ \ \ \ \ \rightarrow 0,01\\ 2H_2O+2e\ \longrightarrow 2OH^-\ \ \ \ \ \ +\ \ \ \ \ \ H_2\\ mol: \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ 0,02\ \ \gets \ \ \ \ (0,02-0,01) \end{matrix}\right.\)
\(\Rightarrow \left\{\begin{matrix} \qquad \ \ \ Cu^{2+} & +2OH^- & \longrightarrow & Cu(OH)_2 \\ mol: 0,02 & 0,02 & \rightarrow & 0,01 \end{matrix}\right.\Rightarrow m=0,01.98=0,98 \ gam\)
Câu trả lời của bạn
+ Do V1 : V2 = 4 : 7 ⇒ tự chọn lượng chất với V1 = 0,4 mol, V2 = 0,7 mol
+ Thí nghiệm 1:
\(\left\{\begin{matrix} \qquad \ \ \ H^++CO_{3}^{2-} & \longrightarrow & HCO_{3}^{-} & \\ mol:0,1y \gets 0,1y & \longrightarrow & 0,1y & \\ \qquad \ \ \ \ H^+ &+ & HCO_{3}^{-} & \longrightarrow CO_2+H_2O \\ mol:(0,1x-0,1y) & & 0,1y & 0,4 \end{matrix}\right.\)
+ Thí nghiệm 2:
\(\left\{\begin{matrix} \qquad \ \ CO_{3}^{2-} & +2H^+ & \longrightarrow & CO_2+H_2O\\ mol:0,1y & 0,1x & & 0,7 \qquad \ \ \ \ \ \end{matrix}\right.\)
Do thí nghiệm 1 có khí thoát ra nên H+ phải còn dư sau phản ứng với \(CO_{3}^{2-}\Rightarrow 0,1y
Vậy ở thí nghiệm 2, ta có: \(n_{CO_2}=0,05x \ mol=0,7 \ mol \Rightarrow x=14\). (Đơn giản hơn thì chia hệ số cân bằng mol phản ứng tính theo chất cho giá trị nhỏ hơn).
Khi đó, ta có: 0,1y > 0,4 ⇒ số mol CO2 ở thí nghiệm 1 tính thoe H+ ⇔ 0,1.14 – 0,1y = 0,4 mol → y = 10
Vậy x : y = 14 : 10 = 7 : 5
Câu trả lời của bạn
Vì nước vôi có tính bazơ nên có thể xử lý chất thải có tính axit.
A. Cr.
B. Sr.
C. Al.
D. Fe.
Câu trả lời của bạn
Đáp án đúng: B
Câu trả lời của bạn
Ta có: \(n_{CO_2}=0,08 \ mol\) và \(n_{OH^-}=0,088 \ mol\)
PTHH:
\(\begin{matrix} CO_2 & +2OH^- & \rightarrow & CO_{3}^{2-} & +H_2O \\ X & 2X & & & \\ CO_2 & +OH^- & \rightarrow & HCO_{3}^{-} & \\ y & y & & & \end{matrix}\)
Ta có hệ phương trình: \(\left\{\begin{matrix} x+y=0,08\\ 2x+y=0,088 \end{matrix}\right.\rightarrow \left\{\begin{matrix} x=0,008\\ y=0,072 \end{matrix}\right.\)
Vậy m = 0,008.197=1,576 gam
Câu trả lời của bạn
Không mất tính tổng quát giả sử hỗn hợp muối thu được sau phản ứng gồm: Na2CO3: y mol NaHCO3: z mol.
Áp dụng định luật bảo toàn nguyên tố [Na; C ] và giải hệ 3 phương trình ta được:
0,2x + 0, 08 x 2 = 2y + z (1).
0,15 + 0, 08 = y + z (2).
106y + 84z = 19,98 (3).
Giải 1, 2, 3 ta được x = 0, 5; y = 0, 03; z = 0, 2.
Lưu ý: Nếu đề bài thay đổi dữ kiện đầu bài là dung dịch X có chứa 19,98g muối khan thành dung dịch X có chứa 19,98g chất tan. Khi ấy, ta phải xét hai trường hợp hoặc X chứa Na2CO3 và NaHCO3 hoặc X sẽ chứa NaOH dư và Na2CO3. Phụ thuộc vào số mol các chất tính nếu trường hợp nào số mol âm thì xét trường hợp còn lại.
Câu trả lời của bạn
Các dung dịch tạo kết tủa với Ba là: NaHCO3; (NH4)2CO3 (tạo BaCO3); MgCl2 (tạo Mg(OH)2); CuSO4 (tạo Cu(OH)2 và BaSO4).
Câu trả lời của bạn
Ta có: \(n_{BaCO_3}= 0,08\ mol\)
\(\rightarrow n_{K_2CO_3}= 0,08 \Rightarrow n_{KOH} = 0,08 mol \times n_{CaCO_3}= 0,1 \ mol\). Khi đun nóng thì KHCO3 sẽ phân hủy thành CO2; K2CO3; H2O.}
⇒ Lượng CaCO3 tạo thành do K2CO3 (từ KHCO3 phân hủy) là:
\(n_{CaCO_3}= 0,02\ (mol)\)
⇒tổng nC= 0,12 → m = 8,96 (g); a = 0,12M
Câu trả lời của bạn
Ta có: nNa = 0,3.
Dung dịch X chứa NaCl và NaOH dư.
Dễ dàng tính được nNaCl = 0,14; nNaOH = 0,16.
Ta có: \(a = m_{AgCl}+ m_{Ag_2O}= 38,65g\)
(AgOH sau khi được tạo ra thì phân hủy ngay thành Ag2O kết tủa màu đen).
Câu trả lời của bạn
Các trường hợp phản ứng với Ba(HCO3)2 là:CuSO4, NaOH, NaHSO4, K2CO3, Ca(OH)2, H2SO4, HNO3, HCl.
Câu trả lời của bạn
Ta có n\(\tiny H_2\) = 0,1 mol
⇒ n kim loại = 0,2 mol
⇒ M trung bình = 3,8 : 0,2 = 19
⇒ Li và Na
Câu trả lời của bạn
Giả sử hỗn hợp chỉ có \(CaCO_3 \Rightarrow n_{max} = 0,207 \Rightarrow n_{CO_2} = 0,207\)
Giả sử hỗn hợp chỉ có \(K_2CO_3 \Rightarrow n_{min} = 0,15 \Rightarrow n_{CO_2} = 0,15\)
\(n_{Ba(OH)_2} = 0,18\)
TH số mol \(CO_2\) min: \(\begin{matrix} CO_2 & + &Ba(OH)_2 &\rightarrow &BaCO_3 &+ &H_2O\\ 0,15 & &0,18 & & 0,15 \end{matrix}\)
\(\Rightarrow m_{BaCO_3} = 0,15 \times 197 = 29,55\)
TH số mol CO2 max: \(\begin{matrix} CO_2 & + &Ba(OH)_2 &\rightarrow &BaCO_3 &+ &H_2O\\ 0,207 & &0,18 & & 0,18 \end{matrix}\)
\(\begin{matrix} CO_2 & + &BaCO_3 &+ &H_2O&\rightarrow &Ba(HCO_3)_2 \\ 0,207 &\rightarrow & 0,207 \end{matrix}\)
\(n_{BaCO_3}\) còn lại \(= 0,18 – 0,027 =0,153 \Rightarrow m_{BaCO_3} = 0,153 \times 197 = 30,14g\)
Câu trả lời của bạn
Bazơ tạo ra clorua vôi ⇒ phải chứa Ca.
Câu trả lời của bạn
nHCl=0,25.
Gọi 2 KL đó là A, B.
⇒ các chất tan tạo thành có thể là AlCl2; BCl2; A(OH)2 và B(OH)2.
n\(\tiny ACl_2\) = n\(\tiny BCl_2\)
* TH1: acid dư ⇒ chất tan chỉ có AlCl2; BCl2 và HCl
nA = nB = nHCl dư = 0,255 = 0,05.
⇒ MA, B = 24,5.
⇒ Đáp án A.
* TH2: KL dư ⇒ A và B phải có ít nhất 1 KL tan trong nước. Giả sử là A (nếu chỉ có 1 KL tan trong nước).
⇒ Chất tan chắc chắn có ACl2; BCl2; A(OH)2 hoặc B(OH)2 hoặc cả 2.
n\(\tiny A(OH)_2\) = n\(\tiny ACl_2\) = n\(\tiny BCl_2\) = n\(\tiny HCl_4\) = 0,0625.
⇒ nA + nB ≤ 0,0625 x 3 = 0,1875.
MA, B ≤ 13.
⇒ Đáp án A
A. Al.
B. Zn.
C. Mg.
D. K.
Câu trả lời của bạn
Kim loại tác dụng được với nước ở nhiệt độ thường trong 4 chất chỉ có Kali thỏa mãn.
A. Giấm ăn.
B. Muối ăn.
C. Phèn chua.
D. Nước vôi.
Câu trả lời của bạn
Vì chất thải có tính axit nên cần chất có tính bazo.
Câu trả lời của bạn
Theo bài ra, ban đầu có 4 mol HCO3–, 3 mol OH–.
⇒ 3 mol HCO– sẽ tác dụng với 3 mol OH– trước tạo 3 mol CaCO3 ⇒ hết Ca2+.
Còn lại 1 mol Na+ tác dụng nốt với 1 mol HCO3–.
⇒ NaHCO3.
A. Cho khí Cl2 đi từ từ qua dung dịch NaOH, Na2CO3.
B. Sục khí Cl2 vào dung dịch KOH.
C. Cho khí Cl2 vào dung dịch Na2CO3.
D. Điện phân dung dịch NaCl không màng ngăn.
Câu trả lời của bạn
Đáp án đúng: D
Phương pháp điều chế trong công nghiệp ⇒ rẻ, đơn giản.
⇒ Điện phân dung dịch NaCl không màng ngăn.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *