Nội dung bài học trình bày cụ thể, tỉ mỉ về Crom và hợp chất của crom. Thông qua bài học các em học sinh biết được vị trí của Crom trong Bảng hệ thống tuần hoàn các nguyên tố hóa học; cấu tạo nguyên tử, tính chất vật lí - hóa học và phương pháp điều chế. Biết được tính chất và ứng dụng của một số hợp chất quan trọng của Crom như oxit và muối Crom (III), Crom (VI).
Là kim loại cứng nhất, có thể rạch được thuỷ tinh.
Trong các hợp chất crom có số oxi hoá từ +1 → +6 (hay gặp +2, +3 và +6).
Cr bền với nước và không khí do có lớp màng oxit rất mỏng, bền bảo vệ ⇒ Mạ crom lên sắt để bảo vệ sắt và dùng Cr để chế tạo thép không gỉ.
Chú ý: Cr không tác dụng với dung dịch HNO3 hoặc H2SO4 đặc, nguội.
| Đặc điểm | Crom (III) oxit – Cr2O3 | Crom (III) hiđroxit – Cr(OH)3 |
| Tính chất vật lí | Cr2O3 là chất rắn, màu lục thẩm, không tan trong nước. | Cr(OH)3 là chất rắn, màu lục xám, không tan trong nước. |
| Tính chất hóa học |
Cr2O3 + 2NaOH (đặc) → 2NaCrO2 + H2O Cr2O3 + 6HCl → 2CrCl3 + 3H2 |
Cr(OH)3 + NaOH → NaCrO2 + 2H2O Cr(OH)3+ 3HCl → CrCl3 + 3H2O
2CrCl3 + Zn → 2CrCl2 + ZnCl2 2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O |
| Đặc điểm | Crom (VI) oxit – CrO3 | Muối crom (VI) |
| Tính chất vật lí | CrO3 là chất rắn màu đỏ thẫm. | - Là những hợp chất bền. + Na2CrO4 và K2CrO4 có màu vàng (màu của ion CrO42-) + Na2Cr2O7 và K2Cr2O7 có màu da cam (màu của ion Cr2O72-) |
| Tính chất hóa học |
CrO3 + H2O → H2CrO4 (axit cromic) 2CrO3 + H2O → H2Cr2O7 (axit đicromic)
Một số chất hữu cơ và vô cơ (S, P, C, C2H5OH) bốc cháy khi tiếp xúc với CrO3. |
\(\begin{array}{l} {K_2}C{r_2}{O_7} + 6FeS{O_4} + 7{H_2}S{O_4} \to \\ {\rm{ }}3Fe{(S{O_4})_3} + C{r_2}{(S{O_4})_3} + {K_2}S{O_4} + 7{H_2}O \end{array}\)
\(Cr_{2}O_{7}^{2-}+H_{2}O\Leftrightarrow 2CrO_{4}^{2-}+2H^{+}\) |
Cho sơ đồ phản ứng: Cr\(\overset{Cl_{2}, du}{\rightarrow}\) X \(\overset{+KOH,+Cl_{2}}{\rightarrow}\) Y
Biết Y là hợp chất của crom. Hai chất X và Y lần lượt là
\(Cr + Cl_2\rightarrow CrCl_3(X)\)
\(CrCl_3 + Zn\overset{H^+}{\rightarrow}CrCl_2+ZnCl_2\)
\(CrCl_3 + KOH + Cl_2 \rightarrow K_2CrO_4 (Y) + KCl + H_2O\)
Cho sơ đồ chuyển hóa sau: \({K_2}C{r_2}{O_7}\overset{FeSO_{4}+H_{2}SO_{4}}{\rightarrow}X\overset{NaOH(d-)}{\rightarrow}Y\overset{Br_{2}+NaOH}{\rightarrow}Z\)
Biết X, Y và Z là các hợp chất của crom. Hai chất Y và Z lần lượt là
- Các phản ứng xảy ra là:
FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 (X) + H2O
Cr2(SO4)3 + NaOH dư→ NaCrO2 (Y) + Na2SO4 + H2O
NaCrO2 + Br2 + NaOH → Na2CrO4 (Z) + NaBr + H2O
Cho m gam bột crom phản ứng hoàn toàn với dung dịch HCl (dư) thu được V lít khí H2 (đktc). Mặt khác cũng m gam bột crom trên phản ứng hoàn toàn với khí O2 (dư) thu được 15,2 gam oxit duy nhất. Giá trị của V là
\(\\ 4Cr+3O_2\rightarrow 2Cr_2O_3 \\ 0,2 \hspace{40pt}\leftarrow 0,1\)
\(\\ Cr+2HCl\rightarrow CrCl_2+H_2 \\ 0,2 \hspace{110pt} 0,2\)
\(V_{H_2}=4,48 (l)\)
Hòa tan hoàn toàn 11,15 gam hỗn hợp X gồm crom và thiếc vào dung dịch HCl dư thu được3,36 lít H2 (đktc). Số mol O2 cần dùng để đốt cháy hoàn toàn 11,15 gam X là:
X gồm x mol Cr và y mol Sn
Phản ứng với HCl:
Cr + HCl → CrCl2 + H2
Sn + HCl → SnCl2 + H2
⇒ \(\left\{\begin{matrix} x + y = n_{H_2} =0,15\ mol\\ 52x + 119y = 11,15\ g \end{matrix}\right.\)
⇒ x = 0,1 mol; y = 0,05 mol
Khi phản ứng với oxi:
2Cr + \(\frac{3}{2}\) O2 → Cr2O3
Sn + O2 → SnO2
⇒ n\(\tiny O_2\) = 0,75 × 0,1 + 0,05 = 0,125 mol
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm Al và Cr2O3, thu được hỗn hợp Y. Chia hỗn hợp Y thành hai phần bằng nhau.
+ Phần 1 phản ứng vừa đủ 2,5 lít dung dịch H2SO4 0,5M, nóng (không có không khí).
+ Phần 2 phản ứng vừa đủ 3,2 lít dung dịch HNO3 1M, thu được 11,2 lít khí NO (đo ở đktc, sản phẩm khử duy nhất).
Hiệu suất của phản ứng nhiệt nhôm là:
\(\\ n_{H_{2}SO_{4}} = 2,5. 0,5 = 1,25 \ mol\)
\(n_{HNO_{3}} = 3,2.1 = 3,2 \ mol\)
n NO = 0,5 mol
\(n_{NO_{3}^-}\) (muối) = 3,2 – 0,5 = 2,7 mol
\(n_{SO_{4}^{2-}}\) = 1,25 mol
Ta thấy có sự chênh lệch điện tích NO3– và SO42 –, chính là do Cr sinh ra
⇒ nCr = 1,7 – 1,25. 2 = 0,2 mol
Cr + 4HNO3 → Cr(NO3)3 + NO + 2H2O
0,2 0,8 0,2 0,2
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
0,3 1,2 0,3
2Al + Cr2O3 → Al2O3 + 2Cr
0,2 0,1 0,1 0,2
\(\Rightarrow n _{Al_{2}O_{3}} = 0,1\)
Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O
0,1 0,6
Cr2O3 + 6HNO3 → 2Cr(NO3)3 + 3H2O
0,1 ← 3,2 – 0,8 – 1,2 – 0,6
\(\\ \Rightarrow \sum n_{Cr_{2}O_{3}bd} = 0,2 \\ \sum n _{Al \ bd}= 0,5\)
⇒ Hiệu suất tính theo Cr2O3 ⇒ \(H\%=\frac{0,1}{0,2}=50\%\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hoá học 12 Bài 34có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Hiện tượng xảy ra khi cho dung dịch KOH loãng vào dung dịch K2Cr2O7 là:
Nhận xét nào sau đây không đúng?
Cho phương tình hóa học của phản ứng : 2Cr + 3Sn2+ → 2Cr3+ + 3Sn.
Nhận xét nào sau đây về phản ứng trên là đúng?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hoá học 12 Bài 34.
Bài tập 1 trang 155 SGK Hóa học 12
Bài tập 2 trang 155 SGK Hóa học 12
Bài tập 3 trang 155 SGK Hóa học 12
Bài tập 4 trang 155 SGK Hóa học 12
Bài tập 5 trang 155 SGK Hóa học 12
Bài tập 1 trang 190 SGK Hóa học 12 nâng cao
Bài tập 2 trang 190 SGK Hóa học 12 nâng cao
Bài tập 3 trang 190 SGK Hóa học 12 nâng cao
Bài tập 4 trang 190 SGK Hóa 12 Nâng cao
Bài tập 5 trang 190 SGK Hóa 12 Nâng cao
Bài tập 1 trang 194 SGK Hóa học 12 nâng cao
Bài tập 3 trang 194 SGK Hóa học 12 nâng cao
Bài tập 4 trang 194 SGK Hóa học 12 nâng cao
Bài tập 34.1 trang 80 SBT Hóa học 12
Bài tập 34.2 trang 80 SBT Hóa học 12
Bài tập 34.3 trang 80 SBT Hóa học 12
Bài tập 34.4 trang 80 SBT Hóa học 12
Bài tập 34.5 trang 81 SBT Hóa học 12
Bài tập 34.6 trang 81 SBT Hóa học 12
Bài tập 34.7 trang 81 SBT Hóa học 12
Bài tập 34.8 trang 81 SBT Hóa học 12
Bài tập 34.9 trang 81 SBT Hóa học 12
Bài tập 34.10 trang 82 SBT Hóa học 12
Bài tập 34.11 trang 82 SBT Hóa học 12
Bài tập 34.12 trang 82 SBT Hóa học 12
Bài tập 34.13 trang 82 SBT Hóa học 12
Bài tập 34.14 trang 82 SBT Hóa học 12
Bài tập 34.15 trang 83 SBT Hóa học 12
Bài tập 34.16 trang 83 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Hiện tượng xảy ra khi cho dung dịch KOH loãng vào dung dịch K2Cr2O7 là:
Nhận xét nào sau đây không đúng?
Cho phương tình hóa học của phản ứng : 2Cr + 3Sn2+ → 2Cr3+ + 3Sn.
Nhận xét nào sau đây về phản ứng trên là đúng?
Cho các chất sau: Cr, Cr2O3, Cr(OH)3, CrO3, K2CrO4, CrSO4. Số chất tan trong dung dịch NaOH loãng, dư chỉ tạo ra dung dịch là:
Khi cho Kalidicromat vào dung dịch HCl dư đun nóng xảy ra phản ứng: K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O
Nếu dùng 5,88g K2Cr2O7 thì số mol HCl bị Oxi hóa là:
Cho dung dịch chứa 1 mol KOH vào dung dịch chứa 0,4 mol CrCl2 rồi để trong không khí đến phản ứng hoàn toàn thì lượng kết tủa cuối cùng thu được là bao nhiêu gam?
Trộn bột nhôm với m gam hỗn hợp X gồm CuO, MgO, Cr2O3 và FexOy (trong FexOy oxi chiếm 27,59% theo khối lượng) rồi đun nóng thì thu được 240 gam hỗn hợp Y.
- Để hòa tan hoàn toàn hỗn hợp Y thì phải dùng hết 450ml dung dịch NaOH loãng 2M
- Lấy ½ hỗn hợp Y cho tác dụng hoàn toàn với dung dịch HNO3 thì thu được 12,32 lit khí NO (sản phẩm khử duy nhất). Thành phần phần trăm của FexOy trong hỗn hợp X là:
Thêm 0,02 mol NaOH vào dung dịch chứa 0,01 mol CrCl2 rồi để trong không khí đến phản ứng hoàn toàn thì khối lượng kết tủa cuối cùng thu được là:
Tiến hành phản ứng nhiệt nhôm với một hỗn hợp gồm 8,1 gam Al và 15,2 gam Cr2O3, sau phản ứng thu được hẳn hợp X. Cho hỗn hợp X vào dung dịch NaOH dư, đun nóng thấy thoát ra 5,04 lít H2 (đktc). Khối lượng crom thu được là:
Muốn điều chế 6,72 lít khí đo (đktc) thì khối lượng K2Cr2O7 tối thiều cần dùng đế tác dụng với dung dịch HCl đặc, dư là
Phát biểu nào sau đây không đúng ?
A. Hợp chất Cr(II) có tính khử đặc trưng còn hợp chất Cr(VI) có tính oxi hoá mạnh.
B. Các hợp chất Cr2O3, Cr(OH)3, CrO, Cr(OH)2 đều có tính chất lưỡng tính.
C. Các hợp chất CrO, Cr(OH)2 tác dụng được với dung dịch HCl còn CrO3 tác dụng được với dung dịch NaOH.
D. Thêm dung dịch kiềm vào muối đicromat, muối này chuyển thành muối cromat.
Cho dung dịch chứa 0,5 mol NaOH vào dung dịch chứa 0,2 mol CrCl2 rồi để trong không khí đến phản ứng hoàn toàn. Khối lượng kết tủa cuối cùng thu được là
A. 10,3 g.
B. 20,6 g.
C. 8,6 g.
D. 17,2 g.
Hiện tượng nào dưới đây đã miêu tả không đúng ?
A. Thổi khí NH3 qua CrO3 đốt nóng thấy chất rắn chuyển từ màu đỏ sang màu lục thẫm.
B. Nung Cr(OH)2 trong không khí thấy chất rắn chuyển từ màu lục xám sang màu lục thẫm.
C. Thêm lượng dư NaOH vào dung dịch K2Cr2O7 thì dung dịch chuyển từ màu da cam sang màu vàng.
D. Thêm lượng dư NaOH và Cl2 vào dung dịch CrCl2 thì dung dịch màu xanh chuyển sang màu vàng.
Có các phương trình hoá học sau :
1. CrO + 2HCl → CrCl2 + H2O
2. CrClO + 2NaOH → Cr(OH)2 + 2NaCl
3. 4Cr(OH)2 + O2 + 2H2O → 4Cr(OH)3
4. Cr(OH)2 + 2HCl → CrCl2 + 2H2O
5. 4CrCl2 + 4HCl + O2 → 4CrCl3 + 2H2O
Những phản ứng minh hoạ tính khử của hợp chất crom (II) là
A. 1,2.
B. 3, 5.
C. 3,4.
D. 2, 4.
Thể tích của dung dịch K2Cr2O7 0,05M vừa đủ phản ứng với dung dịch chứa 0,06 mol FeSO4 trong môi trường H2SO4 dư là
A. 100 ml.
B. 150 ml.
C. 200 ml.
D. 250 ml.
Để oxi hóa hoàn toàn 0,01 mol CrCl4 thành K2Cr2O4 bằng Cl2 khi có mặt KOH, lượng tối thiểu Cl2 và KOH tương ứng là
A. 0,03 mol và 0,04 mol
B. 0,03 mol và 0,08 mol
C. 0,015 mol và 0,08 mol
D. 0,015 mol và 0,04 mol
Cho sơ đồ các chuỗi phản ứng sau :
1) Cr2O3 → A1 → A2 → A3 → A4 → A5 → A6 → A7 → Cr2O3
2,
Biết rằng :
- A1... A7 là các đơn chất hoặc hợp chất của crom.
- X1... X3 là các hợp chất của crom.
Hãy viết PTHH (có ghi điều kiện) theo các chuỗi phản ứng trên.
Viết phương trình hoá học của các phản ứng trong quá trình chuyển hoá sau:
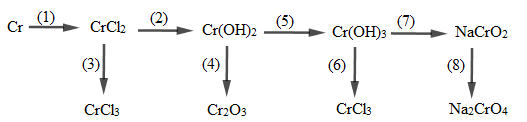
Cr → CrCl3 → Cr(OH)3 → NaCrO2 → Na2CrO4 → Na2Cr2O7
Cho từ từ dung dịch NaOH vào dung dịch chứa 9,02 g hỗn hợp muối Al(NO3)3 và Cr(NO3)3 cho đến khi lượng kết tủa thu được là lớn nhất. Tách kết tủa ra khỏi dung dịch, rửa và nung đến khối lượng không đổi thu được 2,54 g chất rắn. Tính phần trăm khối lượng các muối trong hỗn hợp ban đầu.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
– Phần 1. Phản ứng vừa đủ với 250 ml dung dịch NaOH 1M (loãng).
– Phần 2. Phản ứng hoàn toàn với dung dịch HCl loãng (dư), thu được 6,384 lít H2 (đktc). Giả sử trong phản ứng nhiệt nhôm, Cr2O3 chị bị khử thành Cr.
Hiệu suất phản ứng nhiệt nhôm là
A. 40%.
B. 60%.
C. 25%.
D. 75%
Câu trả lời của bạn
Trong mỗi phần (24,99 gam) chứa:
nAl ban đầu = nNaOH = 0,25
—> nCr2O3 ban đầu = 0,12
2Al + Cr2O3 —> 2Cr + Al2O3
2x……….x………….2x
—> nAl dư = 0,25 – 2x và nCr = 2x
—> nH2 = 1,5(0,25 – 2x) + 2x = 0,285
—> x = 0,09
—> H = x/0,12 = 75%
Câu trả lời của bạn
Kim loại 40% —> Gốc SO4 chiểm 60%
Muối sunfat có x gốc SO4
—> M muối = 96x/60% = 160x
—> x = 1, M muối = 160: CuSO4
Oxit là CuO —> %Cu = 80%
a, Tính % theo thể tích của khí CO2 trong hỗn hợp khí X.
b, Tìm công thức oxit sắt?
Câu trả lời của bạn
Khí X gồm CO2 (a) và CO dư (b)
nCO ban đầu = a + b = 0,2
mX = 44a + 28b = 0,2.2.20
—> a = 0,15 và b = 0,05
—> CO2 (75%) và CO (25%)
yCO + FexOy —> xFe + yCO2
…………0,15/y………………0,15
—> M = 56x + 16y = 8y/0,15
—> x/y = 2/3
—> Fe2O3.
Câu trả lời của bạn
B chứa Cu, Fe, MgO, NaOH, Ba(OH)2, Na2O, BaO
X chứa NaOH, Ba(OH)2
D chứa Cu, Fe, MgO
M chứa FeCl2, MgCl2
R là Cu
Y là BaSO4.
TN1: Hấp thụ hết V lít khí CO2 (đktc) vào dung dịch chứa 0,3 mol Ca(OH)2, phản ứng hoàn toàn thu được m gam chất rắn.
TN2: Hấp thụ hết V lít khí CO2 (đktc) vào dung dịch chứa 0,3 mol Ca(OH)2 và 0,1 mol NaOH, phản ứng hoàn toàn thu được 2m gam chất rắn.
Tìm x, m
Câu trả lời của bạn
Đặt y = m/100
TN1: nCaCO3 = y —> nCa(HCO3)2 = 0,3 – y
—> nCO2 = x = y + 2(0,3 – y) (1)
TN2: Nếu Ca2+ đã kết tủa hết
—> 0,3 = 2y (2)
(1)(2) —> x = 0,45 và y = 0,15 —> m = 15
Nếu Ca2+ chưa kết tủa hết:
—> Dung dịch thu được chứa Ca2+ (0,3 – 2y), Na+ (0,1) và HCO3- (x – 2y)
Bảo toàn điện tích: 2(0,3 – 2y) + 0,1 = x – 2y (3)
(1)(3) —> x = 0,5 và y = 0,1 —> m = 10
A. 6,0
B. 6,1
C. 6,2
D. 6,3
Câu trả lời của bạn
Đáp án B
Câu trả lời của bạn
MD = 38/3 —> D gồm H2O và H2 với nH2O : nH2 = 2 : 1
Do D chứa H2 nên A là Fe(OH)2.
xFe(OH)2 —> FexOy + (2x – y)H2O + (y – x)H2
—> 2x – y = 2(y – x)
—> 4x = 3y
—> x/y = 3/4 —> B là Fe3O4.
A. 32,0.
B. 25,6.
C. 21,2.
D. 24,0.
Câu trả lời của bạn
Đặt nO = 2x —> nHCl = nN = nO/2 = x
—> m = 16.2x/40%
Bảo toàn khối lượng: m + 36,5x = 2m – 17,4
—> m = 32 và x = 0,4
A. 46,59
B. 35,61
C. 17,8
D. 68,89
Câu trả lời của bạn
Quy đổi E thành C2H3ON (0,7), CH2 (a) và H2O (b)
mE = 0,7.57 + 14a + 18b = 52,8
Đốt F tốn O như đốt E nên:
nO2 = 0,7.2,25 + 1,5a = 2,475
—> a = 0,6 và b = 0,25
—> Số C = (a + 0,7.2)/b = 8
Các peptit 8C có dạng Ala-Val (x), (Gly)(Ala)2 (y) và (Gly)4 (z)
nN = 2x + 3y + 4z = 0,7
nC = 8x + 8y + 8z = a + 0,7.2
Muối gồm C2H3ON (0,7), CH2 (a) và KOH (0,7)
—> m muối = 87,5 —> nGlyK = y + 4z = 0,4
—> x = 0,15; y = 0 và z = 0,1
—> Các peptit gồm Ala-Val, Val-Ala (tổng 0,15 mol) và (Gly)4 (0,1 mol)
—> %(Gly)4 = 46,59%
A. 2,30
B. 3,30
C. 2,53
D. 3,53
Câu trả lời của bạn
Z là NH2-CH2-COOCH3 nên T gồm CH3OH (u mol) và CH3NH2 (v mol)
mT = 32u + 31v = 2,53
Với Na lượng chất dùng một nửa, khí thoát ra gồm H2 và CH3NH2.
n khí = 0,5.0,5u + 0,5v = 0,0275
—> u = 0,05 và v = 0,03
Hai muối kế tiếp nhau nên Y là NH2-CH2-CONH-CH(CH3)-COONH3-CH3
Muối gồm GlyNa (u + v = 0,08) và AlaNa (v = 0,03)
—> mGlyNa : mAlaNa = 2,33
A. 0,12.
B. 0,98.
C. 0,99.
D. 0,10.
Câu trả lời của bạn
Từ số mol X1, X2, X3 —> Số mol ancol T (Dạng R(OH)2) có thể là 0,065; 0,045; 0,04
—> Chọn nT = 0,04 vì R + 32 = 2,4/0,04 —> R = 28
Vậy T là C2H4(OH)2 (0,04) và X3 là muối cacboxylat.
Đặt n, m, p là số C của X1, X2, X3
—> nCO2 = 0,13n + 0,09m + 0,08p + 0,04.2 = 0,85
—> 13n + 9m + 8p = 77
—> n = 2, m = p = 3 là nghiệm duy nhất
Các muối là GlyNa (0,13), AlaNa (0,09) và C2HvCOONa (0,08)
—> nGly : nAla = 13 : 9
2X + 3Y —> [(Gly)13(Ala)9]k + 4H2O
Tổng liên kết pi = 13 —> Tổng liên kết pi trong X và Y ≤ 11
—> Tổng số mắt xích của X và Y ≤ 11
—> Tổng số mắt xích của 2X và 3Y ≤ 2.2 + 3.9 = 31
—> 22k ≤ 31 —> k = 1 là nghiệm duy nhất.
Đặt x, y là số N của X, Y —> 2x + 3y = 22k = 22 (1)
Đặt z là số liên kết pi của Z. Do Z có dạng (C2HvCOO)2C2H4 nên z = 2, 4, 6 (2)
—> x + y + z = 13 (3)
(1)(2)(3) —> x = 5; y = 4; z = 4 là nghiệm duy nhất
Đốt M cũng tốn O2 giống đốt các sản phẩm GlyNa (0,13), AlaNa (0,09), C2H3COONa (0,08), C2H4(OH)2 (0,04)
—> nO2 = 0,13.2,25 + 0,09.3,75 + 0,08.3 + 0,04.2,5 = 0,97
A. 2.
B. 3.
C. 5.
D. 4.
Câu trả lời của bạn
Các chất tác dụng với dung dịch HCl: glyxin, anilin, etylamin, axit glutamic.
NH2-CH2-COOH + HCl —> NH3Cl-CH2-COOH
C6H5NH2 + HCl —> C6H5NH3Cl
C2H5NH2 + HCl —> C2H5NH3Cl
NH2-C3H5(COOH)2 + HCl —> NH3Cl-C3H5(COOH)2
(b) Nhúng thanh sắt vào nước.
(c) Nhúng thanh bạc vào dung dịch H2SO4 loãng.
(d) Nhúng thanh nhôm vào dung dịch KOH.
Trong các thí nghiệm trên, số thí nghiệm xảy ra phản ứng ở điều kiện thường là
A. 4.
B. 3.
C. 2.
D. 1.
Câu trả lời của bạn
Có 2 thí nghiệm xảy ra phản ứng:
(a) Cu + FeCl3 —> CuCl2 + FeCl2
(d) Al + H2O + KOH —> KAlO2 + H2
A. 150.
B. 50.
C. 100.
D. 200.
Câu trả lời của bạn
nHCl = nN = 2nN2 = 0,1
—> VddHCl = 100 ml
A. Cho Cr(OH)3 vào dung dịch HCl.
B. Cho Cr vào dung dịch H2SO4 loãng, nóng.
C. Cho Cr vào dung dịch H2SO4 đặc, nguội.
D. Cho CrO3 vào H2O.
Câu trả lời của bạn
Chọn C
C
Chọn C.
Cr, Al và Fe không tác dụng với H2SO4 và HNO3 đặc nguội.
A. Cr(OH)3 và Na2CrO4
B. Cr(OH)3 và NaCrO2
C. NaCrO2 và Na2CrO4
D. Cr2(SO4)3 và NaCrO2
Câu trả lời của bạn
C
Đáp án là C.
C
Câu C.
- Các phản ứng xảy ra là:
FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 (X) + H2O
Cr2(SO4)3 + NaOH dư → NaCrO2 (Y) + Na2SO4 + H2O
NaCrO2 + Br2 + NaOH → Na2CrO4 (Z) + NaBr + H2O
Câu trả lời của bạn
Cr2O3 là oxit lưỡng tính nên tác dụng được với dung dịch HCl và dung dịch NaOH:
Cr2O3 + 6HCl → 2CrCl3 + 3H2O
Cr2O3 + 2NaOH + 3H2O → 2Na[Cr(OH)4]
A. 10,3
B. 5,15
C. 15,45
D. 7,725
Câu trả lời của bạn
A
Ta có: \({n_{O{H^ - }}} = 2{n_{{H_2}}} = 0,5\)
\( \Rightarrow 3 < \frac{{{n_{O{H^ - }}}}}{{{n_{C{r^{3 + }}}}}} = \frac{{0,5}}{{0,15}} < 4 \Rightarrow \) kết tủa tan một phần.
Áp dụng công thức Áp dụng công thức: \({n_{O{H^ - }}} = 4{n_{C{r^{3 + }}}} - {n_ \downarrow } \Rightarrow {n_ \downarrow } = 4.0,15 - 0,5 = 0,1 \Rightarrow {m_{ \downarrow Cr{{(OH)}_3}}} = 10,3\) (gam).
Chọn A.
Câu trả lời của bạn
phản ứng oxi hóa - khử là 1, 3, 4, 5, 8
A. Crom (VI) oxit là oxit bazơ.
B. Ancol etylic bốc cháy khi tiếp xúc với CrO3.
C. Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+.
D. Crom (III) oxit và crom (II) hiđroxit đều là chất có tính lưỡng tính.
Câu trả lời của bạn
- Crom (VI) oxit là oxit bazơ không đúng vì: CrO3 là oxit axit.
- Ancol etylic bốc cháy khi tiếp xúc với CrO3: đúng vì CrO3 có tính oxi hóa mạnh.
- Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+ đúng vì dung dịch HCl không có tính oxi hóa trong khi đó Cr có 3 số oxi hóa phổ biến +2, +3, +6.
Vậy: Crom (VI) oxit là oxit bazơ là sai.
→ Đáp án A

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *