Tiết học ôn tập, hệ thống hóa kiến thức về tính chất vật lí, hóa học của kim loại và vận dụng vào việc giải các bài tập liên quan đến kim loại.
Các phát biểu sau đây Đúng hay Sai? Vì sao?
a. Kim loại có độ cứng lớn nhất là Cr.
b. Kim loại dẫn điện tốt nhất là Cu.
c. Kim loại có nhiệt độ nóng chảy cao nhất là W.
d. Kim loại có khối lượng riêng nhỏ nhất là Li.
a. Đúng. Kim loại cứng nhất là Cr, kim loại mềm nhất là Cs.
b. Sai. Độ dẫn điện giảm dần theo dãy: Ag > Cu > Au > Al > Fe.
c. Đúng. Kim loại có nhiệt độ nóng chảy cao nhất là W, kim loại có độ nóng chảy thấp nhất là Hg.
d Đúng. Kim loại có khối lượng riêng lớn nhất là Os, kim loại có khối lượng riêng nhỏ nhất là Li.
Cho hỗn hợp X gồm Fe, Cu vào dung dịch HNO3 loãng, nóng thu được khí NO, dung dịch Y và còn lại chất rắn chưa tan Z. Cho Z tác dụng với dung dịch H2SO4 loãng thấy có khí thoát ra. Thành phần chất tan trong dung dịch Y là:
Theo thứ tự phản ứng thì Fe phản ứng trước
\(Fe + 4HN{O_3} \to Fe{(N{O_3})_3} + N{O^ \uparrow } + 2{H_2}O\)
X + HNO3 loãng nóng -> Y + chất rắn Z không tan
=> Z có Cu và có thể có Fe(dư)
Vì Z + H2SO4 loãng thấy có khí thoát => Z phải có Fe dư
\(F{e_{(du)}} + 2Fe{(N{O_3})_3} \to 3Fe{(N{O_3})_2}\)
=> trong Y chỉ có Fe(NO3)2
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3 khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm 2 muối) và chất rắn Y (gồm 2 kim loại). 2 muối trong X là:
(1) Mg + 2Ag+ → Mg2+ + 2Ag
(2) Fe + 2Ag+ → Fe2+ + 2Ag
(3) Fe2+ + Ag+ → Fe3+ + Ag
Vì Chất rắn Y gồm 2 kim loại ⇒ đó là Ag và Fe ⇒ không thể xảy ra (3) và Ag+ phải hết
⇒ X gồm Mg2+ và Fe2+
Lấy 14,3g hỗn hợp X gồm Mg, Al, Zn đem đốt nóng trong oxi dư, sau khi phản ứng xảy ra hoàn toàn thì nhận được 22,3g hỗn hợp Y gồm 3 oxit. Tính thể tích dung dịch HCl 2M tối thiểu cần dùng để hòa tan hỗn hợp Y.
Bảo toàn khối lượng : mX + mO (pứ) = mY => nO(pứ) = 0,5 mol
Phản ứng tổng quát : \(O + 2{H^ + } \to {H_2}O\)
\(\Rightarrow {n_{HCl}} = 2{n_{{O^{2 - }}}} = 2.0,5 = 1{\rm{ }}(mol)\)
=> Vdd HCl = 0,5 lit = 500 ml
Cho a mol Fe phản ứng vừa đủ với b mol H2SO4 (đặc, nóng) thu được khí SO2 (sản phẩm khử duy nhất) và 5,04 gam muối. Biết tỉ lệ a : b = 3 : 7. Giá trị của a là:
Muối gồm: \(\left\{\begin{matrix} FeSO_{4}: \ x \ mol \ \ \ \ \\ Fe_{2}(SO_{4})_{3}: \ y \ mol \end{matrix}\right. \rightarrow 152x+400y = 5,04 \ \ (1)\)
Số mol e nhường = 2x + 6y → Số mol SO2 = x + 3y
→ Số mol H2SO4 phản ứng = 2x + 6y (mol)
Theo bài ra ta có:
\(\frac{n_{Fe}}{n_{H_{2}SO_{4}}} = \frac{3}{7} \Rightarrow \frac{x+2y}{2x+6y} = \frac{3}{7} \Rightarrow x - 4y = 0 \ \ (2)\)
Giải (1) và (2) ta được: \(\left\{\begin{matrix} x = 0,02 \ \\ y = 0,005 \end{matrix}\right. \Rightarrow a = x + 2y = 0,03 \ (mol)\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 12 Bài 22có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Cho các kim loại: Al, Cu, Au, Ag. Kim loại dẫn điện tốt nhất trong các kim loại này là:
Dung dịch Fe2(SO4)3 không phản ứng với chất nào sau đây?
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian, quan sát thấy hiện tượng gì?
Dẫn lượng khí CO dư đi qua ống sứ đựng m gam oxit sắt từ nung nóng. Sau khi phản ứng xảy ra hoàn toàn thì thu được 5,88 gam sắt. Giá trị của m là:
Điện phân (điện cực trơ, hiệu suất 100%) 300 ml dung dịch CuSO4 0,5M với cường độ dòng điện không đổi 2,68 A, trong thời gian t giờ thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X thấy xuất hiện 45,73 gam kết tủa. Giá trị của t là:
Ngâm thanh Cu (dư) vào dung dịch AgNO3 thu được dung dịch X. Sau đó ngâm thanh Fe(dư) vào dung dịch X thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y có chứa chất tan là:
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Dẫn khí H2 dư qua bột Mg nung nóng
(c) Cho dung dịch AgNO3 tác dụng với dung dịch Fe(NO3)2 dư
(d) Cho Na vào dung dịch MgSO4
(e) Nhiệt phân Hg(NO3)2
(g) Đốt Ag2S trong không khí
(h) Điện phân dung dịch Cu(NO3)2 với cực dương làm bằng đồng, cực âm làm bằng thép.
Số thí nghiệm không tạo thành kim loại là:
Câu 8-20: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 12 Bài 22.
Bài tập 1 trang 100 SGK Hóa học 12
Bài tập 2 trang 100 SGK Hóa học 12
Bài tập 3 trang 100 SGK Hóa học 12
Bài tập 4 trang 100 SGK Hóa học 12
Bài tập 5 trang 101 SGK Hóa học 12
Bài tập 6 trang 101 SGK Hóa học 12
Bài tập 7 trang 101 SGK Hóa học 12
Bài tập 8 trang 101 SGK Hóa học 12
Bài tập 9 trang 101 SGK Hóa học 12
Bài tập 10 trang 101 SGK Hóa học 12
Bài tập 22.1 trang 49 SBT Hóa học 12
Bài tập 22.2 trang 49 SBT Hóa học 12
Bài tập 22.3 trang 49 SBT Hóa học 12
Bài tập 22.4 trang 50 SBT Hóa học 12
Bài tập 22.5 trang 50 SBT Hóa học 12
Bài tập 22.6 trang 50 SBT Hóa học 12
Bài tập 22.7 trang 50 SBT Hóa học 12
Bài tập 22.8 trang 50 SBT Hóa học 12
Bài tập 22.9 trang 50 SBT Hóa học 12
Bài tập 22.10 trang 50 SBT Hóa học 12
Bài tập 22.11 trang 51 SBT Hóa học 12
Bài tập 22.12 trang 51 SBT Hóa học 12
Bài tập 22.13 trang 51 SBT Hóa học 12
Bài tập 22.14 trang 51 SBT Hóa học 12
Bài tập 22.15 trang 51 SBT Hóa học 12
Bài tập 22.16 trang 51 SBT Hóa học 12
Bài tập 22.17 trang 52 SBT Hóa học 12
Bài tập 22.18 trang 52 SBT Hóa học 12
Bài tập 22.19 trang 52 SBT Hóa học 12
Bài tập 1 trang 125 SGK Hóa học 12 nâng cao
Bài tập 2 trang 125 SGK Hóa học 12 nâng cao
Bài tập 3 trang 125 SGK Hóa học 12 nâng cao
Bài tập 4 trang 125 SGK Hóa học 12 nâng cao
Bài tập 5 trang 126 SGK Hóa học 12 nâng cao
Bài tập 6 trang 126 SGK Hóa học 12 nâng cao
Bài tập 7 trang 126 SGK Hóa học 12 nâng cao
Bài tập 8 trang 126 SGK Hóa học 12 nâng cao
Bài tập 9 trang 126 SGK Hóa học 12 nâng cao
Bài tập 10 trang 126 SGK Hóa học 12 nâng cao
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Cho các kim loại: Al, Cu, Au, Ag. Kim loại dẫn điện tốt nhất trong các kim loại này là:
Dung dịch Fe2(SO4)3 không phản ứng với chất nào sau đây?
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian, quan sát thấy hiện tượng gì?
Dẫn lượng khí CO dư đi qua ống sứ đựng m gam oxit sắt từ nung nóng. Sau khi phản ứng xảy ra hoàn toàn thì thu được 5,88 gam sắt. Giá trị của m là:
Điện phân (điện cực trơ, hiệu suất 100%) 300 ml dung dịch CuSO4 0,5M với cường độ dòng điện không đổi 2,68 A, trong thời gian t giờ thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X thấy xuất hiện 45,73 gam kết tủa. Giá trị của t là:
Ngâm thanh Cu (dư) vào dung dịch AgNO3 thu được dung dịch X. Sau đó ngâm thanh Fe(dư) vào dung dịch X thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y có chứa chất tan là:
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Dẫn khí H2 dư qua bột Mg nung nóng
(c) Cho dung dịch AgNO3 tác dụng với dung dịch Fe(NO3)2 dư
(d) Cho Na vào dung dịch MgSO4
(e) Nhiệt phân Hg(NO3)2
(g) Đốt Ag2S trong không khí
(h) Điện phân dung dịch Cu(NO3)2 với cực dương làm bằng đồng, cực âm làm bằng thép.
Số thí nghiệm không tạo thành kim loại là:
Để tách Ag khỏi hỗn hợp bột (Ag, Cu, Fe) mà không là thay đổi khối lượng Ag ta dùng dung dịch nào sau đây?
Cho hỗn hợp X gồm 0,56 gam Fe và Mg tác dụng với 250 ml dung dịch CuSO4. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,92 gam kim loại. Nồng độ mol/l của dung dịch CuSO4 là:
Cho 2,24 gam bột sắt vào 200 ml dung dịch CuSO4 0,05M.Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y.Gía trị của m là:
Ngâm một thanh sắt có khối lượng 20 gam vào 200 ml dung dịch hỗn hợp Cu(NO3)2 1M và AgNO3 0,5M, sau một thời gian thấy khối lượng thanh sắt tăng 10%. Hỏi khối lượng dung dịch đã thay đổi như thế nào?
Cho 0,02 mol Fe vào 100 ml dung dịch AgNO3 1 M. Khi phản ứng xảy ra hoàn toàn thì khối lượng Ag thu được là:
Dung dịch X gồm AgNO3 và Cu(NO3)2 có cùng nồng độ mol. Lấy 1 lượng hỗn hợp gồm 0,03 mol Al và 0,05 mol Fe cho vào 100 ml dung dịch X; phản ứng kết thúc thu được chất rắn Y chứa 3 kim loại. Cho Y vào HCl dư thu được 0,07 g khí. Nồng độ của 2 muối là:
Dung dịch X gồm CuCl2 0,2M; FeCl2 0,3M; FeCl3 0,3M. Cho m (g) bột Mg vào 100ml dung dịch X khuấy đều đến khi phản ứng kết thúc thu được dung dịch B. Thêm dung dịch KOH dư vào B được kết tủa D. Nung D trong không khí đến khối lượng không đổi thu được 5,4 g chất rắn E. Giá trị của m là:
Ngâm một lá kẽm nhỏ trong dung dịch có chứa 2,38 gam ion kim loại M2+ sau khi phản ứng xong, khối lượng lá kẽm tăng thêm 1,08 gam. Ion kim loại trong dung dịch là:
Nhận xét nào về tính chất vật lí của kim loại dưới đây là không đúng ?
Nhiệt độ nóng chảy : Hg < Al < W.
Tính cứng : Cs < Fe < W < Cr
Tính dẫn điện và nhiệt: Fe < Al < Au < Cu < Ag.
Phát biểu đúng ?
Liên kết kim loại là lực hút tĩnh điện giữa các electron tự do gắn các ion dương kim loại với nhau.
Lớp ngoài cùng của nguyên tử kim loại thường có từ 1 đến 5 electron.
Tính chất vật lí chung của kim loại như: dẻo, dẫn điện, dẫn nhiệt, ánh kim… là do các ion dương kim loại ở các nút mạng tinh thể gây ra.
Tất cả các kim loại đều ở trạng thái rắn và có cấu tạo mạng tinh thể. Liên kết kim loại là lực hút tĩnh điện giữa các electron tự do gắn các ion dương kim loại với nhau.
Cho các phản ứng sau :
X + HNO3(đặc, nóng) → A + NO2 + H2O
A + Cu → X + D
X có thể là kim loại nào trong số các kim loại sau ?
Cho hai thanh kim loại M hóa trị 2 với khối lượng bằng nhau. Nhúng thanh thứ nhất vào dung dịch CuSO4 và thanh thứ hai vào dung dịch Pb(NO3)2 một thời gian, thấy khối lượng thanh thứ nhất giảm và khối lượng thanh thứ hai tăng. Kim loại M là:
Mg.
Ni.
Cho 8,3 gam hỗn hợp X gồm Al, Fe (nAl = nFe) vào 100 ml dung dịch Y gồm Cu(NO3)2 và AgNO3. Sau khi phản ứng kết thúc thu được chất rắn Y gồm 3 kim loại. Hòa tan hoàn toàn chất rắn Y vào dung dịch HCl dư thấy có 1,12 lít khí thoát ra (đktc) và còn lại 28 gam chất rắn không tan Z. Nồng độ mol của Cu(NO3)2 và của AgNO3 lần lượt là:
2M và 1M.
0,2M và 0,1M.
1M và 2M.
Cho hỗn hợp Al, Fe vào dung dịch chứa AgNO3 và Cu(NO3)2 được dung dịch X và chất rắn Y gồm 3 kim loại. Chất rắn Y gồm
A. Al, Fe, Cu.
B. Fe, Cu,Ag.
C. Al, Cu, Ag.
D. Al, Fe,Ag.
Cho các dung dịch sau đựng trong các lọ riêng biệt: NaCl, NH4Cl, FeCl2, FeCl3, (NH4)2SO4. Kim loại nào sau đây có thể phân biệt tất cả các dung dịch trên
A. Al
B. Mg
C. Ba
D. Na
Hãy trình bày phương pháp hoá học để điều chế từng kim loại từ hỗn hợp muối sau:
a) AgNO3 và Pb(NO3)2.
b) AgNO3 và Cu(NO3)2.
c) AgNO3, Cu(NO3)2 và Pb(NO3)2.
Viết phương trình hoá học của các phản ứng.
Có sáu dung dịch, mỗi dung dịch chỉ có một loại cation: Zn2+, Cu2+, Mg2+, Fe2+, Ag+, Pb2+ và sáu kim loại là : Zn, Cu, Mg, Fe, Ag, Pb.
a) Hãy lập bảng để trình bày những kim loại nào có thể phản ứng với những dung dịch chứa cation nào ?
b) Từ những kết quả trong bảng có thể rút ra kết luận gì về tính oxi hoá của ion Ag+ và Mg2+, tính khử của kim loại Ag và Mg ?
c) Sắp xếp những cặp oxi hoá- khử của những chất nói trên theo một thứ tự nhất định về tính chất hoá học.
Người ta phủ một lớp bạc lên một vật bằng đồng có khối lượng 8,84g bằng cách ngâm vật đó trong dung dịch AgNO3. Sau một thời gian lấy vật ra khỏi dung dịch, rửa nhẹ, làm khô, khối lượng của vật là 10,36g.
a) Cho biết các cặp oxi hoá - khử của kim loại trong phản ứng. Vai trò của các chất tham gia phản ứng. Viết phương trình hoá học dạng ion thu gọn.
b) Tính khối lượng bạc phủ trên bề mặt vật bằng đồng. Giả thiết toàn bộ bạc thoát ra đều bám vào vật bằng đồng.
Pha chế dung dịch CuSO4 bằng cách hoà tan 87g CuSO4.5H2O trong nước, thu được 750 ml dung dịch.
a) Tính nồng độ mol của dung dịch CuSO4 đã pha chế.
b) Có bao nhiêu ion Cu2+ và SO42- trong 1 ml dung dịch ?
c) Thêm một lượng mạt sắt dư vào 50 ml dung dịch CuSO4 trên. Hãy cho biết khối lượng các kim loại tham gia và tạo thành sau phản ứng.
Chia 100 g dung dịch muối có nồng độ 6,8% làm hai phần bằng nhau.
- Phần một cho tác dụng với dung dịch NaOH dư, tạo ra một bazơ không tan, làm khô chất này thu được một oxit có khối lượng 2,32 g.
- Phần hai cho tác dụng với dung dịch NaCl dư thu được 2,87 g kết tủa không tan trong dung dịch axit.
a) Xác định công thức hoá học của muối có trong dung dịch ban đầu.
b) Trình bày các phương pháp hoá học điểu chế kim loại từ muối tìm được ở trên.
Ngâm một lá kim loại có khối lượng 50 gam trong dung dịch HCl, sau khi thu được 336 ml H2 (đktc) thì khối lượng lá kim loại giảm 1,68%. Xác định kim loại đã dùng.
Trong một bình kín dung tích không đổi 16,8 lít chứa khí Cl2 (đktc) và một ít bột kim loại M. Sau khi phản ứng hoàn toàn giữa Cl2 và M, áp suất khí trong bình còn lại 0,8 atm, lượng muối tạo thành là 16,25 gam. Nhiệt độ bình không đổi 0°C, thể tích kim loại M và muối rắn của nó không đáng kể. Xác định kim loại M.
a) Phản ứng hóa học xảy ra trong pin điện hóa :
2Cr + 3Cu2+ → 2Cr3+ + 3Cu
Eo của pin điện hóa là :
A. 0,40V
B. 1,08V
C. 1,25V
D. 2,5V
Biết Eo Cu2+/Cu = +0,34; Eo Cr3+/Cr = -0,74 V
b) Phản ứng hóa học xảy ra trong pin điện hóa :
2Au3+ + 3Ni → 2Au + 3Ni2+
Eo của pin điện hóa là :
A. 3,75 V
B. 2,25 V
C. 1,76 V
D. 1,25 V
a. Chất nào sau đây có thể oxi hóa Zn thành Zn2+?
A. Fe
B. Ag+
C. Al3+
D. Ca2+
b. Kim loại Zn có thể khử được các ion nào sau đây?
A. Na+
B. H+
C. Ca2+
D. Mg2+
Trong quá trình pin điện hóa Zn – Ag hoạt động, ta nhận thấy :
A. khối lượng của điện cực Zn tăng
B. Khối lượng của điện cực Ag giảm
C. Nồng độ của ion Zn2+ trong dung dịch tăng
D. Nồng độ của ion Ag+ trong dung dịch tăng
Dưới đây là hình vẽ của 4 sơ đồ pin điện hóa chuẩn. Hãy cho biết sơ đồ nào được vẽ và chú thích đúng, sai. Đề nghị sửa lại những chỗ sai.
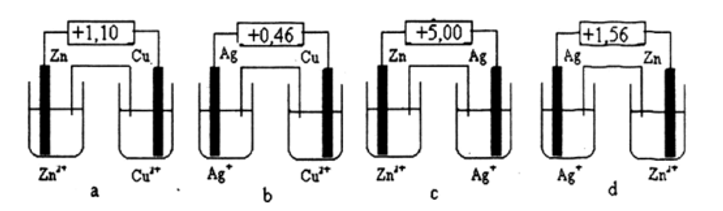
Cho biết Eo (Ag+/Ag) = +0,80 V
Eo (Cu2+/Cu) = +0,34 V
Eo (Zn2+/Zn) = -0,76 V
Khi nhúng một lá Zn vào dung dịch muối Co2+, nhận thấy có một lớp kim loại Co phủ ngoài lá kẽm. Khi nhúng lá Pb và dung dịch muối trên, không nhận thấy hiện tượng nào xảy ra.
a. Kim loại nào có tính khử mạnh nhất trong số 3 kim loại trên
b. Cation nào có tính oxi hóa mạnh nhất trong số 3 cation kim loại trên
c. Sắp xếp cặp oxi hóa – khử của những kim loại trên theo chiều tính oxi hóa của cation tăng dần.
d. Viết phương trình hóa học của phản ứng xảy ra giữa các cặp oxi hóa – khử
Hãy giải thích hiện tượng thí nghiệm: Ngâm một lá Zn nhỏ, tinh khiết trong dung dịch HCl thấy bọt khí H2 thoát ra ít và chậm. Nếu nhỏ thêm vài giọt dung dịch CuSO4 thấy bọt khí H2 thoát ra rất nhiều và nhanh.
Cho cặp oxi hóa – khử sau : Ag+/Ag; Fe2+/Fe; Zn2+/Zn
a) Hãy viết các phản ứng biến đổi qua lại giữa cation kim loại và nguyên tử kim loại trong mỗi cặp
b) Hãy cho biết trong các cặp oxi hóa – khử đã cho, chất nào có tính
1. oxi hóa mạnh nhất?
2. oxi hóa yếu nhất ?
3. Khử mạnh nhất?
4. Khử yếu nhất?
Hãy tính thế điện cực chuẩn của cặp oxi hóa – khử Eo (Zn2+/Zn ). Biết rằng Epđh Zn-Cu = 1,10 V và Eo (Cu2+/Cu ) = +0,34 V
Có những pin điện hóa được tạo thành từ những cặp oxi hóa – khử sau :
a) Pb2+/Pb và Fe2+/Fe
b) Ag+/Ag và Fe2+/Fe
c) Ag+/Ag và Pb2+/Pb
Hãy tính suất điện động chuẩn của mỗi pin điện hóa
Biết rằng : Eo (Ag+/Ag) = +0,80 V
Eo (Pb2+/Pb ) = -0,13 V
Eo (Fe2+/Fe) = -0,44 V
Có những pin điện hóa được ghép bởi những cặp oxi hóa – khử chuẩn sau :
a) Pb2+/Pb và Zn2+/Zn
b) Mg2+/Mg và Pb2+/Pb
Hãy tính thế điện cực chuẩn?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
+) nGlixerol = 0,1 = nY + nZ; nX + 3(nY + nZ) = nNaOH = 0,32; nY = 1,5nX à nX = 0,02; nY = 0,03; nZ = 0,07.
\(\left| \begin{array}{l} {C_{15}}{H_{31}}COOH:x\\ {C_{17}}{H_{33}}COOH:y\\ {C_3}{H_2}:0,1 \end{array} \right. \to \left\{ \begin{array}{l} nNaOH = x + y = 0,32\\ BTH:32x + 34y + 2.0,1 = 2n{H_2}O = 5,3 \end{array} \right. \Rightarrow \left\{ \begin{array}{l} x = 0,24\\ y = 0,08 \end{array} \right.\\\)
\( TH1: {\rm{ \backslash }}[\left| \begin{array}{l} X:{C_{15}}{H_{31}}COOH:0,02\\ Y:{({C_{17}}{H_{33}}COO)_n}{C_3}{H_5}{(OOC{C_{15}}{H_{31}})_{3 - n}}:0,03\\ Z:{({C_{17}}{H_{33}}COO)_m}{C_3}{H_5}{(OOC{C_{15}}{H_{31}})_{3 - m}}:0,07 \end{array} \right. \to 0,03n + 0,07m = 0,08 \Rightarrow ko{\rm{ cap thoa man}}\)
TH2: \(\left| \begin{array}{l} X:{C_{17}}{H_{33}}COOH:0,02\\ Y:{({C_{17}}{H_{33}}COO)_n}{C_3}{H_5}{(OOC{C_{15}}{H_{31}})_{3 - n}}:0,03\\ Z:{({C_{17}}{H_{33}}COO)_m}{C_3}{H_5}{(OOC{C_{15}}{H_{31}})_{3 - m}}:0,07 \end{array} \right. \to 0,03n + 0,07m + 0,02 = 0,08 \Rightarrow \left\{ \begin{array}{l} n = 2\\ m = 0 \end{array} \right.\)
→ mX = 0,02.282 = 5,64
Câu trả lời của bạn
+) BTE: netđ = 4nO2 = 2nSO2 → nSO2 = 4.0,03/2 = 0,06 (mol)
+) nH2SO4 = 2nSO2 + nO = 2. 0,06 + 0,2222m/16 = 0,12 + 0,2222m/16
+) BTNT H → nH2O = nH2SO4 = 0,12 + 0,2222m/16
BTKL: m + 98(0,12 + 0,2222m/16) = (m + 15,36) + 0,06. 64 + 18.(0,12 + 0,2222m/16) → m = 8,64
Câu trả lời của bạn
+) nFe(NO3)2 : a (mol); nCu(NO3)2 = 2a (mol); trong Y là HNO3 : 4NO2 + O2 + H2O → 4HNO3
→ pH = 1 → [H+] = 0,1 → nHNO3 = 0,1.1,2 = 0,12
+) BTN: 2a + 2.2a = 0,12 → a = 0,02 (mol); từ phản ứng trên → nO2 = ¼ nNO2 = 0,03 (mol)
Cu(NO3)2 → CuO + 2NO2 + ½ O2
0,04------------------ 0,08-------0,02 (mol)
2Fe(NO3)2 →Fe2O3 + 4NO2 + ½ O2
0,02----------------------0,04----0,005
KNO3 → KNO2 + ½ O2
x-----------------------0,5x
→ 0,5x + 0,005 + 0,02 = 0,03→ x = 0,01 (mol)
→ m = 0,01.101 + 0,02.180 + 0,04.188 = 12,13
A. 4
B. 2.
C. 3.
D. 1.
Câu trả lời của bạn
(a) Sai vì phân lân cung cấp nguyên tố phốtpho
(b) Đúng vì: FeCl2 + 3AgNO3 → 2AgCl + Ag + Fe(NO3)3 (2 chất Ag, AgCl là chất kết tủa)
(c) Sai vì tạo kết tủa, không tạo khí: 2NaHCO3 + Ba(OH)2 → BaCO3 + Na2CO3 + 2H2O
(d) Sai vì trong môi trường khí Cl2 không phải dung dịch chất điện ly.
Câu trả lời của bạn
+) \(\frac{{{M}_{Y}}}{{{M}_{X}}}=\frac{{{n}_{X}}}{{{n}_{Y}}}\Leftrightarrow 1,4=\frac{a}{{{n}_{Y}}}\Rightarrow {{n}_{Y}}=\frac{5}{7}a\) ; nCO2 = 0,22 (mol)
+Y: \(\left| \begin{align} & C{{H}_{2}}:0,22 \\ & {{H}_{2}}:b(mol) \\ \end{align} \right.\)→ npi = nBr2 = nY – nH2/ tách ra = 5/7a – b = 0,08 (1)
→ nH2O = b + 0,22 ; Xét hỗn hợp X: BTH: 2nH2O = 6nC2H6 + 2(nC2H2 + nC4H2 + nH2)
→ 2. (b + 0,22) = 6. 0,05 + 2(a – 0,05) à 2a – 2b = 0,24 (2)
Từ 1, 2 ta có: a = 0,14; b = 0,02
(1) E + 3NaOH à 2X + Y + Z
(2) F + 2NaOH à 2X + Z
(3) X + HCl à T + NaCl
(4) T + Z à G + H2O
Biết E, F chỉ chứa chức este, trong phân tử số nguyên tử O bằng số nguyên tử C, MF<ME<180.
Cho các phát biểu sau:
(a) Chất T có nhiệt độ sôi cao hơn ancol metylic.
(b) 1 mol chất Z tác dụng Na dư thu được 1 mol H2.
(c) Chất Y tác dụng H2SO4 loãng thu được axit axetic.
(d) Chất G là hợp chất hữu cơ đa chức.
(e) Trong phân tử X và Z đều không có liên kết pi.
Số phát biểu đúng là
A. 3 B. 1 C. 4. D. 2.
Câu trả lời của bạn
+) từ phản ứng (1) E là este 3 chức: C6H8O6; Pứ (2) F lè este 2 chức: C4H6O4.
E có CTCT: HCOO – CH2 – COO – C2H4 – OOCH; X: HCOONa; Y: HO – CH2 – COONa; Z: C2H4(OH)2
F: (HCOO)2C2H4; T: HCOOH; G: HCOO – CH2 – CH2 – OH.
(a) Đúng vì T (HCOOH) có liên kết hidro bền hơn so với ancol metylic (CH3OH)
(b) Đúng vì Z là C2H4(OH)2 có 2 nhóm OH: C2H4(OH)2 + 2Na à C2H4(ONa)2 + H2.
(c) Sai vì tạo ra HO – CH2 – COOH không phải là axit axetic (CH3COOH).
(d) Sai vì G là hợp chất tạp chức ( este và axit)
(e) Sai vì X có có 1 liên kết pi ở nhóm chức
A. 3.
B. 5.
C. 2.
D. 4.
Câu trả lời của bạn
(a) Sai vì triolein chất béo ko no nên ở trạng thái lỏng.
(b) Đúng vì Lysin + Quỳ tím → Xanh; Axit Glutamic + Quỳ tím → đỏ
(c) Đúng vì PVC có cấu tạo: (-CH2 – CHCl-)n.
(d) Đúng vì tinh dầu chuối là isoamyl axetat (CH3COOCH2CH2CH(CH3)2).
(e) Sai vì sản phẩm tạo ra muối natri của các α- aminoaxit.
(a) Kim loại M là Zn
(b) giá trị của m là 19,75 gam.
(c) Nếu thời gian điện phân là 3474 giây thì nước bắt đầu điện phân ở anot.
(d) Bỏ qua sự điện ly của nước, dung dịch Y chứa các ion Na+, H+, SO42-.
Số nhận định đúng là
A. 3 B. 1 C. 2. D. 4.
Câu trả lời của bạn
+) netđ = IT/F = 0,14 (mol).
+) TH1: NaCl điện phân hết trước: netđ = 2nCl2 + 4nO2 = 0,14
nCl2 + nO2 = 0,09 → nCl2 = 0,11; nO2 = -0,01 (loại)
+) TH2: MSO4 điện phân hết trước: netđ = 2nCl2 = 0,14 → nCl2 = 0,07 (mol); nH2 = 0,09 - 0,02 = 0,02 (mol)
Δm = mKL + mCl2 + mH2 → 8,26 = mM + 0,07.71 + 2.0,02 → M = 3,25 (g)
Xét catot: netđ = 2nM + 2nH2 → 0,14 = 2nM + 2.0,02 → nM = 0,05 → M = 3,25/0,05 = 65
à M là Zn à (a) Đúng
+) khi t = 5404 = 2. 2702 → netđ = 2.0,14 = 0,28 (mol)
- Catot: netđ = 2nM + 2nH2 → 0,28 = 2.0,05 + 2nH2 à nH2 = 0,09 (mol)
- Anot: netđ = 2nCl2 + 4nO2 = 0,28; nCl2 + nO2 + nH2 = 0,21 → nCl2 + nO2 = 0,21 – 0,09 = 0,12
→ nCl2 = 0,1; nO2= 0,02
→ m = mZnSO4 + mNaCl = 0,05.161 + 0,2.58,5 = 19,75 à (b) đúng
+) t = 3474 → netđ = 0,18
- Anot: netd = 0,18 < 2nCl2 = 2.0,1 = 0,2 → Clo chưa điện phân hết → H2O chưa bị điện phân → (c) Sai
→ do đp t = 2702 thì clo vẫn còn dư nên dd Y: SO42-, Na+, Cl-, OH- → (d) Sai;
A. 19,02%.
B. 22,15%.
C. 17,04%.
D. 14,67%.
Câu trả lời của bạn
+) mkt = mAgCl + mAg → 103,35 = 0,66.143,5 + 108nAg → nAg = 0,08; BTE: nAg = nFe2+ = 0,08
+) Xét T: nOH/kết tủa = nHCl = 0,29.2 = 0,58 = n(đt âm)
+) Xét rắn oxit: n(đt âm) = 2nO = nOH + 0,08 → nO = (0,58 + 0,08)/2 → nO = 0,33 → mKL = 17,6 – 0,33.16 = 12,32 (g)
→ mT = m + 5,82 = mKL + mOH = 12,32 + 0,58.17 à m = 16,36 (g)
+) BTĐT trong dung dịch muối Q: nđt (+) = nOH/T + nNH4 + nK = 0,58 + 0,02 + 0,08 = 0,68 (mol) = nđt (-) = nCl + nNO3
→ nNO3 = 0,68 – 0,66 = 0,02
→ mmuối = mKL + mK + mCl + mNO3 + mNH4 = 12,32 + 0,08.39 + 0,66.35,5 + 0,02.62 + 0,02.18 = 40,47
+) BTNTH: nHCl = 4nNH4 + 2nH2O ó 0,66 = 4.0,02 + 2nH2O → nH2O = 0,29 (mol)
+) BTKL: mV + mKNO3 + mHCl = mQ + mKhí + mH2O
→ 16,36 + 0,08.101 + 0,66.36,5 = 40,47 + mkhi + 0,29.18 → mkhi = 2,84 à Mtb khí = 31,5
TH1: 2 khí (N2, N2O) → nN2 = 0,07; nN2O = 0,02
+) BTNT N: 2nCu(NO3)2 + nKNO3 = 2nkhí + nNH4 + nNO3/muối
→ 2nCu(NO3)2 + 0,08 = 2.0,09 + 0,02 + 0,02 → nCu(NO3)2 = 0,07 (mol)
+) Trong V: mV = mKL + mO + mNO3 → 16,36 = 12,32 + 16nO + 62. 2.0,07 à nO < loại.
TH2: TH1: 2 khí (NO, N2O) → nNO = 0,08; nN2O = 0,01
+) BTNT N: 2nCu(NO3)2 + nKNO3 = nNO + 2nN2O + nNH4 + nNO3/muối
→ 2nCu(NO3)2 + 0,08 = 0,08 + 2.0,01 + 0,02 + 0,02 à nCu(NO3)2 = 0,03 (mol)
+) Trong V: mV = mKL + mO + mNO3 → 16,36 = 12,32 + 16nO + 62. 2.0,03→ nO = 0,02 à nCuO = 0,02.
→ \(\sum{{{n}_{Cu}}=0,02+0,03=0,05}\)
\(\left\{ \begin{array}{l} M{g^{2 + }}:x\\ F{e^{2 + }}:0,08\\ F{e^{3 + }}:y\\ C{u^{2 + }}:0,05 \end{array} \right. \to \left\{ \begin{array}{l} 24x + 56y + 0,05.64 + 0,08.56 = 12,32\\ 2x + 3y + 2.0,08 + 2.0,05 = {n_{OH}} = 0,58 \end{array} \right. \Rightarrow \left\{ \begin{array}{l} x = 0,1\\ y = 0,04 \end{array} \right.\)
%mMg = 0,1.24/16,36 = 14,67%.

Câu trả lời của bạn
Câu trả lời của bạn
\(Fe \to \left\{ \begin{array}{l}
FeS{O_4}\\
Cu
\end{array} \right. \Rightarrow {m_{{\rm{dd}}}} \downarrow = 64a - 56a = 8a = 0.8 \Rightarrow a = 0,1 \Rightarrow {m_{Fe}} = 6,4.g\)
Câu trả lời của bạn
\(100.g.Fe + \left\{ \begin{array}{l}
Cu{\left( {N{O_3}} \right)_2}:0,02\\
AgN{O_3}:0,02
\end{array} \right.\)
Câu trả lời của bạn
\(Fe+\left\{ \begin{align}
& Cu{{\left( N{{O}_{3}} \right)}_{2}}:0,05 \\
& AgN{{O}_{3}}:0,02 \\
\end{align} \right.\)
Khối lượng thanh sắt tăng lên bằng khối lượng bạc và đồng bám vào trừ khối lượng sắt pu 0,02.108+64.0,05-0,01.56-56.0,05=2.g
Câu trả lời của bạn
- khối lượng thanh Zn giảm 0,5 g suy ra khối lương muối tăng lên 0,5 g suy khối lượng muối ban đầu 13,6-0,5=13,1.g
Câu trả lời của bạn
\(\left\{ \begin{array}{l}
Fe:a\\
Zn:b
\end{array} \right. \to 64a - 56a = 65b - 64b \Rightarrow 8a = b \Rightarrow \% {m_{Zn}} = \frac{{65.8}}{{65.8 + 56}}.100 = 90,27\% .g\)
Câu trả lời của bạn
Có ngay muối M(NO3)2 :0,1 .mol\(M{{\left( N{{O}_{3}} \right)}_{2}}~:0,1\text{ }.mol\Rightarrow {{M}_{M{{\left( N{{O}_{3}} \right)}_{2}}}}=188\Rightarrow M:64.Cu\)
Câu trả lời của bạn
\(0,01.mol.Ba \to m.g.\left\{ \begin{array}{l}
Cu{(OH)_2}:0,01\\
BaS{O_4}:0,01
\end{array} \right. \Rightarrow m = 3,31.g\)
Câu trả lời của bạn
\(0,2.mol.Ba \to \left\{ \begin{array}{l}
Fe{(OH)_2}:0,15\\
BaS{O_4}:0,15
\end{array} \right. \to m.g.\left\{ \begin{array}{l}
F{e_2}{O_3}:0,075\\
BaS{O_4}:0,15
\end{array} \right. \Rightarrow m = 46,95.g\)
Câu trả lời của bạn
Câu trả lời của bạn
\(\left\{ \begin{array}{l}
SO_4^{2 - }:0,1\\
A{l^{3 + }}:a\\
C{u^{2 + }}:b
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
3a + 2b = 0,2\\
64(0,1 - b) - 27a = 1,38
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
a = 0,02\\
b = 0,07
\end{array} \right. \Rightarrow {m_{Cu \uparrow }} = 0,03.64 = 1,92\)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *