Ở bài học trước chúng ta đã tìm hiểu và biết cách tính nồng độ dung dịch. Nhưng làm thế nào để pha chế dung dịch theo nồng độ cho trước? Chúng ta cùng tìm hiểu nội dung bài học sau:
Đầu tiên ta xác định chất tan, dung môi là chất nào?
Có 2 kiểu pha chế:
Bài tập 1: Từ muối CuSO4, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 50 gam dung dịch CuSO4 10%.
a) Tính toán
Đề bài cho khối lượng chất tan là 50 gam dung dịch CuSO4 và nồng độ phần trăm của dung dịch C% = 10%.
Vận dụng công thức tính khối lượng chất tan ta có:
\(m_{CuSO_{4}} = \frac{{C\% .{m_{dd}}}}{{100\% }}\) = \(\frac{{10\%.50 }}{{100\% }} = 5(gam)\)
Các em lưu ý tới công thức tính khối lượng dung dịch là mdung dịch = mdung môi + mchất tan
Có khối lượng chất tan (5gam CuSO4), có khối lượng dung dịch (50 gam). Như vậy ta suy ra được khối lượng dung môi (nước)
mdung dịch = mdung môi + mchất tan ⇒ mdung môi = mdung dịch - mchất tan = 50 - 5 = 45 (gam)
Vậy khối lượng nước cần dùng cho sự pha chế là 45 gam.
b) Cách pha chế:
Hình 1: Quá trình pha chế 50 gam dung dịch CuSO4 10%
Bài tập 2: Từ muối CuSO4, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 50 ml dung dịch CuSO4 1M.
a) Tính toán
Từ công thức tính nồng độ mol của dung dịch nhận thấy có chứa 3 ẩn là số mol (n), thể tích (V) và nồng độ mol (CM).
Đề bài cung cấp 2 dữ kiện là thể tích dung dịch và nồng độ mol (1mol/l)
Vì đơn vị của nồng độ mol là mol/lít nên dữ kiện ml phải đổi về lít: 50 ml = \(\frac{{50}}{{1000}} = 0,05(lit)\)
Cho nguyên tử khối của Cu = 64, S = 32, O = 16
Cụ thể như sau:
Số mol CuSO4 chứa trong 50 ml dung dịch CuSO4 1M là:
\(n = {C_M}.V = 1.0,05 = 0,05(mol)\)
Khối lượng CuSO4 chứa trong 50 ml dung dịch CuSO4 1M là:
\({m_{CuS{O_4}}} = {n_{CuS{O_4}}}.{M_{CuS{O_4}}} = 0,05.(64 + 32 + 16.4) = 8(gam)\)
Vậy khối lượng CuSO4 cần thêm vào là 8 gam để tạo 50 ml dung dịch CuSO4 1M.
b) Cách pha chế
Bước 2: Tiến hành pha chế
Hình 2: Quá trình pha chế 50 ml dung dịch CuSO4 1M
Bài tập 1: Từ muối MgSO4, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 100ml dung dịch MgSO4 0,4 M từ dung dịch MgSO4 2M.
a) Tính toán
Từ công thức tính nồng độ mol của dung dịch nhận thấy có chứa 3 ẩn là số mol (n), thể tích (V) và nồng độ mol (CM).
Đề bài cung cấp 2 dữ kiện là thể tích dung dịch (100 ml) và nồng độ mol (0,4M)
Lưu ý: Vì đơn vị của nồng độ mol là (mol/lit) nên thể tích phải đổi từ ml sang lít.
Cho nguyên tử khối của Mg = 24, S = 32, O = 16
Cụ thể như sau:
Đổi 100ml thành 0,1 lít
Số mol chất tan có trong 100ml dung dịch 0,4M:
\({n_{MgS{O_4}}} = {C_M}.V = 0,4.0,1 = 0,04(mol)\)
+ Thể tích dung dịch MgSO4 2M trong đó có 0,04 mol MgSO4:
\(V' = \frac{n}{{{C_M}'}} = \frac{{0,04}}{2} = 0,02(lit)=20(ml)\)
b) Cách pha chế
Hình 3: Quá trình pha loãng dung dịch MgSO4 2M
Bài tập 2: Từ muối NaCl, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 150g dung dịch NaCl 2,5% từ dung dịch NaCl 10%.
a) Tính toán
Khối lượng NaCl trong 150g dung dịch NaCl 2,5% là:
\({m_{NaCl}} = \frac{{C\% .{m_{{\rm{dd}}}}}}{{{\rm{100\% }}}} = \frac{{2,5.150}}{{100}} = 3,75(g)\)
Khối lượng dung dịch NaCl ban đầu chứa 3,75g NaCl là:
\({m_{{\rm{dd}}}} = \frac{{{m_{ct}}.100\% }}{{C\% }} = \frac{{3,75.100}}{{10}} = 37,5(g)\)
Khối lượng nước cần dùng là:
mdm= 150 – 37,5 = 112,5(g)
b) Cách pha chế
Lưu ý: Khi cân dung dịch ta cân cả dung dịch và bình chứa dung dịch nên ta sẽ cân riêng bình đựng, sau đó lấy tổng khối lượng trừ đi khối lượng bình là ra được khối lượng dung dịch chứa trong bình. Cụ thể như bài này. Khối lượng bình rỗng là 50 gam, tổng khối lượng bình và dung dịch là 87,8 gam. Như vậy ta vừa cân được 87,5 - 50 = 37,5 gam dung dịch.
Hình 4: Đầu tiên ta cân bình rỗng
Hình 5: Sau đó, cân cả khối lượng của bình và dung dịch
Hình 6: Quá trình pha chế dung dịch NaCl 2,5%
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 43có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Muốn pha 300ml dung dịch NaCl 3M thì khối lượng NaCl cần lấy là:
Muốn pha 150g dung dịch CuSO4 2% từ dung dịch CuSO4 20% thì khối lượng dung dịch CuSO4 20% cần lấy là:
Có 60g dung dịch NaOH 20%. Khối lượng NaOH cần cho thêm vào dung dịch trên để được dung dịch 25% là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 43.
Bài tập 1 trang 149 SGK Hóa học 8
Bài tập 2 trang 149 SGK Hóa học 8
Bài tập 3 trang 149 SGK Hóa học 8
Bài tập 4 trang 149 SGK Hóa học 8
Bài tập 5 trang 149 SGK Hóa học 8
Bài tập 43.1 trang 59 SBT Hóa học 8
Bài tập 43.2 trang 59 SBT Hóa học 8
Bài tập 43.3 trang 59 SBT Hóa học 8
Bài tập 43.4 trang 59 SBT Hóa học 8
Bài tập 43.5 trang 59 SBT Hóa học 8
Bài tập 43.6 trang 59 SBT Hóa học 8
Bài tập 43.7 trang 59 SBT Hóa học 8
Bài tập 43.8 trang 60 SBT Hóa học 8
Bài tập 43.9 trang 60 SBT Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Muốn pha 300ml dung dịch NaCl 3M thì khối lượng NaCl cần lấy là:
Muốn pha 150g dung dịch CuSO4 2% từ dung dịch CuSO4 20% thì khối lượng dung dịch CuSO4 20% cần lấy là:
Có 60g dung dịch NaOH 20%. Khối lượng NaOH cần cho thêm vào dung dịch trên để được dung dịch 25% là:
Để pha 100g dung dịch CuSO4 4% thì khối lượng nước cần lấy là:
Muốn pha 250ml dung dịch NaOH nồng độ 0,5M từ dung dịch NaOH 2M thì thể tích dung dịch NaOH 2M cần lấy là:
Bằng cách nào sau đây có thể pha chế được dung dịch NaCl 15%.
Để tính nồng độ mol của dung dịch KOH, người ta làm thế nào?
Để tính nồng độ phần trăm của dung dịch H2SO4, người ta làm thế nào?
Muốn pha 400ml dung dịch CuCl2 0,2M thì khối lượng CuCl2 cần lấy là
Cho 3 mẫu thử mất nhãn là Fe2O3,CuO, Al2O3. Để phân biệt mấy dung dịch trên, cần sử dụng mấy chất để phân biệt? là những chất nào
Làm bay hơi 60 g nước từ dung dịch có nồng độ 15% được dung dịch mới có nồng độ 18%. Hãy xác định khối lượng của dung dịch ban đầu?
Đun nhẹ 20 g dung dịch CuSO4 cho đến khi nước bày hơi hết, người ta thu được chất rắn màu trắng là CuSO4 khan. Chất này có khối lượng là 3,6 g. Hãy xác định nồng độ phần trăm của dung dịch CuSO4
Cân lấy 10,6 g Na2CO3 cho vào cốc chia độ có dung tích 500 ml. Rót từ từ nước cất vào cốc cho đến vạch 200 ml. Khuấy nhẹ cho Na2CO3 tan hết, ta được dung dịch Na2CO3. Biết 1 ml dung dịch này cho khối lượng là 1,05 g. Hãy xác định nồng độ phần trăm (C%) và nồng độ mol của dung dịch vừa pha chế được?
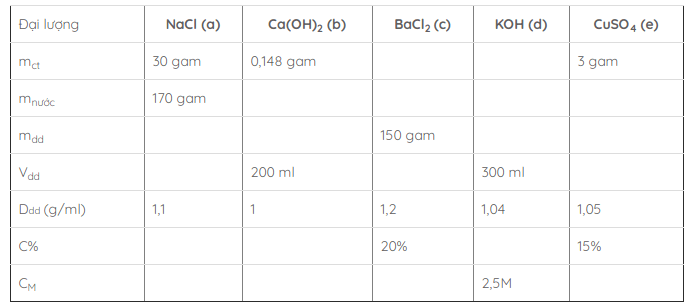
Hãy điền những giá trị chưa biết vào những ô trống trong bảng, bằng cách thực hiện các tính toán theo mỗi cột?
Tìm độ tan của một muối trong nước bằng phương pháp thực nghiệm người ta có được những kết quả sau:
- Nhiệt độ của dung dịch muỗi bão hòa là 200C.
- Chén sứ nung có khối lượng 60,26 g.
- Chén sứ đựng dung dịch muối có khối lượng 86,26 g.
- Khối lượng chén nung và muối kết tinh sau khi làm bay hết hơi nước là 66,26 g.
Hãy xác định độ tan của muối ở nhiệt độ 200C.
Từ dung dịch MgSO4 2M làm thế nào pha chế được 100ml dung dịch MgSO4 0,4M?
Từ dung dịch NaCl 1M, hãy trình bày cách pha chế 250ml dung dịch NaCl 0,2M.
Hãy trình bày cách pha chế 150ml dung dịch HNO3 0,25M bằng cách pha loãng dung dịch HNO3 5M có sẵn.
Từ glucozo (C6H12O6) vào nước cất, hãy trình bày cách pha chế 200g dung dịch glucozo 2%.
Hãy trình bày cách pha chế các dung dịch theo những yêu cầu sau:
a) 250ml dung dịch có nồng độ 0,1M của những chất sau:
- NaCl
- KNO3
- CuSO4
b) 200g dung dịch có nồng độ 10% của mỗi chất nói trên.
Có những dung dịch ban đầu như sau:
a) NaCl 2M
b) MgSO4 0,5M
c) KNO3 4M
Làm thế nào có thể pha chế được những dung dịch theo những yêu cầu sau:
- 500m dung dịch NaCl 0,5M
- 2 lit dung dịch MgSO4 0,2M
- 50ml dung dịch KNO3 0,2M.
Từ những muối và nước cất, hãy trình bày cách pha chế các dung dịch sau:
a) 2,5kg dung dịch NaCl 0,9%
b) 50g dung dịch MgCl2 4%
c) 250g dung dịch MgSO4 0,1%
Có 2 lọ đựng dung dịch H2SO4. Lọ thứ nhất có nồng độ 1mol/l, lọ thứ hai có nồng độ 3 mol/l. Hãy tính toán và trình bày cách pha chế 50ml dung dịch H2SO4 có nồng độ 1,5mol/l từ 2 dung dịch axit đã cho.
Cần dùng bao nhiêu ml dung dịch NaOH 3% có khối lượng riêng là 1,05g/ml và bao nhiêu mililit dung dịch NaOH 10% có khối lượng riêng là 1,12g/ml để pha chế được 2 lít dung dịch NaOH 8% có khối lượng riêng là 1,10g/ml.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Dung dịch HCl có nồng độ 36% (D=1,19 g/ml) và dung dịch HCl 12% (D=1,04 g/ml) tính khối lượng mỗi dung dịch để pha chế thành 22 dung dịch HCl 20% (D=1,1g/ml)
Câu trả lời của bạn
Tính số gam muối và nước cần để pha chế thành
a) 120g dung dịch nồng độ 5%
b) 25g dung dịch có nồng độ 0.5%
Mình học lớp 9 mà mới vô học nên ôn lại :< Help me :<
Câu trả lời của bạn
a) m muối=m chất tan= \(120.\dfrac{5\%}{100\%}=6g\)
mH2O=120-6=114g
b) m muối=m chất tan=\(25.\dfrac{0,5\%}{100\%}=0,125g\)
mH2O=25-0,125=24,875g
Hoà tan hết 71g P2O5 vào H2O thu đc dd axit có nồng độ 46% tính khối lượng nước đã dùng
Câu trả lời của bạn
Ta có: nP2O5= 71/142= 0,5(mol)
Ta có: PTHH: P2O5 +3H2O -> 2H3PO4
- Gọi mH2O là x (g)
=> nH3PO4= 2.0,5= 1(mol)
=> mH3PO4= 1.98= 98(g)
=> \(C\%_{ddH_3PO_4}=\dfrac{98}{98 +x}.100=46\%\)
Gỉai ptrình trên, ta được: \(x\approx115,043\)
=> mH2O ~ 115,043(g)
giúp vs
trong phòng thí nghiệm có chứa dung dịch HCl 0,8M,dung dịch NaOH 0,4M,nước cất,các dụng cụ cần thiết coi như có đủ.Hãy tính toán và trình bày cách pha chế 500 ml dung dịch HCl 0,2M và NaCl 0,25M
mai phải nộp rồi,làm gấp
PLEASE
Câu trả lời của bạn
Bạn cho mình hỏi 500ml ddHCl 0,2 M và 500ml ddNaCl 0,25M
hay là hai cái cộng lại bằng 500ml![]()
Người ta trộn 8g chất lỏng này vs 6g chất lỏng khác có khối lượng riêng nhỏ hơn nó là 0,2g/cm3 để dc hh có D = 0,7g/cm3. Tìm khối lượng riêng của mỗi chất lỏng ? bik D=m/V
Câu trả lời của bạn
-Gọi 8(g) chất rắn có khối lượng kí hiệu D1
Gọi 6(g) chất rắn có khối lượng kí hiệu D2
Theo sơ đồ đường chéo ta có:
\(\Rightarrow\)\(\dfrac{8}{6}=\dfrac{0,7-D2}{D1-0,7}\)
Mà D1=D2+0,2
Theo vào hệ pt: \(\Rightarrow\)D2=0,586g/cm3
\(\Rightarrow\)D1=D2+0,2=0,786g/cm3
Vậy 8(g) chất lỏng có D1=0,786g/cm3 và 6(g) chất lỏng có D2=0,586g/cm3
Chúc bạn học tốt!
bác sĩ thưởng khuyên sử dụng 1 gói Oresol ( có nồng độ phần trăm dd là 2% ) sau mỗi lần tiêu chảy. Biết rằng mỗi gói có chứa 4g thuốc dạng bột. Cần pha 1 gói thuốc vào bao nhiu ml nước để sử dụng ?
Câu trả lời của bạn
Áp dụng công thức tính nồng độ % ta có
\(C\%=\dfrac{m_{chattan}}{m_{dd}}.100\Rightarrow m_{dd}=\dfrac{m_{chattan}}{C\%}.100\)= \(\dfrac{4}{2\%}.100=200g\)
mà mdd= mchattan + mH2O
=> mH2O = 196g
=> VH2O = 196ml (Vì 1g nước có thể tích là 1ml)
Bài 3: Xác định FeSO4 .7H2O cần lấy để hòa tan vào 278g H2O thu đc dd FeSO4 4%
Bài 4: Hòa tan 36g CuSO4 vào H2O thu đc 165,84ml dd CuSO4 . Tính C% dd thu đc biết khối lượng riêng của dd=1,206g/ml
Câu trả lời của bạn
Bài 4 nha bạn
cần lấy bao nhiêu gam tinh thể cuso4.5h2o và đ cuso4 5% để khi trộn vào nhau thì thu đc 400g dd cuso4 10%
Câu trả lời của bạn
Gọi khối lượng của CuSO4.5H2O và dung dịch CuSO4 5% cần lấy là x, y ta có:
x + y=400 (1)
nCuSO4.5H2O = \(\dfrac{x}{250}\)
=> mCuSO4 (1) = \(\dfrac{16x}{25}\)
mCuSO4 (5%) = y.5% = 0,05y
mCuSO4 (10%) = 400.10% = 40
=> \(\dfrac{16x}{25}\) + 0,05y = 40 (2)
Từ (1) và (2) ta có hệ \(\left\{{}\begin{matrix}x+y=400\\\dfrac{16x}{25}+0,05y=40\end{matrix}\right.\)
<=> \(\left\{{}\begin{matrix}x=\dfrac{2000}{59}\\y=\dfrac{21600}{59}\end{matrix}\right.\)
Xác định khối lượng KCl kết tinh đc sau khi lm nguội 604 g đbh KCl ở \(80^0\) xuống \(20^0\) .\(S_{KCl}\) ở \(80^0\) =51g ở \(20^0\) là 34 g
Câu trả lời của bạn
Ở 80oC: 51(g) KCl + 100(g) H2O => 151(g) dung dịch KCl bào hòa
=> x (g) KCl + y (g) H2O ==> 604 (g) dung dịch KCl bão hòa
=> {x=604×51151=204(g)y=604×100151=400(g){x=604×51151=204(g)y=604×100151=400(g)
Ở 20oC: 34(g) KCl + 100(g) H2O => Dung dịch bão hòa
=> a (gam) KCl + 400 (g) H2O => Dung dịch bão hòa
=> a = 400×34100=136(gam)400×34100=136(gam)
=> Khối lượng KCl kết tinh: 204 - 136 = 68 (gam)
Để hòa tan 3,6 gam Magie phải dùng bao nhiêu ml dung dịch hỗn hợp HCl 1M và H2SO4 0.7M
Câu trả lời của bạn
Mg + 2HCl ->MgCl2 + H2
Mg + H2SO4 -> MgSO4 + H2
nMg=\(\dfrac{3,6}{24}=0,15\left(mol\right)\)
Gọi x là V hh dung dịch
\(\dfrac{1}{2}\)x+0,7x=0,15
=>x=0,125 hay 125ml
Bài 6:
Xác định lượng SO3 và lượng H2SO4 49% để trộn thành 450 gam dung dịch H2SO4 73,5%.
Bài 7:
Khi cho a gam dung dịch H2SO4 nồng độ A% tác dụng với một lượng hỗn hợp 2 kim loại Na và Mg (Dùng dư) thì khối lượng khí H2 tạo thành là 0,05a gam. Tính A.
Bài 8:
Hòa tan hoàn toàn 10,2 gam một kim loại oxit hóa trị III cần 331,8 gam dung dịch H2SO4 thì vừa đủ. Dung dịch sau phản ứng có nồng độ 10 %.
A, Tìm tên kim loại.
B, Tính C% của dung dịch axit.
Bài 9:
Cho 600 gam dung dịch CuSO4 10 % bay hơi ở 200C tới khi dung dịch bay hết 400 gam nước. Tính khối lượng CuSO4.5H2O kết tinh. Biết dung dịch bão hòa chứa 20% CuSO4 ở 200C.
Bài 10:
Thêm dần dung dịch KOH 33,6% vào 40,3 ml dung dịch HNO3 37,8% (D = 1,24 g/ml) đến khi trung hòa hoàn toàn, thu được dung dịch A. Hạ nhiệt độ về 00C thu được dung dịch B có nồng độ 11,6% và khối lượng muối tách ra là m gam.
A, Tính m.
B, Dung dịch B là dung dịch bão hòa hay chưa bão hòa?
Câu trả lời của bạn
8.
\(m_{H_2SO_4}=\dfrac{10.331,8}{100}=33,18\left(g\right)\)
\(n_{H_2SO_4}=\dfrac{33,18}{98}=0,3\left(mol\right)\)
Gọi R là kim loại cần tìm
cthc: \(R_2O_3\)
Pt: \(R_2O_3+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2O\)
\(2M_R+48\) 3mol
10,2 g 0,3mol
\(\Rightarrow\dfrac{2M_R+48}{10,2}=\dfrac{3}{0,3}\)
\(\Rightarrow M_R=27\)
Vậy R là Nhôm ( Al )
b) \(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,1mol 0,3mol
Lập tỉ số: \(n_{Al_2O_3}:n_{H_2SO_4}=0,1=0,1\)
\(C\%_{H_2SO_4}=\dfrac{0,3.98.100}{331,8}=8,86\%\)
Bài 1:
Cho các chất sau: H2O, KOH, K2O, CO2, HCl, FeCl2, CH3COONa. Hãy cho biết những cặp chất nào có thể tác dụng được với nhau. Viết phương trình hóa học.
Bài 2:
Nêu hiện tượng, giải thích và viết phương trình hóa học xảy ra khi:
A, Sục khí CO2 từ từ vào dung dịch nước vôi.
B, Cho từ từ dung dịch HCl vào dung dịch Na2CO3.
C, Cho từ từ dung dịch Na2CO3 vào dung dịch HCl.
D, Cho từ từ dung dịch NaOH vào dung dịch AlCl3.
E, Cho từ từ dung dịch AlCl3 vào dung dịch NaOH.
Bài 3:
Trình bày cách pha chế 400g dung dịch CuSO4 10 % từ CuSO4.5H2O và nước (Các dungh cụ cần thiết coi như có đủ).
Bài 4:
Bằng kiến thức hóa học hãy giải thích các cách làm sau đây:
A, Khi muối dưa người ta thường chọn dưa già, rửa sạch phơi héo và khi muối có cho thêm một ít đường?
B, Khi ăn cơm, càng nhai kỹ càng thấy ngọt?
C, Khi bị say sắn người ta thường uống nước đường (Saccarozơ)
D, Khi nấu cơm nếp thường cho ít nước hơn khi nấu cơm tẻ?
Bài 5:
Cân bằng các phản ứng hóa học sau:
1. Cu + H2SO4 (đặc) –t0-> CuSO4 + SO2 + H2O
2. FeS2 + O2 –t0-> Fe2O3 + SO2
3. FexOy + HNO3 --> Fe(NO3)3 + NO + H2O
4. Al + Fe2O3 –t0-> Al2O3 + FenOm
Câu trả lời của bạn
Bài 1:
Cho các chất sau: H2O, KOH, K2O, CO2, HCl, FeCl2, CH3COONa. Hãy cho biết những cặp chất nào có thể tác dụng được với nhau. Viết phương trình hóa học.
\(K_2O+H_2O\rightarrow2KOH\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
\(KOH+HCl\rightarrow KCl+H_2O\)
\(2KOH+FeCl_2\rightarrow Fe\left(OH\right)_2+2KCl\)
\(K_2O+CO_2-->K_2CO_3\)
\(K_2O+2HCl-->2KCl+H_2O\)
\(CH_3COONa+HCl-->CH_3COOH+NaCl\)
Bài 2:
Nêu hiện tượng, giải thích và viết phương trình hóa học xảy ra khi:
A, Sục khí CO2 từ từ vào dung dịch nước vôi.
Hiện tượng: Xuất hiện kết tủa trắng trong dung dịch, kết tủa dâng lên đến cực đại rồi tan dần đến hết.
Giai thích: CO2 td với dd Ca(OH)2 tạo kết tủa CaCO3 màu trắng, lượng CO2
dư tiếp tục tác dụng làm kết tủa tan ra tạo dung dịch trong suốt Ca(HCO3)2
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
Bài 1:a)Hãy tính toán và nêu cách pha chế 500ml dd NaCl 0,9% (d=1,009g/cm3) (nước muối sinh lý) từ muối ăn nguyên chất và nước cất
b)Nêu các cách điều chế NaOH và Mg(OH)2 từ những loại hợp chất khác nhau và chỉ bằng một phản ứng
Bài 2:a)Hòa tan m gam tinh thể Na2CO3.5H2O vào V ml dd Na2CO3 C% (khối lượng riêng bằng D g/ml) thu được dd X. Lập công thúc tính nồng % của dd X theo m, V, C% và D
b)Hòa tan hết 3,2 gam oxit M2Om (M là kim loại) trong một lượng vừa đủ dd H2SO4 10% thu được dd muối có nồng độ 12,9%. Sau phản ứng đem cô bớt dd và làm lạnh nó, thu được 7,868 gam tinh thể muối với hiệu suất kết tinh là 70%. Xác định công thức của tinh thể muối đó
Bài 3:Nung a gam Cu trong V lít O2 đến phản ứng hoàn toàn thu được chất rắn A. Đun nóng A trong b gam dd H2SO4 98% (lượng vừa đủ) sau khi tan hết được dd B chứa 19,2 gam muối và khí SO2. Cho khí SO2 hấp thụ hoàn toàn bởi 300ml dd NaOH 0,1M thu được 2,3gam hỗn hợp 2 muối. Tính a, b, và V (ở đktc)
Bài 4:A là dd H2SO4 0,2M, B là dd H2SO4 0,5M. Phải trộn A và B theo tỷ lệ thể tích như thế nào để được dd H2SO4 0,3M
Bài 5:Rót 400ml dd BaCl2 5,2% (D=1,003g/ml) vào 100ml dd H2SO4 20% (D=1,4g/ml). Xác định nồng độ % các chất trong dd còn lại sau khi tách bỏ kết tủa
Câu trả lời của bạn
Bài 2b:
M2Om+mH2SO4\(\rightarrow\)M2(SO4)m+mH2O
-Giả sử có 1mol M2Om phản ứng.
M2Om+mH2SO4\(\rightarrow\)M2(SO4)m+mH2O
1mol\(\rightarrow\)mmol...............1mol
\(m_{dd_{H_2SO_4}}=\dfrac{98m.100}{10}=980mgam\)
\(m_{dd}=2M+16m+980m=2M+996m\)
\(m_{M_2\left(SO_4\right)_m}=\left(2M+96m\right)gam\)
\(\dfrac{2M+96m}{2M+996m}.100=12,9\rightarrow M\approx18,65m\)
Nghiệm phù hợp m=3 và M=56(Fe)\(\rightarrow Fe_2O_3\)
Fe2O3+3H2SO4\(\rightarrow\)Fe2(SO4)3+3H2O
\(n_{Fe_2O_3}=\dfrac{3,2}{160}=0,02mol\)
-Vì hiệu suất 70% nên số mol Fe2(SO4)3 kết tinh là:
\(0,02.\dfrac{70}{100}=0,014mol\rightarrow n_{Fe_2\left(SO_4\right)_3.nH_2O}=0,014mol\)
0,014(400+18n)=7,868\(\rightarrow400+18n=562\rightarrow18n=162\rightarrow n=9\)
Công thức tinh thể: Fe2(SO4)3.9H2O
1. Thí nghiệm: Từ muối ăn tinh khiết, nước cất và các dụng cụ cần thiết, hãy pha chế và giải thích cách pha chế để thu được :
- 100g dung dịch muối ăn nồng độ 10%
- 100ml dung dịch muối ăn nồng độ 2M
Câu trả lời của bạn
TN1:
mNaCl trong dd=100.10%=10(g)
Vậy ta cân 10 g NaCl và 90 g H2O rồi trộn lẫn khuấy đều với nhau thì ta được dd muối ăn có nồng độ 10%
TN2:
nNaCl=0,1.2=0,2(mol)
mNaCl=58,5.0,2=11,7(g)
Vậy để có 200 ml dd NaCl 2M ta cần lấy 11,7 g NaCl và 200ml nước
1. Giải thích vì sao nước luộc rau muống bị chuyển màu khi vắt chanh.
2. Nước muối sinh lí (dung dịch NaCl 0,9%) được sử dụng nhiều ttrong y học, trong cuộc sống hằng ngày nước muối sinh lí cũng có rất nhiều ứng dụng như dùng để súc miệng, ngâm, rửa rau quả,... Trình bày cách pha chế 2 lít nước muối sinh lí.
HELP ME!![]()
![]()
![]()
Câu trả lời của bạn
1
trong nước rau muống có chứa một lượng kiềm Ca(OH)2, chất diệp lục phản ứng như chất chỉ thị màu.
Trong khi nước chanh chứa lượng axit hữu cơ yếu là axit citric khá cao lên đến 8% khối lượng khô trong quả, nên khi vắt chanh sẽ làm thay đổi độ axit của nước rau. Điều này khiến cho màu của nước rau muống chuyển từ xanh sang vàng hoặc đỏ, tùy theo nồng độ axit.
Mọi người xem và giải hộ mình câu về phần tính nồng độ % nha . Cảm ơn mọi người !!!
Tính C% của dung dịch thu được trog trường hợp sau :
-Cho 16 gam HCl vào 200 gam dung dịch HCl
( Mọi người xét xem có sai đề ko )
Câu trả lời của bạn
Bạn đang học pha trộn dung dịch hả ?
Nếu không phải thì mình nghĩ đề là : 16g CuO -> 200g dd HCl
Dung dịch chưa bão hòa và dung dịch bão hòa :
Mô tả cách tiến hành thì nghiệm để :
- Chuyển dung dịch muối ăn chưa bão hòa thành dung dịch muối ăn bão hòa ( ở nhiệt độ phòng )
- Chuyển dung dịch muối ăn bão hòa thành dung dịch muối ăn chưa bão hòa ( ở nhiệt độ phòng )
Câu trả lời của bạn
-Cho thêm muối
-Cho thêm nước
Có 2 lọ đựng dd HCl . Lọ thứ 1 có nồng độ 1 mol/l . Lọ thứ 2 có nồng độ 3 m/l . Hãy pha chế thành 50 ml dd HCl có nồng độ 2 M từ dd trên
Câu trả lời của bạn
Gọi a, b lần lượt là thể tích dung dịch HCl của lọ thứ 1và lọ thứ 2 (a, b > 0 , lít)
=>: \(a+b=0,05\left(I\right)\)
Ta có: \(n_{HCl}\)(lọ 1) \(=a.1=a\left(mol\right)\)
\(n_{HCl}\)(lọ 2) \(=3b\left(mol\right)\)
\(n_{HCl}\left(sau\right)=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow a+3b=0,1\left(II\right)\)
Từ (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,025\left(lit\right)=25\left(ml\right)\\b=0,025\left(lit\right)=25\left(ml\right)\end{matrix}\right.\)
Vậy....
cho 1 dd axit sunfuric trong đó số mol H2SO4 =sỐ mol H2O .tính nồng độ %
Câu trả lời của bạn
Giả sử số mol đều là x mol
\(m_{H_2SO_4}=98x\)
\(m_{H_2O}=18x\)
\(C\%_{H_2SO_4}=\dfrac{98x.100}{98x+18x}=\dfrac{9800}{116}\approx85,5\%\)
Cho 100g dd HNO3 10% vào 200g dd kOH. Tính C% KOH
Câu trả lời của bạn
HNO3+KOH->KNO3+H2O
nHNO3=\(\dfrac{100\cdot10}{100\cdot63}=\dfrac{10}{63}mol\)
=>nKOH=\(\dfrac{10}{63}\)(mol)
=>C%KOH=\(\dfrac{\dfrac{10}{63}\cdot56\cdot100}{200}=93,33\%\)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *