Nội dung bài học nói đến các khái niệm về nguyên tử, cấu tạo hạt nhân, các loại hạt cơ bản cấu thành nguyên tử. Ta biết mọi vật thể tự nhiên hay nhân tạo đều được tạo ra từ chất này hay chất khác. Thế các chất được tạo từ đâu? Chúng ta cùng tìm hiểu qua bài học sau.
1 hạt nhân mang điện tích dương.
Vỏ tạo bởi 1 hay nhiều electron mang điện tích âm.
Hình 1: Kích thước nguyên tử
Hình 2: Cấu tạo hạt nhân nguyên tử
Hạt nhân nguyên tử tạo bởi các hạt proton và nơtron.
a. Hạt proton
b. Hạt nơtron
Trong mỗi nguyên tử:
Số p = số e
Số lớp electron của nguyên tử:
H2 : 1 (1e) → 1e ngoài cùng .
O2 : 2 (8e) → 6e ngoài cùng.
Na : 3 (11e) →1e ngoài cùng.
Số e tối đa ở lớp 1: 2e
Số e tối đa ở lớp 2: 8e
Hình 3: Cấu tạo nguyên tử Hidro, Oxi, Nitơ
Sau bài học cần nắm: Xác định được số đơn vị điện tích hạt nhân, số p, số e, số lớp e, số e trong mỗi lớp dựa vào sơ đồ cấu tạo nguyên tử của một vài nguyên tố cụ thể (H, C, Cl, Na).
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 4có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Chọn từ thích hợp điền vào chỗ trống” nguyên tử là hạt ……., vì số electron có trong nguyên tử bằng đúng số proton tronh hạt nhân”
Cho các nguyên tử với các thành phần câu tạo như sau:
X(6n,5p,5e) ; Y(10n,10p,10e) ; Z(5n,5p,5e) ; T(11n,12p,12e) .
Ở đây có bao nhiêu nguyên tố hóa học?
Nguyên tử liên kết được với nhau là nhờ:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 4.
Bài tập 1 trang 15 SGK Hóa học 8
Bài tập 2 trang 15 SGK Hóa học 8
Bài tập 3 trang 15 SGK Hóa học 8
Bài tập 4 trang 15 SGK Hóa học 8
Bài tập 5 trang 15 SGK Hóa học 8
Bài tập 4.1 trang 4 SBT Hóa học 8
Bài tập 4.2 trang 5 SBT Hóa học 8
Bài tập 4.3 trang 5 SBT Hóa học 8
Bài tập 4.4 trang 5 SBT Hóa học 8
Bài tập 4.5 trang 5 SBT Hóa học 8
Bài tập 4.6 trang 6 SBT Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Chọn từ thích hợp điền vào chỗ trống” nguyên tử là hạt ……., vì số electron có trong nguyên tử bằng đúng số proton tronh hạt nhân”
Cho các nguyên tử với các thành phần câu tạo như sau:
X(6n,5p,5e) ; Y(10n,10p,10e) ; Z(5n,5p,5e) ; T(11n,12p,12e) .
Ở đây có bao nhiêu nguyên tố hóa học?
Nguyên tử liên kết được với nhau là nhờ:
Nguyên tử Canxi có số Proton trong hạt nhân là 20. Số e ở lớp ngoài cùng của canxi là
Nguyên tử được tạo bởi các loại hạt
Điền từ còn thiếu vào chỗ trống
“Nguyên tử là hạt vô cùng nhỏ và (1) về điện. Nguyên tử gồm hạt nhân mang điện tích dương và vỏ tạo bởi (2) mang (3)”
Chọn đán án đúng nhất
Chọn đáp án sai
Nguyên tử có khả năng liên kết với nhau. Tại sao? Chọn đáp án đúng
Cho biết số p, số e, số lớp e và số e lớp ngoài cùng của (I)
.png)
Hãy chép các câu sau đây với đầy đủ các cụm từ phù hợp.
“……….là hạt vô cùng nhỏ, trung hòa về điện : từ …………tạo ra mọi chất. Nguyên tử gồm …………mang điện tích dương và vỏ tạo bởi……………”
a) Nguyên tử tạo thành từ ba loại hạt nhỏ hơn nữa, nó là những loại nào?
b) Hãy nói tên, kí hiệu và điện tích của những hạt mang điện.
c) Những nguyên tử cùng loại có cùng số hạt nào trong hạt nhân?
Vì sao nói khối lượng của hạt nhân được coi là khối lượng của nguyên tử?
a) Trong nguyên tử, electron chuyển động và sắp xếp như thế nào?
b) Nhờ đâu mà nguyên tử có khả năng liên kết?
Cho biết sơ đồ của một số nguyên tử sau:
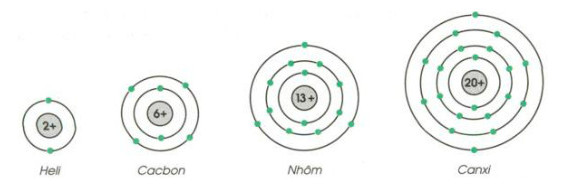
Hãy chỉ ra: số p trong hạt nhân, số e trong nguyên tử và số e lớp ngoài cùng của mỗi nguyên tử.
Điền tên hạt nào tạo thành nguyên tử vào các câu sau đây (chép vào ở bài tập):
a) ... và ... có điện tích như nhau, chỉ khác dấu.
b) …. và …. có cùng khối lượng, còn …. có khối lượng rất bé, không đáng kể.
c) Những nguyên tử cùng loại có cùng số …. trong hạt nhân.
d) Trong nguyên tử ... luôn chuyển động rất nhanh và sắp xếp thành từng lớp.
Có thể dùng các cụm từ sau đây để nói về nguyên tử:
A. Vô cùng nhỏ.
B. Trung hòa về điện.
C. Tạo ra các chất.
D. Không chia nhỏ hơn trong phản ứng hóa học.
Hãy chọn cụm từ phù hợp (A, B, C hay D?) với phần còn lại trống trong câu:
"Nguyên tử là hạt ..., vì số electron có trong nguyên tử bằng đúng số proton trong hạt nhân".
Cho biết sơ đồ một số nguyên tử sau:
Hãy chỉ ra số proton trong hạt nhân, số electron trong nguyên tử, số lớp electron và số electron lớp ngoài cùng của mỗi nguyên tử.
Theo sơ đồ một số nguyên tử ở bài tập 4.3, hãy chỉ ra:
a) Mỗi nguyên tử có mấy lớp electron.
b) Những nguyên tử nào có cùng một số lớp electron.
c) Nguyên tử nào có số lớp electron như nguyên tử natri. (xem sơ đồ trong Bài 4 - SGK).
Yêu cầu như bài 4.4.
a) Nguyên tử nào có số electron lớp ngoài cùng như nguyên tử natri.
b) Nguyên tử cacbon (xem sơ đồ trong bài tập 5, bài 4 – SGK) có số lớp electron như nguyên tử nào.
c) Nguyên tử nào có số electron lớp ngoài cùng như nguyên tử cacbon.
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
a) Vẽ sơ đồ đơn giản của năm nguyên tử mà trong hạt nhân có số proton bằng 7, 9, 15, 17, 19.
b) Mấy nguyên tử có số electron ở lớp ngoài cùng bằng 5, mấy nguyên tử có số electron ở lớp ngoài cùng bằng 7 ?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Giúp em bài này vs ạ
Tổng số hạt p,n,e có trong loại nguyên tử của nguyên tố X là 28, số hạt không mang điện chiếm 35,7% . Tính số hạt protron trong X?
Câu trả lời của bạn
Ta có : e+p+n = 28 (1)
Mặt khác : n = 35,7/100 (e+p+n)
=>n = 9,996
Thay n= 9,996 vào (1) ta có:
e+p+ 9,996= 28
e+p= 28-9,996
e+p=18.004
mà e=p => 2e=18,004
e= 18,004 : 2
e= 9,002
Vậy p=9,002
Câu trả lời của bạn
Nguyên tử là những hạt cực kỳ nhỏ bé, không mang điện, cấu tạo nên một chất.
Câu trả lời của bạn
- Vì hạt nhân gồm có proton và neutron
=> Tổng số hạt trong hạt nhân = số proton + số neutron
=> 27 = số proton + số neutron
- Mà số đơn vị điện tích hạt nhân = số proton = 13 = số electron
=> Số neutron = 27 – 13 = 14
Vậy trong nguyên tử nhôm có: 13 hạt electron, 13 hạt proton, 14 hạt neutron
| Nguyên tử | Số proton | Số neutron | Số electron | Điện tích hạt nhân |
| Hydrogen | 1 | 0 | ? | ? |
| Carbon | ? | 6 | 6 | ? |
| Nhôm | 13 | 14 | ? | ? |
Câu trả lời của bạn
| Nguyên tử | Số proton | Số neutron | Số electron | Điện tích hạt nhân |
| Hydrogen | 1 | 0 | 1 | +1 |
| Carbon | 6 | 6 | 6 | +6 |
| Nhôm | 13 | 14 | 13 | +13 |
Hạt nào mang điện tích âm?
Hạt nào mang điện tích dương?
Hạt nào không mang điện?
Câu trả lời của bạn
Trong các hạt cấu tạo nên nguyên tử:
Hạt mang điện tích âm: electron (e)
Hạt mang điện tích dương: proton (p)
Hạt không mang điện: neutron (n)
Hạt nào mang điện tích âm?
Hạt nào mang điện tích dương?
Hạt nào không mang điện?
Câu trả lời của bạn
Hạt mang điện tích âm là : Electron kí hiệu là e.
Hạt mang điện tích dương là :Proton kí hiệu là p.
Hạt không mang điện là :Neutron kí hiệu là n.
Câu trả lời của bạn
Hai chất có chứa nguyên tử oxygen là: đường ăn, nước.
tính thể tích , khối lượng , phân tử khối cảu các hỗn hợp : a) 5,6g N2 và 0,5 mol SO2 b) 4,8g O3 và 2,24 lít CO2 ở điều kiện tiêu chuẩn
Câu trả lời của bạn
đốt cháy hết 11,2 lít khí A trong O. Sau phản ứng thu được khí CO2 và hơi nước, biết khí A có tỉ khối đối với không khí là 0,552. Thành phần theo khối lượng của khí A là: 75% C và 25% H (thể tích các khí đo ở đktc) a) xác định CTHH của khí A. b) Viết phương trình hóa học của phản ứng. c) Tính thể tích khí O cần để đốt cháy hết lượng khí A nói trên. d) tính thể tích và khối lượng khí CO2. e) Tính khối lượng của nước thu được bằng hai cách
Câu trả lời của bạn
không biết làm có ví dụ cụ thể không
nguyên tử A có tổng số hạt là 52, trong đó số mang điện lại nhiều hơn số không mang điện là 16. số hạt nơtron của nguyên tử A là :
A. 18
B. 17
C. 16
D.15
Câu trả lời của bạn
CÂU A BẰNG 18 NHA
a, khí hiđro
b, không khí
c, khí meta
Câu trả lời của bạn
a, Na nặng hơn H2 23/2 = 11.5 lần
b, Na nhẹ hơn không khí 23/29 ~ 0.79 lần
c, Na nặng hơn CH4 (Khí metan) 23/16 = 1.4375 lần
CHÚC BẠN HỌC TỐT!
Câu trả lời của bạn
Câu trả lời của bạn
kí hiệu 3 nguyên tử đồng là 3Cu
kí hiệu của 3 nguyên tử đông là:3Cu
Kí hiệu 3 nguyên tử đồng là: 3 Cu.
Câu trả lời của bạn
Số hạt không mang điện là nơtron mà notron=proton
=> số hat proton là: 12
số hạt nơtron là: 12
số hạt electron là: 34-12=22
Electron trong nguyên tử hidro chuyển động xung quanh hạt nhân bên trong một khối cầu có bán kính lớn hơn bán kính hạt nhân là 10000 lần. Nếu ta phóng đại hạt nhân lên thành một quả bóng có đường kính 6cm thì bán kính khối cầu tức là bán kính nguyên tử sẽ là bao nhiêu mét?
Câu trả lời của bạn
Bán kính của hạt nhân bằng 6/2 = 3 (cm). Bán kính của nguyên tử là : 3 x 10000 = 30000 (cm) = 300 (m).
Tính khối lượng nguyên tử tuyệt đối, khối lượng nguyên tử tương đối, Khối lượng hạt nhân của các nguyên tử sau: CA(20p,20n), CL(17p,18n), N(7p,7n), S(16p,16n), P(15p,16n), Al(13p,14p)
Từ đó cho biết khối lượng phân tử của các chất(Tính theo hai đơn vị kg và DVC):Ca(OH)2, Al2(SO4)3, CA3(PO4)2.
Câu trả lời của bạn
Câu trả lời của bạn
Hướng dẫn: Ta có: nS = 8/32 = 0,25 (mol)
Số nguyên tử nhôm = 2 x số nguyên tử S
nAl = 2 x nS = 2 x 0,25 = 0,5 (mol)
MAl = 0,5 x 27 = 13,5 gam (gam)
Câu trả lời của bạn
Gọi p, n, e lần lượt là số proton, nơtron và electron.
Theo đề bài, ta có: p + n + e = 40 (1)
Vì p = e nên (1) → 2p + n = 40 (*)
Mà: 2p – n = 12 (**)
Từ (*) và (**) → n = 14
Câu trả lời của bạn
- Số nguyên tử H trong 6.1023 phân tử H2 là:
2.6.1023 = 1,2.1024 (nguyên tử)
- Số nguyên tử H trong 3.1023 phân tử H2O là:
2.3.1023 = 6.1023 (nguyên tử)
- Số mol CH4 là 0,6 : 16 = 0,0375 mol
→ Số nguyên tử H trong 0,6 gam CH4 là:
0,0375.4. 6.1023 = 9.1022 (nguyên tử)
- Số mol NH4Cl là 1,5 : 53,5 = 0,028 mol
→ Số nguyên tử H trong 1,5 gam NH4Cl là:
0,028.4. 6.1023 = 6,72.1022 (nguyên tử)
Vậy trong 1,5 gam NH4Cl có số nguyên tử H ít nhất, nên khối lượng H cũng là ít nhất.
Câu trả lời của bạn
NTK(Z) = 5,312.10-23/1,66.10-24 = 32 (đvC): lưu huỳnh (S).

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *