Ở chương V các em đã học xong về oxi, hiđro, nước; phản ứng oxi hóa - khử; phản ứng thế... Tiết học này các em sẽ được học bài luyện tập, để làm một số bài tập định tính và một số bài tập định lượng về những kiến thức trên qua bài học này.
1. Khí Hiđro có tính khử, ở nhiệt độ thích hợp Hiđro không những kết hợp được với đơn chất oxi mà còn có thể kết hợp với nguyên tố oxi trong một số oxit kim loại. Các phản ứng này đều tỏa nhiệt.
2. Khí Hiđro có nhiều ứng dụng, chủ yếu do tính chất rất nhẹ (nhẹ nhất trong các chất khí), tính khử và khi cháy tỏa nhiều nhiệt.
3. Có thể điều chế khí Hiđro trong phòng thí nghiệm bằng cách cho dung dịch axit clohiđric HCl hoặc dung dịch axit sunfuric H2SO4 loãng tác dụng với kim loại như Zn, Fe, Al. Có thể thu khí Hiđro vào bình bằng hai cách: đẩy không khí và đẩy nước (miệng bình úp xuống dưới)
4. Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố trong hợp chất.
5. Quá trình tách nguyên tử Oxi khỏi hợp chất là sự khử. Chất chiếm oxi hoặc chất nhường oxi cho chất khác là chất khử.
6. Sự tác dụng của oxi với một chất là sự oxi hóa. Đơn chất oxi hoặc chất nhường oxi cho chất khác là chất oxi hóa.
7. Phản ứng oxi hóa khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
| Khí O2 | Khí H2 | |
| Tính chất hóa học | Tính oxi hóa Tác dụng với kim loại, phi kim,hợp chất. | Tính khử Tác dụng với khí oxi và oxit kim loại |
| Điều chế trong PTN | Nhiệt phân hợp chất giàu oxi: KClO3, KMnO4… | Một số kim loại(Mg,Zn,Al…) tác dụng với dung dịch HCl, H2SO4 loãng. |
| Loại phản ứng | Phản ứng phân hủy: 2KClO3 | Phản ứng thế: Zn +2HCl → ZnCl2 + H2↑ |
| Cách thu | Đẩy không khí Đẩy nước | Đẩy không khí Đẩy nước |
| Ứng dụng | Sự hô hấp Sự đốt nhiên liệu Thuốc nổ | Nhiên liệu và bơm vào khinh khí cầu Làm nguyên liệu |
Bảng: Tóm tắt tính chất và ứng dụng của Oxi và Hiđro
Lập phương trình hóa học của các phản ứng sau và cho biết chúng thuộc loại phản ứng hóa học nào?
a) Điphotpho penta oxit + nước → axit photphoric (H3PO4)
b) Kẽm + axit sunfuric (H2SO4) → Kẽm sunfat (ZnSO4)+ hiđro
c) Thủy ngân (II) oxit Thủy ngân + oxi
a) P2O5 + 3H2O → 2 H3PO4
Đây là phản ứng hóa hợp
b) Zn + H2SO4 → ZnSO4 + H2↑
Đây là phản ứng thế
c) HgO Hg + O2↑
Đây là phản ứng phân hủy
Người ta dùng V(lít) khí H2 khử hoàn toàn hỗn hợp hai Oxit kim loại gồm: CuO và Fe2O3 ở nhiệt độ thích hợp. Sau phản ứng thu được 12g hỗn hợp gồm 2 kim loại trong đó có 6,4g Cu.
a) Viết các phương trình hóa học xảy ra.
b) Hãy tính V(lít) khí H2 cần dùng để khử hỗn hợp 2 Oxit đó. (Các thể tích khí đo ở đktc)
a) Phương trình hóa học:
H2 + CuO Cu + H2O (1)
3H2 + Fe2O3 2Fe + 3H2O (2)
b) Khối lượng của kim loại Fe là:
\({m_{Fe}} = {m_{hh}} - {m_{CuO}} = 12 - 6,4 = 5,6(gam)\)
Số mol của Sắt và Đồng lần lượt là:
\(\begin{array}{l} {n_{Fe}} = \frac{{{m_{Fe}}}}{M} = \frac{{5,6}}{{56}} = 0,1(mol)\\ {n_{CuO}} = \frac{{{m_{CuO}}}}{M} = \frac{{6,4}}{{64}} = 0,1(mol) \end{array}\)
Phương trình hóa học:
H2 + CuO Cu + H2O (1)
1 mol 1 mol
0, 1 mol \(\leftarrow\) 0,1 mol
3H2 + Fe2O3 2Fe + 3H2O (2)
3 mol 2 mol
0,15 mol \(\leftarrow\) 0,1 mol
Theo phương trình (1) và (2) thì số mol Hiđro sinh ra ở hai phản ứng là:
\(\begin{array}{l} {n_{{H_2}(1)}} = {n_{Cu}} = 0,1(mol)\\ {n_{{H_2}(2)}} = {n_{Fe}} = 0,15(mol) \end{array}\)
Tổng số mol khí Hiđro sinh ra là:
\(\sum {{n_{{H_2}}}} = 0,1 + 0,15 = 0,25(mol)\)
Thể tích khí Hiđro cần dùng ở đktc là:
\({V_{{H_2}}} = 22,4.{n_{{H_2}}} = 22,4 \times 0,25 = 5,6(lit)\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 34có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Nhờ tính chất nào mà khí hiđro có thể tác dụng được với một số oxit kim loại ở nhiệt độ thích hợp:
Ứng dụng của hiđro chủ yếu dựa vào tính chất
Hóa chất điều để điều chế hiđro trong phòng thí nghiệm là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 34.
Bài tập 1 trang 118 SGK Hóa học 8
Bài tập 2 trang 118 SGK Hóa học 8
Bài tập 3 trang 119 SGK Hóa học 8
Bài tập 4 trang 119 SGK Hóa học 8
Bài tập 5 trang 119 SGK Hóa học 8
Bài tập 6 trang 119 SGK Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Nhờ tính chất nào mà khí hiđro có thể tác dụng được với một số oxit kim loại ở nhiệt độ thích hợp:
Ứng dụng của hiđro chủ yếu dựa vào tính chất
Hóa chất điều để điều chế hiđro trong phòng thí nghiệm là:
Thu khí hiđro trong phòng thí nghiệm bằng phương pháp nào?
Phản ứng thế là phản ứng hóa học xảy ra giữa:
Cho các phản ứng sau, phản ứng nào không phải phản ứng thế
Trong các loại phản ứng dưới đây, phản ứng nào chắc chắn là phản ứng oxi hóa – khử
Cho thanh Al ngâm vào dung dịch axit clohidric thấy có khí bay lên. Xác định khí đó
Cho thanh đồng ngâm vào 400ml dung dịch axit sunfuric loãng 2M thấy trong dung dịch có khí và V bằng bao nhiêu?
Tính m(g) H2O khi cho 2,24(l) H2 tác dụng với 6,72 (l) O2(đktc)
Viết phương trình hóa học biểu diễn phản ứng của hiđro với các chất: O2, Fe2O3, Fe3O4, PbO ở nhiệt độ thích hợp. Ghi rõ điều kiện phản ứng. Giải thích và cho biết mỗi phản ứng trên thuộc loại phản ứng gì?
Có 3 lọ đựng riêng biệt các chất khí sau: khí oxi, không khí, và hiđro. Bằng thí nghiệm nào có thể nhận ra chất khí trong mỗi lọ?
Cho dung dịch axit sunfuric loãng, nhôm và các dụng cụ thí nghiệm như hình vẽ.
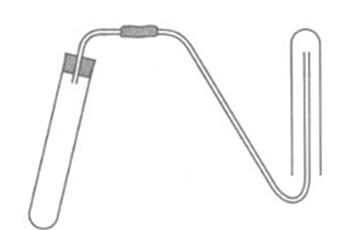
Hãy chọn câu trả lời đúng trong các câu sau:
A. Có thể dùng các hóa chất và dụng cũ đã cho để điều chế và thu khí oxi.
B. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu không khí.
C. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí hiđro.
D. Có thể dùng để điều chế hidro nhưng không thu được khí hiđro.
a) Lập phương trình hóa học của các phản ứng sau:
Cacbon đioxit + nước → Axit cacbonic (H2CO3).
Lưu huỳnh đioxit + nước → Axit sunfurơ (H2SO3).
Kẽm + axit clohiđric → Kẽm clorua + H2.
Điphotpho + nước → Axit photphoric (H3PO4).
Đồng (II) oxit + hiđro → Chì (Pb) + H2O.
b) Mỗi phản ứng hóa học trên đây thuộc loại phản ứng nào? Vì sao?
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

Câu trả lời của bạn
nZn=6,5:65=0,1(mol)
Zn + 2HCl → ZnCl2 + H2
0,1--------------0,1-------0,1
VH2=0,1*22,4=2,24(l)
mZnCl2=0,1*136=13,6(g)
Cho mình 5 sao và like nha
Câu trả lời của bạn
Gọi công thức hóa học của X: CxOy (x, y ³ 1)
Phần trăm khối lượng của Oxi có trong X là: 100% - %mC = 72,73%
Ta có:
\(\eqalign{
& \% {m_C} = {{{m_C}} \over {{m_X}}} \times 100\% \Leftrightarrow {{12x} \over {{m_X}}} \times 100\% = 27,27\% \cr
& \% {m_O} = {{{m_O}} \over {{m_X}}} \times 100\% \Leftrightarrow {{16y} \over {{m_X}}} \times 100\% = 72,73\% \cr
& \Rightarrow {{\% {m_C}} \over {\% {m_O}}} = {{12x} \over {12y}} \cr
& \Leftrightarrow {{27,27\% } \over {72,73\% }} = {{12x} \over {16y}} \cr
& \Leftrightarrow {x \over y} = {1 \over 2} \cr} \)
Chọn x = 1 và y =2
=> Công thức hóa học của X là CO2
Câu trả lời của bạn
Xét 1 mol mỗi chất
M(NH2)2CO = (14 + 1.2).2 + 12 + 16 = 60 đvC \( \Rightarrow \% N = {{28} \over {60}}.100\% = 46,67\% \)
M(NH4)2SO4 = (14 + 1.4).2 + 32 + 16.4 = 132 đvC \( \Rightarrow \% N = {{28} \over {132}}.100\% = 21,21\% \)
MCa(NO3)2 = 40 + (14 + 16.3).2 = 164 đvC \( \Rightarrow \% N = {{28} \over {164}}.100\% = 17,07\% \)
MNH4NO3 = 14 + 1.4 + 14 + 16.3= 80 đvC \( \Rightarrow \% N = {{28} \over {80}}.100\% = 35\% \)
Vậy hàm lượng nito có trong phân Ure nhiều nhất
Câu trả lời của bạn
Phần trăm của Cu có trong CuO là:
\(\% Cu = {{{m_{Cu}}} \over {{m_{CuO}}}}.100\% = {{64} \over {64 + 16}}.100\% = 80\% \)
Câu trả lời của bạn
Phân tử khối của MgO là: MCaO = 40 + 16 = 56 g/ mol (0,5đ)
%Ca = 40/56 x100% = 71,43%. (0,5đ)
%O = 100% - 71,43% = 28,57 % (0,5đ)
Câu trả lời của bạn
Phân tử khối của MgO là: MMgO = 24 + 16 = 40 g. (0,5đ)
%Mg = 24/40 x100% = 60%. (0,5đ)
%O = 100% - 60% = 40% (0,5đ)
Câu trả lời của bạn
Đặt công thức X là FexOy
Trong X chứa 70%Fe và 30%O nên ta có:
\(\eqalign{
& x:y = {{\% F{\rm{e}}} \over {{M_{F{\rm{e}}}}}}:{{\% O} \over {{M_O}}} \cr
& \,\,\,\,\,\,\,\,\,\, = {{70} \over {56}}\,\,\,\,\,:\,\,\,\,{{30} \over {16}} \cr
& \,\,\,\,\,\,\,\,\,\, = 1,25\,\,:\,\,\,1,875 \cr
& \,\,\,\,\,\,\,\,\,\, = \,\,\,\,2\,\,\,\,\,\,:\,\,\,\,3 \cr} \)
=> công thức đơn giản nhất của X là: Fe2O3
Vì X có tỉ khối so với H2 là 80 nên MX= 80×MH2 = 80 ×2 = 160 (g/mol)
Ta có: (Fe2O3)n = 160
=> 160n = 160
=> n = 1
Vậy công thức phân tử của X là Fe2O3
Câu trả lời của bạn
\(\% {m_{Fe}} = \frac{{2.56}}{{2.56 + 16.3}}.100\% = 70\% \)
Câu trả lời của bạn
\(\begin{gathered}
\% Fe\,(trong\,F{e_2}{O_3}) = \frac{{56 \times 2}}{{56 \times 2 + 16 \times 3}}.100\% = 70\% \hfill \\
\% Fe\,(trong\,F{e_3}{O_4}) = \frac{{56 \times 3}}{{56 \times 3 + 16 \times 4}}.100\% = 72,4\% \hfill \\
\% Fe\,(trong\,FeC{O_3}) = \frac{{56}}{{56 + 12 + 16 \times 3}}.100\% = 48,3\% \hfill \\
\% Fe\,(trong\,Fe{S_2}) = \frac{{56}}{{56 + 32 \times 2}}.100\% = 46,67\% \hfill \\
\end{gathered} \)
=> phần trăm sắt trong Fe3O4 là cao nhất
Câu trả lời của bạn
Trong hợp chất Ca3PO4: \(\% Ca = \frac{{40.3}}{{40.3 + 31 + 16.4}}.100\% = 55,81\% \)
Trong hợp chất CaHPO4 : \(\% Ca = \frac{{40}}{{40 + 1 + 31 + 16.4}}.100\% = 29,41\% \)
Trong hợp chất Ca(H2PO4)2: \(\% Ca = \frac{{40}}{{40 + 1.2.2 + 31.2 + 16.4.2}}.100\% = 17,09\% \)
Trong hợp chất Ca(HSO4)2: \(\% Ca = \frac{{40}}{{40 + 1.2 + 32.2 + 16.4.2}}.100\% = 17,09\% \)
Ca3PO4 có tỉ lệ Ca cao nhất
a) SO2 và SO3
b) KNO2 và KNO3
c) Fe(OH)2 và Fe(OH)3
Câu trả lời của bạn
a.
\(S{O_2}:\% {m_{SO2}} = {{32} \over {32 + 2.16}}.100\% = 50\% \)
%O = 100%-50%=50 %
\(S{O_3}:{\rm{ }}\% {\rm{ }}{m_{SO3}} = {{32} \over {32 + 16.3}}.100\% = 40\% \)
% O= 100% −40%= 60%
b.
\(KN{O_2}:\% K = {{39} \over {39 + 14 + 16.2}}.100\% = 45,88\% \)
\(\% N = {{14} \over {39 + 14 + 16.3}}.100\% = 13,86\% \)
%O= 100% −45,88%−16,47%=37,65%
\(KN{O_3}:{\rm{ }}\% {\rm{ }}K = {{39} \over {39 + 14 + 16.3}}.100\% = 38,61\% \)
\(\% N{\rm{ }} = {{14} \over {39 + 14 + 16.3}}.100\% = 13,86\% \)
% O=52,47%
c.
\(Fe{\left( {OH} \right)_2}:{\rm{ }}\% {\rm{ }}Fe = {{56} \over {56 + 16.2 + 1.2}}.100\% = 62,22\% \)
\(\% O = {{16.2} \over {56 + 16.2 + 1.2}}.100\% = 35,55\% \)
%H=2,23%
\(Fe{\left( {OH} \right)_3}:{\rm{ }}\% Fe{\rm{ }} = {{56} \over {56 + 16.3 + 1.3}}.100\% = 52,34\% \)
\(\% O = {{16.3} \over {56 + 16.3 + 1.3}}.100\% = 44,86\% \)
%H=2,8%
Câu trả lời của bạn
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCa =(40.100):100 = 40 gam
mC =(12.100):100 = 12 gam
mO =(48.100):100 = 48 gam
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất là:
nCa = 40:40 = 1 mol
nC = 12:12 = 1 mol
nO = 48:16 = 3 mol
Vậy công thức hoá học của hợp chất là: CaCO3
Câu trả lời của bạn
Giả sử công thức hoá học của hợp chất A là: NaxClyOz ( x, y, z nguyên dương)
−Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
MNa = (30,87 . 74,5) : 100 = 23 gam
MCl = (47,65 . 74,5) : 100 = 35,5 gam
%O = 100% - (30,87% + 47,65%) = 21,48%
mO = (21,48 . 74,5) : 100 = 16 gam
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất A là:
x = 23 : 23 =1 mol
y = 35,5 : 35,5 = 1 mol
z = 16 : 16 = 1 mol
Vậy công thức hoá học của hợp chất A là: NaClO
Câu trả lời của bạn
M CuSO4 = 64 + 32 + 16 . 4 = 160 (g/mol)
\( => {\text{ }}{n_{CuSO4}} = \frac{{3,2}}{{160}} = {\text{ }}0,02{\text{ }}\left( {mol} \right)\)
=> mCu = 0,02. 64 = 1,28(g); mS = 0,02 . 32 = 0,64 (g); mO = 3,2 − 1,28 − 0,64 =1,28(g)
Câu trả lời của bạn
\({M_{C{a_3}{{(P{O_4})}_2}}} = 40.3 + 31.2 + 16.4.2 = 310\left( {g/mol} \right)\)
Áp dụng công thức với chất có công thức: AXBYCZ
Ta có:
\(\eqalign{
& {m_A} = {{x.{M_A}} \over {{M_{{A_x}{B_y}{C_z}}}}} \times {m_{{A_x}{B_y}{C_z}}} \cr
& {m_P} = {{x.{M_P}} \over {{M_{C{a_3}{{(P{O_4})}_2}}}}} \times {m_{C{a_3}{{(P{O_4})}_2}}} \cr
& \Rightarrow {m_{C{a_3}{{(P{O_4})}_2}}} = {{{m_P} \times {M_{C{a_3}{{(P{O_4})}_2}}}} \over {x \times {M_P}}} = {{3,1 \times 310} \over {2.31}} = 15,5\,(g) \cr} \)
Câu trả lời của bạn
Gọi CTPT A: CxHyOz (x, y, x )
Xét 1 mol hợp chất A
\({m_C} = \frac{{52,17}}{{100}}.46 = 24(g) = > {n_C} = \frac{{24}}{{12}} = 2\left( {mol} \right)\)
\({m_H} = \frac{{13,05}}{{100}}.46 = 6(g) = > {n_H} = \frac{6}{1} = 6(mol)\)
\({m_O} = \frac{{34,78}}{{100}}.46 = 16(g) = > n{}_O = \frac{{16}}{{16}} = 1(mol)\)
Vậy công thức hóa học của A là: C2H6O
Câu trả lời của bạn
Lấy 1 mol H2O2 => khối lượng H2O2 = 34 (g)
Thành phần % của H và O trong hỗn hợp trên là :
\(\eqalign{
& \% H = {{{m_{{H}}}} \over {{m_{{H_2}{O_2}}}}}.100\% = {2 \over {34}}.100\% = 5,88\% \cr
& \% O = 100\% - 5,88\% = 94,12\% \cr} \)
Câu trả lời của bạn
- Giả sử công thức hoá học của hợp chất A là: MgxCyOz ( x, y, z nguyên dương)
-Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
MMg = (28,57.84):100 = 24 gam
MC = (14,29.84):100 = 12 gam
%O = 100%-(28,57%+14,19%)=57,14%
mO= (57,14.84):100 = 48 gam
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất A là:
x = 24:24 =1 mol
y = 12:12 = 1 mol
z = 48:16 =3 mol
Vậy công thức hoá học của hợp chất A là: MgCO3.
Câu trả lời của bạn
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCu =(40.160):100 = 64 gam
mS =(20.160):100 = 32 gam
mO =(40.160):100 = 64 gam
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất là:
nCu = 64:64 = 1 mol
nS = 32:32 = 1 mol
nO = 64:16 = 4 mol
Vậy công thức hoá học của hợp chất là: CuSO4
Câu trả lời của bạn
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mK = ( 82,98%.94):100 = 78 gam.
%O =100%- 82,98% = 17,02%
=> mO = (17,02.94):100=16 gam
=> Hoặc mO = 94-78 = 16 gam
- Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là:
nK = 78:39 = 2 mol
nO = 16:16=1 mol
=> Vậy công thức hoá học của hợp chất là K2O

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *