Oxit là gì? Có máy loại oxít? Công thức hóa học oxit gồm những nguyên tố nào? Cách gọi tên oxít như thế nào? Để hiểu rõ hơn tiết học này các em sẽ tìm hiểu về Oxit.
Ví dụ: P2O5; N2O5...
NO,CO không phải là oxit axit
Oxit bazơ : thường là oxit của kim loại và tương ứng với 1 bazơ.
Ví dụ: Al2O3; CaO…
Chú ý: Mn2O7,Cr2O7... không phải là oxit bazơ
Ví dụ: CuO tên là Đồng (II) oxit; FeO gọi là Sắt (II) oxit; Fe2O3 gọi là Sắt (III) oxit ...
Ví dụ: SO2 tên là lưu huỳnh đioxit; CO2 tên là cacbon đioxit...
| Chỉ số | Tên tiền tố |
| 1 | mono |
| 2 | đi |
| 3 | tri |
| 4 | tetra |
| 5 | penta |
| ... | ... |
Hình 1: Sơ đồ tư duy bài Oxit
Trong các hợp chất sau, hợp chất nào thuộc loại oxit ?
a. K2O d. H2S
b. CuSO4 e. SO3
c. Mg(OH)2 f. CuO
Oxit là hợp chất của 2 nguyên tố, trong đó có 1 nguyên tố là oxi.
Vậy đáp án là: K2O, SO3, CuO
Hãy viết công thức các axit tương ứng với oxit axit và bazơ tương ứng với oxit bazơ dưới đây:
Oxit axit: CO2, P2O5, SO3
Oxit bazơ: K2O, CaO, MgO
Oxit axit Axit tương ứng
CO2 H2CO3
P2O5 H3PO4
SO3 H2SO4
Oxit bazơ Bazơ tương ứng
K2O KOH
CaO Ca(OH)2
MgO Mg(OH)2
Đọc tên các oxit axit sau: SO3, N2O5, CO2, SO2.
Hãy ghép nội dung ở cột A với cột B để được câu trả lời ở cột C.
Xác định các oxit axit để hoàn thành cột D.
| Công thức hóa học của oxit (A) | Tên gọi Oxit (B) | Trả lời (C) | Oxit axit (D) |
| 1. SiO2 | a. Lưu huỳnh trioxit | 1 - b | X |
| 2. Al2O3 | b. Silic đioxit | 2 - d | |
| 3. SO3 | c. Sắt (III) oxit | 3 - a | X |
| 4. Fe2O3 | d. Nhôm oxit | 4 - c | |
| 5. SO2 | e. Điphotpho pentaoxit | 5 - g | X |
| g. Lưu huỳnh đioxit |
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 26có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Công thức Fe2O3 có tên gọi là gì?
ZnO thuộc loại oxit gì?
Tiền tố của chỉ số nguyên tử của Phi kim hoặc oxi bằng 3 thì có tên là gì?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 26.
Bài tập 1 trang 91 SGK Hóa học 8
Bài tập 2 trang 91 SGK Hóa học 8
Bài tập 3 trang 91 SGK Hóa học 8
Bài tập 4 trang 91 SGK Hóa học 8
Bài tập 5 trang 91 SGK Hóa học 8
Bài tập 26.1 trang 35 SBT Hóa học 8
Bài tập 26.2 trang 35 SBT Hóa học 8
Bài tập 26.3 trang 36 SBT Hóa học 8
Bài tập 26.4 trang 36 SBT Hóa học 8
Bài tập 26.5 trang 36 SBT Hóa học 8
Bài tập 26.6 trang 36 SBT Hóa học 8
Bài tập 26.7 trang 36 SBT Hóa học 8
Bài tập 26.8 trang 36 SBT Hóa học 8
Bài tập 26.9 trang 36 SBT Hóa học 8
Bài tập 26.10 trang 36 SBT Hóa học 8
Bài tập 26.11 trang 36 SBT Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Công thức Fe2O3 có tên gọi là gì?
ZnO thuộc loại oxit gì?
Tiền tố của chỉ số nguyên tử của Phi kim hoặc oxi bằng 3 thì có tên là gì?
Axit tương ứng của oxit axit SO3 là:
Bazơ tương ứng với oxit bazơ CuO là:
Hợp chất nào sau đây không phải là oxit
Tên gọi của P2O5
Oxit nào sau đây là oxit axit
Chỉ ra các oxit bazo: P2O5, CaO, CuO, BaO, Na2O, P2O3
Chỉ ra công thức viết sai: CaO, CuO, NaO, CO2, SO
Chọn từ thích hợp trong khung, điền vào ô trống trong các câu sau đây:
Nguyên tố, oxi, hợp chất, oxit, hai.
Oxit là ... của ... nguyên tố, trong đó có một ... là ... Tên của oxit là tên ... cộng với từ ...
a) Lập công thức hóa học của một loại oxit của photpho, biết rằng hóa trị của photpho là V.
b) Lập công thức hóa học của crom (III) oxit.
a) Hãy viết công thức hóa học của hai oxit axit và hai oxit bazơ.
b) Nhận xét về thành phần trong công thức của các oxit đó.
c) Chỉ ra cách gọi tên mỗi oxit đó.
Cho các oxit có công thức hóa học sau:
a) SO3
b) N2O5
c) CO2
d) Fe2O3
e) CuO
g) CaO
Những chất nào thuộc oxit bazơ? Những chất nào thuộc loại oxit axit?
Một số chất có công thức hóa học sau:
Na2O, NaO, CaCO3, Ca(OH)2, HCl, CaO, Ca2O, FeO.
Hãy chỉ ra những công thức hóa học viết sai?
Dãy gồm các chất thuộc loại oxit axit là :
A. CO2, SO2, Na2O, SO3, NO2
B. CaO, CO2, SO2, P2O5
C. CO2, SO2, SO3, P2O5, NO2
D. NO2, P2O5, Fe2O3, CaO
Dãy gồm các chất thuộc loại oxit bazơ là:
A. FeO, CaO, CO2, NO2
B. CaO, K2O, MgO, Fe2O3
C. CaO, NO2, P2O5, MgO
D. CuO, Mn2O3, CO2, SO3
Có một sô công thức hóa học được viết như sau: KO, Al2O3, FeO, CaO, Zn2O, Mg2O, N2O, PO, SO, S2O
Hãy chỉ ra những công thức viết sai.
Hãy viết tên và công thức hóa học của 4 oxit axit và 4 oxit bazo. Hãy chỉ ra các oxit tác dụng được với nước (nếu có).
Hãy điều chế ba oxit. Viết các phương trình phản ứng.
Lập công thức các bazo ứng với cac oxit sau đây: CuO, FeO, Na2O, BaO, Fe2O3, MgO.
Viết phương trình biểu diễn những chuyển hóa sau:
a) natri → natri oxit → natri hidroxit.
b) Cacbon → cacbon đioxit → axit cacbon (H2CO3).
Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một lạo quặng sắt (thành phần chính là Fe2O3). Khi phân tích mẫu quặng này, người ta nhận thấy có 2,8g sắt. Trong mẫu quặng trên, khối lượng sắt (III) oxit Fe2O3 ứng với hàm lượng sắt nói trên là:
A. 6g
B. 8(g)
C. 4g
D. 3g
Hãy chọn đáp số đúng.
Tỉ lệ khối lượng của nito và oxi trong một oxit của nito là 7 : 20. Công thức của oxit là:
A. N2O
B. N2O3
C. NO2
D. N2O5
Hãy chọn đáp số đúng.
Cho 28,4g điphotpho penoxit P2O5 vào cốc có chứa 90g H2O để tạo thành axit photphoric H3PO4. Khối lượng axit H3PO4 tạo thành là:
A. 19.6g
B. 58,8g
C.39,2g
D.40g
Hãy chọn đáp số đúng.
Một oxit tạo thành bởi mangan và oxi, trong đó tỉ lệ khối lượng giữa mangan và oxi là 55 : 24. Hãy xác định công thức phân tử của oxi.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
a) Viết PTHH.
b) Xác định thành phần phần trăm theo thể tích của hỗn hợp khí.
Câu trả lời của bạn
a) PTHH:
\(CO_2 + Ca(OH)_2 \rightarrow CaCO_3 + H_2O\)
\(CuO + CO \rightarrow Cu + CO_2\)
Chất kết tủa trắng là \(CaCO_3\)
Kim loại màu đỏ là: Cu
b) Số mol các chất tạo thành là:
\(n_{CaCO_3} = 0,01\); \(n_{Cu} = 0,01\) (mol).
Theo phương trình hóa học, số mol các chất phản ứng là:
\(n_{CO_2} = n_{CaCO_3} = 0,01\); \(n_{CO} = n_{Cu} = 0,01\) (mol).
Phần trăm thể tích của các khí trong hỗn hợp ban đầu là:
\(\%V_{CO_2} = \frac{0,01\times 22,4}{(0,01 + 0,01)\times 22,4}\times 100\% = 50\%\)
\(\%V_{CO} = \frac{0,01\times 22,4}{(0,01 + 0,01)\times 22,4}\times 100\% = 50\%\)
Câu trả lời của bạn
| Thuốc thử | NaCl | \(Na_2CO_3\) | \(Na_2SO_4\) | \(Ba(NO_3)_2\) |
| HCl | Không có hiện tượng gì | Có khí thoát ra (1) | Không có hiện tượng gì | Không có hiện tượng gì |
| \(Na_2CO_3\) | Không có hiện tượng gì | Đã nhận biết | Không có hiện tượng gì | Xuất hiện kết tủa trắng (2) |
| \(Ba(NO_3)_2\) | Không có hiện tượng gì | Xuất hiện kết tủa trắng (3) | Đã nhận biết |
Vậy, ta chỉ cần sử dụng thêm $HCl$ cũng có thể nhận biết các dung dịch muối trên.
PTHH:
(1) \(Na_2CO_3 + HCl \rightarrow NaCl + CO_2 + H_2O\)
(2) \(Na_2CO_3 + Ba(NO_3)_2 \rightarrow NaNO_3 + BaCO_3\)
(3) \(Ba(NO_3)_2 + Na_2SO_4 \rightarrow NaNO_3 + BaSO_4\)
Câu trả lời của bạn
Vôi sống để trong không khí sẽ bị chuyển hóa thành vôi tôi và muối cacbonat:
\(CaO + H_2O \rightarrow Ca(OH)_2\)
\(Ca(OH)_2 + CO_2\rightarrow CaCO_3 + H_2O\)
Ống thủy tinh hở miệng đựng dung dịch axit sunfuric.
Bình đựng dung dịch natri hidro cacbonat có nồng độ cao.
Bình thường, bình chữa cháy được để thẳng đứng, không được để nằm. Khi chữa cháy, phải dốc ngược bình lên.
Vì sao bình chữa cháy loại này khi bảo quản phải để thẳng đứng nhưng khi chữa cháy lại phải dốc ngược bình lên? Viết PTHH của phản ứng xảy ra trong bình cứu hỏa.
Câu trả lời của bạn
Bình chữa cháy loại này khi bảo quản phải để đứng không được để nằm vì nếu để nằm, axit sẽ chảy ra ngoài và phản ứng với natri hidrocacbonat làm mất tác dụng chữa cháy của nó.
Khi chữa cháy phải dốc ngược bình để các chất phản ứng với nhau.
PTHH: \(NaHCO_3 + H_2SO_4 \rightarrow Na_2SO_4 + CO_2 + H_2O\)
(1) \(...\;CuO\; +\; ...\;HCl \;\rightarrow\; ...\;CuCl_2\; +\; ...\;H_2O\)
(2) \(...\;CO_2\; +\; ...\;NaOH \;\rightarrow\; ...\;Na_2CO_3\; +\; ...\;H_2O\)
(3) \(...\;K_2O\; +\; ...\;H_2O \;\rightarrow\; ...\;KOH\)
(4) \(...\;Cu(OH)_2\;\overset{t^0}{\rightarrow}\; ...\;CuO\; +\; ...\;H_2O\)
(5) \(...\;SO_2\; +\; ...\;H_2O \;\rightarrow\; ...\;H_2SO_3\)
(6) \(...\;Mg(OH)_2\; +\; ...\;H_2SO_4 \;\rightarrow\; ...\;MgSO_4\; +\; ...\;Na_2SO_4\)
(7) \(...\;CuSO_4\; +\; ...\;NaOH \;\rightarrow\; ...\;Cu(OH)_2\; +\; ...\;H_2O\)
(8) \(...\;AgNO_3\; +\; ...\;HCl \;\rightarrow\; ...\;AgCl\; +\; ...\;HNO_3\)
(9) \(..\;H_2SO_4\; +\; ...\;ZnO\;\rightarrow\; ...\;ZnSO_4\; +\; ...\;H_2O\)
Câu trả lời của bạn
(1) \(CuO\; +\; 2\;HCl \;\rightarrow\;CuCl_2\; +\;2\;H_2O\)
\(\text{Oxit bazo}....\text{Axit}.......\text{Muối}....\text{Nước}............................................\)
(2) \(CO_2\; +\; 2\;NaOH \;\rightarrow\; Na_2CO_3\; +\;H_2O\)
\(\text{Oxit axit}.....\text{Bazo}........\text{Muối}......\text{Nước}........................................\)
(3) \(K_2O\; +\;H_2O \;\rightarrow\;2\;KOH\)
\(\text{Oxit bazo}...\text{Nước}.....\text{Bazo}.......................................................\)
(4) \(Cu(OH)_2\;\overset{t^0}{\rightarrow}\;CuO\; +\;H_2O\)
\(....\text{Bazo}.....\text{Oxit bazo}...\text{Nước}..................................................\)
(5) \(SO_2\; +\;H_2O \;\rightarrow\; H_2SO_3\)
\(\text{Oxit axit}..\text{Nước}......\text{Axit}........................................................\)
(6) \(Mg(OH)_2\; +\;H_2SO_4 \;\rightarrow\;MgSO_4\; +\; 2\;H_2O\)
\(...\text{Oxit bazo}......\text{Axit}.......\text{Muối}......\text{Nước}....................................\)
(7) \(CuSO_4\; +\; 2\;NaOH \;\rightarrow\;Cu(OH)_2\; +\; Na_2SO_4\)
\(....\text{Muối}.......\text{Bazo}......\text{Bazo mới}.....\text{Muối mới}.................................\)
(8) $AgNO_3\; +\;HCl \;\rightarrow\; AgCl\; +\; HNO_3\)
\(....\text{Muối}.....\text{Axit}...\text{Muối mới}..\text{Axit mới}.........................................\)
(9) \(H_2SO_4\; +\; ZnO\;\rightarrow\; ZnSO_4\; +\; H_2O\)
\(...\text{Axit}...\text{Oxit bazo}.....\text{Muối}.....\text{Nước}..........................................\)
Câu trả lời của bạn
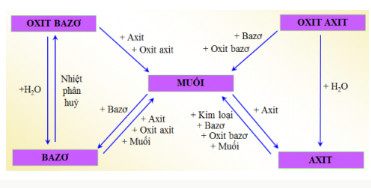
Các loại hợp chất vô cơ trên có thể chuyển hóa cho nhau thông qua phản ứng trao đổi.
Cho biết những cặp chất nào trong ví dụ trên có thể phản ứng với nhau. Viết PTHH của phản ứng.
Câu trả lời của bạn
Các loại hợp chất vô cơ đã học:
Oxit: \(CO_2,\;K_2O,\;...\)
Axit: \(HCl,\; H_2SO_4\)
Bazo: \(KOH,\; Ca(OH)_2,\;...\)
Muối: \(NaCl,\; BaSO_4,\;...\)
PTHH:
\(CO_2 + 2KOH \rightarrow K_2CO_3 + H_2O\)
\(CO_2 + Ca(OH)_2 \rightarrow CaCO_3 + H_2O\)
\(K_2O + 2HCl \rightarrow 2KCl + H_2O\)
\(K_2O + H_2SO_4 \rightarrow K_2SO_4 + H_2O\)
\(HCl + KOH \rightarrow KCl + H_2O\)
\(2HCl + Ca(OH)_2 \rightarrow CaCl_2 + 2H_2O\)
\(H_2SO_4 + 2KOH \rightarrow K_2SO_4 + 2H_2O\)
\(H_2SO_4 + Ca(OH)_2 \rightarrow CaSO_4 + 2H_2O\)
Câu trả lời của bạn
\(K_2O +2HCl \rightarrow 2KCl + H_2O\)
\(CO_2 +2NaOH \rightarrow Na_2CO_3+ H_2O$\)
\(SO_2 +H_2O \rightarrow H_2SO_3\)
\(BaCl_2 +H_2SO_4 \rightarrow BaSO_4 + 2HCl\)
\(Zn+2HCl \rightarrow ZnCl_2 + H_2\)
\(Cu(OH)_2 +H_2SO_4 \rightarrow CuSO_4 + 2H_2O\)
\(Ba(OH)_2 +Na_2SO_4 \rightarrow BaSO_4 + 2NaOH\)
\(Mg(OH)_2 \overset{t^0}{\rightarrow} MgO + H_2O\)
\(Na_2O +H_2O \rightarrow 2NaOH\)
a) Dựa vào mối quan hệ giữa các chất, em hãy sắp xếp các chất trên thành sơ đồ chuyển hóa phù hợp (mỗi mũi tên biểu diễn một PTHH).
b) Viết các PTHH của sơ đồ chuyển hóa ở phần a.
Câu trả lời của bạn
a) \(Na_2O \overset{(1)}{\rightarrow} NaOH \overset{(2)}{\rightarrow} Na_2SO_3 \overset{(4)}{\rightarrow} SO_2 \overset{(3)}{\rightarrow} H_2SO_3\)
b)
(1) \(Na_2O + H_2O \rightarrow 2NaOH\)
(2) \(2NaOH + H_2SO_3 \rightarrow Na_2SO_3 + 2H_2O\)
(3) \(Na_2SO_3 + 2HCl \rightarrow 2NaCl + SO_2 + H_2O\)
(4) \(SO_2 + H_2O \rightarrow H_2SO_3\)
a) Dựa vào mối quan hệ giữa các chất, em hãy sắp xếp các chất trên thành một dãy chuyển đổi hóa học.
b) Viết các PTHH cho dãy chuyển hóa trên.
Câu trả lời của bạn
a) \(Na \overset{(1)}{\rightarrow} Na_2O \overset{(2)}{\rightarrow} NaOH \overset{(3)}{\rightarrow} Na_2CO_3 \overset{(4)}{\rightarrow} Na_2SO_4 \overset{(5)}{\rightarrow} NaCl\)
b)
(1) \(4Na + O_2 \rightarrow 2Na_2O\)
(2) \(Na_2O + H_2O \rightarrow 2NaOH\)
(3) \(2NaOH + CO_2 \rightarrow Na_2CO_3 + H_2O\)
(4) \(Na_2CO_3 + H_2SO_4 \rightarrow Na_2SO_4 +CO_2 + H_2O\)
(5) \(Na_2SO_4 + BaCl_2 \rightarrow 2NaCl + BaSO_4\)
Câu trả lời của bạn
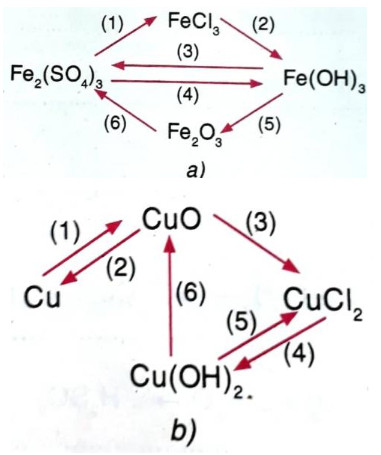
a)
(1) \(Fe_2(SO_4)_3 + 3BaCl_2 \rightarrow 2FeCl_3 + 3BaSO_4\)
(2) \(FeCl_3 + 3NaOH \rightarrow Fe(OH)_3 + 3NaCl\)
(3) \(2Fe(OH)_3 + 3H_2SO_4\rightarrow Fe_2(SO_4)_3 + 6H_2O\)
(4) \(Fe_2(SO_4)_3 + 6KOH \rightarrow 2Fe(OH)_3 + 3 K_2SO_4\)
(5) \(2Fe(OH)_3 \overset{t^0}{\rightarrow } Fe_2O_3 + 3H_2O\)
(6) \(Fe_2O_3 + 3H_2SO_4 \rightarrow Fe_2(SO_4) + 3H_2O\)
b)
(1) \(2Cu + O_2 \rightarrow 2CuO\)
(2) \(2CuO \overset{t^0}{\rightarrow }2Cu + O_2\)
(3) \(CuO + 2HCl \rightarrow CuCl_2 +H_2O\)
(4) \(CuCl_2 + 2NaOH \rightarrow Cu(OH)_2 + 2NaCl\)
(5) \(Cu(OH)_2 + 2HCl \rightarrow CuCl_2 + 2H_2O\)
(6) \(Cu(OH)_2 \overset{t^0}{\rightarrow } CuO + H_2O\)

Câu trả lời của bạn
Câu trả lời của bạn
Câu trả lời của bạn
Bari oxit có công thức hóa học là BaO
Câu trả lời của bạn
- Oxit bazơ là oxit của kim loại và tương ứng với một bazơ.
- Ví dụ: BaO, FeO, K2O,...
BaO tương ứng với bazơ bari hiđroxit Ba(OH)2.
FeO tương ứng với bazơ sắt (II) hiđroxit Fe(OH)2.
K2O tương ứng với bazơ kali hiđroxit KOH.
- Chú ý: Một số kim loại nhiều hóa trị cũng tạo ra oxit axit.
Ví dụ: mangan (VII) oxit Mn2O7 là oxit axit, tương ứng với axit pemanganic HMnO4.
Câu trả lời của bạn
nS = 3,2/32 = 0,1 mol; nO2 = 2,24/22,4= 0,1 mol
S + O2 → SO2
0,1 0,1 0,1
Theo phương trình hóa học S và O2 phản ứng hết; Sau phản ứng thu được 0,1 mol SO2.
mSO2 = 0,1.(32 + 16.2) = 6,4 gam.
Câu trả lời của bạn
nO2 = 2,4 /32 = 0,075 mol
2KClO3 → 2KCl + 3O2
0,05 0,075
Theo PTHH có số mol KClO3 = 0,05 mol
Khối lượng KClO3 là:
m = n.M = 0,05. (39 + 35,5 + 16.3) = 6,125 gam.
Câu trả lời của bạn
mN / mO = 7/8
nN = 1/2
nO = 1/2
nN / nO = 1: 1
⇒ Công thức cần tìm là NO
Câu trả lời của bạn
- Oxit là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxi.
- Ví dụ một số oxit: CuO, NO2, CO, K2O,...
- Tổng quát: Công thức hóa học của oxit: MxOy
Trong đó:
M là nguyên tố khác oxi (M có hóa trị n)
x, y lần lượt là chỉ số kèm theo của nguyên tố M, O.
→ Theo quy tắc hóa trị có: n.x = II. Y
- Oxit được phân thành hai loại chính là oxit axit và oxit bazơ.
Câu trả lời của bạn
- Đối với oxit của kim loại:
Tên oxit = tên kim loại + hóa trị (nếu kim loại có nhiều hóa trị) + oxit
Ví dụ:
K2O: Kali oxit
Al2O3: Nhôm oxit
FeO: sắt (II) oxit
Fe2O3: sắt(III) oxit
CuO: đồng (II) oxit.
- Đối với oxit của phi kim:
Tên oxit = tiền tố chỉ số nguyên tử phi kim + tên phi kim + tiền tố chỉ số nguyên tử oxi + oxit
Cụ thể:
Tiền tố mono là 1; đi là 2; tri là 3; tetra là 4; penta là 5, hexa là 6; hepta là 7...
Ví dụ:
CO: cacbon mono oxit, nhưng thường đơn giản đi gọi cacbon oxit.
SO2: lưu huỳnh đioxit,
P2O5: điphotpho pentaoxit.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *