Nội dung bài học trình bày vị trí của kim loại trong Bảng hệ thống tuần hoàn; cấu tạo của kim loại cũng như liên kết kim loại.
Nguyên tử của hầu hết các nguyên tố kim loại đều có ít electron ở lớp ngoài cùng (1, 2 hoặc 3e).
Ví dụ: Na: [Ne]3s1 Mg: [Ne]3s2 Al: [Ne]3s23p1
Trong chu kì, nguyên tử của nguyên tố kim loại có bán kính nguyên tử lớn hơn và điện tích hạt nhân nhỏ hơn so với các nguyên tử của nguyên tố phi kim.
Ví dụ: 11Na 12Mg 13Al 14Si 15P 16S 17Cl
0,157 0,136 0,125 0,117 0,110 0,104 0,099
Lập phương tâm diện: Cu, Ag, Au, Al...
Lập phương tâm khối: Li, Na, K,...
Lục phương: Be, Mg, Zn...
Liên kết kim loại là liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể do có sự tham gia của các electron tự do.
Cation M+ có cấu hình electron ở phân lớp ngoài cùng là 2p6. Nguyên tử M là:
Cation M+ mất đi 1electron nên khi trung hòa về điện tích ta có cấu hình của M là : 1s22s22p63s1. Vậy tổng số electron là 11, suy ra kim loại M là Natri.
A, B, C là các kim loại chuyển tiếp và đều thuộc chu kỳ 4 trong bảng tuần hoàn (ZA < ZB < ZC). Biết rằng tổng số electron lớp ngoài cùng của A, B và C bằng 4; tổng số electron ở lớp ngoài cùng và phân lớp sát ngoài cùng của B là 8. A, B, C là các nguyên tố nào?
Cấu hình electron của A, B, C có dạng: \([Ar]3d^a4s^a4p^b\)
Do tổng số electron lớp ngoài cùng của A, B, C = 4 nên phải có hai nguyên tố có cấu hình electron lớp ngoài cùng dạng 4s1 và một nguyên tố còn lại 4s2
Vì B có tổng số electron ở lớp ngoài cùng và phân lớp sát ngoài cùng là 8 nên B có cấu hình: \([Ar]3d^64s^ 2\)
Vậy A là: \([Ar]3d^54s^ 1\) và C là: \([Ar]3d^104s^ 1 \rightarrow A: \ _{24}Cr; \ B: \ _{26}Fe; \ C: \ _{29}Cu\)
Trong mạng tinh thể kim loại có những thành phần nào? Có mấy loại mạng tinh thể. Lấy ví dụ.
Trong mạng tinh thể kim loại có các ion dương kim loại và các electron tự do.
Có 3 loại mạng tinh thể là
+ Lập phương tâm diện: Cu, Ag, Au, Al...
+ Lập phương tâm khối: Li, Na, K,...
+ Lục phương: Be, Mg, Zn...
Cho 1,2 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 1,12 lít H2 (đktc). Kim loại đó là:
M + 2HCl → MCl2 + H2
⇒ nM = \(n_{H_{2}}\) = 0,05 mol
⇒ MM = 24g (Mg)
Hòa tan hết 8 gam hỗn hợp X gồm Fe và Mg bằng dung dịch H2SO4 loãng, dư thu được 4,48 lít khí H2 ở đktc. Phần trăm khối lượng của Fe trong hỗn hợp X là:
Hướng dẫn:
Theo bài giải ra có hệ pt:
\(\left\{\begin{matrix} 56n_{Fe} + 24n_{Mg} = 8 \\ 2n_{Fe} + 2n_{Mg} = 0,2 \end{matrix}\right. \Rightarrow \left\{\begin{matrix} n_{Fe} = 0,1 \\ n_{Mg} = 0,1 \end{matrix}\right. \Rightarrow \%m_{Fe} = \frac{0,1.56}{8} .100\% = 70 \ \%\)
Trong hỗn hợp X gồm Fe2O3; ZnO; Cu tác dụng với dung dịch HCl dư thu được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH loãng dư thu được lượng kết tủa gồm:
Hướng dẫn:
X + HCl vẫn có kim loại dư ⇒ đó là Cu
⇒ Xảy ra phản ứng: 2Fe3+ + Cu → 2Fe2+ + Cu2+ (Fe3+ hết)
⇒ Y gồm: Fe2+; Zn2+; Cu2+
Y + NaOH dư thì Zn(OH)2 tan ⇒ kết tủa gồm: Fe(OH)2; Cu(OH)2
Bài 2:
Hỗn hợp X gồm Zn, Mg và Fe. Hòa tan hết 23,40 gam hỗn hợp X vào dung dịch HCl thu được 11,20 lit khí (đktc). Để tác dụng với vừa hết 23,40 g hỗn hợp X cần 12,32 lit khí Clo (dktc). Khối lượng của Fe trong hỗn hợp là:
Hướng dẫn:
Bảo toàn e:
+) X + HCl: 2nZn + 2nMg + 2nFe = 2n\(\tiny H_2\) = 1,0 mol
+) X + Cl2: 2nZn + 2nMg + 3nFe = 2n\(\tiny Cl_2\) = 1,1 mol
⇒ nFe = 1,1 - 1,0 = 0,1 mol ⇒ mFe = 5,6 g
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 12 Bài 17có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Ion M2+ có cấu hình electron ở lớp ngoài cùng là 3s23p6. Vị trí M trong bảng hệ thống tuần hoàn là:
Ion X2+ có cấu hình electron ở trạng thái cơ bản là 1s22s22p6. Số hạt mang điện trong ion X2+ là:
Kim loại tan trong dung dịch HCl là:
Các kim loại có cấu tạo mạng tinh thể lục phương là:
Hòa tan hoàn toàn 19,5 gam Zn và 4,8 gam Mg bằng dung dịch H2SO4 loãng, thu được V lít H2 (đktc). Giá trị của V là:
Phát biểu nào sau đây là sai ?
Nguyên tố X ở ô số 24 của bảng tuần hoàn. Một học sinh đã đưa ra các nhận xét về nguyên tố X như sau :
(1) X có 6 e hoá trị yà là nguyên tố kim loại.
(2) X là một nguyên tố nhóm d.
(3) X nằm ở chu kì 4 của bảng tuần hoàn.
(4) Ở trạng thái cơ bản, X có 6 e ở phân lớp s;
Trong các nhận xét trên, số nhận xét đúng là
Câu 8-20: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 12 Bài 17.
Bài tập 1 trang 82 SGK Hóa học 12
Bài tập 2 trang 82 SGK Hóa học 12
Bài tập 3 trang 82 SGK Hóa học 12
Bài tập 4 trang 82 SGK Hóa học 12
Bài tập 5 trang 82 SGK Hóa học 12
Bài tập 6 trang 82 SGK Hóa học 12
Bài tập 7 trang 82 SGK Hóa học 12
Bài tập 8 trang 82 SGK Hóa học 12
Bài tập 9 trang 82 SGK Hóa học 12
Bài tập 1 trang 112 SGK Hóa 12 Nâng cao
Bài tập 2 trang 122 SGK Hóa 12 Nâng cao
Bài tập 3 trang 112 SGK Hóa 12 Nâng cao
Bài tập 4 trang 112 SGK Hóa 12 nâng cao
Bài tập 5 trang 112 SGK Hóa học 12 nâng cao
Bài tập 6 trang 112 SGK Hóa 12 Nâng cao
Bài tập 7 trang 112 SGK Hóa 12 Nâng cao
Bài tập 8 trang 112 SGK Hóa 12 Nâng cao
Bài tập 9 trang 113 SGK Hóa 12 Nâng cao
Bài tập 10 trang 113 SGK Hóa 12 nâng cao
Bài tập 11 trang 113 SGK Hóa 12 Nâng cao
Bài tập 12 trang 113 SGK Hóa 12 Nâng cao
Bài tập 17.1 trang 35 SBT Hóa học 12
Bài tập 17.2 trang 35 SBT Hóa học 12
Bài tập 17.3 trang 35 SBT Hóa học 12
Bài tập 17.4 trang 35 SBT Hóa học 12
Bài tập 17.5 trang 36 SBT Hóa học 12
Bài tập 17.6 trang 36 SBT Hóa học 12
Bài tập 17.7 trang 36 SBT Hóa học 12
Bài tập 17.8 trang 36 SBT Hóa học 12
Bài tập 17.9 trang 36 SBT Hóa học 12
Bài tập 17.10 trang 36 SBT Hóa học 12
Bài tập 17.11 trang 36 SBT Hóa học 12
Bài tập 17.12 trang 37 SBT Hóa học 12
Bài tập 17.13 trang 37 SBT Hóa học 12
Bài tập 17.14 trang 37 SBT Hóa học 12
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Ion M2+ có cấu hình electron ở lớp ngoài cùng là 3s23p6. Vị trí M trong bảng hệ thống tuần hoàn là:
Ion X2+ có cấu hình electron ở trạng thái cơ bản là 1s22s22p6. Số hạt mang điện trong ion X2+ là:
Kim loại tan trong dung dịch HCl là:
Các kim loại có cấu tạo mạng tinh thể lục phương là:
Hòa tan hoàn toàn 19,5 gam Zn và 4,8 gam Mg bằng dung dịch H2SO4 loãng, thu được V lít H2 (đktc). Giá trị của V là:
Phát biểu nào sau đây là sai ?
Nguyên tố X ở ô số 24 của bảng tuần hoàn. Một học sinh đã đưa ra các nhận xét về nguyên tố X như sau :
(1) X có 6 e hoá trị yà là nguyên tố kim loại.
(2) X là một nguyên tố nhóm d.
(3) X nằm ở chu kì 4 của bảng tuần hoàn.
(4) Ở trạng thái cơ bản, X có 6 e ở phân lớp s;
Trong các nhận xét trên, số nhận xét đúng là
Xét 2 nguyên tố ở vị trí 19 và 29 trong bảng tuần hoàn. Kết luận nào sau đây là sai ?
Mạng tinh thể kim loại gồm có:
Cấu hình electron nguyên tử của ba nguyên tố X, Y, Z lần lượt là 1s22s22p63s2, 1s22s22p63s23p64s1, 1s22s22p63s1. Nếu xếp theo chiều tăng dần tính kim loại thì cách sắp xếp nào sau đây đúng ?
Kết luận nào sau đây sai?
Các nguyên tố nhóm A có cấu hình e lớp ngoài cùng ns2 đều là các kim loại.
Nguyên tố có Z = 19 có bán kính lớn hơn nguyên tố có Z = 11
Li là kim loại có độ âm điện lớn nhất trong số các kim loại kiềm
R là một kim loại thuộc nhóm IA của bảng tuần hoàn. Lấy 17,55 gam R tác dụng với 25 gam dung dịch HCl 29,2%. Sau khi phản ứng xảy ra hoàn toàn cho bốc hơi cẩn thận dung dịch tạo thành trong điều kiện không có không khí thì thu được 28,9 gam hỗn hợp rắn gồm hai chất. Kim loại R là:
Kim loại M phản ứng với oxi để tạo thành oxit. Khối lượng oxi đã phản ứng bằng 40% khối lượng kim loại đã dùng. Kim loại M là:
Một viên bi sắt có đường kính 2cm ngập trong một cốc chứa 100ml axit có pH = 0, phản ứng xảy ra hoàn toàn. Bán kính viên bi sắt sau phản ứng (coi rằng viên bi bị mòn đều từ mọi phí, khối lượng riêng của sắt là 7,8 g/cm3) là:
Nhóm A bao gồm các nguyên tố:
Nguyên tố s
Nguyên tố p
Nguyên tố d và nguyên tố f.
Cho nguyên tố có kí hiệu là 12X. Vị trí của X trong bảng tuần hoàn:
Nhóm IIA, chu kì 3
Nhóm IA, chu kì 3
Nhóm IIIA, chu kì 2
X, Y là 2 muối cacbonat của kim loại nhóm IIA thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Hoà tan 28,4 gam hỗn hợp X, Y bằng dung dịch HCl thu được 6,72 lít khí CO2 (đktc). Các kim loại nhóm IIA là:
Be và Mg.
Mg và Ca.
Khi hoà tan hoàn toàn 3 gam hỗn hợp hai kim loại nhóm IA trong dung dịch HCl dư thu được 0,672 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được a gam muối khan, giá trị của a là
4,90 gam
5,71 gam
Độ âm điện của các nguyên tố: Na, Mg, Al, Si. Xếp theo chiều tăng dần là:
Na < Mg < Al < Si
Si < Al < Mg < Na
Si < Mg < Al < Na
Bán kính nguyên tử các nguyên tố: Na, Li, Be, B. Xếp theo chiều tăng dần là:
B < Be < Li < Na
Na < Li < Be < B
Li < Be < B < Na
Hai lá kim loại cùng chất, có khối lượng bằng nhau. Một được ngâm vào dung dịch Cd(NO3)2, một được ngâm vào dung dịch Pb(NO3)2. Cả hai lá kim loại đều bị oxi hóa thành ion kim loại 2+. Sau một thời gian, lấy các lá kim loại ra khỏi dung dịch. Nhận thấy khối lượng lá kim loại được ngâm trong muối Cađimi tăng thêm 0,47%; còn lá kia tăng thêm 1,42%. Biết khối lượng của hai lá kim loại tham gia phản ứng là như nhau. Hãy xác định tên của lá kim loại đã dùng.
Liên kết kim loại là liên kết được hình thành do
A. các đôi electron dùng chung giữa 2 nguyên tố
B. sự nhường cặp electron chưa tham gia liên kết của nguyên tử này cho nguyên tử kia để tạo thành liên kết giữa 2 nguyên tử
C. lực hút tĩnh điện giữa ion dương và ion âm
D. sự tham gia của các electron tự do giữa các nguyên tử và ion kim loại trong mạng tinh thể
Những nhóm nguyên tố nào dưới đây ngoài nguyên tố kim loại còn có nguyên tố phi kim
A. Tất cá các nguyên tố f
B. Tất cá các nguyên tố d
C. Tất cá các nguyên tố s (trừ nguyên tố H)
D. Tất cá các nguyên tố p
Tính chất hóa học đặc trưng của kim loại là tính khử (dễ bị oxi hóa thành ion dương) vì:
A. Nguyên tử kim loại thường có 5, 6, 7 electron lớp ngoài cùng.
B. Nguyên tử kim loại có năng lượng ion hóa nhỏ.
C. Kim loại có xu hướng thu thêm electron để đạt cấu hình của khí hiếm.
D. Nguyên tử kim loại có độ âm điện lớn.
Cho các kim loại: Na, Ca, Fe, Zn, Cu, Ag. Những kim loại không khử được H2O, dù ở nhiệt độ cao là
A. Fe, Zn, Cu, Ag
B. Cu,Ag
C. Na, Ca, Cu, Ag
D. Fe, Cu, Ag
Cho a mol Mg và b mol Zn vào dung dịch chứa c mol Cu2+và d mol Ag+. Biết rằng a < c + d/2. Để được dung dịch chứa 3 ion kim loại thì mối quan hệ giữa b và a, c, d là
A. b > c - a
B. b < c - a
C. b > c - a + d/2
D. b < c - a + d/2
M là kim loại trong số các kim loại sau: Cu, Ba, Zn, Mg. Dung dịch muối MCl2 phản ứng với dung dịch Na2CO3 hoặc Na2SO4 tạo kết tủa, nhưng không tạo kết tủa khi phản ứng với dung dịch NaOH. Kim loại M là
A. Mg
B. Cu
C. Ba
D. Zn
Tổng số hạt proton, nơtron, electron trong nguyên tử của một nguyên tố là 155.Số hạt mang điện nhiều hơn số hạt không mang điện là 33. Nguyên tố đó là
A. bạc.
B. đồng,
C. chì.
D. sắt.
Một nguyên tử có tổng số hạt proton, nơtron, electron là 40. Đó là nguyên tử của nguyền tố nào sau đây ?
Ạ. Canxi
B. Bari
C. Nhôm
D. Sắt
Những tính chất vật lí chung của kim loại (tính dẻo, dẫn nhiệt, dẫn điện, ánh kim) gây ra do
A. khối lượng nguyên tử kim loại
B. cấu trúc mạng tinh thể kim loại mạnh
C. tính khử của kim loại
D. Các electron tự do trong kim loại
Dãy sắp xếp nào sau đây đúng theo thứ tự giảm dần bán kính của nguyên tử và ion?
A. Ne > Na+ > Mg2+
B. Na+ > Ne > Mg2+
C. Na+ > Mg2+ > Ne
D. Mg2+ > Na+ > Ne
Nguyên tử Na và Cl có các lớp electron là: (Na) 2/8/1; (Cl) 2/8/7. Trong phản ứng hóa học các nguyên tử Na và Cl đạt được cấu hình bền với 8 e lớp ngoài cùng bằng cách
A. hai nguyên tử góp chung electron
B. nguyên tử Na nhường 1e cho nguyên tử Cl để cho lớp electron ngoià cùng của nguyên tử Na và Cl đều có 8e
C. nguyên tử Cl nhường 7e cho nguyên tử Na để cho lớp electron ngoài cùng của nguyên tử Cl và Na đều có 8e
D. tùy điều kiện phản ứng mà nguyên tử Na nhường e hoặc nguyên tử Cl nhường e
Viết cấu hình electron nguyên tử của các nguyên tố kim loại : K, Ca, Al, Fe, Cu, Cr. Có nhận xét gì về cấu hình electron nguyên tử của các nguyên tố
Hãy so sánh số electron ở lớp ngoài cùng của nguyên tử kim loại nhóm IA, IIA và phi kim nhóm VIA, VIIA.
Dựa vào khối lượng riêng của kim loại, hãy tính thể tích mol kim loại và ghi kết quả vào bảng sau:
| Tên kim loại | Khối lượng riêng (g/cm3) | Thể tích mol (g/cm3) |
| Kali (K) | 0,86 | |
| Natri (Na) | 0,97 | |
| Magie (Mg) | 1,74 | |
| Nhôm (AI) | 2,70 | |
| Kẽm (Zn) | 7,14 | |
| Sắt (Fe) | 7,87 | |
| Đồng (Cu) | 8,92 | |
| Bạc (Ag) | 10,50 | |
| Vàng (Au) | 19,30 |
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Thành phần % theo khối lượng của axit cacboxylic có phân tử khối nhỏ hơn trong X là
A. 28,64%.
B. 19,63%.
C. 30,62%.
D. 14,02%
Thành phần % theo khối lượng của axit cacboxylic có phân tử khối lớn hơn trong X gần nhất là
A. 14,0%.
B. 19,6%.
C. 30,6%.
D. 20,0%.
Câu trả lời của bạn
Quy đổi X thành Gly (a), HCOOH (b), CH2 (c) và CO2 (d)
nNaOH = a + b + d = 0,5
m muối = 75a + 46b + 14c + 44d + 0,5.40 – 0,5.18 = 41,05
nO2 = 2,25a + 0,5b + 1,5c = 0,7875
nCO2 + nN2 = 2a + b + c + d + 0,5a = 0,925
—> a = 0,15; b = 0,3; c = 0,2; d = 0,05
—> nGlu = d = 0,05 và nGly = a – d = 0,1
Bảo toàn C —> nC của axit cacboxylic = 0,4
—> Số C = 0,4/b = 1,333
—> HCOOH (0,2) và CH3COOH (0,1)
—> %HCOOH = 30,62% và %CH3COOH = 19,97%
A. 48,4.
B. 44,8.
C. 46,2.
D. 42,6.
Câu trả lời của bạn
X gồm CH3COONa (x), CaO (y) và NaOH (x + y)
—> Y gồm Na2CO3 (x), NaOH dư (y) và CaO (y)
Y + H2O —> CaCO3 (y) và dung dịch Z chứa Na2CO3 dư (x – y) và NaOH (3y)
Khi bắt đầu thoát khí:
nH+ = x – y + 3y = 0,5
Khi khí thoát ra hết:
nH+ = 2(x – y) + 3y = 0,7
—> x = 0,3 và y = 0,1
—> mX = 46,2 gam
(2) Khí CO2 là khí gây ra hiệu ứng nhà kính.
(3) Cho Ba dư vào dung dịch Al2(SO4)3 thu được khí và sau phản ứng thu được 2 loại kết tủa.
(4) Để khử độc cho phòng thí nghiệm bị nhiểm khí Clo người ta dùng khí amoniac.
(5) Dung dịch thu được sau khi điện phân dung dịch NaCl có màng ngăn chứa NaOH và NaCl, để tách chúng ra khỏi nhau người ta dùng phương pháp kết tinh.
(6) Cho dung dịch NaOH vào dung dịch FeCl2 (trong không khí) lúc đầu thấy xuất hiện kết tủa mà trắng xanh sau đó chuyển dần sang màu nâu đỏ.
(7) Cho dung dịch Na2CO3 vào dung dịch AlCl3, thu được kết tủa keo trắng và có khí thoát ra.
Có bao nhiêu khẳng định đúng?
A. 3
B. 4
C. 5
D. 6
Câu trả lời của bạn
(1) Đúng, cặp điện cực là Fe-Cu
(2) Đúng
(3) Sai, kết tủa chỉ có BaSO4.
(4) Đúng: NH3 + Cl2 —> N2 + NH4Cl
(5) Đúng, NaOH có độ tan lớn hơn nên NaCl sẽ kết tinh trước.
(6) Đúng, Fe(OH)2 (trắng xanh) bị oxi hóa dần thành Fe(OH)3 (nâu đỏ).
(7) Đúng: Na2CO3 + AlCl3 + H2O —> Al(OH)3 + NaCl + CO2
.png)
Giá trị của b bằng
A. 2,50.
B. 2,80.
C. 2,70.
D. 2,60.
Câu trả lời của bạn
B gồm N2 (0,15) và H2 (0,15)
Bảo toàn N —> nNH4+ = 0,06
Bảo toàn electron —> a = 0,76
nH+ phản ứng = 12nN2 + 2nH2 + 10nNH4+ = 2,7
—> nH+ dư = b – 2,7
nNaOH = nH+ dư + nNH4+ + 4nAl3+ – nAl(OH)3
—> 2,68 = (b – 2,7) + 0,06 + 0,76.4 – 13.0,76/19
—> b = 2,8
A. 12,89%.
B. 16,11%.
C. 9,67%.
D. 3,22%.
Câu trả lời của bạn
nMg2+ = nMg(OH)2 = 0,21
nNH4+ = nNH3 = 0,02
nOH- = 2nMg2+ + nNH4+ + 4nAl3+ = 0,68
—> nAl3+ = 0,06
Dung dịch Y chứa Mg2+ (0,21), Al3+ (0,06), NH4+ (0,02), K+ (a + 0,69) và SO42- (0,69)
Bảo toàn điện tích —> a = 0,07
Bảo toàn khối lượng —> nH2O = 0,245
Bảo toàn H —> nH2 = 0,06
Đặt x, y là số mol NO và N2O
—> x + y + 0,06 = 0,115
m khí = 30x + 44y + 0,06.2 = 0,115.2.198/23
—> x = 0,04 và y = 0,015
nH+ = 4nNO + 10nN2O + 2nH2 + 10nNH4+ + 2nO
—> nO = 0,03
—> nAl2O3 = 0,01
Bảo toàn Al —> nAl = 0,04
—> %Al = 12,89%
A. 12,89%.
B. 16,11%.
C. 9,67%.
D. 3,22%.
Câu trả lời của bạn
nMg2+ = nMg(OH)2 = 0,21
nNH4+ = nNH3 = 0,02
nOH- = 2nMg2+ + nNH4+ + 4nAl3+ = 0,68
—> nAl3+ = 0,06
Dung dịch Y chứa Mg2+ (0,21), Al3+ (0,06), NH4+ (0,02), K+ (a + 0,69) và SO42- (0,69)
Bảo toàn điện tích —> a = 0,07
Bảo toàn khối lượng —> nH2O = 0,245
Bảo toàn H —> nH2 = 0,06
Đặt x, y là số mol NO và N2O
—> x + y + 0,06 = 0,115
m khí = 30x + 44y + 0,06.2 = 0,115.2.198/23
—> x = 0,04 và y = 0,015
nH+ = 4nNO + 10nN2O + 2nH2 + 10nNH4+ + 2nO
—> nO = 0,03
—> nAl2O3 = 0,01
Bảo toàn Al —> nAl = 0,04
—> %Al = 12,89%
(b) P, C, S tự bốc cháy khi tiếp xúc với CrO3.
(c) Trong công nghiệp thực phẩm NaHCO3 được dùng làm bột nở.
(d) Thành phân hóa học chính của đạm ure là (NH2)2CO.
(e) Trong các kim loại, sắt là nguyên tố có hàm lượng cao nhất trong vỏ quả đất.
Dãy gồm tất cả các phát biểu sai là
A. (a), (e).
B. (a), (c), (e).
C. (a),(c) (d).
D. (a), d) (e).
Câu trả lời của bạn
(a) Sai, thu được khí than ướt.
(b) Đúng
(c) Đúng
(d) Đúng
(e) Sai, Fe là kim loại có hàm lượng cao thứ 2, sau nhôm.
A. 19,56.
B. 20,16.
C. 18,64.
D. 17,96.
Câu trả lời của bạn
Y chứa 3 muối gồm AlCl3 (a), CuCl2 (b) và FeCl2 (2b) (Bảo toàn electron nên nCu = nFe2O3).
Y + AgNO3 —> 143,5(3a + 6b) + 108.2b = 116,28
Y + NaOH dư —> 98b + 90.2b = 16,68
—> a = 0,12 và b = 0,06
—> Y chứa Al2O3 (0,06), Cu (0,06), Fe2O3 (0,06)
—> mX = 19,56 gam
Câu trả lời của bạn
Đặt a, b là số mol CaCO3, MgCO3 trong X.
—> mX = 100a + 84b = 100 (1)
E là Ca(OH)2 (a mol)
nCaCO3 = 0,4 —> nCa(HCO3)2 = a – 0,4
Bảo toàn C —> a + b = 0,4 + 2(a – 0,4) (2)
(1)(2) —> a = 167/230; b = 15/46
—> %CaCO3 = 72,61%
A. 0,865 lít.
B. 0,560 lít.
C. 0,760 lít.
D. 0,785 lít.
Câu trả lời của bạn
Khí Z chứa NO (0,03) và H2 (0,13)
Bảo toàn khối lượng: mX + mKHSO4 = m muối + mZ + mH2O
—> nH2O = 0,33
Bảo toàn H —> nKHSO4 = 2nH2 + 4nNH4+ + 2nH2O
—> nNH4+ = 0,05
Bảo toàn N —> 2nFe(NO3)2 = nNO + nNH4+
—> nFe(NO3)2 = 0,04
Bảo toàn O —> nFeO + 6nFe(NO3)2 = nNO + nH2O
—> nFeO = 0,12
Đặt a, b là số mol Al, Zn
—> mX = 27a + 65a + 0,12.72 + 0,04.180 = 29,64
Y không phản ứng với Cu nên Y không chứa Fe3+. Bảo toàn electron:
3a + 2b = 3nNO + 2nH2 + 8nNH4+
—> a = b = 0,15
Bảo toàn Fe —> nFe2+(Y) = 0,16
—> nNaOH max = 4a + 4b + 0,16.2 + 0,05 = 1,57
—> VddNaOH = 0,785 lít
A. 4.
B. 1.
C. 2.
D. 3.
Câu trả lời của bạn
Các chất bị thủy phân trong cả môi trường axit và môi trường bazơ là: (2), (3), (4), (6)
Biết X có công thức phân tử C6H10O4 và chứa hai chức este. X1 có nhiều hơn X2 một nguyên tử cacbon. X3 không hòa tan Cu(OH)2. Phát biểu nào sau đây đúng?
A. Cho a mol X3 tác dụng hoàn toàn với Na dư thì thu được a/2 mol H2.
B. X5 không tham gia phản ứng tráng bạc.
C. X6 là anđehit axetic.
D. X4 có phân tử khối là 60.
Câu trả lời của bạn
(b), (c) —> X1, X2 đều là các muối có 1Na
X1 nhiều hơn X2 một nguyên tử C và X3 không hòa tan Cu(OH)2 nên:
X là HCOO-CH2-CH2-CH2-OOC-CH3
X1 là CH3COONa; X4 là CH3COOH
X2 là HCOONa; X5 là HCOOH
X6 là CH2(CHO)2
—> Phát biểu D đúng.
(b) Cho dung dịch Ba(OH)2 dư vào dung dịch phèn chua.
(c) Sục khí NH3 đến dư vào dung dịch Al2(SO4)3.
(d) Cho từ từ dung dịch HCl đến dư vào dung dịch chứa NaAlO2.
(e) Sục khí CO2 đến dư vào dung dịch NaAlO2.
(f) Cho từ từ dung dịch Al(NO3)3 đến dư vào dung dịch NaOH và khuấy đều.
Số thí nghiệm xuất hiện kết tủa sau đó kết tủa tan tạo dung dịch trong suốt là
A. 2.
B. 4.
C. 1.
D. 3.
Câu trả lời của bạn
(a) CO2 + Ca(OH)2 —> CaCO3 + H2O
CO2 + H2O + CaCO3 —> Ca(HCO3)2
(b) Ba2+ + SO42- —> BaSO4
Al3+ + OH- —> Al(OH)3
Al(OH)3 + OH- —> AlO2- + H2O
(c) NH3 + H2O + Al2(SO4)3 —> Al(OH)3 + (NH4)2SO4.
(d) HCl + NaAlO2 + H2O —> NaCl + Al(OH)3
Al(OH)3 + HCl —> AlCl3 + H2O
(e) CO2 + H2O + NaAlO2 —> NaHCO3 + Al(OH)3
(f) Al(NO3)3 + NaOH —> NaAlO2 + NaNO3 + H2O
NaAlO2 + Al(NO3)3 + H2O —> Al(OH)3 + NaNO3
A. 30,4.
B. 22,0.
C. 20,1.
D. 19,2.
Câu trả lời của bạn
nAl = 0,3; nCl- = 1,2
—> Dung dịch sau phản ứng chứa Al3+ (0,3), Cl- (1,2), bảo toàn điện tích —> Fe2+ (0,15)
—> Kim loại tách ra gồm Cu (0,3) và Fe (0,2 – 0,15 = 0,05)
—> m = 22 gam
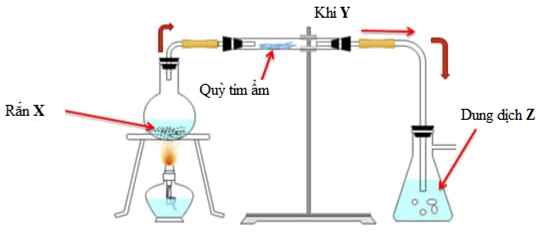
Các chất Y và Z lần lượt là
A. NH3 và NaAlO2.
B. CO2 và NaAlO2.
C. NH3 và AlCl3.
D. CO2 và Ca(AlO2)2.
Câu trả lời của bạn
Quỳ tím hóa xanh nên khí Y có tính bazơ —> Y là NH3
—> Z là AlCl3
X là hỗn hợp NH4Cl + CaO.
NH4Cl + CaO —> CaCl2 + NH3 + H2O
NH3 + H2O + AlCl3 —> Al(OH)3 + NH4Cl
(c) Nhỏ vài giọt nước brom vào dung dịch anilin.
(d) Cho dung dịch NaOH vào dung dịch glyxin.
(e) Cho dung dịch metyl fomat vào dung dịch AgNO3/NH3 dư, đun nóng.
Số thí nghiệm xảy ra phản ứng là
A. 5.
B. 4.
C. 3.
D. 2.
Câu trả lời của bạn
(a) HCOOH + C2H5NH2 —> HCOONH3C2H5
(b) Không phản ứng
(c) C6H5NH2 + Br2 —> C6H2Br3-NH2 + HBr
(d) NH2-CH2-COOH + NaOH —> NH2-CH2-COONa + H2O
(e) HCOOCH3 + AgNO3 + NH3 + H2O —> CH3-O-COONH4 + Ag + NH4NO3.
A. 52,48 gam.
B. 42,58 gam.
C. 52,68 gam.
D. 13,28 gam.
Câu trả lời của bạn
nH2SO4 = nH2 = 0,1
—> mddH2SO4 = 0,1.98/20% = 49
—> mdd sau phản ứng = m kim loại + mddH2SO4 – mH2 = 52,48 gam
– TN2: Để thanh thép trong không khí ẩm,
– TN3: Cho bột nhôm phản ứng với O2 nung nóng.
– TN4: Cho từng giọt dung dịch Fe(NO3)2 vào dung dịch AgNO3.
– TN5: Nhúng lá sắt nguyên chất vào dung dịch CuSO4.
Số thí nghiệm xảy ra ăn mòn điện hoá học là
A. 4.
B. 1.
C. 2
D. 3.
Câu trả lời của bạn
Ăn mòn điện hóa xuất hiện khi có cặp điện cực tiếp xúc với nhau và cùng tiếp xúc với dung dịch điện li.
Có 2 thí nghiệm xảy ra ăn mòn điện hóa:
TN2: Fe-C
TN5: Fe-Cu
A. 200.
B. 100.
C. 300.
D. 150.
Câu trả lời của bạn
nFe2O3 = 0,01
Fe2O3 + 3H2SO4 —> Fe2(SO4)3 + 3H2O
0,01………….0,03
—> Vdd = 150 ml
Câu trả lời của bạn
MO + H2 —> M + H2O
0,04….0,04……………0,04
M3O4 + 4H2 —> 3M + 4H2O
0,05…….0,2………………..0,2
—> nH2 tổng = 0,24 —> V = 5,376 lít
Bảo toàn khối lượng:
14,8 + 0,24.2 = mM + 0,24.18
—> mM = 10,96

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *