Ở chương V các em đã học xong về oxi, hiđro, nước; phản ứng oxi hóa - khử; phản ứng thế... Tiết học này các em sẽ được học bài luyện tập, để làm một số bài tập định tính và một số bài tập định lượng về những kiến thức trên qua bài học này.
1. Khí Hiđro có tính khử, ở nhiệt độ thích hợp Hiđro không những kết hợp được với đơn chất oxi mà còn có thể kết hợp với nguyên tố oxi trong một số oxit kim loại. Các phản ứng này đều tỏa nhiệt.
2. Khí Hiđro có nhiều ứng dụng, chủ yếu do tính chất rất nhẹ (nhẹ nhất trong các chất khí), tính khử và khi cháy tỏa nhiều nhiệt.
3. Có thể điều chế khí Hiđro trong phòng thí nghiệm bằng cách cho dung dịch axit clohiđric HCl hoặc dung dịch axit sunfuric H2SO4 loãng tác dụng với kim loại như Zn, Fe, Al. Có thể thu khí Hiđro vào bình bằng hai cách: đẩy không khí và đẩy nước (miệng bình úp xuống dưới)
4. Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố trong hợp chất.
5. Quá trình tách nguyên tử Oxi khỏi hợp chất là sự khử. Chất chiếm oxi hoặc chất nhường oxi cho chất khác là chất khử.
6. Sự tác dụng của oxi với một chất là sự oxi hóa. Đơn chất oxi hoặc chất nhường oxi cho chất khác là chất oxi hóa.
7. Phản ứng oxi hóa khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
| Khí O2 | Khí H2 | |
| Tính chất hóa học | Tính oxi hóa Tác dụng với kim loại, phi kim,hợp chất. | Tính khử Tác dụng với khí oxi và oxit kim loại |
| Điều chế trong PTN | Nhiệt phân hợp chất giàu oxi: KClO3, KMnO4… | Một số kim loại(Mg,Zn,Al…) tác dụng với dung dịch HCl, H2SO4 loãng. |
| Loại phản ứng | Phản ứng phân hủy: 2KClO3 | Phản ứng thế: Zn +2HCl → ZnCl2 + H2↑ |
| Cách thu | Đẩy không khí Đẩy nước | Đẩy không khí Đẩy nước |
| Ứng dụng | Sự hô hấp Sự đốt nhiên liệu Thuốc nổ | Nhiên liệu và bơm vào khinh khí cầu Làm nguyên liệu |
Bảng: Tóm tắt tính chất và ứng dụng của Oxi và Hiđro
Lập phương trình hóa học của các phản ứng sau và cho biết chúng thuộc loại phản ứng hóa học nào?
a) Điphotpho penta oxit + nước → axit photphoric (H3PO4)
b) Kẽm + axit sunfuric (H2SO4) → Kẽm sunfat (ZnSO4)+ hiđro
c) Thủy ngân (II) oxit Thủy ngân + oxi
a) P2O5 + 3H2O → 2 H3PO4
Đây là phản ứng hóa hợp
b) Zn + H2SO4 → ZnSO4 + H2↑
Đây là phản ứng thế
c) HgO Hg + O2↑
Đây là phản ứng phân hủy
Người ta dùng V(lít) khí H2 khử hoàn toàn hỗn hợp hai Oxit kim loại gồm: CuO và Fe2O3 ở nhiệt độ thích hợp. Sau phản ứng thu được 12g hỗn hợp gồm 2 kim loại trong đó có 6,4g Cu.
a) Viết các phương trình hóa học xảy ra.
b) Hãy tính V(lít) khí H2 cần dùng để khử hỗn hợp 2 Oxit đó. (Các thể tích khí đo ở đktc)
a) Phương trình hóa học:
H2 + CuO Cu + H2O (1)
3H2 + Fe2O3 2Fe + 3H2O (2)
b) Khối lượng của kim loại Fe là:
\({m_{Fe}} = {m_{hh}} - {m_{CuO}} = 12 - 6,4 = 5,6(gam)\)
Số mol của Sắt và Đồng lần lượt là:
\(\begin{array}{l} {n_{Fe}} = \frac{{{m_{Fe}}}}{M} = \frac{{5,6}}{{56}} = 0,1(mol)\\ {n_{CuO}} = \frac{{{m_{CuO}}}}{M} = \frac{{6,4}}{{64}} = 0,1(mol) \end{array}\)
Phương trình hóa học:
H2 + CuO Cu + H2O (1)
1 mol 1 mol
0, 1 mol \(\leftarrow\) 0,1 mol
3H2 + Fe2O3 2Fe + 3H2O (2)
3 mol 2 mol
0,15 mol \(\leftarrow\) 0,1 mol
Theo phương trình (1) và (2) thì số mol Hiđro sinh ra ở hai phản ứng là:
\(\begin{array}{l} {n_{{H_2}(1)}} = {n_{Cu}} = 0,1(mol)\\ {n_{{H_2}(2)}} = {n_{Fe}} = 0,15(mol) \end{array}\)
Tổng số mol khí Hiđro sinh ra là:
\(\sum {{n_{{H_2}}}} = 0,1 + 0,15 = 0,25(mol)\)
Thể tích khí Hiđro cần dùng ở đktc là:
\({V_{{H_2}}} = 22,4.{n_{{H_2}}} = 22,4 \times 0,25 = 5,6(lit)\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 34có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Nhờ tính chất nào mà khí hiđro có thể tác dụng được với một số oxit kim loại ở nhiệt độ thích hợp:
Ứng dụng của hiđro chủ yếu dựa vào tính chất
Hóa chất điều để điều chế hiđro trong phòng thí nghiệm là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 34.
Bài tập 1 trang 118 SGK Hóa học 8
Bài tập 2 trang 118 SGK Hóa học 8
Bài tập 3 trang 119 SGK Hóa học 8
Bài tập 4 trang 119 SGK Hóa học 8
Bài tập 5 trang 119 SGK Hóa học 8
Bài tập 6 trang 119 SGK Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Nhờ tính chất nào mà khí hiđro có thể tác dụng được với một số oxit kim loại ở nhiệt độ thích hợp:
Ứng dụng của hiđro chủ yếu dựa vào tính chất
Hóa chất điều để điều chế hiđro trong phòng thí nghiệm là:
Thu khí hiđro trong phòng thí nghiệm bằng phương pháp nào?
Phản ứng thế là phản ứng hóa học xảy ra giữa:
Cho các phản ứng sau, phản ứng nào không phải phản ứng thế
Trong các loại phản ứng dưới đây, phản ứng nào chắc chắn là phản ứng oxi hóa – khử
Cho thanh Al ngâm vào dung dịch axit clohidric thấy có khí bay lên. Xác định khí đó
Cho thanh đồng ngâm vào 400ml dung dịch axit sunfuric loãng 2M thấy trong dung dịch có khí và V bằng bao nhiêu?
Tính m(g) H2O khi cho 2,24(l) H2 tác dụng với 6,72 (l) O2(đktc)
Viết phương trình hóa học biểu diễn phản ứng của hiđro với các chất: O2, Fe2O3, Fe3O4, PbO ở nhiệt độ thích hợp. Ghi rõ điều kiện phản ứng. Giải thích và cho biết mỗi phản ứng trên thuộc loại phản ứng gì?
Có 3 lọ đựng riêng biệt các chất khí sau: khí oxi, không khí, và hiđro. Bằng thí nghiệm nào có thể nhận ra chất khí trong mỗi lọ?
Cho dung dịch axit sunfuric loãng, nhôm và các dụng cụ thí nghiệm như hình vẽ.
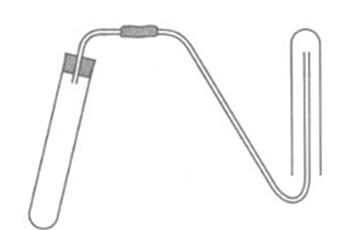
Hãy chọn câu trả lời đúng trong các câu sau:
A. Có thể dùng các hóa chất và dụng cũ đã cho để điều chế và thu khí oxi.
B. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu không khí.
C. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí hiđro.
D. Có thể dùng để điều chế hidro nhưng không thu được khí hiđro.
a) Lập phương trình hóa học của các phản ứng sau:
Cacbon đioxit + nước → Axit cacbonic (H2CO3).
Lưu huỳnh đioxit + nước → Axit sunfurơ (H2SO3).
Kẽm + axit clohiđric → Kẽm clorua + H2.
Điphotpho + nước → Axit photphoric (H3PO4).
Đồng (II) oxit + hiđro → Chì (Pb) + H2O.
b) Mỗi phản ứng hóa học trên đây thuộc loại phản ứng nào? Vì sao?
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Cho 16g hỗn hợp gồm Mg và MgO phản ứng với HCl thu 5,6l H2. Tính m từng chất trong hỗn hợp đầu
Câu trả lời của bạn
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
MgO + 2HCl \(\rightarrow\) MgCl2 + H2O
Mg + 2HCl \(\rightarrow\) MgCl2 + H2
de: 0,25 \(\leftarrow\) 0,25
\(m_{Mg}=0,25.24=6g\)
\(m_{MgO}=16-6=10g\)
C1: Dẫn 17,92 lít H2(đktc) vào 1 bình kín có chứa 69,6 gam bột Fe3O4 nung nóng:
H2 + Fe3O4 → Fe + H2O
a. Sau phản ứng chất nào còn dư? Dư bao nhiêu?
b. Muốn điều chế đc VH2 trên cần bao nhiêu gam kẽm tác dụng vs dung dịch Axit sunfuric loãng
Zn + H2SO4 → ZnSO4 + H2
C2: Nhiệt phân 24, 5 gam KClO3 , khí sinh ra cho tác dụng vs 32g Cu đun nóng. Tính khối lượng CuO tạo thành.
KClO3 → KCl + O2
Cu + O2 → CuO
Câu trả lời của bạn
Đề 3
PHẦN BÀI TẬP: 1. Bổ túc và hoàn thành phương trình phản ứng sau:
a. Al + H2SO4 → …… + H2
b. ……………. → KCl + O2
c. CH4 + …… .→ CO2 +H2O
d. CuO + H2 → Cu +………
2 Trình bày tính chất hóa học của Oxi.
3. Hòa tan hoàn toàn11,2 gam Fe vào dung dịch axit sun fu ric. Tính
a. Thể tích khí hi đro sinh ra ở đktc
b. Khôí lượng của muối sắt II sunfat (FeSO4) tạo thành
4. Một dung dịch CuSO4 có khối lượng riêng là 1,206 g/ml. Khi cô can 165,84 ml dung dịch này ngưới ta thu được 36 gam CuSO4 , Hãy xác định nồng đô phần trăm của dung dịch CuSO4 đã dùng.
(Biết Fe= 56: H= 1: S=32: O =16: Cu= 64)
Câu trả lời của bạn
3.
nFe=11,2/56=0,2(mol)
Fe+H2SO4--->FeSO4+H2
0,2___________0,2___0,2
VH2=0,2.22,4=4,48(l)
mFeSO4=0,2.152=30,4(g)
Câu 2 :
Trên 2 đĩa cân để hai cốc đựng dung dịch HCl và H2SO4 sao cho cân ở vị trí thăng bằng :
- Cho vào cốc đựng dung dịch HCl 25 g CaCO3
- Cho vào cốc đựng dung dịch H2SO4 a g Al .
Cân ở vị trí thăng bằng . Tính a , biết có các phản ứng xảy ra hoàn toàn theo phương trình :
CaCO3 + 2 HCl ----> CaCl2 + H2O + CO2
2 Al + 3H2SO4 ----> Al2(SO4)3 + 3H2
Câu 3 :
Có hỗn hợp khí CO và CO2 . Nếu cho hỗn hợp khí đi qua dung dịch Ca(OH)2 dư thì thu được 1 g chất kết tủa màu trắng . Nếu cho hỗn hợp khí này đi qua bột CuO nóng dư thì thu được 0,46 g Cu .
a)Viết phương trình phản ứng xảy ra ?
b) Tính thể tích của hỗn hợp khí ở đktc và thể tích của mỗi khí có ở trong hỗn hợp .
Câu trả lời của bạn
Câu 1:
CaCO3 + 2 HCl ----> CaCl2 + H2O + CO2(1)
2 Al + 3H2SO4 ----> Al2(SO4)3 + 3H2(2)
Do cân ở vị trí cân bằng
=>mCO2=mH2
nCaCO3=25/100=0,25(mol)
Theo pt(1): nCO2=nCaCO3=0,25(mol)
=>mCO2=0,25.44=11(g)
Vì mH2=mCO2=>mH2=11(g)
=>nH2=11/2=5,5(mol)
Theo pt (2):
nAl=2/3nH2=2/3.5,5~3,67(mol)
=>mAl=3,67.27~99(g)
Vậy a=99 (g)
đễ hòa tan hoàn toàn 7,2 gam một kim loại M có hóa trị 2 cần dùng đến 200 ml dung dịch axit clohiđric 3M. kim loại M là?
Câu trả lời của bạn
nHCl = 3 . 0,2 = 0,6 mol
Pt: M + ...2HCl --> MCl2 + H2
0,3 mol<-0,6 mol
Ta có: \(7,2=0,3M_M\)
\(\Rightarrow M_M=\dfrac{7,2}{0,3}=24\)
=> M là Magie (Mg)
Hòa tan hoàn toàn 4,6 gam Natri kim loại vào nước người ta được dung dịch kiềm. để Trung Hoà hết lượng kiềm trong dung dịch cần bao nhiêu lít Axitclohydric 0,1M ?
Câu trả lời của bạn
nNa = \(\dfrac{4,6}{23}=0,2\) mol
Pt: 2Na + 2H2O --> 2NaOH + H2
0,2 mol-------------> 0,2 mol
.....NaOH + HCl --> NaCl + H2O
0,2 mol--> 0,2 mol
VHCl cần dùng = \(\dfrac{0,2}{0,1}=2\left(l\right)\)
Co 9,28g Fe3O4 tác dụng với khí Hiđro đung nóng.Sau phản ứng thu dược chất rắn A và 1,12 lít khí và hới ở điều kiện tiêu chuẩn có khối lượng 0,74g.
a.Tính thể tích H2(BĐ)
b.Tính khối lượng A
Câu trả lời của bạn
a, sô mol khí hidro phản ứng là :\(n=\dfrac{9,28}{232}=0,04\left(mol\right)\)
Thể tích khí hidro tham gia phản ứng (đktc) là: \(V=n.22,4=0,04.22,4=0,896\left(mol\right)\)
b,
Theo quy tắc bảo toàn khối lượng, có: \(m_{Fe_3O_4}+m_{H_2}=m_A+m_{H_2O}\)
\(\Leftrightarrow9,28+\)
==" nhìn lại đê cho kiệm nhỉ khí và hới nào vậy bạn :D
Đốt cháy hoàn toàn 1 hỗn hợp gồm CO và H2, cần dùng 4,48 l khí O2 ở đktc. Thể tích khí sinh ra chứa 3,36l khí CO2.
a)Viết pt phản ứng.
b) tính % theo thể tích mỗi khí có trong hỗn hợp ban đầu.
P/s: Làm giúp mình với, đang cần gấp trong tối nay!!! @-@
Câu trả lời của bạn
PT: 2CO + O2 ---t°---> 2CO2 (1)
2H2 + O2 ---t°---> 2H2O (2)
nCO2= 4,48/22,4=0,2(mol)
theo pt (1) ta có:
nO2= 1/2nCO2= 1/2.0,2=0,1(mol)
mO2=0,1.32= 3,2(g)
nCO= nCO2 = 0,2(mol)
=>nO2(2) = 3,2- (0,1.32)/32 = 0,09(mol)
Theo pt (2) ta có:
nH2 = nO2.2 = 0,09.2 = 0,18(mol)
=> %mCO = 0,2.28/0,2.28+0,18.2.100%= 0,875%
%H2 = 100% - 0,875% = 99,125%
1/ cho các chất sau: Fe2O3, N2,Br2,NaCl,Al2O3,Na2O,P,S,PPO,K,Cu,Ag,Fe3O4,Al,SiO2,N2O5,SO2,NH3,H2S
viết phương trình phản ứng(nếu có) ghi rỗ điều kiện
a/ với oxi
b/ với H2
c/ với H2O
Câu trả lời của bạn
b.
Fe2O3 + 3H2 \(\underrightarrow{t^o}\) 2Fe + 3H2O
Fe3O4 + 4H2 \(\underrightarrow{t^o}\) 3Fe + 4H2O
c.
Na2O + H2O \(\rightarrow\) 2NaOH
2K + 2H2O \(\rightarrow\) 2KOH + H2
N2O5 + H2O \(\rightarrow\) 2HNO3
SO2 + H2O \(\rightarrow\) H2SO3
2NH3 + H2O \(\rightarrow\) (NH3)2O + H2
Câu1:Trong phòng thí nghiệm người ta dùng hidro khử Fe2O3 thu được 5.6 (g) sắt
A) Tính khối lượng Fe2O3 tham gia phản ứng
B) Tinhs khối lượng Fe3O4 thu được kh đốt toàn bộ lượng sắt trên với 2.24 lit oxit (đktc)
Câu2 : Dùng khí hidro để khử hoàn toàn 69.6 gam oxit sắt từ
A) Viết phương trình hóa học của phản ứng
B) Tính thể tích và khối lượng khí hidro cần dùng cho phản ứng (đktc)
C) Tính số gam kim loại tạo thành sau phản ứng
Câu trả lời của bạn
nFe=5,6/56=0,1(mol)
pt: Fe2O3+3H2--->2Fe+3H2O
0,05____________0,1
mFe2O3=0,05.160=8(g)
b) nO2=2,24/22,4=0,1(mol)
3Fe+2O2--->Fe3O4
3____2
0,1___0,1
Ta có: 0,1/3<0,1/2
=>O2 dư
Theo pt: nFe3O4=1/3nFe=1/3.0,1=0,033(mol)
=>mFe3O4=0,033.232=7,656(g)
1.hai nguyên tử A và B có tỉ lệ nguyên tử khối 3:2 biết tổng nguyên tử khối của A và B là 40 đvC.Tìm nguyên tử A và B
2.Nguyên tử khối của tử Y và nguyên tử C tỉ lệ 2:1.Tìm nguyên tử Y
giúp mik với,mik gấp lắm ý,MIK CẢm ơn
bài này ko làm cũng đc nha:
3.phân biệt 3 khí nito,oxi,cacbonic ở 3 bình bị mất nhãn
Câu trả lời của bạn
câu 2 tương tự. Thay M của C = 12 vô bờ giải luôn
câu 1: em hãy giải thích các hiện tượng sau:
a)Khí nitơ và khí cacbonic đều không duy trì sự cháy.Khí nào được đùng để dập tắt đám cháy?tại sao?
b)Tại sao khi mở nắp chai nước ngọt ta thấy có hiện tượng sủi bỏi khí?
câu 2:em hãy nêu hiện tượng và giải thích trong mỗi trường hợp sau:
a) Khi quạt gió vào bếp củi vừa mới tắt
b)khi quạt gió vào ngọn nến đang cháy
help help me pls !!!
Câu trả lời của bạn
1a)Phương pháp dập lửa chủ yếu dựa theo nguyên tắc đẩy khí O2 tách rời khỏi vật liệu gây cháy.
Nếu dùng N2 thì có thể thỏa mãn được yêu cầu là N2 không duy trì sự cháy nhưng N2 nhẹ hơn O2. (dN2/O2 <1) nên khi thổi N2 ra, N2 không thể đẩy O2 bay lên phía trên mà bay lên trước. Việc dập lửa không hiệu quả.
Vì vậy, khi dập lửa chủ yếu ngươi ta dùng khí CO2 để dập vì CO2 không duy trì sự cháy và nặng hơn O2 nên có thể đẩy O2 ra khỏi vật gây cháy.
2.Nguyên nhân là do
Tại nhà máy, khi sản xuất người ta nén khí CO2 ( cacbonic ) vào chai nước ngọt ở áp suất cao để bảo quản nước rồi đóng nắp chai lại nên khí CO2 tan và bão hòa vào nước ngọt.
- Khi mở chai nước ngọt áp suất trong chai giảm độ tan của khí CO2 giảm . =>Khi khí CO2 được nén trong bình thì khí này thoát khỏi chất lỏng nên sủi bọt.
2a)Khi quạt gió vào bếp củi vừa bị tắt, lượng oxi sẽ tăng lên làm cho sự cháy diễn ra mạnh hơn và lửa sẽ bùng cháy lên.
b)Khi quạt gió vào ngọn nến đang cháy, nến tắt là do ngọn lửa của nến nhỏ nên khi quạt lượng gió vào nhiều sẽ làm nhiệt độ hạ thấp đột ngột nên nến bị tắt
Có hỗn hợp gồm Fe và Fe3O4, chia hỗn hợp thành 2 phần
_Phần 1: Ngâm trong dung dịch HCl dư, pứ xog thu đc 3,36 lít khí H2( đktc)
_Phần 2: Nung nóng và cho dòng khí H2 dư đi qua thì thu đc 25,2g Fe a. Viết PTHH xảy ra b. Tính thành phần % theo khốii lượng của mỗi chất trog hỗn hợp ban đầu
Giúp mình với, mình cần gấp :( cảm ơn nhiều ><
Câu trả lời của bạn
2 phần có bằng nhau không bạn?
hãy viết phương trình hóa học của các phản ứng giữa khí H2 với hỗn hợp Chì (II)Oxit và Sắt (III)Oxit ở nhiệt độ thích hợp
Câu trả lời của bạn
Pt: PbO + H2 --to--> Pb + H2O
......Fe2O3 + 3H2 --to--> 2Fe + 3H2O
cho các chất Na2O, H2O, H2SO4, H2, CuO, SO2, KMnO4, HgO, C ,O2, C2H6O, Zn, K, Al(OH)3, H2S, FeS, Na.
a, viết phương trình phản ứng các chất trên với O2,H2 (nếu xảy ra).
b,Điều chế O2,H2 từ những chất trên.
cần gấp !!!!!!!!
Câu trả lời của bạn
cho các chất Na2O, H2O, H2SO4, H2, CuO, SO2, KMnO4, HgO, C ,O2, C2H6O, Zn, K, Al(OH)3, H2S, FeS, Na.
a, viết phương trình phản ứng các chất trên với O2,H2 (nếu xảy ra).
b,Điều chế O2,H2 từ những chất trên.
Giải
a, Với O2
O2 + 2H2 → 2H2O
O2 + C → CO2
C2H6O + 3O2 -> 2CO2 + 3H2O
2Zn + O2 → 2ZnO
4K+ O2 → 2K2O
4Na + O2 → 2Na2O
Với H2
Na2O + H2 → 2Na + H2O
CuO + H2 → Cu + H2O
HgO + H2 → Hg + H2O
O2 + 2H2 → 2H2O
b, Điều chế Oxi
2KMnO4 → K2MnO4 + MnO2 + O2
điều chế hiđro
Zn + H2SO4 → ZnSO4 + H2
2.cho 15,68 l hỗn hợp gồm hai khí CO và CO2 ở (đktc) có khối lượng là 27,6(g).Tính thành phần % theo khối lượng mỗi khí trong hỗn hợp
3.một muối ngậm nước cso.CT là CaSO4 , H2O . bt 19,1 (g) mẫu có chứa 4g nước, hãy xác định CT phân tử muối ngậm trên.
4.cho 32,4g kim loại . AL tác dụng với 21,504 lít O2 (đktc)
a) chất nào dư sau phản ứng ? khối lượng chất còn dư là bao nhiêu (g)
b) cho toàn bộ lượng kim loại AL ở trên vào dung dịch axit HCL sau phản ứng sảy ra hoàn toàn thu được bao nhiêu lít H2 (đktc)
GIÚP MÌNH GIẢI VỚI !!!!!
CẢM ƠN NHIỀU *CẦN GẤP LẮM Ạ*
Câu trả lời của bạn
3.một muối ngậm nước cso.CT là CaSO4 , H2O . bt 19,1 (g) mẫu có chứa 4g nước, hãy xác định CT phân tử muối ngậm trên.
Sửa đề: một muối ngậm nước cso.CT là CaSO4 , H2O . bt 19,11 (g) mẫu có chứa 4g nước, hãy xác định CT phân tử muối ngậm trên.
Theo đầu bài ta có tỉ lệ: \(\dfrac{M_{CaSO_4.nH_2O}}{m_{CaSO_4.nH_2O}}=\dfrac{M_{H_2O}}{m_{H_2O}}\Leftrightarrow\dfrac{136+18n}{19,11}=\dfrac{18n}{4}\)
Giải ra ta được n = 2
Vậy CTHH của muối là: \(CaSO_4.2H_2O\)
Câu 2: Hãy so sánh cách thu khí Oxi và Hiđro bằng cách đẩy nước và đẩy không khí
Câu 3: Khử 48 gam Đồng (II) oxit bằng khí Hiđro
a. Viết phương trình phản ứng
b. Tính số gam Đồng thu được
c. Tính thể tích khí Hiđro (điều kiện tiêu chuẩn) cần dùng
d. Tính khối lượng nước thu được
Câu trả lời của bạn
Câu 2:
Vì Oxi nặng hơn không khí nên khi thu khí người ta thường để lọ ngửa miệng lên trên còn Hiđro nhẹ hơn không khí nên khi thu khí người ta thường úp miệng bình xuống
Câu 3:
\(n_{CuO}=\dfrac{m_{Cuo}}{M_{Cuo}}=\dfrac{48}{80}=0,6\left(mol\right)\)
a. \(CuO+H_{_{ }2}\rightarrow H_2O+CuO\)
theo phương trình 1 1 1 1 (mol)
theo bài 0,6 0,6 0,6 0,6 (mol)
b. \(m_{Cu}=0,6.64=38,4\left(g\right)\)
c. \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
d. \(m_{H_2O}=18.0,6=10,8\left(g\right)\)
Câu trả lời của bạn
nCa = \(\frac{8}{40}=0,2\) mol
a) Pt: 2Ca + O2 --to--> 2CaO
....0,2 mol-->0,1 mol-> 0,2 mol
b) VO2 cần dùng = 0,1 . 22,4 = 2,24 (lít)
c) mCaO thu được = 0,2 . 56 = 11,2 (g)
CaO: canxi oxit thuộc oxit bazơ
d) VO2 = 20% Vkk= \(\frac{20.V_{kk}}{100}= 0,2V_{kk}\)
=> Vkk = \(\frac{VO2}{0,2}= \frac{2,24}{0,2}=\) 11,2 (lít)
Bài 1 :Hãy viết phương trình hóa học của các phản ứng giữa khí hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp.
a) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
b) Nếu thu được 12 gam hỗn hợp 2 kim loại (trong đó có 2,8 gam sắt) thì thể tích khí hiđro tối thiểu cần dùng ở đktc là bao nhiêu để khử hỗn hợp trên.
c) Khử hoàn toàn 56 gam hỗn hợp hai oxit trên người ta thu được 43,2 gam hỗn hợp hai kim loại. hãy tính thể tích khí hiđro hoặc khí cacbon oxit cần dùng ở đktc. Biết lượng các khí dùng dư là 20%.
Bài 2: Hãy viết phương trình hóa học của các phản ứng giữa khí hiđro với hỗn hợp các chất oxit sắt từ và sắt (II) oxit ở nhiệt độ thích hợp.
a) Nếu thu được 26,2 gam sắt người ta phải dùng 11,2 lít khí hiđro ở đktc. Hãy tínhkhối lượng hỗn hợp hai oxit đã dùng.
b) Để khử hoàn toàn 49,2 gam hỗn hợp hai oxit trên người ta phải dùng 17,92 lít khí hiđro ở đktc. Hãy tính khối lượng mỗi oxit và khối lượng sắt sinh ra. Biết phản ứng xảy ra với hiệu suất là 100%.
Câu trả lời của bạn
Bài 1 :Hãy viết phương trình hóa học của các phản ứng giữa khí hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp.
Trả lời:
PTHH: H2 + CuO → Cu + H2O
3H2 + Fe2O3 → 2Fe + 3H2O
Đốt cháy hoàn toàn 4,6 gam 1 hỗn hợp chất A gòm C, H, O. Thu được 8,8 gam CO2 và 5,4 gam H2O . Tỉ khối hơi của A so với H2 là 25. Xác định công thức hóa học.
Câu trả lời của bạn
CHÚC BẠN HỌC TỐT!
Theo đề bài, ta có:\(\left\{{}\begin{matrix}n_{CO2}=\dfrac{8,8}{44}=0,2\left(mol\right)\\n_{H2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_C=0,2\left(mol\right)\\n_H=0,3.2=0,6\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_C+m_H=12.0,2+1.0,6=3\left(g\right)\)
\(\Rightarrow m_O=4,6-3=1,6\left(g\right)\)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
\(\Rightarrow0,2:0,6:0,1=2:6:1\)
Vậy CTHH là C2H6O..........

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *