Ở chương V các em đã học xong về oxi, hiđro, nước; phản ứng oxi hóa - khử; phản ứng thế... Tiết học này các em sẽ được học bài luyện tập, để làm một số bài tập định tính và một số bài tập định lượng về những kiến thức trên qua bài học này.
1. Khí Hiđro có tính khử, ở nhiệt độ thích hợp Hiđro không những kết hợp được với đơn chất oxi mà còn có thể kết hợp với nguyên tố oxi trong một số oxit kim loại. Các phản ứng này đều tỏa nhiệt.
2. Khí Hiđro có nhiều ứng dụng, chủ yếu do tính chất rất nhẹ (nhẹ nhất trong các chất khí), tính khử và khi cháy tỏa nhiều nhiệt.
3. Có thể điều chế khí Hiđro trong phòng thí nghiệm bằng cách cho dung dịch axit clohiđric HCl hoặc dung dịch axit sunfuric H2SO4 loãng tác dụng với kim loại như Zn, Fe, Al. Có thể thu khí Hiđro vào bình bằng hai cách: đẩy không khí và đẩy nước (miệng bình úp xuống dưới)
4. Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố trong hợp chất.
5. Quá trình tách nguyên tử Oxi khỏi hợp chất là sự khử. Chất chiếm oxi hoặc chất nhường oxi cho chất khác là chất khử.
6. Sự tác dụng của oxi với một chất là sự oxi hóa. Đơn chất oxi hoặc chất nhường oxi cho chất khác là chất oxi hóa.
7. Phản ứng oxi hóa khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
| Khí O2 | Khí H2 | |
| Tính chất hóa học | Tính oxi hóa Tác dụng với kim loại, phi kim,hợp chất. | Tính khử Tác dụng với khí oxi và oxit kim loại |
| Điều chế trong PTN | Nhiệt phân hợp chất giàu oxi: KClO3, KMnO4… | Một số kim loại(Mg,Zn,Al…) tác dụng với dung dịch HCl, H2SO4 loãng. |
| Loại phản ứng | Phản ứng phân hủy: 2KClO3 | Phản ứng thế: Zn +2HCl → ZnCl2 + H2↑ |
| Cách thu | Đẩy không khí Đẩy nước | Đẩy không khí Đẩy nước |
| Ứng dụng | Sự hô hấp Sự đốt nhiên liệu Thuốc nổ | Nhiên liệu và bơm vào khinh khí cầu Làm nguyên liệu |
Bảng: Tóm tắt tính chất và ứng dụng của Oxi và Hiđro
Lập phương trình hóa học của các phản ứng sau và cho biết chúng thuộc loại phản ứng hóa học nào?
a) Điphotpho penta oxit + nước → axit photphoric (H3PO4)
b) Kẽm + axit sunfuric (H2SO4) → Kẽm sunfat (ZnSO4)+ hiđro
c) Thủy ngân (II) oxit Thủy ngân + oxi
a) P2O5 + 3H2O → 2 H3PO4
Đây là phản ứng hóa hợp
b) Zn + H2SO4 → ZnSO4 + H2↑
Đây là phản ứng thế
c) HgO Hg + O2↑
Đây là phản ứng phân hủy
Người ta dùng V(lít) khí H2 khử hoàn toàn hỗn hợp hai Oxit kim loại gồm: CuO và Fe2O3 ở nhiệt độ thích hợp. Sau phản ứng thu được 12g hỗn hợp gồm 2 kim loại trong đó có 6,4g Cu.
a) Viết các phương trình hóa học xảy ra.
b) Hãy tính V(lít) khí H2 cần dùng để khử hỗn hợp 2 Oxit đó. (Các thể tích khí đo ở đktc)
a) Phương trình hóa học:
H2 + CuO Cu + H2O (1)
3H2 + Fe2O3 2Fe + 3H2O (2)
b) Khối lượng của kim loại Fe là:
\({m_{Fe}} = {m_{hh}} - {m_{CuO}} = 12 - 6,4 = 5,6(gam)\)
Số mol của Sắt và Đồng lần lượt là:
\(\begin{array}{l} {n_{Fe}} = \frac{{{m_{Fe}}}}{M} = \frac{{5,6}}{{56}} = 0,1(mol)\\ {n_{CuO}} = \frac{{{m_{CuO}}}}{M} = \frac{{6,4}}{{64}} = 0,1(mol) \end{array}\)
Phương trình hóa học:
H2 + CuO Cu + H2O (1)
1 mol 1 mol
0, 1 mol \(\leftarrow\) 0,1 mol
3H2 + Fe2O3 2Fe + 3H2O (2)
3 mol 2 mol
0,15 mol \(\leftarrow\) 0,1 mol
Theo phương trình (1) và (2) thì số mol Hiđro sinh ra ở hai phản ứng là:
\(\begin{array}{l} {n_{{H_2}(1)}} = {n_{Cu}} = 0,1(mol)\\ {n_{{H_2}(2)}} = {n_{Fe}} = 0,15(mol) \end{array}\)
Tổng số mol khí Hiđro sinh ra là:
\(\sum {{n_{{H_2}}}} = 0,1 + 0,15 = 0,25(mol)\)
Thể tích khí Hiđro cần dùng ở đktc là:
\({V_{{H_2}}} = 22,4.{n_{{H_2}}} = 22,4 \times 0,25 = 5,6(lit)\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 34có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Nhờ tính chất nào mà khí hiđro có thể tác dụng được với một số oxit kim loại ở nhiệt độ thích hợp:
Ứng dụng của hiđro chủ yếu dựa vào tính chất
Hóa chất điều để điều chế hiđro trong phòng thí nghiệm là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 34.
Bài tập 1 trang 118 SGK Hóa học 8
Bài tập 2 trang 118 SGK Hóa học 8
Bài tập 3 trang 119 SGK Hóa học 8
Bài tập 4 trang 119 SGK Hóa học 8
Bài tập 5 trang 119 SGK Hóa học 8
Bài tập 6 trang 119 SGK Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Nhờ tính chất nào mà khí hiđro có thể tác dụng được với một số oxit kim loại ở nhiệt độ thích hợp:
Ứng dụng của hiđro chủ yếu dựa vào tính chất
Hóa chất điều để điều chế hiđro trong phòng thí nghiệm là:
Thu khí hiđro trong phòng thí nghiệm bằng phương pháp nào?
Phản ứng thế là phản ứng hóa học xảy ra giữa:
Cho các phản ứng sau, phản ứng nào không phải phản ứng thế
Trong các loại phản ứng dưới đây, phản ứng nào chắc chắn là phản ứng oxi hóa – khử
Cho thanh Al ngâm vào dung dịch axit clohidric thấy có khí bay lên. Xác định khí đó
Cho thanh đồng ngâm vào 400ml dung dịch axit sunfuric loãng 2M thấy trong dung dịch có khí và V bằng bao nhiêu?
Tính m(g) H2O khi cho 2,24(l) H2 tác dụng với 6,72 (l) O2(đktc)
Viết phương trình hóa học biểu diễn phản ứng của hiđro với các chất: O2, Fe2O3, Fe3O4, PbO ở nhiệt độ thích hợp. Ghi rõ điều kiện phản ứng. Giải thích và cho biết mỗi phản ứng trên thuộc loại phản ứng gì?
Có 3 lọ đựng riêng biệt các chất khí sau: khí oxi, không khí, và hiđro. Bằng thí nghiệm nào có thể nhận ra chất khí trong mỗi lọ?
Cho dung dịch axit sunfuric loãng, nhôm và các dụng cụ thí nghiệm như hình vẽ.
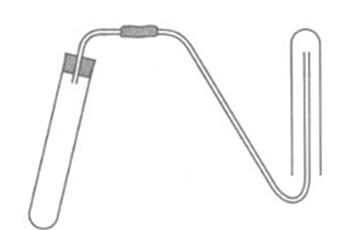
Hãy chọn câu trả lời đúng trong các câu sau:
A. Có thể dùng các hóa chất và dụng cũ đã cho để điều chế và thu khí oxi.
B. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu không khí.
C. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí hiđro.
D. Có thể dùng để điều chế hidro nhưng không thu được khí hiđro.
a) Lập phương trình hóa học của các phản ứng sau:
Cacbon đioxit + nước → Axit cacbonic (H2CO3).
Lưu huỳnh đioxit + nước → Axit sunfurơ (H2SO3).
Kẽm + axit clohiđric → Kẽm clorua + H2.
Điphotpho + nước → Axit photphoric (H3PO4).
Đồng (II) oxit + hiđro → Chì (Pb) + H2O.
b) Mỗi phản ứng hóa học trên đây thuộc loại phản ứng nào? Vì sao?
a) Hãy viết phương trình hóa học của các phản ứng giữa hiđro với hỗn hợp đồng (II) oxit và sắt (III) oxit ở nhiệt độ thích hợp?
b) Trong các phản ứng hóa học trên, chất nào là chất khử, chất nào là chất oxi hóa? Vì sao?
c) Nếu thu được 6,00 gam hỗn hợp hai kim loại, trong đó có 2,8g sắt thì thể tích (ở đktc) khí hiđro vừa đủ cần dùng để khử đồng (II) oxit và sắt (III) oxit là bao nhiêu?
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Sục x(lít) CO2 (đktc) vào 400ml dung dịch Ba(OH)2 0,5M thì thu được 4,925g kết tủa.Tính x
Câu trả lời của bạn
TH1: CO2 hết và Ca(OH)2 dư. → VCO2 = 0,56(l)
TH2: CO2 dư và Ca(OH)2 hết. → VCO2 = 8,4(l)
Hòa tan 2,8 g kim loại R chưa rõ hóa trị trg dd HCl dư thu đc 1,12 l khí hiđro. Xác định tên R
Câu trả lời của bạn
Gọi a là hóa trị của R
nH2 = \(\dfrac{1,12}{22,4}=0,05\) mol
Pt: 2R + 2aHCl --> 2RCla + aH2
...\(\dfrac{0,1}{a}\) mol<------------------0,05 mol
Ta có: \(2,8=\dfrac{0,1}{a}M_R\)
\(\Leftrightarrow M_R=\dfrac{2,8a}{0,1}=28a\)
Biện luận:
| a | 1 | 2 | 3 |
| MR | 28 (loại) | 56 (nhận) | 84 (loại) |
Vậy R là Sắt (Fe)
Có hỗn hợp khí CO và CO2 . Nếu cho hôn hợp khí đi qua dung dịch Ca(OH)2 dư thì thu được 1g chất kết tủa màu trắng . Nếu cho hỗn hợp khí này đi qua bột CuO nóng dư thì thu được 0,46g Cu
a) Viết phương trình phản ứng xảy ra?
b) Tính thể tích của hỗn hợp khí ở đktc và thể tích của mỗi khí có trong hỗn hợp.
Câu trả lời của bạn
a) nCaCO3 = \(\dfrac{1}{100}=0,01\) mol
nCu = \(\dfrac{0,46}{64}=0,007\) mol
Pt: CO2 + Ca(OH)2 ---> CaCO3 + H2O
0,01 mol<-----------------0,01 mol
....CuO + CO --to--> Cu + CO2
...........0,07 mol<--0,07 mol
b) VCO2 = 0,01 . 22,4 = 0,224 (lít)
VCO = 0,07 . 22,4 =1,568 (lít)
Vhh = VCO2 + VCO = 0,224 + 1,568 = 1,792 (lít)
1.Axit là những chất làm cho quỳ tím chuyển san màu nào trong số các màu cho dưới đây?
a. Xanh
b. Đỏ
c. Tím
d. Không xác định được
2.Trong các chất dưới đây, chất nào làm quỳ tím hóa đỏ?
a. Nước
b. Rượu(cồn
c. Axit
d. Nước vôi
3.Một số hóa chất được để trên 1 ngăn tủ có khung bằng kim loại. Sau một năm người ta thấy khung kim loại bị gỉ.Hóa chất nào dưới đây có khả năng gây ra hiện tượng trên?
a. Rượu etylic(etanol)
b. Dây nhôm
c.Dầu hỏa
d. Axit clohidric
4. Một cchất lỏng không màu có khả năng hóa đỏ một chất chỉ thị thông dụng.Nó tác dụng với một số kim loại giải phóng hidro và nó giải phóng khí Co2 khi thêm vaò muối hidrocacbonat. Kết luận nào dưới đây là phù hợp nhất cho chất lỏng ban đầu?
a. Nó là một kiềm
b. Nó là 1 bazo
c, Nó là một muối
d. Nó là 1 axit
5.Cặp nào sau đây khi tan trong nước chúng tác dụng với nhau tạo ra chất kết tủa?
a. NaCl và AgNo3
b.NaOH và Hcl
c. KOH và Nacl
d. Cuso4 và hcl
6. Cặp nào sau đây khi tan trong nước chúng tác dụng với nhau tạo ra chất khí bay ra?
a. BaCl2 và H2SO4
b. NaCl và Na2So3
c. HCl và Na2Co3
d. AlCl3 và H2So4
7. Đốt 20ml khí H2 trong 20 ml khí O2. SAu khi đưa về nhiệt độ và áp suất ban đầu, thể tích còn dư sau phản ứng là?
a. Dư 10 ml H2
b. Dư 10ml O2
c. Hai khí vừa hết
d. Không xác định được
8. Cho Cu tác dụng với dd axit Hcl sẽ có hiện tượng sau
a. Chất khí cháy được trong không khí với ngọn lửa màu xanh
b. Chất khí làm đục nước vôi trong
c. Dd có màu xanh
d. KHông có hiện tượng gì
9. Trong số các chất có công thức hóa học dưới đây, chất nào làm quỳ tím hóa đỏ
a. H2O
b. HCL
c. NaOH
d. Cu
10. Trong phòng thí nghiệm có các kim loại Zn và MG, các dung dịch axit H2so4 loãng và Hcl. Muốn điều chế được 1.12 lít khí H2(đktc) phải dùng kim loại nào, Axit nào để chỉ cần một khối lượng nhỏ nhất
a. Mg và H2SO4
b. MG và HCL
c. Zn và h2so4
d. Zn và Hcl
Câu trả lời của bạn
1.Axit là những chất làm cho quỳ tím chuyển san màu nào trong số các màu cho dưới đây?
a. Xanh
b. Đỏ
c. Tím
d. Không xác định được
2.Trong các chất dưới đây, chất nào làm quỳ tím hóa đỏ?
a. Nước
b. Rượu(cồn
c. Axit
d. Nước vôi
3.Một số hóa chất được để trên 1 ngăn tủ có khung bằng kim loại. Sau một năm người ta thấy khung kim loại bị gỉ.Hóa chất nào dưới đây có khả năng gây ra hiện tượng trên?
a. Rượu etylic(etanol)
b. Dây nhôm
c.Dầu hỏa
d. Axit clohidric
4. Một cchất lỏng không màu có khả năng hóa đỏ một chất chỉ thị thông dụng.Nó tác dụng với một số kim loại giải phóng hidro và nó giải phóng khí Co2 khi thêm vaò muối hidrocacbonat. Kết luận nào dưới đây là phù hợp nhất cho chất lỏng ban đầu?
a. Nó là một kiềm
b. Nó là 1 bazo
c, Nó là một muối
d. Nó là 1 axit
5.Cặp nào sau đây khi tan trong nước chúng tác dụng với nhau tạo ra chất kết tủa?
a. NaCl và AgNo3
b.NaOH và Hcl
c. KOH và Nacl
d. Cuso4 và hcl
6. Cặp nào sau đây khi tan trong nước chúng tác dụng với nhau tạo ra chất khí bay ra?
a. BaCl2 và H2SO4
b. NaCl và Na2So3
c. HCl và Na2Co3
d. AlCl3 và H2So4
7. Đốt 20ml khí H2 trong 20 ml khí O2. SAu khi đưa về nhiệt độ và áp suất ban đầu, thể tích còn dư sau phản ứng là?
a. Dư 10 ml H2
b. Dư 10ml O2
c. Hai khí vừa hết
d. Không xác định được
8. Cho Cu tác dụng với dd axit Hcl sẽ có hiện tượng sau
a. Chất khí cháy được trong không khí với ngọn lửa màu xanh
b. Chất khí làm đục nước vôi trong
c. Dd có màu xanh
d. KHông có hiện tượng gì
9. Trong số các chất có công thức hóa học dưới đây, chất nào làm quỳ tím hóa đỏ
a. H2O
b. HCL
c. NaOH
d. Cu
10. Trong phòng thí nghiệm có các kim loại Zn và MG, các dung dịch axit H2so4 loãng và Hcl. Muốn điều chế được 1.12 lít khí H2(đktc) phải dùng kim loại nào, Axit nào để chỉ cần một khối lượng nhỏ nhất
a. Mg và H2SO4
b. MG và HCL
c. Zn và h2so4
d. Zn và Hcl
Câu trả lời của bạn
Ta có:
nhh=0,5+0,2 =0,7 (mol)
=> Vhh=\(\dfrac{0,7}{22,4}=15,68\left(l\right)\)
Có 4 lọ đựng riêng biệt các khí: N2, H2, CO2, O2. Bằng TN nào nhận ra các chất khí trong mỗi lọ
Câu trả lời của bạn
Trích mẫu thử
Cho ca(OH)2 vào các mẫu thử
mẫu thử làm đục nước vôi trog=>CO2
CO2+Ca(Oh)2--->CaCO3+H2O
Cho CuO nung nóng vào các mẫu thử
Chất rắn từ màu đen chuyển sang màu đỏ=>H2
CuO+H2--->Cu+H2O
Cho que đóm còn tàn dư vào 2 lọ còn lại
Que đóm bùng cháy=>O2
Que đóm tắt=>N2
Tính số phân tử P2O5 số nguyên tử P và nguyên tử O có trong 7,07g phân tử P2 O5Giúp e vs ,ai nhanh và đúng e tick 3 cái hì giải chi tiết giùm nhé
-Loveee
Câu trả lời của bạn
\(n_{P_2O_5}\)=7,07:142=0,05(mol)
=>nP=2\(n_{P_2O_5}\)=2.0,05=0,1(mol)
=>nO=5\(n_{P_2O_5}\)=0,05.5=0,25(mol)
Vậy số phân tử P2O5 là:
0,05.6,023.1023=3,0115.1022 phân tử
Số nguyên tử P là:
0,1.6,023.1023=6,023.1022 nguyên tử
Số nguyên tử O là:
0,25.6,023.1023=1,50575.1023 nguyên tử
Trong số các chất dưới đây hãy chỉ ra và giải thích chất nào là đơn chất, là hợp chất:
a)Khí ozon có phân tử gồm 3O liên kết vói nhau
b)Axit photphoric có phân tử gồm 3H, 1P và 4O liên kết vói nhau
c)Natri cacbonat(sôđa) có phân tử gồm 2 Na, 1C và 3O liên kết với nhau
d)Khí flo có phân tử gồm 2f liên kết vói nhau
e)Rượu etylic(cồn) có phân tử gồm 2C,6H và 1O liên kết vói nhau
f)Đường có phân tử gồm 12C, 22H và 11O liên kết vói nhau.
Câu trả lời của bạn
a) O3: Đơn chất
b)H3PO4: Hợp chất
c) Na2CO3: Hợp chất
d) F2: Đơn chất
e) C2H6O; Hợp chất
f) C12H22O11: Hợp chất
Hòa tan 2,4 gam Mg và 11,2 gam Fe vào 100ml dung dịch CuSo4 2M thì tách ra chất rắn A và nhận đc dung dịch B . Thêm NaOH dư vào dung dịch B rồi lọc kết tủa tách ra nung đến lượng không đổi trong không khí thu được a gam chất rắn D . Viết PTHH , tính lượng chất rắn A và lượng chất rắn D
Câu trả lời của bạn
Theo đề bài ta có : \(\left\{{}\begin{matrix}nMg=\dfrac{2,4}{24}=0,1\left(mol\right)\\nFe=\dfrac{11,2}{56}=0,2\left(mol\right)\end{matrix}\right.\) ; \(nCuSO4=2.0,1=0,2\left(mol\right)\)
Ta có PTHH :
\(Mg+C\text{uS}O4->MgSO4+Cu\)
0,1mol....0,1mol............0,1mol....0,1mol
\(Fe+C\text{uS}O4->FeSO4+Cu\)
0,2mol.....0,2mol........0,2mol.......0,2mol
Chất rắn A được tách ra là Cu
DD B là gồm MgSO4 và FeSO4
Ta có :
\(2NaOH+MgSO4->Mg\left(OH\right)2\downarrow+Na2SO4\)
0,2mol.............0,1mol.............0,1mol
\(2NaOH+FeSO4->Na2SO4+Fe\left(OH\right)2\downarrow\)
0,4mol............0,2mol...............................0,2mol
Ta có kết tủa thu được là \(Fe\left(OH\right)2\) và Mg(OH)2
Ta có :
\(Fe\left(OH\right)2-^{t0}->FeO+H2O\)
0,2mol........................0,2mol
\(Mg\left(OH\right)2-^{t0}->MgO+H2O\)
0,1mol..............................0,1mol
=> \(m\left(ch\text{ất}-r\text{ắn}\right)=mFe+mMg=0,2.72+0,1.40=18,4\left(g\right)\)
Vậy.............
Cho các kim loại Zn, Al, Fe lần lượt tác dụng với dung dịch H2SO4 loãng.
a. Viết các phương trình hh của phản ứng.
b. Cho cùng 1 khối lượng các kim loại trên tác dụng hết với axit dư thì kim loại nào cho nhiều khí Hiđro nhất ?
c. Nếu thu đc cùng 1 thể tích khí Hiđro thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất ?
" Ak mak mk làm bài tập ở phần bài luyện tập 6 chứ k phải là hok đến đây rồi đâu ^ - ^ "
Câu trả lời của bạn
a: Zn + H2SO4 ----> ZnSO4 + H2 (1)
2Al + 3H2SO4 ------> Al2(SO4)3 + 3H2 (2)
Fe + H2SO4 ----> FeSO4 + H2 (3)
b: Giả sử khối lượng kim loại Zn, Al, Fe là a(gam)
---> nFe= \(\dfrac{a}{56}\) ----> nH2(3) = \(\dfrac{a}{56}\)
---> nZn= \(\dfrac{a}{65}\) ------> nH2 (1) = \(\dfrac{a}{65}\)
-----> nAl= \(\dfrac{a}{27}\) ----> nH2(2)= \(\dfrac{3}{2}\)nAl ---->nH2(2)= \(\dfrac{a}{18}\)
Do \(\dfrac{a}{65}\)<\(\dfrac{a}{56}\)<\(\dfrac{a}{18}\)-----> Al cho nhiều hiđro nhất
c: Giải tương tự như câu b ----> Khối lượng kim loại phản ứng ít nhất là Al
Cho 24.10^23 nguyên tử Zn tác dụng với dung dịch HCl theo sơ đồ phản ứng sau: Zn+HCl -> ZnCl2+H2.
a) Tính số phân tử HCl đã dùng.
b) Tính thể tích H2 thu được ở đktc
Câu trả lời của bạn
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
Tỉ lệ: 1:2:1:1
a, \(n_{Zn}\)=\(2n_{HCl}\)=\(n_{H_2}\)=\(\dfrac{24.10^{23}}{6.10^{23}}\)=4(mol)
\(\Rightarrow\)\(n_{HCl}\)=2(mol)
\(\Rightarrow\)Số phân tử HCl là:
2.6.1023=12.1023(phân tử)
b,\(V_{H_2}\)=2.22,4=44,8(lít)
Thành phần chính của đất đèn là Canxi Cacbua. Khi cho đất đèn tác dụng với phản ứng sau:
Canxi Cacbua + Nước -----> Canxi Hiđroxit + Khí Axetilen
Biết rằng khi cho 80kg đắt đèn và 36kg nước thu được 74kg Canxi Hiđroxit và 26kg khí Axetilen
a) Viết công thức về khối lượng phản ứng
b) Tính tỉ lệ phần trăm về khối lượng Canxi Cacbua có trong đất đèn
Câu trả lời của bạn
CaC2 + 2H2O -> Ca(OH)2 + C2H2
Theo ĐLBTKL cho PTHH trên ta có:
mCaC2+ mH2O=mCa(OH)2+mC2H2
=>mCaC2=74+26-36=64(kg)
%mCaC2=\(\dfrac{64}{80}.100\%=80\%\)
1, Để điều chế 1 tấn KNO3 người ta cho KOH tác dụng với HNO3. Tính khối lượng của KOH và HNO3 cần dùng để điều chế.
2, Một loại thép có chứa 98% là sắt được điều chế bằng cách cho Fe2O3 tác dụng với H2 . Tính khối lượng của Fe2O3 và thể tích khí H2 cần điều chế 10 tấn thép loại trên.
3, CaCO3 được dùng để sản xuất CaO . Tính khối lượng CaCO3 cần dùng để điều chế 5,6 tấn CaO.
4, Đốt cháy 12 tấn cacbon cần bao nhiêu mét khối ko khí. Biết rằng khí oxi chiếm 1/5 V ko khí .
Câu trả lời của bạn
Bài 3 :
Ta có PTHH :
CaCO3 \(-^{t0}->CaO+Co2\)
100 kg-----------> 56 kg
x kg--------------> 5600 kg
=> x = mCaCO3(cần) = \(\dfrac{5600.100}{56}=10000\left(kg\right)=10\left(t\text{ấn}\right)\)
Bài 4 :
Ta có PTHH :
C + O2 \(-^{t0}->Co2\)
Để đốt cháy 12kg C thì cần 32 kg khí oxi
Vậy để đốt cháy 12000 kg C thì cần x kg khí oxi
=> x = \(\dfrac{12000.32}{12}=32000\left(kg\right)=>nO2=\dfrac{32000000}{32}=1000000\left(mol\right)=>Vkk=5.Vo2\left(\text{đ}ktc\right)=5.1000000.22,4=112000000\left(l\right)=112000\left(m^3\right)\)
Một hỗn hợp gồm Zn và Fe có khối lượng là 37,2 gam . Hòa tan hỗn hợp này trong 2 lít dung dịch H2SO4 0,5M
a) Chứng tỏ rằng hỗn hợp này tan hết ?
b) Nếu dùng một lượng hỗn hợp Zn và Fe gấp đôi trường hợp trước, lượng H2SO4 vẫn như cũ thì hỗn hợp mới này có tan hết hay không?
c) Trong trường hợp (a) hãy tính khối lượng mỗi kim loại trong hỗn hợp biết rằng lượng H2 sinh ra trong phản ứng vừa đủ tác dụng với 48 gam CuO?
Câu trả lời của bạn
Zn+H2SO4--->ZnSO4+H2
x______x_______x_____x
Fe+H2SO4--->FeSO4+H2
y____y_________y____y
Ta có: 65x+56y=37,2
Giả sự hỗn hợp chỉ chứa toàn Zn
65(x+y)>37,2
=>x+y>0,57(1)
Giả sự hỗn hợp chỉ chứa toàn Fe
56(x+y)<37,2
=>x+y<0,66(2)
Từ (1) và (2) =>0,57<x+y<0,66
Mà theo các pt: nH2SO4=x+y=0,5.2=1(mol)
===>Hỗn hợp tan hết,axit dư
b) Dùng lượng Zn và Fe gấp đôi
Ta có: 1,14<x+y<1,32
Mà H2SO4 vẫn giữu nguyên 1 mol
===>Hỗn hợp k tan hết
c) nCuO=48/80=0,6(mol)
H2+CuO--->Cu+H2O
x+y__x+y
Hệ pt:
\(\left\{{}\begin{matrix}x+y=0,6\\65x+56y=37,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,4\\y=0,2\end{matrix}\right.\)
=>mZn=0,4.65=26(g)
=>mFe=0,2.56=11,2(g)
Trong khí ( gas ) thường dùng có thành phần chính là propan ( C3H8 ) và butan ( C4H10 ) .
a) Viết PTHH của phản ứng xảy ra ở điều kiện thường khi đốt cháy hết khí ( gas ) , giả thiết rằng phản ứng chỉ tạo ra sản phẩm CO2 và H2O .
b) Tính thể tích CO2 thoát ra ở điều kiện thường khi đốt cháy hết 1kg gas có thành phần chứa 26,4% propan và 69,6% butan , còn lại là tạp chất trơ không cháy ( cho rằng 1 mol khí chiếm 24 lít trong điều kiện thường ) .
Câu trả lời của bạn
Cho hỗn hợp HgO, Fe2O3 có khối lượng bằng 53,7g phản ứng hết với 15,6l H2(đktc). Tính khối lượng mỗi kim loại thu được sau phản ứng
Câu trả lời của bạn
Gọi x,y lần lượt là số mol của HgO, Fe2O3
nH2 = \(\dfrac{15,6}{22,4}=0,7\) mol
Pt: HgO + H2 --to--> Hg + H2O
........x.........x................x
....Fe2O3 + 3H2 --to--> 2Fe + 3H2O
.......y...........3y................2y
Ta có hệ pt:\(\left\{{}\begin{matrix}217x+160y=53,7\\x+3y=0,7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
mHg thu được = 0,1 . 201 = 20,1 (g)
mFe thu được = 2 . 0,2 . 56 = 22,4 (g)
Phi kim với kim loại cái nào cứng hơn?Vì sao?
Câu trả lời của bạn
kim loại cứng hơn phi kim.
Vd: sắt là kim loại, oxi là phi kim. Thử đưa tay cầm thanh sắt và chụp vào không khí => ta thấy sắt cứng hơn oxi
Quặng nào nhiều sắt nhất
a, hematit chứa 60% \(Fe_2O_3\)
b, hematit chứa 63% \(Fe_2O_3.H_2O\)
Câu trả lời của bạn
a,
Quang hematit (a) có :
\(\%_{Fe}=60\%.\dfrac{2.56}{160}=0,42\%\)
Quang hematit (b) chứa :
\(\%_{Fe}=63\%.\dfrac{2.56}{160+18}=0,40\%\)
Vậy quặng hematit (a) chứa nhiều sắt hơn .
cho 13,5g kim loại M tác dụng với dd HCL dư thu được 16,8 lít khí đo ở đktc.tìm M
Câu trả lời của bạn
\(PTHH:2M+x2HCl\rightarrow2MCl_x+xH_2\)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
=>\(n_M=\dfrac{0,75.2}{x}=\dfrac{1,5}{x}\)
Ta có: \(M=\dfrac{13,5}{\dfrac{1.5}{x}}=\dfrac{13,5x}{1,5}=9x\)
Biện luận : Với x = 1 => M = 9 (loại)
Với x = 2 => M = 18 (loại)
Với x = 3 => M = 27 ( thỏa mãn)
Vậy M là Nhôm, KHHH Al
Cho 19.5 gam kẽm tác dụng vào dung dich có 18.25 gam axit clohidric
A) Viết PTHH phản ứng xảy ra
B) Khi phản ứng kết thúc, chất nào dư , dư bao nhiêu gam ?
C) Thể tích chất khí sinh ra sau phản ứng (đktc)
Câu trả lời của bạn
nZn=19,5/65=0,3(mol)
mHCl=18,25/36,5=0,5(mol)
pt: Zn+2HCl--->ZnCl2+H2
1______2
0,3_____0,5
Ta có: 0,3/1>0,5/2
=>Zn dư
mZn dư=0,05.65=3,25(mol)
Theo pt: nH2=1/2nHCl=1/2.0,5=0,25(mol)
=>VH2=0,25.22,4=5,6(l)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *