Mời quý thầy, cô và các em cùng DapAnHay khám phá nội dung Bài 14: Tính biến thiên Enthalpy của phản ứng hóa học chương trình SGK Hóa học 10 Chân trời sáng tạo. Thông qua bài học này các em sẽ xác định được sự biến thiên Enthalpy cũng như cách để tính toán năng lượng biến thiên của một phản ứng. Mời quý thầy, cô và các em theo dõi nội dung chi tiết bài học bên dưới nhé!
- Tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết
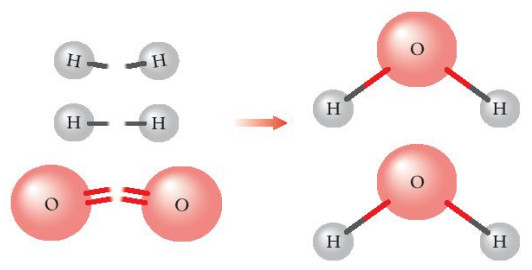
Hình 14.1. Sự hình thành phân tử nước
- Phản ứng hóa học xảy ra khi có sự phá vỡ các liên kết hoá học của chất đầu (cđ) và hình thành các liên kết hoá học của sản phẩm (sp). Sự phá vỡ các liên kết cần cung cấp năng lượng, sự hình thành các liên kết lại giải phóng năng lượng.
- Cho phản ứng tổng quát ở điều kiện chuẩn: aA (g) + bB (g) → mM (g) + nN (g)
- Tính \({\Delta _r}H_{298}^0\) của phản ứng khi biết các giá trị năng lượng liên kết (Eb) theo công thức:
\({\Delta _r}H_{298}^0\) = a x Eb (A) + b x Eb (B) – m x Eb (M) - n x Eb (N) (1)
- Tính biến thiển enthalpy của phản ứng dựa vào năng lượng liên kết được áp dụng cho phản ứng trong đó các chất đều có liên kết cộng hoá trị ở thể khí khi biết giá trị năng lượng liên kết của tất cả các chất trong phản ứng.
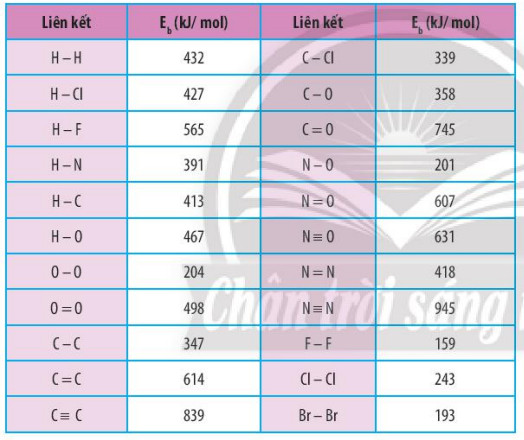
Bảng 14.1. Năng lượng liên kết của một số liên kết cộng hoá trị
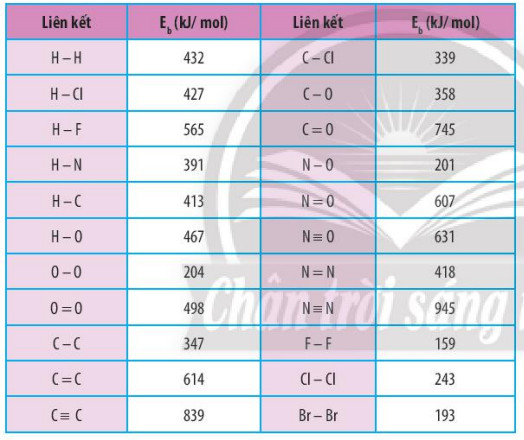
Ví dụ 1: Dựa vào năng lượng liên kết ở Bảng 14.1, tính biến thiện enthalpy của phản ứng:
H2(g) + Cl2(g) → 2HCl(g)
- Bước 1: Tính năng lượng cần thiết để phá vỡ 1 mol H - H và 1 mol Cl - Cl
+ Tổng năng lượng thu vào để phá vỡ các liên kết: Eb (H -H) + Eb (C - C) = 432 +243 = 675 kJ
- Bước 2: Tính năng lượng toả ra khi hình thành 2 mol H - Cl
+ Tổng năng lượng toả ra để hình thành liên kết: 2 x Eb (H-Cl) = 2 x 427 = 854 kJ
- Bước 3: Tính biến thiên enthalpy của phản ứng theo công thức (1)
+ \({\Delta _r}H_{298}^0\) = 675 - 854 = -179 kJ
+ Do \({\Delta _r}H_{298}^0\) < 0 nên phản ứng toả nhiệt.
Ví dụ 2: Tính biến thiên enthanny của phản ứng tạo thành ammonia (sử dụng năng lượng liên kết ở Bảng 14.1). Cho biết phản ứng thu nhiệt hay toả nhiệt và vẽ sơ đồ biểu diễn biến thiên enthalpy của phản ứng.
3H2(g) + N2(g) → 2NH3 (g)
\({\Delta _r}H_{298}^0\) = 3 x Eb (H2) + Eb (N2) - 2 x Eb (NH3)
= 3 x Eb(H - H) + Eb(N - N) – 2 x 3 x Eb(N - H) = 3 x 432 + 945 - 2 x 3 x 391 = -105 kJ.
- Do \({\Delta _r}H_{298}^0\) < 0 nên phản ứng toả nhiệt.
- Sơ đồ biểu diễn biến thiên enthalpy của phản ứng:
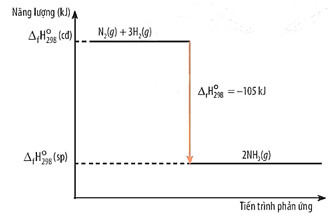
Hình 14.2.Sơ đồ biểu diễn biến thiên enthalpy
| Tổng quát: \({\Delta _r}H_{298}^0 = \sum {E_b}(c{\rm{d}}) - \sum {E_b}(sp)\) Với \(\sum {E_b}(c{\rm{d}})\), \(\sum {E_b}(s{\rm{p}})\): tổng năng lượng liên kết trong phân tử chất đầu và sản phẩm của phản ứng. |
|---|
- Tính biến thiên enthalpy của phản ứng dựa vào enthalpy tạo thành
- Cho phương trình hoá học tổng quát: aA + bB → MM + nN
- Có thể tính được biến thiên enthalpy chuẩn của một phản ứng hoá học (\({\Delta _r}H_{298}^0\)) khi biết các giá trị \({\Delta _f}H_{298}^0\) của tất cả các chất đầu và sản phẩm theo công thức sau:
\({\Delta _r}H_{298}^0 = m.{\Delta _f}H_{298}^0(M) + n.{\Delta _f}H_{298}^0(N) - a.{\Delta _f}H_{298}^0(A) - b.{\Delta _f}H_{298}^0(B)\) (2)
Ví dụ 3: Cho enthalpy tạo thành chuẩn của các chất tương ứng trong phương trình.
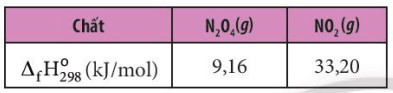
- Tính biến thiên enthalpy của phản ứng sau: 2NO2 (g) → N2O4 (g)
- Theo công thức (2), ta có: \({\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0({N_2}{O_4}) - 2.{\Delta _f}H_{298}^0(N{O_2})\)= 9,16 – 2 x 33,20 = -57,24 kg
- Do \({\Delta _r}H_{298}^0\) < 0 nên phản ứng toả nhiệt.
Ví dụ 4: Cho nhiệt tạo thành chuẩn của các chất tương ứng trong phương trình.
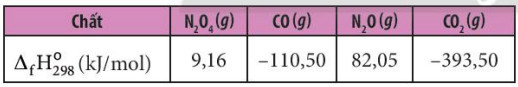
- Tính biến thiên enthalpy của phản ứng sau: N2O4 (g) + 3CO (g) → N2O (g) + 3CO2 (8)
- Theo công thức (2), ta có:
\({\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0({N_2}O) + 3.{\Delta _f}H_{298}^0(C{O_2}) - {\Delta _f}H_{298}^0({N_2}{O_4}) - 3.{\Delta _f}H_{298}^0(CO)\)
= 82,05 + 3 x (-393,50) - 9,16 - 3x (-110,50) = -776,11 kJ
- Do \({\Delta _f}H_{298}^0\) < 0 nên phản ứng toả nhiệt.
| Tổng quát: \({\Delta _r}H_{298}^0 = \sum {\Delta _f}H_{298}^0(sp) - \sum {\Delta _f}H_{298}^0(cd)\) Với \(\sum {\Delta _f}H_{298}^0(sp);\sum {\Delta _f}H_{298}^0(cd)\): tổng enthalpy tạo thành ở điều kiện chuẩn tương ứng của sản phẩm, chất đầu của phản ứng. |
|---|
Bài 1: Methane cháy tỏa nhiệt lớn nên được dùng làm nhiên liệu. Khi trộn methane và oxygen với tỉ lệ thích hợp thì sẽ tạo ra hỗn hợp nổ
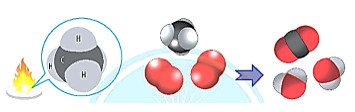
Biến thiên enthalpy của phản ứng trên được tính toán dựa trên các giá trị nào?
Hướng dẫn giải
- Trong bất cứ phản ứng hóa học nào, nhiệt có thể hoặc là được thu vào hoặc là thoát ra môi trường xung quanh. Nhiệt độ trao đổi giữa phản ứng hóa học và môi trường xung quanh được gọi là entanpy của phản ứng, ký hiệu là H. Tuy nhiên, H không thể đo được một cách trực tiếp, thay vào đó, việc đo sự thay đổi nhiệt độ của phản ứng theo thời gian được sử dụng để tính sự biến thiên của entanpy theo thời gian (ký hiệu là ∆H). Biết ∆H của một phản ứng, ta có thể xác định được đó là phản ứng thu nhiệt (nhiệt của phản ứng lấy từ môi trường) hay tỏa nhiệt (nhiệt của phản ứng tỏa ra môi trường).
- Biến thiên enthalpy của phản ứng được tính toán dựa trên giá trị năng lượng liên kết hoặc dựa vào enthalpy tạo thành.
Bài 2: Tính biến thiên enthalpy của phản ứng phân hủy trinitroglycerin (C3H5O3(NO2)3), theo phương trình sau (biết nhiệt tạo thành của nitroglycerin là -370,15 kJ/mol):
4 C3H5O3(NO2)3(s) → 6N2(g) + 12CO2(g) + 10H2O(g) + O2(g)
Hãy giải thích vì sao trinitroglycerin được ứng dụng làm thành phần thuốc súng không khói.
Hướng dẫn giải
| Chất | C3H5O3(NO2)3(s) | N2(g) | CO2(g) | H2O(g) | O2(g) |
| \({\Delta _f}H_{298}^o\) | -370,15 | 0 | -393,50 | -241,82 | 0 |
\({\Delta _r}H_{298}^o\) = 6.\({\Delta _f}H_{298}^o\)(N2) + 12.\({\Delta _f}H_{298}^o\)(CO2) + 10.\({\Delta _f}H_{298}^o\)(H2O) + \({\Delta _f}H_{298}^o\)(O2) - 4.\({\Delta _f}H_{298}^o\)(C3H5O3(NO2)3)
= 6.0 + 12.(-393,50) + 10.(-241,82) + 1.0 – 4.(-370,15) = -5659,60 kJ < 0
→ Phản ứng phân hủy trinitroglycerin tỏa ra lượng nhiệt rất lớn → Gây tính sát thương cao
→ Trinitroglycerin được ứng dụng làm thành phần của thuốc súng không khói.
Sau bài học này, học sinh sẽ:
- Tính được \({\Delta _r}H_{298}^0\) của một phản ứng dựa vào bảng số liệu năng lượng liên kết, nhiệt tạo thành cho sẵn.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Chân trời sáng tạo Bài 14 cực hay có đáp án và lời giải chi tiết.
Cho phản ứng: CH4(g) + H2O(l) → CO(g) + 3H2(g) \({\Delta _r},H_{298}^0\) = 250 kJ.
Ở điều kiện chuẩn, để thu được 1 gam H2, phản ứng này cần hấp thu nhiệt lượng bằng bao nhiêu
Tính \({\Delta _r},H_{298}^0\) các phản ứng đốt cháy hoàn toàn 1 mol C2H4(g). Biết các sản phẩm thu được đều ở thể khí.
Kết luận nào sau đây sai ?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Chân trời sáng tạo Bài 14để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 88 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 2 trang 89 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 3 trang 89 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 89 SGK Hóa học 10 Chân trời sáng tạo - CTST
Vận dụng trang 90 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 90 SGK Hóa học 10 Chân trời sáng tạo - CTST
Vận dụng trang 91 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 4 trang 91 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 91 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 1 trang 92 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 2 trang 92 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 3 trang 93 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 4 trang 93 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 5 trang 93 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 6 trang 93 SGK Hóa học 10 Chân trời sáng tạo - CTST
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Cho phản ứng: CH4(g) + H2O(l) → CO(g) + 3H2(g) \({\Delta _r},H_{298}^0\) = 250 kJ.
Ở điều kiện chuẩn, để thu được 1 gam H2, phản ứng này cần hấp thu nhiệt lượng bằng bao nhiêu
Tính \({\Delta _r},H_{298}^0\) các phản ứng đốt cháy hoàn toàn 1 mol C2H4(g). Biết các sản phẩm thu được đều ở thể khí.
Kết luận nào sau đây sai ?
Cấu trúc mạng NaCl (muối ăn) là gì?
Đặc điểm nado khiến liên kết ion khác với liên kết cộng hóa trị?
Khẳng định sai về 3 ion: Na+, Mg2+, F-?
Xác định điện hóa trị của canxi (Ca) trong CaCl2?
Xác định loại liên kết ở C biết cho biết tổng số electron trong anion AB32- là 42. Trong các hạt nhân A cũng như B có số proton bằng với số nơtron. Khi đốt hỗn hợp A, B thu được một hợp chất C.
Cấu hình electron phân lớp ngoài cùng của các nguyên tử R, X, Y lần lượt là 2p4, 3s1, 3p1.Xác định số hạt mang điện giữa các phân tử hợp chất ion đơn giản giữa X và R, giữa Y và R?
Iot, băng phiến dễ hòa tan trong các dung môi nào dưới đây:
Quan sát Hình 14.1 cho biết liên kết hóa học nào bị phá vỡ, liên kết hóa học nào được hình thành khi H2 phản ứng với O2 tạo thành H2O (ở thể khí)?
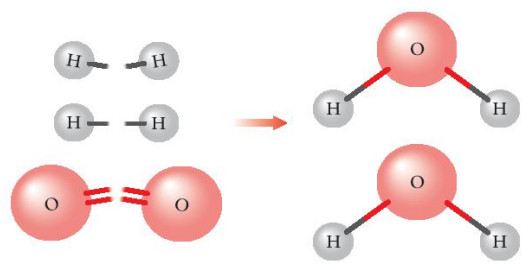
Hình 14.1. Sự hình thành phân tử nước
Tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết phải viết được công thức cấu tạo của tất cả các chất trong phản ứng để xác định số lượng và loại liên kết. Xác định số lượng mỗi loại liên kết trong các phân tử sau: CH4, CH3Cl, NH3, CO2.
Dựa vào năng lượng liên kết ở Bảng 14.1, tính biến thiên enthalpy của phản ứng và giải thích vì sao nitrogen (N\( \equiv \)N) chỉ phản ứng với oxygen (O=O) ở nhiệt độ cao hoặc có tia lửa điện để tạo thành nitrogen monoxide (N=O).
N2(g) + O2(g) \(\xrightarrow{{{t^o}}}\) 2NO(g)
Xác định \({\Delta _r}H_{298}^o\) của phản ứng sau dựa vào giá trị Eb ở Bảng 14.1:
CH4(g) + Cl2(g) \(\xrightarrow{{askt}}\) CH3Cl(g) + HCl(g)
Hãy cho biết phản ứng trên tỏa nhiệt hay thu nhiệt?
Bảng 14.1. Năng lượng liên kết của một số liên kết cộng hoá trị
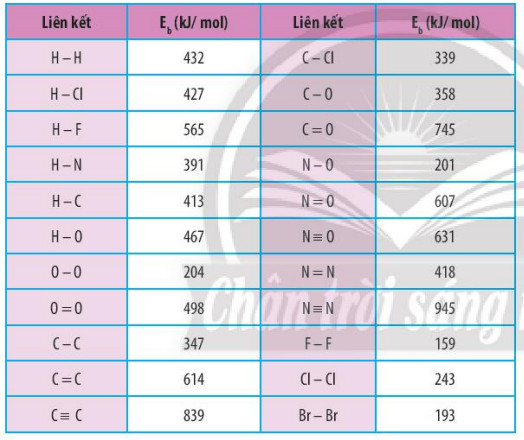
Dựa vào số liệu về năng lượng liên kết ở Bảng 14.1, hãy tính biến thiên enthalpy của 2 phản ứng sau:
2H2(g) + O2(g) \(\xrightarrow{{{t^o}}}\)2H2O(g) (1)
C7H16(g) + 11O2(g) \(\xrightarrow{{{t^o}}}\) 7CO2(g) + 8H2O(g) (2)
So sánh kết quả thu được, từ đó cho biết H2 hay C7H16 là nhiên liệu hiệu quả hơn cho tên lửa (biết trong C7H16 có 6 liên kết C-C và 16 liên kết C-H)
Tính \({\Delta _r}H_{298}^o\) của hai phản ứng sau:
3O2(g) → 2O3(g) (1)
2O3(g) → 3O2(g) (2)
Liên hệ giữa giá trị \({\Delta _r}H_{298}^o\) với độ bền của O3, O2 và giải thích, biết phân tử O3 gồm 1 liên kết đôi O=O và 1 liên kết đơn O-O
Tính biến thiên enthalpy của phản ứng phân hủy trinitroglycerin (C3H5O3(NO2)3), theo phương trình sau (biết nhiệt tạo thành của nitroglycerin là -370,15 kJ/mol):
4 C3H5O3(NO2)3(s) → 6N2(g) + 12CO2(g) + 10H2O(g) + O2(g)
Hãy giải thích vì sao trinitroglycerin được ứng dụng làm thành phần thuốc súng không khói
Giá trị biến thiên enthalpy của phản ứng có liên quan tới hệ số các chất trong phương trình nhiệt hóa học không? Giá trị enthalpy tạo thành thường được đo ở điều kiện nào?
Dựa vào giá trị enthalpy tạo thành ở Bảng 13.1, hãy tính giá trị \({\Delta _r}H_{298}^o\) của các phản ứng sau:
CS2(l) + 3O2(g) \(\xrightarrow{{{t^o}}}\) CO2(g) + 2SO2(g) (1)
4NH3(g) + 3O2 \(\xrightarrow{{{t^o}}}\) 2N2(g) + 6H2O(g) (2)
Tính \({\Delta _r}H_{298}^o\) của các phản ứng sau dựa theo năng lượng liên kết (sử dụng số liệu từ Bảng 14.1):
Bảng 14.1. Năng lượng liên kết của một số liên kết cộng hoá trị
a) N2H4(g) → N2(g) + 2H2(g)
b) 4HCl(g) + O2(g) \(\xrightarrow{{{t^o}}}\) 2Cl2(g) + 2H2O(g)
Dựa vào Bảng 13.1, tính biến thiên enthalpy chuẩn của phản ứng đốt cháy hoàn toàn 1 mol benzene C6H6(l) trong khí oxygen, tạo thành CO2(g) và H2O(l). So sánh lượng nhiệt sinh ra khi đốt cháy hoàn toàn 1,0 g propane C3H8(g) với lượng nhiệt sinh ra khi đốt cháy hoàn toàn 1,0 g benzenne C6H6(l).
Dựa vào enthalpy tạo thành ở Bảng 13.1, tính biến thiên enthalpy chuẩn của phản ứng nhiệt nhôm:
2Al(s) + Fe2O3(s) \(\xrightarrow{{{t^o}}}\) 2Fe(s) + Al2O3(s)
Từ kết quả tính được ở trên, hãy rút ra ý nghĩa của dấu và giá trị \({\Delta _r}H_{298}^o\) đối với phản ứng
Cho phương trình nhiệt hóa học sau:
SO2(g) + ½ O2(g) \(\xrightarrow{{{t^o},{V_2}{O_5}}}\) SO3(g) \({\Delta _r}H_{298}^o\) = -98,5 kJ
a) Tính lượng nhiệt giải phóng ra khi chuyển 74,6 g SO2 thành SO3
b) Giá trị \({\Delta _r}H_{298}^o\) của phản ứng: SO3(g) → SO2(g) + ½ O2(g) là bao nhiêu?
Khí hydrogen cháy trong không khí tạo thành nước theo phương trình hóa học sau:
2H2(g) + O2(g) → 2H2O(g) \({\Delta _r}H_{298}^o\) = -483,64 kJ
a) Nước hay hỗn hợp của oxygen và hydrogen có năng lượng lớn hơn? Giải thích
b) Vẽ sơ đồ biến thiên năng lượng của phản ứng giữa hydrogen và oxygen.
Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) \(\xrightarrow{{{t^o}}}\) 3CO2(g) + 4H2O(g)
Tính biến thiên enthalpy chuẩn của phản ứng dựa vào nhiệt tạo thành của hợp chất (Bảng 13.1) và dựa vào năng lượng liên kết (Bảng 14.1). So sánh hai giá trị đó và rút ra kết luận
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *