Hóa 10 Bài 8: Quy tắc Octet chương trình SGK Chân trời sáng tạo được DapAnHay biên soạn là tóm tắt toàn bộ nội dung của bài học số 8 giúp các bạn học sinh biết được khái niệm về liên kết hóa học và cũng như xác định được được các chất có liên kết trong phân tử. Mời các bạn tham khảo.
- Tìm hiểu sự hình thành liên kết hóa học
- Trong hóa học, liên kết hóa học là lực, giữ cho các nguyên tử cùng nhau trong các phân tử hay các tinh thể.
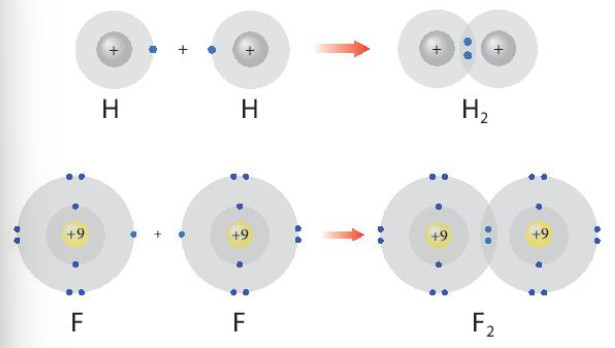
Hình 8.1. Sự hình thành các phân tử hydrogen và flurione
- Phần tử được tạo nên từ các nguyên tử bằng các liên kết hoá học.
- Tìm hiểu cách vận dụng quy tắc octet trong sự hình thành phân tử nitrogen (N2)
+ Để đạt cấu hình electron bền vững của các khí hiểm gần nhất, nguyên tử của các nguyên tố có xu hướng nhường hoặc nhận thêm, hoặc góp chung các electron hoá trị với các nguyên tử khác khi tham gia liên kết hoá học.
+ Ví dụ, liên kết giữa 2 nguyên tử nitrogen (N) trong phân tử nitrogen (N2) được tạo thành do mỗi nguyên tử nitrogen đã góp chung 3 electron hoá trị, tạo nên 3 cặp electron chung như Hình 8.2.
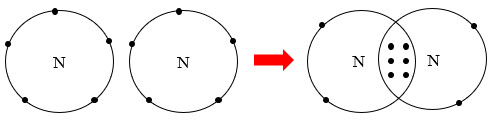
Hình 8.2. Sự hình thành liên kết trong phân tử nitrogen
- Tìm hiểu cách vận dụng quy tắc Octet trong sự hình thành ion dương, ion âm
+ Nguyên tử sodium có 1 electron ở lớp ngoài cùng. Nếu mất đi 1 electron này, nguyên tử sodium sẽ đạt được cấu hình electron bền vững sau:
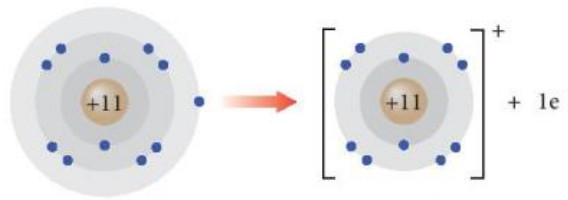
Nguyên tử sodium (Na) lon sodium (Na+)
Hình 8.3. Sự hình thành ion Na+
+ Phần tử thu được mang điện tích dương, gọi là ion sodium, kí hiệu Na+.
+ Tương tự, nguyên tử fluorine có 7 electron ở lớp ngoài cùng. Khi nhận vào 1 electron, nguyên tử fluorine sẽ đạt được cấu hình electron bền vững sau:
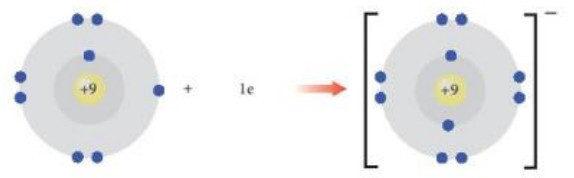
Nguyên tử fluorine (F) Ion fluoride (F-)
Hình 8.4. Sự hình thành ion F-
+ Phần tử thu được mang điện tích âm, gọi là ion fluoride, kí hiệu F-.
+ Không phải trong mọi trường hợp, nguyên tử của các nguyên tố khi tham gia liên kết đếu tuân theo quy tắc Octet.
+ Người ta nhận thấy một số phân tử có thể không tuân theo quy tắc Octet. Ví dụ: NO, BH3, SF6...
+ Với nguyên tử của các nguyên tố nhóm B, người ta áp dụng một quy tắc khác, tương ứng với quy tắc Octet, là quy tắc 18 electron để giải thích xu hướng khi tham gia liên kết hoá học của chúng.
| Quy tắc Octet (bát tử): Trong quá trình hình thành liên kết hoá học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm helium). |
|---|
Bài 1: Khi liên kết với nhau, nguyên tử của các nguyên tố dường như đã cố gắng “bắt chước” cấu hình electron nguyên tử của các nguyên tố khí hiếm để bền vững hơn. Điều này đã được nhà hóa học người Mỹ Lewis (Li-uýt, 1875 – 1946) đề nghị khi nghiên cứu về sự hình thành phân tử từ các nguyên tử. Ông gọi đó là quy tắc octet. Quy tắc Octet là gì?
Hướng dẫn giải
Quy tắc Octet (bát tử): Trong quá trình hình thành liên kết hóa học, nguyên tử của các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có 8 electron tương ứng với khí hiếm gần nhất (hoặc 2 electron với khí hiếm helium)
Bài 2: Nguyên tử của các nguyên tố hydrogen và fluorine có xu hướng cho đi, nhận thêm hay góp chung các electron hóa trị khi tham gia liên kết hình thành phân tử hydrogen fluoride (HF)?
Hướng dẫn giải
- Nguyên tử fluorine và hydrogen đều là phi kim
+ Fluorine có 7 electron lớp ngoài cùng
+ Hydrogen có 1 electron lớp ngoài cùng (lớp 1 có tối đa 2 electron)
→ Cả 2 có xu hướng nhận electron để đạt cấu hình electron của khí hiếm
→ Khi tham gia liên kết hình thành phân tử HF, mỗi nguyên tử sẽ bỏ ra 1 electron để tạo thành 1 cặp electron dùng chung
Bài 3: Khi nguyên tử fluorine nhận thêm 1 electron thì ion tạo thành có cấu hình electron của nguyên tử nguyên tố nào?
Hướng dẫn giải
Khi nguyên tử F nhận thêm 1 electron thì ion tạo thành có cấu hình electron của nguyên tử nguyên tố Ne.
Sau bài học này, học sinh sẽ:
- Trình bày và vận dụng được quy tắt Octet trong quá trình hình thành liên kết hóa học cho các nguyên tố nhóm A.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Chân trời sáng tạo Bài 8 cực hay có đáp án và lời giải chi tiết.
Kim cương được sử dụng làm mũi khoan, dao cắt thủy tinh và bột mài vì kim cương là chất có độ cứng rất lớn. Tính chất trên một phần là do tinh thể kim cương thuộc loại tinh thể
Chỉ ra nội dung sai khi nói về ion :
Cho các ion : Na+, Al3+, SO42-, NO3-, Ca2+, NH4+, Cl–. Hỏi có bao nhiêu cation ?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Chân trời sáng tạo Bài 8để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 52 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 2 trang 52 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 3 trang 53 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 53 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 4 trang 53 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 5 trang 54 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 54 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 1 trang 54 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 2 trang 54 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 3 trang 54 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 4 trang 54 SGK Hóa học 10 Chân trời sáng tạo - CTST
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Kim cương được sử dụng làm mũi khoan, dao cắt thủy tinh và bột mài vì kim cương là chất có độ cứng rất lớn. Tính chất trên một phần là do tinh thể kim cương thuộc loại tinh thể
Chỉ ra nội dung sai khi nói về ion :
Cho các ion : Na+, Al3+, SO42-, NO3-, Ca2+, NH4+, Cl–. Hỏi có bao nhiêu cation ?
Trong các phản ứng hoá học, nguyên tử kim loại có khuynh hướng
Cho các phân tử : H2, CO2, HCl, Cl2. Có bao nhiêu phân tử có cực ?
Liên kết hóa học trong phân tử Br2 thuộc loại liên kết:
Liên kết hóa học giữa các nguyên tử trong phân tử HCl thuộc loại liên kết:
Liên kết trong hợp chất nào dưới đây thuộc loại liên kết ion (biết độ âm điện của Cl(3,16), Al(1,61), Ca(1), S (2,58)
Đặc điểm nào sau đây là đặc điểm về cấu trúc và liên kết trong tinh thể iot:
Nước đá khô thường được dùng để làm lạnh, giữ lạnh nhằm vận chuyển và bảo quản các sản phẩm dễ hư hỏng vì nhiệt độ. Nước đá khô được dùng nhiều trong các ngành công nghiệp thực phẩm, thủy hải sản và còn được dùng để bảo quản vắc xin, dược phẩm trong ngành Y tế – dược phẩm. Thành phàn nước đá khô là CO2, hãy chỉ ra nội dung sai.
Hình 8.1 giải thích sự hình thành phân tử hydrogen (H2) và fluorine (F2) từ các nguyên tử. Theo em, các nguyên tử hydrogen và fluorine đã “bắt chước” cấu hình electron của các nguyên tử khí hiếm nào khi tham gia liên kết?
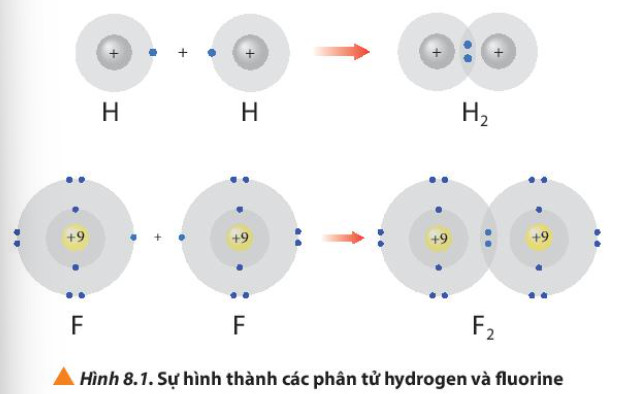
Sử dụng sơ đồ tương tự như Hình 8.1, hãy giải thích sự tạo thành phân tử chlorine (Cl2) và oxygen (O2) từ các nguyên tử tương ứng

Hình 8.1. Sự hình thành các phân tử hydrogen và flurione
Từ Hình 8.2, cho biết mỗi nguyên tử nitrogen đã đạt được cấu hình electron bền vững của nguyên tử khí hiếm nào?
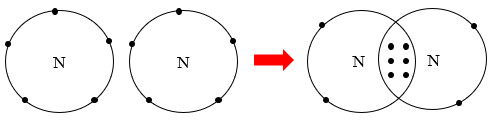
Hình 8.2. Sự hình thành liên kết trong phân tử nitrogen
Nguyên tử của các nguyên tố hydrogen và fluorine có xu hướng cho đi, nhận thêm hay góp chung các electron hóa trị khi tham gia liên kết hình thành phân tử hydrogen fluoride (HF)?
Ion sodium và ion fluoride có cấu hình electron của các khi hiếm tương ứng nào?
Trình bày sự hình thành ion lithium. Cho biết ion lithium có cấu hình electron của khí hiếm tương ứng nào?
Biết phân tử magnesium oxide hình thành bởi các ion Mg2+ và O2-. Vận dụng quy tắc octet, trình bày sự hình thành các ion trên từ những nguyên tử tương ứng.
Nguyên tử của nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khí hiếm argon khi tham gia hình thành liên kết hóa học?
A. Fluorine
B. Oxygen
C. Hydrogen
D. Chlorine
Để đạt quy tắc octet, nguyên tử của nguyên tố potassium (Z = 19) phải nhường đi
A. 2 electron
B. 3 electron
C. 1 electron
D. 4 electron
Vận dụng quy tắc octet, trình bày sơ đồ mô tả sự hình thành phân tử potassium chloride (KCl) từ nguyên tử của các nguyên tố potassium và chlorine.
Giải thích sự hình thành liên kết trong phân tử H2O bằng cách áp dụng quy tắc octet?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *