Bài 11: Liên kết Hydrogen và tương tác Van der Waals chương trình SGK Hóa học 10 chân trời sáng tạo. Với phần lý thuyết đầy đủ và bài tập minh họa đi kèm hướng dẫn giải chi tiết cho từng bài tập có trong chương trình học của sách giáo khoa. Hi vọng, các em học sinh hiểu và nắm vững kiến thức bài học.
a. Tìm hiểu về liên kết hydrogen
- Tìm hiểu về liên kết hydrogen. Nước và hydrogen sulfide (H2S) có cấu trúc phân tử tương tự nhau. Tuy H2S có kích thước phần tử lớn hơn nhưng nhiệt độ sôi của hợp chất này (-60°C) thấp hơn nhiều so với nước (100°C). Điều này có thể được giải thích bởi sự phân cực khác nhau của liên kết trong mỗi phân tử.
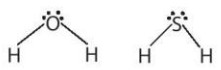
Hình 11.1. Cấu trúc phân tử của nước và hydrogen sulfide
- Lực hút tĩnh điện giữa nguyên tử H mang một phần điện tích dương (linh động) của phân tử H2O này với nguyên tử oxygen mang một phần điện tích âm của phân tử H2O khác, tạo thành liên kết yếu giữa các phần tử nước, gọi là liên kết hydrogen, thường được biểu diễn bằng dấu ba chấm (...).
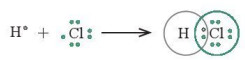
Hình 11.2. Liên kết hydrogen giữa các phân tử nước
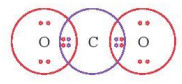
Hình 11.3. Liên kết hydrogen giữa các phần tử ammonia
- Liên kết hydrogen là một loại liên kết yểu, được hình thánh giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cập electron hoá trị chưa tham gia liên kết.
b. Tìm hiểu vai trò, ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
- So với các hợp chất có cấu trúc phân tử tương tự, các hợp chất có liên kết hydrogen đều có nhiệt độ sôi cao hơn do tạo được liên kết hydrogen liền phân tử và tan tốt hơn trong nước do tạo được liên kết hydrogen với các phân tử nước. Nước là một hợp chất có nhiệt độ nóng chảy và nhiệt độ sối cao hơn so với nhiều hợp chất có cùng cấu trúc phân tử nhưng không tạo được liên kết hydrogen giữa các phân tử với nhau.
- Nước là một hợp chất có nhiệt độ nóng chảy và nhiệt độ sối cao hơn so với nhiều hợp chất có cùng cấu trúc phân tử nhưng không tạo được liên kết hydrogen giữa các phân tử với nhau. Ngoài ra, nước còn là một dung môi tốt, không chỉ hoà tan được nhiều hợp chất ion, mà còn hoà tan được nhiều hợp chất có liên kết cộng hoá trị phân cực. Đặc biệt, các hợp chất có thể tạo liên kết hydrogen với nước thường tan tốt trong nước. Hầu hết các phản ứng hoá học quan trọng đối với sự sống đều diễn ra ở môi trường nước bên trong tế bào.
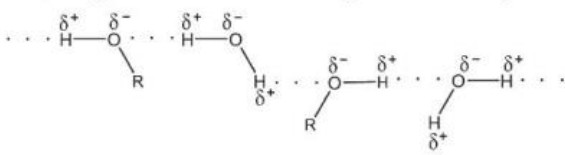
Hình 11.4. Liên kết hydrogen giữa alcohol và nước
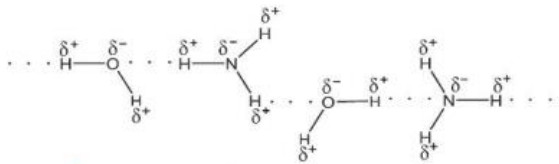
Hình 11.5. Lên kết hydrogen giữa ammonia và nước
- Nước ở trạng thái rắn có thể tích lớn hơn khi ở trạng thái lỏng. Đó là do nước đá có cấu trúc tinh thể phân tử với bốn phân tử H2O phân bổ ở bốn định của một tử diện đểu, bên trong là cấu trúc rỗng (Hình 11.6). Điều này lý giải tại sao nước đá nổi được trên mặt nước lỏng.
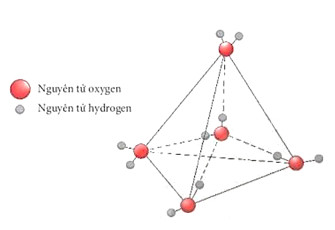
Hình 11.6. Cấu trúc của tinh thể phân tử nước đá
- Nhờ có liên kết hydrogen mà ở điều kiện thường nước ở thể lỏng, có nhiệt độ sôi cao (100°C).
a. Giới thiệu về tương tác van der Waals (van đơ Van)
Trong phân tử, các electron không ngừng chuyển động. Khi các electron di chuyển tập trung về một phía bất kì của phần tử sẽ hình thành nên các lưỡng cực tạm thời. Ví dụ, ta có thể tìm thấy các electron phân bố như Hình 11.7 trong một phân tử.
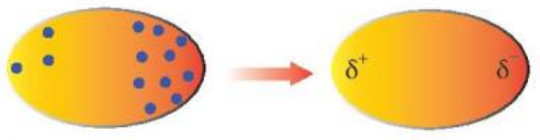
Hình 11.7. Lưỡng cực tạm thời được hình thành do sự phân bố không đồng đều của các electron trong phân tử
- Các phân tử có lưỡng cực tạm thời cũng có thể làm các phân tử lân cận xuất hiện các lưỡng cực cảm ứng. Do đó, các phân tử có thể tập hợp thành một mạng lưới với các tương tác lưỡng cực cảm ứng , được gọi là tương tác van der Waals (Hinh 11.8).
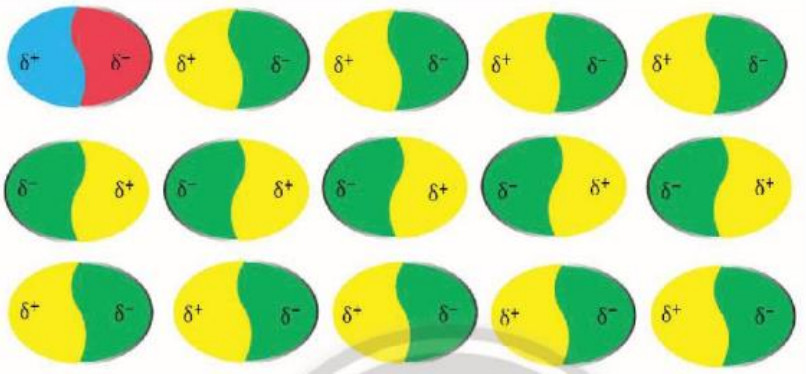
Hình 11.8. Mạng lưới tương tác lưỡng cực cảm ứng được tạo thành bởi lưỡng cực tạm thời
- Tìm hiểu ảnh hưởng của tương tác van der Waals đến nhiệt độ nóng chảy và nhiệt độ sôi các chất
- Tương tác van der Waals được sử dụng để giải thích sự khác biệt về nhiệt độ nóng chảy và nhiệt độ sôi giữa các chất.
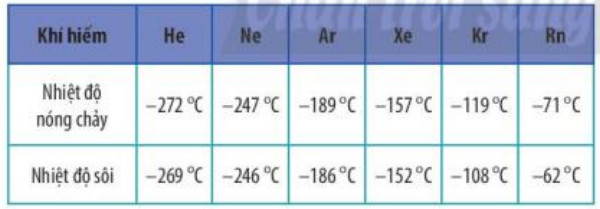
Bảng 11.1. Nhiệt độ sôi và nhiệt độ nóng chảy của các khí hiếm
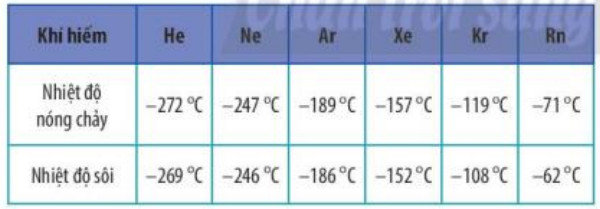
- Tương tác van der Waals là lực tương tác yếu giữa các phân tử, được hình thành do sự xuất hiện của các lưỡng cực tạm thời và lưỡng cực cảm ứng
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất. Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Bài 1: Trong việc hình thành liên kết hóa học, không phải lúc nào các nguyên tử cũng cho, nhận electron hóa trị với nhau như trong liên kết ion. Thay vào đó, chúng có thể cùng nhau sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet. Trong trường hợp này, một loại liên kết hóa học mới được hình thành. Đó là loại liên kết gì?
Hướng dẫn giải
Liên kết mà các nguyên tử sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet được gọi là liên kết cộng hóa trị
Bài 2: Hãy giải thích sự khác nhau về nhiệt độ sôi của butane và isobutane.
Hướng dẫn giải
Đồng phân mạch không phân nhánh butane có nhiệt độ sôi cao hơn so với đồng phân mạch phân nhánh isobutan do diện tích tiếp xúc giữa các phân tử butane lớn hơn nhiều so với isobutane.
Bài 3: Ở áp suất khí quyển, nhiệt độ sôi của H2O là 1000C, CH4 là -161,580C, H2S là -60,280C. Vì sao các chất trên có nhiệt độ sôi khác nhau.
Hướng dẫn giải
- Liên kết hydrogen được hình thành giữa nguyên tử hydrogen với các nguyên tử có độ âm điện lớn và các nguyên tử này phải có 1 ít nhất một cặp electron hóa trị chưa tham gia liên kết.
- Do O và S đều còn 2 cặp electron hóa trị chưa tham gia liên kết, C không còn cặp electron hóa trị tự do nên H2O và H2S có thể tạo liên kết hydrogen trong phân tử, còn CH4 thì không.
→ Nhiệt độ sôi của H2O và H2S lớn hơn CH4.
- Do độ âm điện của O lớn hơn S nên liên kết hydrogen trong phân tử H2O mạnh hơn trong phân tử H2S.
→ Nhiệt độ sôi của H2O lớn hơn H2S.
Sau bài học này, học sinh sẽ:
- Trình bày được khái niệm liên kết hydrogen. Vận dụng để giải thích được sự xuất hiện liên kết hydrogen.
- Nêu được vai trò, ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
- Nêu được khái niệm về tương tác van der Waals và ảnh hưởng của tương tác này tới nhiệt độ nóng chảy, nhiệt độ sôi của các chất.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Chân trời sáng tạo Bài 11 cực hay có đáp án và lời giải chi tiết.
Phân tử BrF5 có cấu trúc hình học dạng:
Liên kết trong tinh thể muối ăn thuộc loại liên kết nào?
Cấu trúc mạng NaCl (muối ăn) là gì?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Chân trời sáng tạo Bài 11để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 67 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 2 trang 68 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 3 trang 68 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 68 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 4 trang 68 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 5 trang 69 SGK Hóa học 10 Chân trời sáng tạo - CTST
Vận dụng trang 69 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 6 trang 69 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 7 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 8 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Vận dụng trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 1 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 2 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 3 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 4 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 5 trang 70 SGK Hóa học 10 Chân trời sáng tạo - CTST
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Phân tử BrF5 có cấu trúc hình học dạng:
Liên kết trong tinh thể muối ăn thuộc loại liên kết nào?
Cấu trúc mạng NaCl (muối ăn) là gì?
Phân tử XeF4 có cấu trúc hình học dạng:
Phân tử Nitơ gồm 2 nguyên tử Nitơ liên kết với nhau bằng
Nguyên tử Al có 3 electron hóa trị. Kiểu liên kết hóa học nào được hình thành khi nó liên kết với 3 nguyên tử flo:
Cho 2 nguyên tố: X (Z=20), Y (Z=17). Công thức hợp chất tạo thành từ X, Y và liên kết trong phân tử lần lượt là
Nguyên tử nguyên tố X có 5e trong các phân lớp s , nguyên tử nguyên tố Y có 11e ở phân lớp p. Hợp chất M tạo bới X và Y chứa liên kết:
Liên kết cộng hóa trị là liên kết được hình thành giữa 2 nguyên tử bằng
P có thể tạo với Cl là PCl3 và PCl5 trong khi N tạo với Cl hợp chất NCl3 đó là do điều nào?
Giữa liên kết S-H và liên kết O-H, liên kết nào phân cực mạnh hơn? Vì sao?
Quan sát các Hình 11.2 và 11.3, em hiểu thế nào là liên kết hydrogen giữa các phân tử?

Hình 11.2. Liên kết hydrogen giữa các phân tử nước

Hình 11.3. Liên kết hydrogen giữa các phần tử ammonia
So sánh độ bền của liên kết hydrogen với liên kết cộng hóa trị và liên kết ion?
Điều gì đã khiến H2O có nhiệt độ sôi cao hơn H2S? Giải thích?
So sánh nhiệt độ sôi và khả năng hòa tan trong nước giữa NH3 và CH4. Giải thích?
Giải thích vì sao một phân tử nước có thể tạo được liên kết hydrogen tối đa với bốn phân tử nước khác?
Vì sao nên tránh ướp lạnh các lon bia, nước giải khát,… trong ngăn đá của tủ lạnh?
Quan sát Hình 11.7, cho biết thế nào là một lưỡng cực tạm thời?
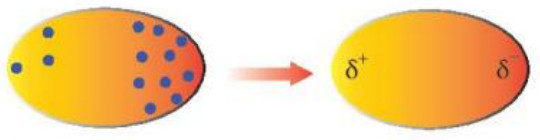
Hình 11.7. Lưỡng cực tạm thời được hình thành do sự phân bố không đồng đều của các electron trong phân tử
Các lưỡng cực tạm thời và lưỡng cực cảm ứng hút nhau bằng lực hút nào?
Giải thích xu hướng biến đổi bán kính nguyên tử, nhiệt độ nóng chảy và nhiệt độ sôi của các nguyên tố khí hiếm trong Bảng 11.1
Bảng 11.1. Nhiệt độ sôi và nhiệt độ nóng chảy của các khí hiếm
Tại sao nhện nước có thể di chuyển trên mặt nước?
Hợp chất nào dưới đây được liên kết hydrogen liên phân tử
A. CH4
B. H2O
C. PH3
D. H2S
Sự phân bố electron không đồng đều trong một nguyên tử hay một phân tử hình thành nên
A. một ion dương
B. một ion âm
C. một lưỡng cực vĩnh viễn
D. một lưỡng cực tạm thời
Khí hiếm nào dưới đây có nhiệt độ sôi thấp nhất?
A. Ne
B. Xe
C. Ar
D. Kr
Biểu diễn liên kết hydrogen giữa các phân tử:
a) Hydrogen fluoride
b) Ethanol (C2H5OH) và nước
Trong hai chất ammonia (NH3) và phosphine (PH3), theo em chất nào có nhiệt độ sôi và độ tan trong nước lớn hơn? Giải thích
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *