Xác định \({\Delta _r}H_{298}^o\) của phản ứng sau dựa vào giá trị Eb ở Bảng 14.1:
CH4(g) + Cl2(g) \(\xrightarrow{{askt}}\) CH3Cl(g) + HCl(g)
Hãy cho biết phản ứng trên tỏa nhiệt hay thu nhiệt?
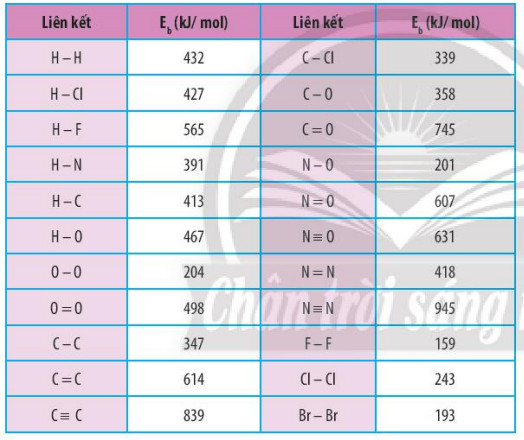
Bảng 14.1. Năng lượng liên kết của một số liên kết cộng hoá trị
Phương pháp giải
Bước 1: Xác định số lượng liên kết và loại liên kết của các chất trong phản ứng
Bước 2: Áp dụng công thức: \({\Delta _r}H_{298}^o\) = \(\Sigma \)Eb(cđ) - \(\Sigma \)Eb(sp)
→ Phản ứng thu nhiệt hay tỏa nhiệt
Lời giải chi tiết
CH4(g) + Cl2(g) \(\xrightarrow{{askt}}\) CH3Cl(g) + HCl(g)
- Chất đầu:
+ CH4 có 4 liên kết C-H
+ Cl2 có 1 liên kết Cl-Cl
- Sản phẩm
+ CH3Cl có 3 liên kết C-H, 1 liên kết C-Cl
+ HCl có 1 liên kết H-Cl
Mà: \({\Delta _r}H_{298}^o\) = \(\Sigma \)Eb(cđ) - \(\Sigma \)Eb(sp)
→ \({\Delta _r}H_{298}^o\) = Eb(CH4) + Eb(Cl2) – Eb(CH3Cl)- Eb(HCl)
= 4 Eb(C-H) + Eb(Cl-Cl) – 3Eb(C-H) - Eb(C-Cl) - Eb(H-Cl)
= 4.413 + 243 – 3. 413 – 339 - 427 = -110 kJ/mol < 0
→ Phản ứng tỏa nhiệt
-- Mod Hóa Học 10