Việc hiểu rõ về các yếu tố ảnh hưởng tới tốc độ phản ứng sẽ giúp ích rất nhiều trong đời sống cũng như trong các ngành công nghiệp, giúp tạo ra thành phẩm với thời gian ngắn hơn rất nhiều. Vậy thế nào là tốc độ phản ứng hóa học? Có những yếu tố nào ảnh hưởng trực tiếp đến tốc độ này. Cùng tìm hiểu thông qua Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng môn Hóa học 10 chương trình SGK Chân trời sáng tạo được DapAnHay biên soạn bên dưới đây:
* Nghiên cứu ảnh hưởng của nồng độ đến tốc độ phản ứng
Thí nghiệm 1: Ảnh hưởng của nồng độ đến tốc độ phản ứng
- Hoá chất: dung dịch sodium thiosulfate (Na2S2O3) 0,15 M; sulfuric acid (H2SO4) 0,10 M; nước cất.
- Dụng cụ: cốc thuỷ tinh 100 mL (được đánh dấu thập ở mặt ngoài đáy cốc), ống đong 50 mL.
- Tiến hành:
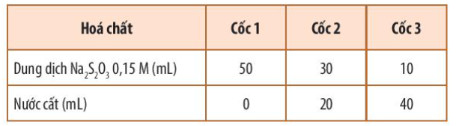
+ Bước 1: Pha loãng dung dịch Na2S2O3 0,15 M để được các dung dịch có nồng độ khác nhau theo Bảng 16.1.
Bảng 16.1. Cách pha loãng dung dịch Na2S2O3
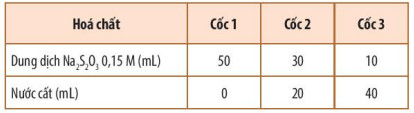
+ Bước 2: Rót đồng thời 10 mL dung dịch H2SO4 0,1 M vào mỗi cốc và khuấy đều.
Phương trình hoá học của phản ứng: Na2S2O3 (aq) + H2SO4 (aq) → Na2SO4 (aq) +S (s) + SO2 (g) + H2O(l)

Hình 16.1. Thí nghiệm ảnh hưởng của nồng độ đến tốc độ phản ứng
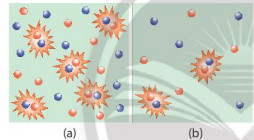
Hình 16.2. Hình minh hoạ chất phản ứng có nồng độ lớn (a) và nồng độ bé (b)
- Nồng độ của các chất phản ứng tăng làm tăng số va chạm hiệu quả nên tốc độ phản ứng tăng.
| Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng. |
|---|
- Nghiên cứu ảnh hưởng của nhiệt độ đến tốc độ phản ứng
Ví dụ 1: Có 2 cốc thủy tinh, mỗi cốc đựng cùng một lượng hỗn hợp dụng dịch oxalic acid (H2C2O4) và dung dịch H2SO4 loãng, tỉ lệ 2:1 về thể tích, cốc (1) được đun nóng, thêm đồng thời cùng một lượng dung dịch KMnO4 vào mỗi cốc (Hình 16.3a), nhận thấy màu của hỗn hợp phản ứng nhạt dần theo thời gian phản ứng (Hình 16.3b).
- Phương trình hoá học của phản ứng: 2KMnO4 (aq) +5H2C2O4 (aq) + 3H2SO4 (aq) →MnSO4 (aq) + K2SO4 (aq) +10CO2(g) +8H2O (1)

Hình 16.3. Thí nghiệm ảnh hưởng của nhiệt độ đến tốc độ phản ứng
- Ở nhiệt độ thường, các chất phản ứng chuyển động với tốc độ nhỏ; khi tăng nhiệt độ, các chất sẽ chuyển động với tốc độ lớn hơn, dẫn đến tăng số va chạm hiệu quả nến tốc độ phản ứng tăng.
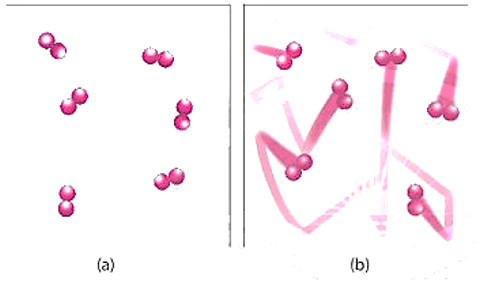
Hình 16.4. Hình minh hoạ chuyển động của chất phản ứng khi chưa đun nóng (a) và được đun nóng (b)
- Kết quả từ các thực nghiệm cho biết, khi nhiệt độ tăng lên 10°C, tốc độ của phần lớn các phản ứng tăng từ 2 đến 4 lần. Số lần tăng này được gọi là hệ số nhiệt độ Van't Hoff (Van-hop), kí hiệu là \(\gamma \).
- Trong Ví dụ 1, nếu nhiệt độ ban đầu của 2 cốc bằng nhau, t1 = 20°C, nhiệt độ của cốc (1) sau khi đun nóng là t2= 60°C, nhiệt độ cốc (2) không thay đổi và tốc độ phản ứng trong cốc (1) gấp 16 lần cốc (2). Khi đó ta có:
\({\gamma ^{\frac{{60 - 20}}{{10}}}} = 16 \to \gamma = 2\)
- Vậy, khi nhiệt độ tăng lên 10°C, thì tốc độ phản ứng tăng 2 lần. Giá trị này là hệ số nhiệt độ Van't Hoff.
| - Khi tăng nhiệt độ, tốc độ phản ứng tăng. - Mối quan hệ giữa nhiệt độ và tốc độ phản ứng hoá học được biểu diễn bằng công thức: \(\frac{{{v_{{t_2}}}}}{{{v_{{t_1}}}}} = {\gamma ^{\frac{{{t_2} - {t_1}}}{{10}}}}\) Trong đó: vt1, vt2 là tốc độ phản ứng ở 2 nhiệt độ t1 và t2; \(\gamma \) là hệ số nhiệt độ Van't Hoff. Quy tắc Vant Hoff chỉ gần đúng trong khoảng nhiệt độ không cao. |
|---|
* Nghiên cứu ảnh hưởng của áp suất đến tốc độ phản ứng
- Trong phản ứng hoá học có sự tham gia của chất khí, áp suất có thể ảnh hưởng đến tốc độ phản ứng.
Ví dụ 2: Một trong những nghiên cứu nhằm giảm thiểu phát thải khí CO2 vào khí quyển gây hiệu ứng nhà kính, là chuyển CO2 thành sản phẩm có giá trị như methanol (CH3OH).
Phản ứng cần thực hiện ở áp suất cao, khoảng 58 – 103 bar để tăng tốc độ phản ứng. Phương trình hoá học của phản ứng:
CO2(g) + 3H2(g) → CH3OH(g) + H2O(g)

Hình 16.5. Minh hoạ khi tăng áp suất của các chất khí tham gia phản ứng
- Khi tăng áp suất thì nồng độ chất khí tăng, nên tốc độ phản ứng tăng.
| Đối với phản ứng có chất khí tham gia, tốc độ phản ứng tăng khi tăng áp suất. |
|---|
a. Nghiên cứu ảnh hưởng của bề mặt tiếp xúc đến tốc độ phản ứng
Thí nghiệm 2: Ảnh hưởng của bề mặt tiếp xúc đến tốc độ phản ứng
- Hoá chất: dung dịch HCl 1 M, đá vôi (CaCO3) dạng khối và dạng hạt nhỏ.
- Dụng cụ: bình tam giác 100 mL, ống đong 50 mL, cân.
- Tiến hành:
+ Bước 1: Cần khoảng 2 g CaCO3 mỗi loại, cho vào 2 bình tam giác (1), (2).
+ Bước 2: Đong khoảng 20 ml dung dịch HCl, rót đồng thời vào mỗi bình tam giác.
Phương trình hoá học của phản ứng:
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + H2O(1) + CO2(g)
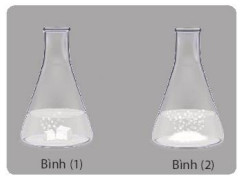
Hình 16.6. Minh hoạ thí nghiệm nghiên cứu ảnh hưởng của bề mặt tiếp xúc đến tốc độ phản ứng
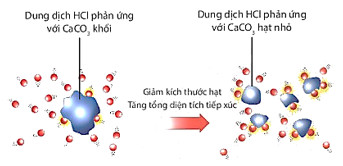
Hình 16.7. Minh hoạ dung dịch HCl phản ứng với CaCO3 có kích thước khác nhau
| Khi tăng diện tích bề mặt tiếp xúc của chất phản ứng, tốc độ phản ứng tăng. |
|---|
- Với một số phản ứng hoá học, để tăng tốc độ phản ứng, người ta sử dụng chất xúc tác, được ghi trên mũi tên trong phương trình hoá học.
* Nghiên cứu ảnh hưởng của xúc tác đến tốc độ phản ứng
- Thí nghiệm 3: Ảnh hưởng của xúc tác đến tốc độ phản ứng
- Hoá chất: dung dịch hydrogen peroxide (H2O2) 30%, bột MnO2
- Dụng cụ: ống nghiệm, tàn đóm đỏ.
- Tiến hành:
+ Bước 1: Rót khoảng 2 mL dung dịch H2O2 vào 2 ống nghiệm (1), (2).
+ Bước 2: Thêm một ít bột MnO2 vào ống nghiệm (2) và đưa nhanh tàn đóm đỏ vào miệng 2 ống nghiệm (Hình 16.8).
Phương trình hoá học của phản ứng:
2H2O2 (aq) → 2H2O (l) + O2 (g)

Hình 16.8. Thí nghiệm nghiên cứu ảnh hưởng của xúc tác đến tốc độ phản ứng
| Chất xúc tác làm tăng tốc độ của phản ứng hoá học, nhưng vẫn được bảo toàn về lượng và chất khi kết thúc phản ứng. |
|---|
* Tìm hiểu các yếu tố ảnh hưởng đến tốc độ phản ứng trong đời sống và sản xuất
- Vận dụng các yếu tố ảnh hưởng đến tốc độ phản ứng sẽ góp phần hiệu quả vào phục vụ đời sống, sản xuất, thúc đẩy quá trình diễn ra nhanh hơn hoặc hạn chế tốc độ của phản ứng, nhằm tối ưu hoá giá trị kinh tế.

(a) Dùng bình chứa oxygen thay cho dùng không khí để đốt cháy acetylene, ứng dụng trong đèn xì acetylene.

(b) Thực phẩm nấu trong nổi áp suất sẽ nhanh chín hơn so với khi nấu ở áp suất thường.

(c) Khi đốt than trong lò, đậy nắp lò sẽ giữ than cháy được lâu hơn

(d) Bảo quản thức ăn trong tủ lạnh để thức ăn lâu bị ôi thiu
Hình 16.9. Ý nghĩa thực tiễn của tốc độ phản ứng trong đời sống và sản xuất
| Kiểm soát tốc độ các phản ứng diễn ra trong đời sống, sản xuất khi vận dụng các yếu tố ảnh hưởng như: nồng độ, nhiệt độ, áp suất, bề mặt tiếp xúc và chất xúc tác giúp mang lại các giá trị hiệu quả. |
|---|
Bài 1: Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn (a), khi nấu một loại thực phẩm bằng nồi áp suất sẽ nhanh chín hơn (b), bệnh nhân sẽ dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí(c),…

a) b) c)
Những yếu tố nào ảnh hưởng đến tốc độ của các quá trình biến đổi trên?
Hướng dẫn giải
(a) Ảnh hưởng của nhiệt độ
(b) Ảnh hưởng của áp suất
(c) Ảnh hưởng của nồng độ
Bài 2: Tìm một số thí dụ cho mỗi loại phản ứng nhanh và chậm mà em quan sát được trong cuộc sống và trong phòng thí nghiệm.
Hướng dẫn giải
Các ví dụ về loại phản ứng:
– Phản ứng nhanh: phản ứng nổ, sự đốt cháy các nhiên liệu (than, dầu, khí đốt,…) phản ứng giữa hai dung dịch AgNO3 và NaCl,…
– Phản ứng chậm: sự gỉ sắt, sự lên men rượu,…
Bài 3: Cho phản ứng hóa học: 2NO(k) + O2(k) → 2NO2(k)
Tốc độ phản ứng hóa học trên được tính theo công thức y = k [NO]2[O2]. Hỏi ở nhiệt độ không đổi, áp suất chung của hệ đã tăng bao nhiêu lần khi tốc độ của phản ứng tăng 64 lần?
Hướng dẫn giải
Đặt x là số lần tăng của áp suất. Theo bài ra ta có v2/v1 = 64 = x3 → x = 4.
Bài 4: Hãy cho biết các yếu tố ảnh hưởng đến tốc độ phản ứng như thế nào? Giải thích.
Hướng dẫn giải
Các yếu tố ảnh hưởng đến tốc độ phản ứng.
a) Ảnh hưởng của nồng độ: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng. Giải thích: Điều kiện để các chất phản ứng với nhau là chúng phải va chạm vào nhau, tần số va chạm càng lớn thì tốc độ phản ứng càng lớn. Khi nồng độ các chất phản ứng tăng, tần số va chạm tăng nên tốc độ phản ứng tăng.
b) Ảnh hưởng của áp suất: Đối với phản ứng có chất khí, khi tăng áp suất, tốc độ phản ứng tăng.
Giải thích: Khi áp suất tăng, nồng độ các chất khí tăng tần số va chạm tăng nên tốc độ phản ứng tăng.
c) Ảnh hưởng của nhiệt độ: Khi tăng nhiệt độ, tốc độ phản ứng tăng.
Giải thích: Khi nhiệt độ tăng dần đến hai hệ quả sau:
– Tốc độ chuyển động của các phân tử tăng, dẫn đến tần số va chạm giữa các phân tử chất phản ứng tăng.
– Tần số va chạm có hiệu quả giữa các phân tử chất phản ứng tăng nhanh.
d) Ánh hưởng của diện tích bề mặt: Khi tăng diện tích bề mặt chất phản ứng, tốc độ phản ứng tăng.
Giải thích: Chất rắn với kích thước hạt nhỏ, có tổng diện tích bề mặt tiếp xúc với chất phản ứng lớn hơn so với chất rắn có kích thước lớn hơn và cùng khối lượng, nên tốc độ phản ứng lớn hơn.
e) Ảnh hưởng của chất xúc tác: Chất xúc tác là chất làm tăng tốc độ phản ứng, nhưng còn lại sau khi phản ứng kết thúc.
Giải thích: Chất xúc tác làm yếu liên kết giữa các nguyên tử của phân tử tham gia phản ứng làm biến đổi cơ chế phản ứng nên làm tăng tốc độ phản ứng.
Sau bài học này, học sinh sẽ:
- Thực hiện được một số thí nghiệm nghiên cứu các yếu tố ảnh hưởng tới tốc độ phản ứng.
- Giải thích được các yếu tố ảnh hưởng tới tốc độ phản ứng như: nồng độ, nhiệt độ, áp suất, diện tích bề mặt, chất xúc tác.
- Nêu được ý nghĩa của hệ số nhiệt độ Vant Hoff (Y).
- Vận dụng được kiến thức tốc độ phản ứng hoá học vào việc giải thích một số vấn đề trong cuộc sống và sản xuất.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Chân trời sáng tạo Bài 16 cực hay có đáp án và lời giải chi tiết.
Khi nhiệt độ tăng lên 100C, tốc độ của một phản ứng hoá học tăng lên 3 lần. Người ta nói rằng tốc độ phản ứng hoá học trên có hệ số nhiệt độ bằng 3. Điều khẳng định nào sau đây là đúng?
Để hoà tan một tấm Zn trong dd HCl ở 200C thì cần 27 phút, cũng tấm Zn đó tan hết trong dd HCl nói trên ở 400C trong 3 phút. Hỏi để hoà tan hết tấm Zn đó trong dd HCl trên ở 550C thì cần bao nhiêu thời gian?
Khi nhiệt độ tăng thêm 10oC tốc độ phản ứng hóa học tăng thêm 3 lần. Để tốc độ phản ứng đó (đang tiến hành ở 300C) tăng lên 81 lần thì cần thực hiện ở nhiệt độ nào?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Chân trời sáng tạo Bài 16để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 98 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 2 trang 99 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 99 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 3 trang 99 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 4 trang 100 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 100 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 5 trang 101 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 101 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 6 trang 101 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 7 trang 101 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 8 trang 102 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 102 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 9 trang 102 SGK Hóa học 10 Chân trời sáng tạo - CTST
Luyện tập trang 103 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải câu hỏi 10 trang 103 SGK Hóa học 10 Chân trời sáng tạo - CTST
Vận dụng trang 104 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 1 trang 104 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 2 trang 104 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 3 trang 104 SGK Hóa học 10 Chân trời sáng tạo - CTST
Giải bài 4 trang 104 SGK Hóa học 10 Chân trời sáng tạo - CTST
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Khi nhiệt độ tăng lên 100C, tốc độ của một phản ứng hoá học tăng lên 3 lần. Người ta nói rằng tốc độ phản ứng hoá học trên có hệ số nhiệt độ bằng 3. Điều khẳng định nào sau đây là đúng?
Để hoà tan một tấm Zn trong dd HCl ở 200C thì cần 27 phút, cũng tấm Zn đó tan hết trong dd HCl nói trên ở 400C trong 3 phút. Hỏi để hoà tan hết tấm Zn đó trong dd HCl trên ở 550C thì cần bao nhiêu thời gian?
Khi nhiệt độ tăng thêm 10oC tốc độ phản ứng hóa học tăng thêm 3 lần. Để tốc độ phản ứng đó (đang tiến hành ở 300C) tăng lên 81 lần thì cần thực hiện ở nhiệt độ nào?
Khi nhiệt độ tăng thêm 10oC, tốc độ phản ứng hóa học tăng lên 2 lần. Tốc độ phản ứng đó sẽ tăng lên bao nhiêu lần khi nâng nhiệt độ từ 25oC lên 75oC?
Cho phương trình hóa học của phản ứng: X + 2Y → Z + T.
Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/L. Sau 20 giây, nồng độ của chất X là 0,008 mol/L. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
Cho phản ứng: 2NO + O2 → 2NO2 xảy ra trong bình kín. Biết nhiệt độ của hệ không đổi. Tốc độ của phản ứng tăng hay giảm bao nhiêu lần khi áp suất của NO tăng 3 lần?
Kẽm ở dạng bột khi tác dụng với dung dịch HCl 1M ở thì tốc độ phản ứng xảy ra nhanh hơn so với kẽm ở dạng hạt. Yếu tố ảnh hưởng đến tốc độ phản ứng trên:
Yếu tố nào sau đây không ảnh hưởng đến tốc độ của phản ứng sau: CaCO3 (r) + 2HCl(dd) → CaCl2 + H2O + CO2 ↑
Phản ứng trong bình kín giữa các phân tử khí xảy ra theo phương trình: A2 + 2B → 2AB. Tốc độ của phản ứng thay đổi như thế nào khi áp suất của A2 tăng lên 6 lần?
Một phản ứng đơn giản xảy ra trong bình kín: \(2NO{\rm{ }}\left( k \right){\rm{ }} + {\rm{ }}{O_{2\;}}\left( k \right){\rm{ }} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over {\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{ }}2N{O_2}\;\left( k \right)\) . Giữ nguyên nhiệt độ, nén hỗn hợp phản ứng xuống còn 1/3 thể tích. Kết luận nào sau đây không đúng ?
Tiến hành thí nghiệm 1 và quan sát hiện tượng của thí nghiệm. Nhận xét mối liên hệ giữa thể tích dung dịch Na2S2O3 với thời gian xuất hiện kết tủa
Quan sát Hình 16.2 và phương trình hóa học của phản ứng, giải thích kết quả thí nghiệm 1
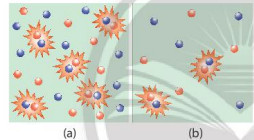
Hình 16.2. Hình minh hoạ chất phản ứng có nồng độ lớn (a) và nồng độ bé (b)
Giữ nguyên nồng độ dung dịch Na2S2O3 ban đầu, pha loãng dung dịch H2SO4 tương tự như cách pha loãng dung dịch Na2S2O3 theo Bảng 16.1, kết quả thí nghiệm sẽ thay đổi thế nào?
Bảng 16.1. Cách pha loãng dung dịch Na2S2O3
Quan sát Hình 16.3, nhận xét sự ảnh hưởng của nhiệt độ đến tốc độ phản ứng

Hình 16.3. Thí nghiệm ảnh hưởng của nhiệt độ đến tốc độ phản ứng
Quan sát Hình 16.4 và phương trình hóa học của phản ứng, giải thích vì sao tốc độ mất màu của KMnO4 trong 2 cốc không giống nhau
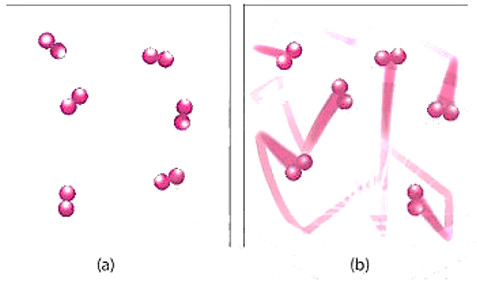
Hình 16.4. Hình minh hoạ chuyển động của chất phản ứng khi chưa đun nóng (a) và được đun nóng (b)
Biết rằng, khi nhiệt độ tăng thêm 10oC, tốc độ của một phản ứng hóa học tăng 4 lần; cho biết tốc độ phản ứng giảm bao nhiêu lần khi nhiệt độ giảm từ 70oC xuống 40oC
Quan sát Hình 16.5, cho biết mật độ phân bố của các phân tử chất khí trong bình kín thay đổi như thế nào khi tăng áp suất của bình?

Hình 16.5. Minh hoạ khi tăng áp suất của các chất khí tham gia phản ứng
Xét các phản ứng xảy ra trong bình kín:
2CO(g) + O2(g) → 2CO2(g) (1)
NH4Cl(s) → NH3(g) + HCl(g) (2)
Yếu tố áp suất ảnh hưởng đến tốc độ của phản ứng nào? Khi tăng áp suất, tốc độ phản ứng thay đổi như thế nào?
Tiến hành thí nghiệm 2 và so sánh tốc độ khí thoát ra trong hai bình tam giác
Nhận xét mối liên hệ giữa tốc độ phản ứng với kích thước của CaCO3
Quan sát Hình 16.7, giải thích kết quả của thí nghiệm 2

Hình 16.7. Minh hoạ dung dịch HCl phản ứng với CaCO3 có kích thước khác nhau
Củi khi được chẻ nhỏ sẽ cháy nhanh hơn và mạnh hơn so với củi có kích thước lớn. Giải thích?
Tiến hành thí nghiệm 3, quan sát hiện tượng và so sánh sự thay đổi của tàn đóm ở 2 ống nghiệm
Tại sao khi nhai kĩ cơm, cảm nhận cơm có vị ngọt hơn?
Quan sát Hình 16.9, cho biết yếu tố nào ảnh hưởng đến tốc độ phản ứng đã được vận dụng trong thực tiễn

(a) Dùng bình chứa oxygen thay cho dùng không khí để đốt cháy acetylene, ứng dụng trong đèn xì acetylene.

(b) Thực phẩm nấu trong nổi áp suất sẽ nhanh chín hơn so với khi nấu ở áp suất thường.

(c) Khi đốt than trong lò, đậy nắp lò sẽ giữ than cháy được lâu hơn

(d) Bảo quản thức ăn trong tủ lạnh để thức ăn lâu bị ôi thiu
Hình 16.9. Ý nghĩa thực tiễn của tốc độ phản ứng trong đời sống và sản xuất
Trong quá trình lên men giấm, người ta thường cho chuối hay nước dừa vào lọ chứa giấm nuôi, giải thích
Hai nhân vật minh họa trong hình bên đang chế biến món gà rán, được thực hiện bằng hai cách. Một người chọn cách chia ra từng phần nhỏ, người còn lại chọn cách để nguyên, giả thiết các điều kiện đều giống nhau (nhiệt độ, lượng dầu ăn,…) Hãy cho biết cách nào món ăn nhanh chín hơn? Giải thích

Nồng độ, nhiệt độ, áp suất, diện tích tiếp xúc, chất xúc tác ảnh hưởng như thế nào đến tốc độ phản ứng
Cho a g kim loại Zn dạng hạt vào lượng dư dung dịch HCl 2M, phương trình hóa học xảy ra như sau:
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Tốc độ khí H2 thoát ra như thế nào khi thay đổi các yếu tố dưới đây
a) Thay a g Zn hạt bằng a g bột Zn
b) Thay dung dịch HCl 2M bằng dung dịch HCl 1M
c) Thực hiện phản ứng ở nhiệt độ cao hơn bằng cách đun nóng nhẹ dung dịch HCl
Cho phương trình hóa học của phản ứng: 2CO(g) + O2(g) → 2CO2(g)
Nếu hệ số nhiệt độ Van’t Hoff bằng 2, tốc độ phản ứng thay đổi như thế nào khi tăng nhiệt độ của phản ứng từ 30oC lên 60oC?
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *