Không khí có là điều rất quen thuộc và tồn tại trong bầu khí quyển xung quanh chúng ta. Vậy bằng cách nào người ta xác định được thành phần của không khí? Không khí có liên quan gì đến sự cháy? Tại sao gió càng lớn thì đám cháy càng lớn? Làm thế nào để dập tắt được sự cháy? Để hiểu rõ hơn tiết học này các em sẽ tìm hiểu nội dung bài học hôm nay.
Hình 1: Thí nghiệm xác định thành phần của không khí
⇒Từ sự thay đổi mực nước trong ống đong ta thấy thể tích của khí oxi trong không khí chiếm 1 phần.
Hay \({V_{{O_2}}} = \frac{1}{5}{V_{kk}}\)
* Kết luận:
Em hãy chọn phương pháp đúng để dập tắt ngọn lửa do xăng dầu.
Phương án A: Dùng quạt để quạt tắt ngọn lửa
Phương án B: Dùng vải dày hoặc cát phủ lên ngọn lửa
Phương án C: Dùng nước tưới lên ngọn lửa
Ta chọn phương pháp B: Dùng vải dày hoặc cát phủ lên ngọn lửa.
Bởi vì:
Phương pháp A: Dùng quạt: Cung cấp thêm oxi, ngọn lửa sẽ cháy lớn hơn
Phương pháp B: Dùng vải dày hoặc cát phủ lên ngọn lửa sẽ ngăn cách được chất cháy với oxi
Phương pháp C: Dùng nước: Xăng dầu nhẹ, nổi lên mặt nước sẽ lan rộng ra làm đám lửa cháy to hơn
a) Khi quạt gió vào bếp củi vừa bị tắt, lượng oxi sẽ tăng lên làm cho sự cháy diễn ra mạnh hơn và lửa sẽ bùng cháy lên.
b) Khi quạt gió vào ngọn nến đang cháy, nến tắt là do ngọn lửa của nến nhỏ nên khi quạt lượng gió vào nhiều sẽ làm nhiệt độ hạ thấp đột ngột nên nến bị tắt.
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 28có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Thành phần không khí gồm:
Quá trình nào dưới đây không làm giảm lượng oxi trong không khí
Khi thổi không khí vào nước nguyên chất, dung dịch thu được hơi có tính axit. khí nào sau đây gây nên tính axit đó?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 28.
Bài tập 1 trang 99 SGK Hóa học 8
Bài tập 2 trang 99 SGK Hóa học 8
Bài tập 3 trang 99 SGK Hóa học 8
Bài tập 4 trang 99 SGK Hóa học 8
Bài tập 5 trang 99 SGK Hóa học 8
Bài tập 6 trang 99 SGK Hóa học 8
Bài tập 7 trang 99 SGK Hóa học 8
Bài tập 28.1 trang 39 SBT Hóa học 8
Bài tập 28.2 trang 39 SBT Hóa học 8
Bài tập 28.3 trang 39 SBT Hóa học 8
Bài tập 28.4 trang 39 SBT Hóa học 8
Bài tập 28.5 trang 39 SBT Hóa học 8
Bài tập 28.6 trang 40 SBT Hóa học 8
Bài tập 28.7 trang 40 SBT Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Thành phần không khí gồm:
Quá trình nào dưới đây không làm giảm lượng oxi trong không khí
Khi thổi không khí vào nước nguyên chất, dung dịch thu được hơi có tính axit. khí nào sau đây gây nên tính axit đó?
Đốt cháy 3,1g photpho trong bình chứa 5g oxi. Sau phản có chất nào còn dư?
Để bảo vệ không khí trong lành chúng ta nên làm gì?
Phương pháp nào để dập tắt lửa do xăng dầu?
Chọn đáp án đúng nhất. Bản chất của phản ứng cháy là:
Điều kiện phát sinh phản ứng cháy là:
Sự giống nhau giữa sự cháy và sự oxi hóa chậm là
Đốt cháy 6,72 lít oxi và 6,2 g P trong bình. Sau phản ứng chất nào còn dư?
Chọn câu trả lời đúng trong các câu sau đây về thành phần của không khí:
A. 21% khí nitơ, 78% oxi, 1% các khí khác (CO2, CO, khí hiếm,…).
B. 21% các khí khác, 78% khí nitơ, 1% khí oxi.
C. 21% khí oxi, 78% khí nitơ, 1% các khí khác.
D. 21% khí oxi, 78% các khí khác, 1% khí nitơ.
Không khí bị ô nhiễm có thể gây ra tác hại gì? Phải làm gì để bảo vệ không khí trong lành?
Giải thích vì sao sự cháy trong không khí xảy ra chậm hơn và tạo ra nhiệt độ thấp hơn so với sự cháy trong oxi?
Điểm giống và khác nhau giữa sự cháy và sự oxi hóa chậm là gì?
Những điều kiện cần thiết để cho một vật có thể cháy và tiếp tục cháy được là gì?
Muốn dập tắt ngọn lửa trên người hoặc ngọn lửa do xăng dầu cháy, người ta thường trùm vải hoặc phủ cát lên ngọn lửa, mà không dùng nước. Giải thích vì sao?
Mỗi giờ một người lớn tuổi hít vào trung bình 0,5 m3 không khí, cơ thể giữ lại 1/3 lượng oxi có trong không khí đó. Như vậy thực tế mỗi người trong một ngày đêm cần trung bình:
a) Một thể tích không khí là bao nhiêu?
b) Một thể tích khí oxi là bao nhiêu?
(Giả sử các thể tích khí được đo ở đktc).
Hãy nêu hiện tượng em thường gặp trong đời sống hàng ngày để chứng tỏ trong không khí có hơi nước, khi cacbonic.
a) Trong đời sống hàng ngày những quá trình sinh ra khí CO2 và quá trình nào làm giảm khí O2?
b) Nồng độ khí CO2 trong không khí cao sẽ làm tăng nhiệt độ của Trái đất (hiệu ứng nhà kính). Theo em biện pháp nào là giảm lượng khí CO2?
a) Cháy (hỏa hoạn) thường gây tác hại nghiêm trọng về vật chất và cả sinh mạng con người. Vậy theo em phải có biện pháp nào để phòng cháy trong gia đình?
b) Để dập tắt các đám cháy người ta dùng nước, điều này có đúng trong mọi trường hợp chữa cháy?
Cho không khí (chứa 80% thể tích là khí nito tác dụng với đồng nung nóng trong thiết bị kín, xảy ra phản ứng oxi hóa đồng thành đồng (II) oxit. Phản ứng xong, người ta thu được 160 cm3 khí nito. Thể tích không khí trong thiết bị trước khi xảy ra phản ứng là:
A. 200 cm3
B. 400 cm3
C. 300 cm3
D. 500 cm3
(Các thể tích khí đo ở đktc)
Để một ít P đỏ vào đĩa nổi trên mặt nước, rồi đốt cháy, úp bình không cháy lên đĩa. Sau đó đậy nắp bình (thiết kế như hình vẽ).
a) Em hãy nêu hiện tượng quan sát được và giải thích, viêt phương trình phản ứng.
b) Cho giấy quỳ tím vào nước trong bình, giấy quỳ có đổi màu không?
Trong một phòng học có chiều dài 12m, chiều rộng 7m, chiều cao 4m.
a) Tính thể tích không khí và oxi có trong phòng học.
b) trong phòng học có 50 em học sinh, hãy tính thể tích khí CO2 thở trong 45 phút, biết rằng một học sinh thử ra 2 lit khí ( thể tích CO2 chiếm 4%) một lần, một phút thở ra khoảng 16 lần.
Trên đĩa cân, ở vị trí cân bằng, có đặt một cốc có dung dịch là 0,5 lit. Sau đó, người ta dùng khí cacbonic CO2 để đẩy không khí khỏi cốc đó. Hỏi phải đặt them vào đĩa cân bên kia quả cân bao nhiêu để cân trở nên thăng bằng? Biết rằng CO2 nặng gấp 1,5 lần không khí, thể tích khí CO2 tính ở đktc.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
a) Xác định kim loại A .
b) Nếu điện phân nóng chảy và có mặt chất xúc tác toàn bộ lượng oxit trên sẽ thu được a gam kim loại A và V lít khí oxi (đktc) . Hãy lập luận tìm ra a và V một cách nhanh nhất mà không phải tính theo phương trình hóa học
Câu trả lời của bạn
a/ Gọi kim loại A có hóa trị là a
\(4A\left(\frac{5,4}{A}\right)+aO_2\rightarrow2A_2O_a\left(\frac{2,7}{A}\right)\)
\(n_A=\frac{5,4}{A}\left(mol\right)\)
\(\Rightarrow\frac{2,7}{A}.\left(2A+16a\right)=10,2\)
\(\Rightarrow A=9a\)
Thế a lần lược 1,2,3.. ta nhận a = 3 suy ra A = 27
Vậy A là Al
b/ Theo đề bài thì ta đã có Al có khối lượng là 5,4 nên khối lượng lúc sau cũng là 5,4 (g).
Theo định luật bảo toàn khối lượng thì
\(10,2=5,4+m_{O_2}\)
\(\Rightarrow m_{O_2}=10,2-5,4=4,8\left(g\right)\)
\(\Rightarrow n_{O_2}=\frac{4,8}{32}=0,15\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)
Câu trả lời của bạn
Gọi x là số mol của CuO
y là số mol của F e 2 O 3 .
Ta có: 80x + 160y = 16 (1)
Khối lượng hỗn hợp giảm do oxit tạo thành kim loại:
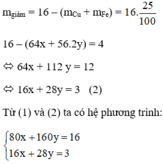
Giải hệ phương trình ta được:
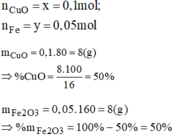
a) Xác định công thức phân tử
b) Để khử hoàn toàn 2,32 g kim loại trên thì cần dùng bao nhiêu gam CO biết hiệu xuất là 30%
Câu trả lời của bạn
a) Đặt CTHH: AxOy
\(m_A=\frac{232.72,41}{100}=168\left(g\right)\)
\(m_O=232-168=64\left(g\right)\)
\(n_O=\frac{64}{16}=4\left(mol\right)\)
Ta có: A.x=168
Lập bảng ta có: x=3; A=56 là thích hợp
CTHH: Fe3O4
b) \(Fe_3O_4+4CO\underrightarrow{t^o}3Fe+4CO_2\)
\(n_{Fe_3O_4}=\frac{2,32}{232}=0,01\left(mol\right)\)
Vì hiệu suất là 30% nên chỉ có 30% lượng oxit sắt từ phản ứng
\(n_{Fe_3O_4}=\frac{0,01.30}{100}=0,003\left(mol\right)\)
\(n_{CO}=3.n_{Fe_3O_4}=3.0,003=0,009\left(mol\right)\)
\(m_{CO}=0,009.28=0,252\left(g\right)\)
Câu trả lời của bạn
4Al + 3O2 => 2Al2O3
2Mg + O2 => 2MgO
giải hệ 27x+24y= 15,6
0,75x+0,5y= 0,4
=> x= 0,4 ;y= 0,2
=> mAl = 0,4.27 = 10,8(g)
%Al = \(\frac{10,8}{15,6}.100\%=69,23\%\)
=> %Mg = 100%- 69,23% = 30,77%
a) Tính thể tích khí oxi cần dùng
b)Tìm số gam KMnO4 cần dùng để điều chế lượng oxi trên
Câu trả lời của bạn
Ta có: NAl = \(\frac{8,1}{27}\)= 0,3 mol
4Al + 3O2 \(\underrightarrow{t}\) 2Al2O3
NO2 = 3/4 NAl = 0,3 . 3/4 = 0,225 mol
VO2 = 0,225 . 22,4 = 5,04 (l)
b) 2KMnO4 \(\underrightarrow{t}\) K2MnO4 + O2 + MnO2
NKMnO4 = 2NO2 = 2. 0,225 = 0,45 mol
mKMnO4 = 0,45 . 158 = 71,1 (g)
5. K + H2O →...
6. H2 + FeO4 →...
7. Al + H2SO4 →...
8. Mg + HCl →...
9.Na + H2O →...
10. CaO + H2O →
11. P2O5 + H2O →
12. SO3 + H2O →...
Câu trả lời của bạn
1, 4Al + 3O2 \(\rightarrow\)2Al2O3
2, 2KMnO4 \(\rightarrow\)K2MnO4 + MnO2 + O2
3, 2KClO3 \(\rightarrow\)2KCl + 3O2
4, CuO + H2 \(\rightarrow\)Cu + H2O
5,2 K+H2O \(\rightarrow\)K2O + H2
6, H2 + Fe3O4 \(\rightarrow\)Fe + H2O
7, 2Al + 3H2SO4 \(\rightarrow\)Al2(SO4)3 + 3H2
, Mg + 2HCl \(\rightarrow\)MgCl2 + H2
9, 2Na + 2H2O \(\rightarrow\)2NaOH + H2
10, CaO + H2O \(\rightarrow\)Ca(OH)2
11, P2O5 + 3H2O \(\rightarrow\)2H3PO4
Câu trả lời của bạn
gọi nMg = x , nP=y
no2 =6,72:32=0,21 mol
pt pứ : 2Mg +O2 => 2MgO (1)
tỉ lệ: 2mol :1mol :2mol
ta có:x :1\2x :x
pt :4P+5O2 =>2P2O5 (2)
tỉ lệ:4mol:5mol:2mol
ta có:y:5\4y:1\2y
từ pt (1) và (2):24x + 31y =8,6 và 1\2x +5\4y= 0,21
=> x=0,29 và y=0,05
=>mMg=24. 0,29 =6,96g
mP= 0,05 . 31 =1,55 g
%Mg=? %P=?
a , tính thể tích Oxi cần dùng để đốt cháy hết 11,2 lít khí metan
b , muốn có thể tích Oxi nói trên cần phải phân hủy bao nhiêu gam kali clorat
Câu trả lời của bạn
PTHH: CH4 + 2O2 -to-> CO2 + 2H2O
a) Ta có:
\(n_{CH_4}=\frac{11,2}{22,4}=0,5\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{O_2}=2.n_{CH_4}=2.0,5=1\left(mol\right)\\ =>V_{O_2\left(đktc\right)}=1.22,4=22,4\left(l\right)\)
b) 2KClO3 -to-> 2KCl + 3O2
Theo câu a, ta có:
\(n_{O_2}=1\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{KClO_3}=\frac{2.1}{3}\approx0,667\left(mol\right)\)
Khối lượng KClO3 đã phản ứng:
\(m_{KClO_3}=0,667.122,5=81,7075\left(g\right)\)
Câu trả lời của bạn
Các PTHH:
*) CH4 + 2O2 =(nhiệt)=> CO2 + 2H2O
*) 2C2H2 + 5O2 =(nhiệt)=> 4CO2 + 2H2O
*) C2H6O + 3O2 =(nhiệt)=> 2CO2 + 3H2O
Câu trả lời của bạn
\(2Na\left(0,05\right)+2HCl\rightarrow2NaCl+H_2\left(0,025\right)\)
\(Mg\left(x\right)+H_2SO_4\rightarrow MgSO_4+H_2\left(x\right)\)
\(n_{Na}=\frac{1,15}{23}=0,05\)
\(\Rightarrow m_{H_2}=0,025.2=0,05\)
Khối lượng cân chứa HCl tăng thêm là: \(1,15-0,05=1,1\)
Gọi số mol Mg cần thêm vào để cân thăng bằng là x thì ta có
\(24x-2x=1.1\)
\(\Leftrightarrow x=0,05\)
\(\Rightarrow m_{Mg}=0,05.24=1,2\)
a, Viết các pt hóa học xảy ra và tính kl mỗi chất trong hỗn hợp
b, Tính thành phần % theo kl của mỗi hợp chất trong hỗn hợp
Câu trả lời của bạn
a. PTHH (1) Ca+H2O->CaO+H2\(\uparrow\)
mol 1 1 1 1
(2) CaO+H2O->Ca(OH)2
mol 1 1 1
n\(_{H^{ }_2}\)=\(\frac{3,36}{22,4}\)=0,15 mol
Theo phương trình ta có: n\(_{Ca}\)=n\(_{H_2}\)=0,15 mol
=>m\(_{Ca}\)=0,15x40=6 g
=>m\(_{CaO}\)=17,2-6=11,2 g
b. %m\(_{Ca}\)=\(\frac{m_{Ca}}{m_{hh}}\)x100%=\(\frac{6}{17,2}\)x100%=34,88%
=>%m\(_{CaO}\)=100%-34,88%=65,12%
a) Hỏi X là nguyên tố hóa học nào ?
b) Hãy viết các phương trình hóa học giải thích hiện tượng xảy ra.
Câu trả lời của bạn
a) Gọi hóa trị của X là a
Ta có PTHH:
4X + aO2 \(\rightarrow\) X2Oa
dẫn toàn bộ lượng sản phẩm X2Oa vào nước vôi trong thấy nước vôi trong bị vẩn đục và nặng thêm 4,4g nên : mX2Oa = 4.4 (g)
Theo ĐLBTKL có : mX + mO2 = mX2Oa
=> 1.2 + mO2 = 4.4
=> mO2 = 4.4 -1.2 =3.2(g)
=> nO2 = m/M = 3.2/32 = 0.1(mol)
Theo PT => nX = 4/a . nO2 = 4/a x 0.1 = 0.4/a (mol)
=> MX = m/n = 1.2 : 0.4/a =3a (g)
LẬp bảng thay hóa trị a lần lượt là I ; II ; III;- ta thấy chỉ có MX = 12 là phù hợp
=> X là nguyên tố Cacbon
- Khí A có tỉ khối đối với không khí là 0,552.
- Thành phần theo khối lượng của khí A là: 75% C và 25% H. các thể tích đều đo ở đktc.
Câu trả lời của bạn
Do khí A có tỉ khối đối với không khí là 0,552
=> MA = 0,552 x 29 = 16 (g/mol)
Đặt CTHH của A là CxHy
=> mC = \(\frac{16\times75}{100}=12\left(gam\right)\)
=> nC = \(\frac{12}{12}=1\left(mol\right)\)
=> mH = 16 - 12 = 4 (gam)
=> nH = \(\frac{4}{1}=4\left(mol\right)\)
=> x : y = 1 : 4
=> CTHH của A: CH4
PTHH: CH4 + 2O2 =(nhiệt)=> CO2 + 2H2O
Ta có: nCH4 = \(\frac{2,24}{22,4}=0,1\left(mol\right)\)
=> nO2 = 0,2 (mol)
=> VO2(đktc) = 0,2 x 22,4 = 4,48 (l)
Câu trả lời của bạn
PTHH:
2Al + 6HCl ===> 2AlCl3 + 3H2
a=========--1,5a
Zn + 2HCl ===> ZnCl2 + H2
a=========-a
Đặt số mol Al, Zn là a (mol)
Lập các số mol theo phương trình, ta có:
nH2 = 1,5a + a = \(\frac{17,92}{22,4}=0,8\left(mol\right)\)
Giải phương trình, ta được a = 0,32 (mol)
=> m = mAl + mZn = 27 x 0,32 + 65 x 0,32 = 29,44 (gam)
Câu trả lời của bạn
S => SO2 => SO3 => H2SO4 => FeSO4
S + O2 => SO2
2SO2 + O2 => SO3
SO3 + H2O => H2SO4
H2SO4 + FeO => FeSO4 + H2O
Câu trả lời của bạn
Ta co pthh
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
Theo de bai ta co
nH2=\(\dfrac{5,6}{22,4}=0,25mol\)
Theo pthh
nZn=nH2=0,25 mol
\(\Rightarrow mZn=0,25.65=16,25g\)
Vay khoi luong kem can dung la 16,25 g
a/ 46,5g photpho
b/ 67,5g nhôm
c/ 30g cacbon
d/ 33,6 l khí hidro
Câu trả lời của bạn
PTHH: 4P + 5O2 -to> 2P2O5 (1)
4Al + 3O2 -to> 2Al2O3 (2)
C+ O2 -to> CO2 (3)
2H2 + O2 -to> 2H2O (4)
- Phương trình 1:
Ta có:
\(n_P=\frac{46,5}{31}=1,5\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{O_2}=\frac{5.1,5}{4}=1,875\left(mol\right)\\ =>V_{O_2\left(đktc\right)}=1,875.22,4=42\left(l\right)\\ m_{O_2}=1,875.32=60\left(g\right)\)
- Phương trình 2:
Ta có:
\(n_{Al}=\frac{67,5}{27}=2,5\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{O_2}=\frac{3.2,5}{4}=1,875\left(mol\right)\\ =>V_{O_2\left(đktc\right)}=1,875.22,4=42\left(l\right)\\ m_{O_2}=1,875.32=60\left(g\right)\)
- Phương trình 3:
Ta có:
\(n_C=\frac{30}{12}=2,5\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{O_2}=n_C=2,5\left(mol\right)\\ =>V_{O_2\left(đktc\right)}=2,5.22,4=56\left(l\right)\\ m_{O_2}=2,5.32=80\left(g\right)\)
- Phương trình 4:
Ta có:
\(n_{H_2}=\frac{33,6}{22,4}=1,5\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{O_2}=\frac{1,5}{2}=0,75\left(mol\right)\)
\(=>V_{O_2\left(đktc\right)}=0,75.22,4=16,8\left(l\right)\\ m_{O_2}=0,75.32=24\left(g\right)\)
Câu trả lời của bạn
- Trích mẫu thử, đánh số thứ tự
- Cho các mẫu thử trên vào nước, nếu chất rắn nào không tan là Fe2O3 , còn lại tan tạo thành 3 dung dịch.
PTHH: Na2O + H2O ===> 2NaOH
CaO + H2O ==> Ca(OH)2
P2O5 + 3H2O ===> 2H3PO4
- Nhỏ 3 dung dịch thu được vào mẩu giấy quì tím:
+) Nếu quì tím chuyển đỏ thì dung dịch đó là H3PO4 => Chất ban đầu là P2O5
+) Nếu quì tím chuyển xanh là NaOH và Ca(OH)2
- Sục CO2 vào 2 dung dịch còn lại, nếu dung dịch nào xuất hiện kết tủa thì dung dịch đó là Ca(OH)2 => Chất ban đầu là CaO
- Còn lại là Na2O
Câu trả lời của bạn
Hỗn hợp chất rắn còn lại 33g
=> \(m_{O_2}=45-33=12g\)
\(n_{O_2}=\frac{12}{32}=0,375mol\)
\(V_{O_2}=0,375.22,4=8,4l\)
a/ Tính thể tích không khí đủ để đốt cháy hết 6 l hỗn hợp A, biết rằng khí oxi chiếm 1/5 thể tích không khí.
b/ Dẫn toàn bộ sản phẩm cháy vào nước vôi trong dư xảy ra phản ứng tạo thành chất không tan là Canxi cacbonat theo phản ứng: CO2 + Ca(OH)2 -> CaCO3 + H2O. Tính khối lượng chất không tan thu được. (Thể tích các khí được đo ở điều kiện thường).
Câu trả lời của bạn
a) Tỉ lệ về số mol là tỉ lệ về thể tích, đặt V meetan là a, V Butan là b, ta có:
a+b=6(l)
a/b=2/3
=> a=2,4;b=3,6 (bài này toán lớp 5 mà, tự giải, tổng và tỉ í)
PT: \(CH_4+2O_2=t^o=>CO_2+2H_2O\)(1)
\(2C_4H_{10}+13O_2=>8CO_2+10H_2O\)(2)
\(n_{CH_4}=\frac{2,4}{22,4}=\frac{3}{28}mol\)
\(n_{O_2}=2.n_{CH_4}=2.\left(\frac{3}{28}\right)=\frac{3}{14}mol\)
\(V_{O_2}=\frac{3}{14}.22,4=4,8l\)
\(n_{C_4H_{10}}=\frac{3,6}{22,4}=\frac{9}{56}mol\)
\(n_{O_2}=\frac{13}{2}.\left(n_{C_4H_{10}}\right)=\frac{13}{2}.\left(\frac{9}{56}\right)=\frac{117}{112}mol\)
\(V_{O_2}=\frac{117}{112}.22,4=23,4l\)
VKK cần dùng: \(\left(23,4+4,8\right).5=141l\)

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *