Nội dung Bài luyện tập 4 củng cố lại các khái niệm: mol, khối lượng mol, thể tích mol chất khí, tỉ khối của chất khí... Tổng kết lại mối quan hệ giữa khối lượng chất, thể tích khí; Vận dụng kiến thức giải bài tập và hiểu các hiện tượng trong thực tế.
| Các cụm từ sau có nghĩa thế nào ? | Ý nghĩa |
| 1 mol nguyên tử Cu | 1N nguyên tử Cu hay 6.1023 nguyên tử Cu |
| 1,5 mol nguyên tử H | 1,5 N nguyên tử H hay 1,5.6.1023 nguyên tử H (9.1023) |
| 2 mol phân tử H2 | 2N phân tử H2 hay 2.6.1023 phân tử H2 (12.1023) |
| 0,15 mol phân tử H2O | 0,15N phân tử H2O hay 0,15.6.1023 phân tử H2O (0,9.1023) |
| Các câu sau có nghĩa thế nào ? | Ý nghĩa |
| Khối lượng mol của nước là 18 g/mol | Khối lượng N phân tử nước là 18 g. Kí hiệu là \({M_{{H_2}O}}\) = 18g/mol |
| Khối lượng mol nguyên tử H là 1g/mol | Khối lượng N nguyên tử H là 1 g. Kí hiệu là MH = 1g/mol |
| Khối lượng mol phân tử H2 là 2 g/mol | Khối lượng N phân tử hiđro là 2 g. Kí hiệu là \({M_{{H_2}}}\) = 2g/mol |
| Ở cùng điều kiện nhiệt độ và áp suất thể tích mol của khí CO2, O2, H2. | \({V_{C{O_2}}} = {V_{{O_2}}} = {V_{{H_2}}}\) |
| Ở ( đktc) Thể tích mol các chất khí CO2, O2, H2 | \({V_{C{O_2}}} = {V_{{O_2}}} = {V_{{H_2}}} = 22,4(lit)\) |
| Thể tích mol của những chất khí khác nhau, ở cùng điều kiện nhiệt độ và áp suất. | Bằng nhau |
| Thể tích mol của những chất khí khác nhau, ở cùng điều kiện nhiệt độ 0oC và áp suất 1 atm. | Bằng nhau và bằng 22,4 lit |
Hình 1: Sự chuyển đổi giữa lượng chất (số mol) - khối lượng chất - thể tích chất khí (đktc)
| Tỉ khối của khí A đối với khí B ( dA/B = 1,5) | Khí A nặng hơn khí B 1,5 lần |
| Tỉ khối của khí CO2 đối với không khí bằng 1,52 | khí CO2 nặng hơn không khí 1,52 lần. |
Trong phòng thí nghiệm, người ta cho 4,6 gam Natri (Na) phản ứng với khí clo (Cl2) sau phản ứng thu được muối Natri clorua (NaCl)
2Na + Cl2 2NaCl
a, Tính thể tích khí clo (ở đktc) cần dùng để phản ứng hết số Natri trên?
b, Tính khối lượng muối Natriclorua tạo thành?
c, Khí clo nặng hay nhẹ hơn không khí bao nhiêu lần?
a) Số mol Natri tham gia phản ứng là:
\({n_{Na}} = \frac{{{m_{Na}}}}{M} = \frac{{4,6}}{{23}} = 0,2(mol)\)
Phương trình phản ứng:
2Na + Cl2 2NaCl
2 mol 1 mol 2 mol
0,2 mol → ? mol ? mol
Số mol clo dùng để phản ứng hết lượng Natri là:
\({n_{C{l_2}}} = \frac{{0,2 \times 1}}{2} = 0,1(mol)\)
Thể tích khí Clo cần dùng là:
\({V_{C{l_2}}} = {n_{C{l_2}}} \times 22,4 = 0,1 \times 22,4 = 2,24(lit)\)
b) Số mol muối Natri tạo thành là: 0,2 mol
Khối lượng muối Natri tạo thành là:
\({{\rm{m}}_{{\rm{Na}}}}{\rm{ = }}{{\rm{n}}_{{\rm{Na}}}}{\rm{.M = 0,2}}{\rm{.23 = 4,6(g)}}\)
c) Khí Clo nặng hơn không khí số lần là:
\({d_{C{l_2}/KK}} = \frac{{{M_{C{l_2}}}}}{{29}} = \frac{{35,5 \times 2}}{{29}} \approx 2,45\)
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 23có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Khí X có tỷ khối so với không khí gần bằng 0,97; X là khí nào trong các chất sau:
Có điểm nào chung cho các lượng chất sau: 9,8 g H2SO4; 4g NaOH; 8g CuO
Cho các chất : FeS, FeS2 , FeO, Fe2O3 . Chất có hàm lượng sắt lớn nhất là :
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 23.
Bài tập 1 trang 79 SGK Hóa học 8
Bài tập 2 trang 79 SGK Hóa học 8
Bài tập 3 trang 79 SGK Hóa học 8
Bài tập 4 trang 79 SGK Hóa học 8
Bài tập 5 trang 79 SGK Hóa học 8
Bài tập 23.1 trang 30 SBT Hóa học 8
Bài tập 23.2 trang 30 SBT Hóa học 8
Bài tập 23.3 trang 31 SBT Hóa học 8
Bài tập 23.4 trang 31 SBT Hóa học 8
Bài tập 23.5 trang 31 SBT Hóa học 8
Bài tập 23.6 trang 31 SBT Hóa học 8
Bài tập 23.7 trang 31 SBT Hóa học 8
Bài tập 23.8 trang 31 SBT Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Khí X có tỷ khối so với không khí gần bằng 0,97; X là khí nào trong các chất sau:
Có điểm nào chung cho các lượng chất sau: 9,8 g H2SO4; 4g NaOH; 8g CuO
Cho các chất : FeS, FeS2 , FeO, Fe2O3 . Chất có hàm lượng sắt lớn nhất là :
Cho các chất Cu2S, CuS, CuO, Cu2O. Hai chất có khối lượng phần trăm Cu bằng nhau là:
Số mol của 16 g CuSO4 là:
Thể tích ở (đktc) của 1,5 mol khí CO2 là:
Thành phần phần trăm của oxy trong hợp chất SO2 là:
Cho 2,7 g nhôm tác dụng với 6,4 g O2 . Hỏi sau phản ứng thu được những chất nào, biết rằng hóa trị cao nhất của nhôm trong hợp chất là III
Cho 1,6 g S cháy trong không khí thấy có khí có khả năng làm mất màu cánh hoa hồng. Tính thể tích khí đó
Tính %mMg trong 1 mol MgSO4
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi?
Hãy tìm công thức hóa học của một hợp chất có thành phần theo khối lượng là 36,8% Fe; 21,0% S; 42,2% O. Biết khối lượng mol của hợp chất bằng 152 g/mol?
Một hợp chất có công thức hóa học là K2CO3. Em hãy cho biết:
a) Khối lượng mol của chất đã cho.
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất.
Có phương trình hóa học sau:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
a) Tính khối lượng canxi clorua thu được khi cho 10 g canxi cacbonat tác dụng với axit clohiđric dư.
b) Tính thể tích khí cacbonic thu được trong phòng thí nghiệm, nếu có 5 g canxi cacbonat tác dụng hết với axit. Biết 1 mol khí ở điều kiện phòng có thể tích là 24 lít.
Khí metan CH4 có trong khí tự nhiên hoặc trong khí bioga. Khí metan cháy trong không khí sinh ra khí cacbon đioxit và nước:
CH4 + 2O2 → CO2 + 2H2O
a) Tính thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2lít khí metan. Các thể tích khí đo cùng điều kiện t0 và p
b) Tính thể tích khí CO2 (đktc) thu được sau khi đốt cháy hoàn toàn 0,15 mol khí metan.
c) Khí metan nặng hay nhẹ hơn không khí bằng bao nhiêu lần?
Hãy điền những chữ và số thích hợp vào chỗ trống trong các câu sau:
a) Một mol nguyên tử Cu có khối lượng ……g và một mol nguyên tử lưu huỳnh có khối lượng …….g kết hợp với nhau tạo thành một …… CuS có khối lượng …..g.
b) ……g chì kết hợp với …..g oxi tạo ra một mol phân tử Pb3O4 có khối lượng …g.
c) Trong 342g đường C12H22O11 có ……mol …..C, ……mol …… H và …………… mol ………O. Khối lượng của …………C là …………g, khối lượng của ………H là ………g, khối lượng của ………O là …………… g.
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng:
- Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl.
- Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O.
- Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O.
- Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O.
- Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
Nung hợp chất canxi cacbonat trong một chén nung, người ta thu được vôi sống có công thức hóa học là CaO và khí thoát ra là CO2. Kết quả của thí nghiệm được ghi lại như sau:
- Khối lượng của chén nung rỗng là 30g.
- Khối lượng của chén nung và canxi cacbonat là 40g.
- Khối lượng của chén nung và CaO là 35,6g.
Hãy điền vào dấu chấm trong những câu sau:
+ Khối lượng của CaO có trong chén sau khi nung là ….g.
+ Số mol của CaO là …
+ Khối lượng khí CO2 thoát ra sau phản ứng là ….g.
+ Số mol của CO2 là …..
+ Phân tử canxi cacbonat bị phân tử thành CaO và CO2, có tỉ lệ số phân tử CaO/ số phân tử CO2 là …
Đốt cháy hoàn toàn cacbon bằng một lượng khí oxi dư, người ta thu được hỗn hợp khí gồm có khí cacbonic (CO2) và khí oxi (O2) dư.
Hãy xác định phần trăm theo khối lượng và thành phần phần trăm theo thể tích của khí oxi trong mỗi hỗn hợp sau:
a) 4g khí cacbonic và 16g khí oxi.
b) 3 mol khí cacbonic và 5 mol khí oxi.
c) 0,3.1023 phân tử CO2 và 0,9.1023 phân tử O2.
Hãy xác định khối lượng và thể tích của những hỗn hợp khí sau ở đktc:
a) 1,5N phân tử oxi + 2,5N phân tử hidro + 0,02N phân tử nito.
b) 1,5 mol phân tử oxi + 1,2 mol phân tử CO2 + 3 mol phân tử nito.
c) 6g hidro + 2,2g khí cacbonic + 1,6g khí oxi.
Đốt cháy hoàn toàn 2,24g Fe, thu được 3,2g oxit sắt. Xác định công thức phân tử của oxit sắt.
Cho dòng khí CO qua hỗn hợp 2 oxit CuO và Fe3O4 nung nóng thu được 29,6g hỗn hợp 2 kim loại trong đó sắt nhiều hơn đồng là 4g.
Tính thể tích khí CO cần dùng (đktc).
Cho 20g một oxit sắt phản ứng hết với dung dịch HCl dư, sau phản ứng thu được 40,625g muối clorua. Xác định công thức phân tử của oxit sắt.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Hợp chất A tạo bởi hidro và nhóm nguyên tử XOy hóa trị 3. Biết rằng phân tử A nặng bằng phân tử khối của H2SO4 và tỉ lệ % khối lượng ôxi trong A là 65,30%.
a)Xác định chỉ số của y Và nguyên tử khối của nguyên tố X
b) viết tên , kí hiệu hóa học X và công thức hóa học A
Câu trả lời của bạn
gọi CTTQ của h/c A là: H3XOy
ta có M A = M H2SO4= 98(g)
khối lượng oxi trong hợp chất A là:
m O2= \(\dfrac{\%O_2.M_A}{100\%}=\dfrac{65,30\%.98}{100\%}\approx64\left(g\right)\)
y= nO2 = \(\dfrac{64}{16}=4\cdot\left(mol\right)\)
nguyên tử khối của X là:
m X = M A- mO2- mH3= 98-64-3=31(g)
vậy X là photpho kí hiệu: P
CTHH : H3PO4
Dùng khí hiđro dư để khử x gam sắt(III) oxit, sau phản ứng người ta thu được y gam sắt kim loại. Nếu dùng lượng sắt này cho phản ứng hoàn toàn với axit clohiđric có dư thì thu được 5,6 lít khí hiđro đo ở điều kiện tiêu chuẩn.
a) Viết các phương trình phản ứng hóa học.
b) Hãy xác định giá trị x, y và lượng muối sắt(II) clorua tạo thành sau phản ứng.
giúp mìh với hix
Câu trả lời của bạn

Làm đc bài nào thì làm nha!
B1: Cho 30,6g 1 oxit kim loại tác dụng vs H2O sinh ra 34,2g 1 hidroxit(OH) kim loại tương ứng. Xác định công thức hóa học của kim loại.
B2: Cho 6,2g oxit kim loại tác dụng vs H2O sinh ra 8g 1 hidroxit(OH) kim loại tương ứng. Xác định công thức hóa học của oxit kim loại.
B3: Cho 5,4g 1 kim loại tác dụng vs Axit clohidric sinh ra 6,72 lít khí H2 ở đktc và muối clorua. Xác định tên kim loại.
B4: Cho 15,6g 1 kim loại phản ứng hoàn toàn vs O2 sinh ra 18,8g 1 oxit tương ứng. Xác định tên kim loại.
Câu trả lời của bạn
Gọi oxit kim loại cần tìm là M2Ox
\(n_{M_2O_n}=\dfrac{30,6}{2M+x.16}\); \(n_{M\left(OH\right)_x}=\dfrac{34,2}{M+17x}\)
PTHH: \(M_2O_x+xH_2O\rightarrow2M\left(OH\right)_x\)
TheoPT: 1 mol n mol 2 mol
Theo ĐB: \(n_{M_2O_x}\) \(n_{M\left(OH\right)_x}\)
Theo PTHH: \(n_{M_2O_x}=\dfrac{n_{M\left(OH\right)_x}}{2}\)
\(\Leftrightarrow\dfrac{30,6}{2M+16x}=\dfrac{34,2}{M+17x}.\dfrac{1}{2}\)
\(\Leftrightarrow30,6.2.\left(M+17x\right)=34,2.\left(2M+16x\right)\)
\(\Leftrightarrow61,2M+1040,4x=68,4M+547,2x\)
\(\Leftrightarrow7,2M=493,2x\)
\(\Leftrightarrow M=68,5x\)
x là hóa trị của
Lập bảng biện luận:
| x | 1 | 2 | 3 |
| M | 68,5 | 137 | 205,5 |
| Kết luận | loại | chọn | loại |
Vậy M là Bari ( Ba)
=> CTHH của Ba là BaO
bài 1: Phân hủy a gam nước thì thu được 0,672 lít hỗn hợp gồm khí oxi và khí Hiđrô (đo ở đktc). Hãy tính a ??
Bài 2: Một hợp chất có khối lượng mol phân tử là 80g có thành phần gồm 80% Cu và 20% O về khối lượng :
a) Lập công thức hóa học của hợp chất ?
b) Cho 16g hợp chất tác dụng hết với axit Clohiđric (HCl). Hãy tính số gam axit cần dùng ( biết sản phẩm của phàn ứng là muối Đồng (II) Clorua(CuCl2) và nước)
GIÚP MK VS MAI MK NỘP RỒIIIIII![]()
Câu trả lời của bạn
Bai 2 :
a) Dat CTHHTQ cua h/c la CuxOy
Theo de bai ta co :
%mCu = 80% => mCu = 64(g) => nCu = 1(mol)
%mO = 20% => mO = 16(g) => nO = 1 (mol)
=> \(\dfrac{x}{y}=\dfrac{nCu}{nO}=\dfrac{1}{1}=>x=1;y=1\)
Vay CTHH la CuO
b)
Theo de bai ta cos : nCuO = 16/80 =0,2(mol)
Ta co PTHH :
\(CuO+2HCl->CuCl2+H2O\)
0,2mol.....0,4mol
=>mHCl(can dung) = 0,4.36,5 = 14,6(g)
Cho 1 hợp chất có công thức hóa học dưới dạng R2OS ,phân tử khối cuarhowpj chất bằng 1/2 đvc trong đó nguyên tố Oxi chiếm 47,06% về khối lượng
a)Xác định tên nguyên tố R
b)viết công thức hóa học của hợp chất
Câu trả lời của bạn
CHÚC BẠN HỌC TỐT!!![]()
![]() (theo mình thì ct có dạng R2Ox)
(theo mình thì ct có dạng R2Ox)
Theo đề bài, ta có: \(\%O=47,06\%\Rightarrow\%R=52,94\%\)
\(\Rightarrow\left\{{}\begin{matrix}\%O=\dfrac{16x}{2R+16x}.100\%=47,06\%\\\%R=\dfrac{2R}{2R+16x}.100\%=52,94\%\end{matrix}\right.\)
\(\Rightarrow\dfrac{\%R}{\%O}=\dfrac{\dfrac{2R}{2R+16x}}{\dfrac{16x}{2R+16x}}=\dfrac{52,94\%}{47,06\%}\)
\(\Rightarrow\dfrac{2R}{16x}=\dfrac{52,94\%}{47,06\%}\)
\(\Rightarrow\dfrac{R}{x}\approx9\)
+) Chọn \(x=1\Rightarrow R=9\) (Loại)
+) Chọn \(x=2\Rightarrow R=18\) (Loại)
+) Chọn \(x=3\Rightarrow R=27\) (Chọn)
+) Chọn \(x=4\Rightarrow R=36\) (Loại)
a) R là Nhôm(Al)
b) CTHH của hợp chất là: Al2S3
Vậy............
chờ 2,8kg bột sắt tác dụng dung dịch HCl 2M.tính:
a)thể tích dung dịch HCl đã dùng
b)tinh the tich khi H2 thoat ra
c)tinh nong do Cm dung dịch sau phản ứng (biết v dung dịch không thay đổi)
Câu trả lời của bạn
a) Ta có: nFe= 2800/56=50(mol)
PTHH: Fe+ 2HCl -> FeCl2 + H2
=> nHCl= 2.50= 100(mol)
=> VddHCl= 100/2= 50(l)
b) nH2=nFeCl2 = nFe= 50(mol)
=> VH2(đktc)= 50.22,4= 1120(l)
c) - Chất có trong dd sau khi phản ứng kết thúc là FeCl2
Vì Vdd sau phản ứng ko thay đổi nên:
Vdd sau = Vdd trc= 50(l)
=> CM(ddsau)= 50/50=1 (M)
Cho 3,2 g lưu huỳnh cháy trong không khí thu được khí sunfuro ( lưu huỳnh dioxit).
a) Viết phương trình phản ứng xảy ra
b) Tính khối lượng lưu huỳnh dioxit tạo thành
c) Tính thể tích không khí cần dùng , biết thể tích không khí bằng 5 lần thể tích khí oxi
Ai giúp với ạ
Câu trả lời của bạn
ta có nS= \(\dfrac{3,2}{32}\)= 0,1( mol)
PTPU
S+ O2\(\xrightarrow[]{to}\) SO2
0,1.............0,1...
=> mSO2= 0,1. 64= 6,4(g)
theo PTPU ta có nO2= nS= 0,1( mol)
=> VO2= 0,1. 22,4= 2,24( lít)
\(\Rightarrow\) Vkk= 2,24. 5= 11,2( lít)
Cho 6, 5 g Zn tác dụng vừa đủ với V lít HCL 1 Md bằng 1, 1 gam /ml
a) tính V
B) Tính C% dd thu được sau phản ứng.
Câu trả lời của bạn
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1.......0,2..............0,1.........0,1
a, \(V=n_{HCl}.M=0,2.1=0,2\left(l\right)\)
b, \(m_{dd}=20.1,1=22\left(g\right)\)
\(m_{ZnCl_2}=136.0,1=13,6\left(g\right)\)
\(m_{H_2}=2.0,1=0,2\left(g\right)\)
=>\(m_{dd_{sau}}=m_{dd}+m_{Zn}-m_{H_2}=22+6,5-0,2=28,3\left(g\right)\)
\(C\%=\dfrac{13,6}{28,3}.100\%=48\%\)
P/S: chả bt đúng sai
Câu 2:Cho kim loại sắt tác dụng vừa đủ với dung dịch axit sunfuric loãng có nồng độ 24,5% thu được 11,2 lít khí hiđro(đo ở đktc)
a)Viết PTHH xảy ra?
b)Tính khối lượng kim loại sắt đã phản ứng?
c)Tính khối lượng dung dịch axit sunfuric 24,5% đã tham gai phản ứng?
d)Tính nồng độ % của dung dịch muối thu được sau phản ứng?
help me pls!!!!
Câu trả lời của bạn
\(Fe+2HCl-->FeCl_2+H_2\)
0,5 1 0,5 0,5
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) =>\(m_{H_2}=0,5.2=1\left(g\right)\)
b)=> \(m_{Fe}=0,5.56=28\left(g\right)\)
c)=>\(m_{HCl}=1.36,5=36,5\left(g\right)\) =>\(m_{d^2HCl}=\dfrac{36,5.100}{24,5}=148,98\left(g\right)\)
d)=>\(m_{d^2sau}=28+148,98-1=175,98\left(g\right)\)
=>\(m_{FeCl_2}=0,5.127=63,5\left(g\right)\)
=>\(C\%_{muối}=\dfrac{63,5}{175,98}.100=36,1\left(g\right)\)
Đốt cháy hoàn toàn hỗn hợp bột Al và Fe trong đó Al có khối lượng là 4,8gam cần dùng hết 6,72 lít khí oxit đktc tính khối lượng ban đầu
Câu trả lời của bạn
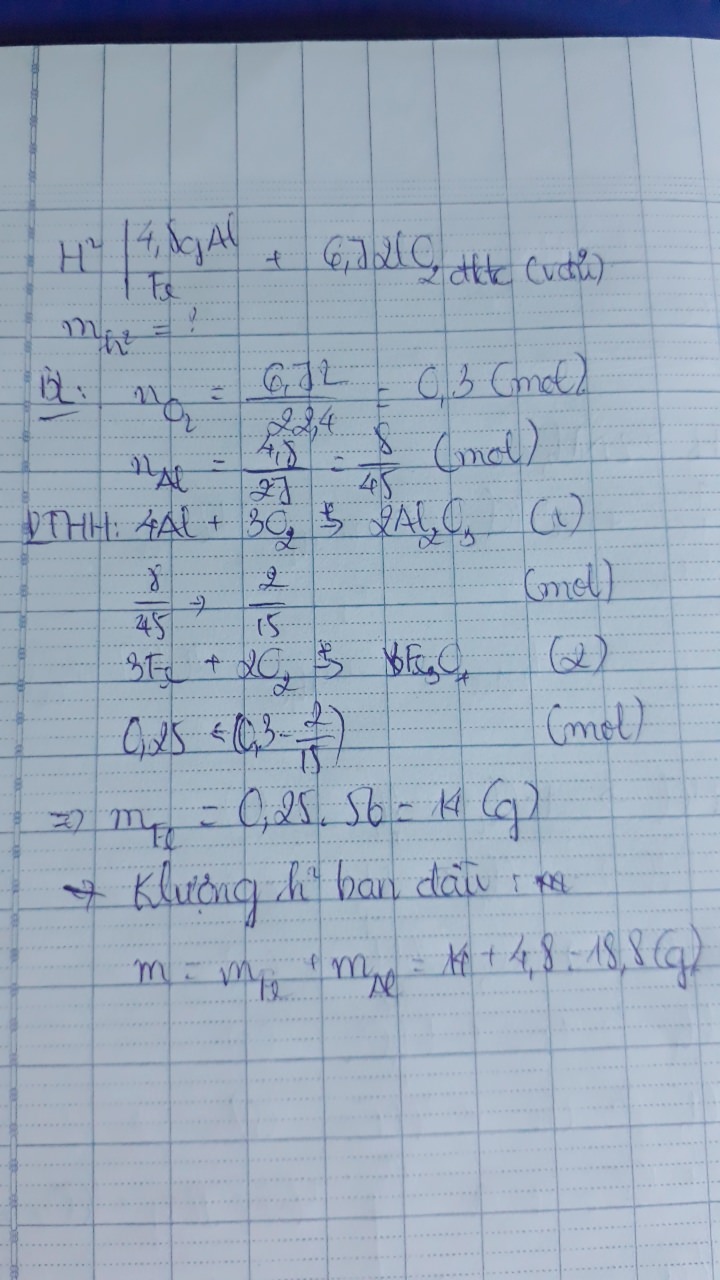
câu 1: Hòa tan hoàn toàn 4,8 gam Magie bằng lượng vừa đủ dung dịch HCl 2M.Sau phản ứng thu đượ dung dịch A và khí B
a)Viết PTHH xảy ra?xác định công thức chất tan trong dung dịch A và khí B?
b)Tính thể tích khí B bay ra ở đktc?
c)Tính thể tích dung dịch HCl 2M đã tham gia phản ứng?
d)Tính nồng độ mol/l của dung dịch A thu được sau phản ứng?
help me help me pls!!!!
Câu trả lời của bạn
+ n Mg = 4,8/24 = 0,2 mol
Gọi Vdd HCl 2M là x ( lít)
-> nHCl (dd đầu) = 2x (mol)
PT
Mg + 2HCl -> MgCl2 + H2
0,2___0,4____0,2_____0,2 (mol)
a, chất tan là MgCl2, khí sinh là là H2
b, V H2 = 0,2 * 22,4 = 4,48l
c, nHCl (dd đầu) = 2x = 0,4 mol
-> x = 0,4/2 = 0,2
-> V dung dịch HCl 2M là 0,2 lít
d, đề bài cho thế này khó quá, mình không tính được thể tích Mg để tính thể tích dung dịch thu được. Mình chỉ có thể giúp bạn tham khảo tới đây thôi, xin lỗi nha.
Bài 1:đốt cháy hoàn toàn 2,4 lít khí H2(đktc) trong khí oxi(O2)thu được hơi nước(H2O).
a,tính khối lượng nước thu được.
b,Tính thể tích khí oxi(đktc) đã phản ứng.
Bài 2:Hòa tan hoàn toàn 1,2 gam magie trong dung dịch axit clohidric HCl thu được muối magie clorua MgCl2 và khí hidro H2.
a,tính thể tích khí hidro thu được ở đktc.
b,tính khối lượng axit đã dùng.
c,tính khối lượng muối thu được.
Câu trả lời của bạn
Bài 1:
PTHH: 2H2 + O2 -----> 2H2O
\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{2,4}{22,4}=\dfrac{3}{28}\approx0,1\left(mol\right)\)
Thay vào PT:
2H2 + O2 ------> 2H2O
2 mol 1 mol 2 mol
0,1mol x mol y mol
=> x = 0,05 mol; y = 0,1 mol
\(\Rightarrow m_{H_2O}=n_{H_2O}\cdot M_{H_2O}=0,1\cdot18=1,8\left(g\right)\)
\(V_{O_2}=n_{O_2}\cdot22,4=0,05\cdot22,4=1,12\left(l\right)\)
Bài 2:
PTHH: Mg + 2HCl ----> MgCl2 + H2
\(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{1,2}{24}=0,05\left(mol\right)\)
Thay vào PT:
Mg + 2HCl ----> MgCl2 + H2
1mol 2 mol 1 mol 1 mol
0,05mol x mol y mol z mol
=> x = 0,1 mol; y = z = 0,05 mol
a, \(V_{H_2}=n_{H_2}\cdot22,4=0,05\cdot22,4=1,12\left(l\right)\)
b,
\(m_{HCl}=n_{HCl}\cdot M_{HCl}=0,1\cdot37,5=3,75\left(g\right)\)
c,
\(m_{MgCl_2}=n_{MgCl_2}\cdot M_{MgCl_2}=0,05\cdot95=4,75\left(g\right)\)
Bài 5: cho 2,7 gam kim loại nhôm tác dụng hết với 300 ml dung dịch HCl dư ?
a) Viết phương trình hoá học của phản ứng xảy ra
b) Tính thể tích khí Hiđrô sinh ra (đktc)
c) Tính khối lượng muốn clorua tạo thành?
d) Tính nồng độ MOL của dung dịch axit đã dùng ?
Câu trả lời của bạn
nAl = 0,1 mol
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
0,1......0,3.............0,1.......0,15
\(\Rightarrow\) VH2 = 0,15.22,4 = 3,36 (l)
\(\Rightarrow\) mAlCl3 = 0,1.133,5 = 13,35 (g)
\(\Rightarrow\) CM HCl = \(\dfrac{0,3}{0,3}\) = 1 (M)
cho 9g hỗn hợp gồm Al và Mg tác dụng với HCl thấy thóat ra 10.08 lít H2 (dktc) tính % khối lượng mỗi kim loại trong hỗn hợp
Câu trả lời của bạn
Al + 3HCl -> AlCl3 + \(\dfrac{3}{2}\)H2
Mg + 2HCl -> MgCl2 + H2
Gọi x,y là mol Al, Mg
=> \(\left\{{}\begin{matrix}27x+24y=9\\\dfrac{3}{2}x+y=\dfrac{10,08}{22,4}\end{matrix}\right.\)=> \(\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)=> \(\left\{{}\begin{matrix}\%mAl=\dfrac{0,2.27}{9}=60\%\\\%mMg=100\%-60\%=40\%\end{matrix}\right.\)
Dẫn 6,72 l khí H2 đi qua 20 g hỗn hợp gồm CuO và Fe2O3 thì phản ứng xảy ra vừa đủ. Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp.
Câu trả lời của bạn
Giải:
Số mol H2 là:
nH2 = V/22,4 = 6,72/22,4 = 0,3 (mol)
PTHH: CuO + H2 -> Cu + H2O
----------x------x-------x------x--
PTHH: Fe2O3 + 3H2 -> 2Fe + 3H2O
------------y--------3y-----2y-----3y--
Gọi nCuO = x (mol) và nFe2O3 = y (mol)
Ta có hpt:
\(\left\{{}\begin{matrix}mCuO+mFe2O3=20\left(g\right)\\nH2=0,3\left(mol\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}80x+160y=20\left(g\right)\\x+3y=0,3\left(mol\right)\end{matrix}\right.\)
Giải hpt, được:
\(\left\{{}\begin{matrix}x=0,15\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
Phần trăm khối lượng mỗi kim loại:
%mCuO = (mct/mhh).100 = (0,15.80/20).100 = 60 %
=> %mFe2O3 = 100 - 60 = 40 %
Vậy ...
Cho 2,4g Mg tác dụng vừa đủ vs m(gam) dd HCl 20%
a) tính thể tích khí thu đc ở đktc
b) tính khối lượng m(gam) dd HCl tham gia pu
c) tính nồng độ phần trăm dd sau phản ứng (cho Mg= 24, H=1,Cl= 35.5)
Câu trả lời của bạn
nMg = \(\dfrac{2,4}{24}=0,1\) mol
Pt: Mg + .....2HCl --> MgCl2 + H2
0,1 mol-> 0,2 mol-> 0,1 mol-> 0,1 mol
VH2 = 0,1 . 22,4 = 2,24 (lít)
mdd HCl pứ = \(\dfrac{0,2\times36,5\times100}{20}=36,5\left(g\right)\)
mdd sau pứ = mMg + mdd HCl pứ - mH2 = 2,4 + 36,5 - 0,1 . 2 = 38,7 (g)
C% dd MgCl2 = \(\dfrac{0,1\times95}{38,7}.100\%=24,55\%\)
nung 73,5g KClO3 ở nhiệt độ cao thu được KCl và khí O2, sau 1 thời gian phản ứng thấy chất rắn thu được có khối lượng là 51,9g. Thể tích của khí oxi thu đc ở đktc là?
Câu trả lời của bạn
Giải✿ :
Số mol KClO3 tham gia phản ứng : nKClO3=\(\dfrac{73,5}{122,5}\)=0,6 (mol)
PTHH: 2KClO3→2KCl+3O2
Theo phương trình ⇒Số mol của O2 là : 0,9 mol
Thể tích O2 thu được ở đktc :
VO2= 0,9.22,4=20,16(lít)
Câu 1: Cho 10g hỗn hợp Mg và Cu vào 120g dd HCl dư thấy tạo ra 5.6l khí ( đktc )
a. PTHH
b. Tính C% dd HCl tham gia phản ứng và C% dd sau phản ứng
c. Dùng lượng khí Hidro trên để khử 32g đồng (II) oxit thu được bao nhiêu g đồng?
Câu 2: Cho m(g) hỗn hợp Ca và CaO phản ứng với 100g nước thu được dd chưa 29.6g bazơ và 3.36 l khí (đktc)
a. PTHH
b. Tính % khối lượng của mỗi kim loại trong hỗn hợp ban đầu
c. Tính C% dd sau phản ứng
Câu 3
Cho 2.7 g Al vào 200 g dd H2SO4 9.8%. Tính C% dd sau phản ứng
Câu 4 Cho 12.4g Na2O vào nước thu được 100ml dd A. Tính CM dd A
Câu trả lời của bạn
Câu 1 :
gọi số mol Mg phản ứng là a, mol Cu phản ứng là b
n H2 = 5,6/22,4 = 0,25 mol
PT
Mg + 2HCl -> MgCl2 + H2
a_____2a______a_____a__ (mol)
Cu + 2HCl -> CuCl2 + H2
b____2b_____b______b__ (mol)
n H2 = a+b = 0,25 (I)
mhỗn hợp kl = 24a + 64b = 10 (II)
giải Hệ PT I,II ta được
a = 0.15
b = 0.1
-> nHCl phản ứng = 2*0,15 + 2* 0,1 = 0,5 mol
-> mHCl phản ứng = 0,5 * 36,5 = 18,25 g
-> C% HCl (dd phản ứng) = 18,25/120 *100% = 15,21%
m dung dịch sau phản ứng = 120 +10 = 130g
C% Cu (dd sau) = 64*0,1 /130 *100% = 4,92%
C% Mg (dd sau) = 24*0,15 / 130 *100% = 2,77%
hòa tan 40,5g nhôm vào 2l dung dịch H2SO4 1,5M thu được muối và khí hidro
a, viết PTHH
b, tính khối lượng chất còn dư sau pư
c, tính thể tích khí hidro thu được( đktc)
d, tính khối lượng của muối thu được( 2 cách)
Câu trả lời của bạn
nAl = 1,5 mol
nH2SO4 = 3 mol
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2
Đặt tỉ lệ ta có
\(\dfrac{1,5}{2}< \dfrac{3}{3}\)
\(\Rightarrow\) H2SO4 dư
\(\Rightarrow\) mH2SO4 dư = ( 3 - 2,25 ).98 = 73,5 (g)
\(\Rightarrow\) VH2 = 2,25.22,4 = 50.4 (l)
* Cách 1
mAl2(SO4)3 = 0,75.342 = 256,5 (g)
* Cách 2
mH2SO4 pư = 2,25.98 = 220,.5 (g)
mH2 = 2,25.2 = 4,5 (g)
Áp dụng D9LBTKL ta có
mAl2(SO4)3 = 40,5 + 220,5 - 4,5 = 256,5 (g)
Trộn \(V_1\) lít \(CH_4\),\(V_2\) lít CO, \(V_3\) lít \(H_2\) thu được hỗn hợp X .Để đốt cháy hoàn toàn 1 lít khí X cần 0,8 lít khí oxi(đktc).Tính thành phần % thể tích \(CH_4\) trong X.
Câu trả lời của bạn
20%

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *