Hôm nay DapAnHay xin gửi đến các bạn lý thuyết Bài 14: Phản ứng hóa học và Enthalpy chương trình SGK Cánh Diều lớp 10. Bài viết tổng hợp toàn bộ lý thuyết liên quan đến phản ứng hóa học và phần bài tập minh họa đi kèm đáp án chi tiết. Mong rằng đây sẽ là tài liệu giúp các bạn củng cố lại kiến thức của mình. Mời các bạn cùng theo dõi!
- Các phản ứng hoá học khi xảy ra luôn kèm theo sự giải phóng hoặc hấp thụ năng lượng. Năng lượng này gọi là năng lượng hoá học.
- Phản ứng giải phóng năng lượng dưới dạng nhiệt gọi là phản ứng toả nhiệt.
- Phản ứng hấp thụ năng lượng dưới dạng nhiệt gọi là phản ứng thu nhiệt.
- Các phản ứng kèm theo sự thay đổi năng lượng dạng nhiệt rất phổ biến trong tự nhiên phản ứng đốt cháy nhiên liệu, phản ứng tạo gỉ sắt, phản ứng oxi hoá glucose trong cơ thể,... đều là các phản ứng toả nhiệt. Các phản ứng trong lò nung vôi, nung clinker xi măng,... là các phản ứng thu nhiệt.
- Với cùng một phản ứng, ở điều kiện khác nhau về nhiệt độ, áp suất thì lượng nhiệt kèm theo cũng khác nhau. Để tiện cho việc so sánh lượng nhiệt kèm theo, người ta sử dụng điều kiện chuẩn và quy định như sau:
- Điều kiện chuẫn là điều kiện ứng với áp suất 1 bar (đối với chất khi), nồng độ 1 mol L-1 (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298K (25°C).
| - Phản ứng giải phóng năng lượng dưới dạng nhiệt gọi là phản ứng toả nhiệt, phản ứng hấp thụ năng lượng dưới dạng nhiệt gọi là phản ứng thu nhiệt. - Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (đối với chất khí), nồng độ 1 mol L-1 (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298 K (25 °C). |
|---|
a. Enthalpy tạo thành chuẩn của một chất hoá học
- Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất, kí hiệu là \({\Delta _f}H_{298}^0\), là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn.
- Khi phản ứng toả nhiệt thì \({\Delta _f}H_{298}^0\) < 0.
- Khi phản ứng thu nhiệt thì \({\Delta _f}H_{298}^0\) >0.
Ví dụ 1: Ở điều kiện chuẩn, phản ứng của 2 mol Na (thể rắn) với 1/2 mol O2 (thể khi) thu được 1 mol Na2O (thể rắn) và giải phóng 417,98 kJ nhiệt. Biết rằng, ở điều kiện chuẩn, Na thể rắn bền hơn Na ở thể lỏng và khi, oxygen dạng phân tử O2, bền hơn dạng nguyên tử O và phân tử O3 (ozone).
- Ta nói enthalpy tạo thành của Na2O rắn ở điều kiện chuẩn là -417,98 kJ mol-1. Phản ứng trên được biểu diễn như sau:
2Na(s) + 1/2O2(g) → Na2O(s)
\({\Delta _f}H_{298}^0\) = -417,98 kJ mol-1
Chú ý: Phải viết thể của các chất trong phản ứng.
Ví dụ 2: Ở điều kiện chuẩn, cần phải cung cấp 26,5 kg nhiệt lượng cho quá trình 0,5 mol H2 (g) phản ứng với 0,5 mol I2 (s) để thu được 1 mol HI (g).
- Như vậy enthalpy tạo thành chuẩn của hydrogen iodide (HI) ở thể khí là 26,5 kJ mol-1
1/2H2 (g) + 1/2I2 (s) → HI (g)
\({\Delta _f}H_{298}^0\) = 26,5 kJ mol-1
- Enthalpy tạo thành chuẩn của các đơn chất bền nhất đều bằng không.
b. Biến thiên enthalpy chuẩn của phản ứng hoá học
- Trong trường hợp chung, các chất phản ứng có thể là đơn chất, cũng có thể là hợp chất. Một cách tổng quát, nhiệt kèm theo (nhiệt lượng toả ra hay thu vào của phản ứng) gọi là biến thiên enthalpy của phản ứng.
- Biến thiên enthalpy chuẩn của một phản ứng hoá học, kí hiệu là \({\Delta _f}H_{298}^0\) chính là nhiệt (toả ra hoặc thu vào) kèm theo phản ứng đó ở điều kiện chuẩn.
- Sau đây là một số ví dụ về biến thiên enthalpy chuẩn của một phản ứng hoá học.
Ví dụ 1: Phản ứng đốt cháy methane (CH4) toả rất nhiều nhiệt: CH4 (g) + 2O2 → CO2 (g) + 2H2O (l) \({\Delta _r}H_{298}^0\) = -890,5kJ
- Như vậy, ở điều kiện chuẩn, khi đốt cháy hoàn toàn 1 mol CH4, sản phẩm là CO2 (g) và H2O (l), thì sẽ giải phóng một nhiệt lượng là 890,5 kg. Lưu ý rằng, cũng phản ứng này, nếu nước ở thể hơi thi giá trị \({\Delta _r}H_{298}^0\) sẽ khác đi. Đây là lí do cần phải ghi rõ thể của các chất khi viết các phản ứng có kèm theo giá trị \({\Delta _r}H_{298}^0\)
Ví dụ 2: Phản ứng nhiệt phân CaCO3 là phản ứng thu nhiệt: CaCO3 (s) → Cao (s) + CO2 (g)
\({\Delta _r}H_{298}^0\) = 179,2 kJ
- Để thu được 1 mol CaO (s), cần phải cung cấp 179,2 kJ nhiệt lượng để chuyển 1 mol CaCO3 (s) thành CaO (s).
Ví dụ 3: Phản ứng trung hoà giữa NaOH và HCl toả nhiệt:
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
\({\Delta _r}H_{298}^0\) = -57,9 kJ
| - Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất, kí hiệu là \({\Delta _f}H_{298}^0\) là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn. Biến thiên enthalpy chuẩn của một phản ứng hoá học, kí hiệu là \({\Delta _r}H_{298}^0\) chính là lượng nhiệt toả ra hoặc thu vào của phản ứng đó ở điều kiện chuẩn. |
|---|
Bài 1: Cho các phản ứng sau:
(1) Phản ứng nung vôi: CaCO3 → CaO + CO2
(2) Phản ứng than cháy trong không khí: C + O2 → CO2
Trong hai phản ứng trên, phản ứng nào là tỏa nhiệt, phản ứng nào là thu nhiệt?
Hướng dẫn giải
- Phản ứng giải phóng năng lượng dưới dạng nhiệt (phản ứng tỏa nhiệt): phản ứng đốt cháy nhiên liệu, phản ứng tạo gỉ sắt, phản ứng oxi hóa glucose trong cơ thể, ...
- Phản ứng hấp thụ năng lượng dưới dạng nhiệt (phản ứng thu nhiệt): phản ứng trong lò nung vôi, nung clinker xi măng, …
(1) Phản ứng thu nhiệt.
(2) Phản ứng tỏa nhiệt.
Bài 2: Hãy nêu hiện tượng của các quá trình: đốt cháy than, ethanol trong không khí. Nhiệt độ môi trường xung quanh thay đổi như thế nào?
Hướng dẫn giải
- Hiện tượng: xuất hiện khí bay ra
C + O2 \(\xrightarrow{{{t^o}}}\)CO2↑
C2H5OH + 3 O2 \(\xrightarrow{{{t^o}}}\)2CO2↑ + 3H2O
- Nhiệt độ môi trường xung quanh tăng lên
Bài 3: Biến thiên enthalpy chuẩn của một phản ứng hóa học được xác định trong điều kiện nào?
Hướng dẫn giải
- Biến thiên enthalpy chuẩn của một phản ứng hóa học được xác định ở điều kiện chuẩn
+ Áp suất 1 bar (đối với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch)
+ Nhiệt độ: 25oC (hay 298K)
Học xong bài học này, em có thể:
- Trình bày được khái niệm phản ứng toả nhiệt, thu nhiệt; điều kiện chuẩn (áp suất 1 bar và thường chọn nhiệt độ 25°C hay 298 K).
- Trình bày được khái niệm enthalpy tạo thành (nhiệt tạo thành) \({\Delta _f}H_{298}^0\) và biến thiên enthalpy (nhiệt phản ứng) \({\Delta _r}H_{298}^0\) của phản ứng hoá học.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Cánh Diều Bài 14 cực hay có đáp án và lời giải chi tiết.
Quá trình tổng hợp nước: H2 + 1/2 O2 → H2O; ΔH= -285,83KJ. Để tạo ra 9g H2O phản ứng đã thoát ra một nhiệt lượng là:
Phản ứng tạo NaCl từ Na và Cl2 có ΔH = -98,25 kcal/mol. Nếu tiến hành phản ứng giữa 46 gam Na với 71 gam Cl2 trong bình kín bằng thép, đặt chìm trong một bể chứa 10 lít nước ở 25oC thì sau phản ứng hoàn toàn nhiệt độ của nước trong bể là (biết nhiệt dung riêng của nước là 4,186 J/g.K và nhiệt lượng sinh ra truyền hết cho nước)
5,350oC
Tiến hành phản ứng phân hủy 1kg glixerol trinitrat (C3H5O9N3) thu được V lít hỗn hợp khí CO2, N2, O2 và hơi nước. Biết ở điều kiện phản ứng 1 mol khí có thể tích 50 lít. Giá trị của V là
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Cánh Diều Bài 14để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Thực hành trang 77 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi trang 78 SGK Hóa học 10 Cánh Diều - CD
Vận dụng 1 trang 78 SGK Hóa học 10 Cánh Diều - CD
Vận dụng 2 trang 78 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 1 trang 79 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 2 trang 79 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 3 trang 79 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 4 trang 79 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi trang 80 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 1 trang 80 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 2 trang 80 SGK Hóa học 10 Cánh Diều - CD
Vận dụng trang 80 SGK Hóa học 10 Cánh Diều - CD
Giải bài 1 trang 81 SGK Hóa học 10 Cánh Diều - CD
Giải bài 2 trang 81 SGK Hóa học 10 Cánh Diều - CD
Giải bài 3 trang 81 SGK Hóa học 10 Cánh Diều - CD
Giải bài 4 trang 81 SGK Hóa học 10 Cánh Diều - CD
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Quá trình tổng hợp nước: H2 + 1/2 O2 → H2O; ΔH= -285,83KJ. Để tạo ra 9g H2O phản ứng đã thoát ra một nhiệt lượng là:
Phản ứng tạo NaCl từ Na và Cl2 có ΔH = -98,25 kcal/mol. Nếu tiến hành phản ứng giữa 46 gam Na với 71 gam Cl2 trong bình kín bằng thép, đặt chìm trong một bể chứa 10 lít nước ở 25oC thì sau phản ứng hoàn toàn nhiệt độ của nước trong bể là (biết nhiệt dung riêng của nước là 4,186 J/g.K và nhiệt lượng sinh ra truyền hết cho nước)
5,350oC
Tiến hành phản ứng phân hủy 1kg glixerol trinitrat (C3H5O9N3) thu được V lít hỗn hợp khí CO2, N2, O2 và hơi nước. Biết ở điều kiện phản ứng 1 mol khí có thể tích 50 lít. Giá trị của V là
Cho Fe, FeO, Fe(OH)2, Fe(OH)3, Fe3O4, Fe2O3, Fe(NO3)2, Fe(NO3)3, FeSO4, Fe2(SO4)3, FeCl3 lần lượt phản ứng với HNO3 đặc, nóng. Số phản ứng thuộc loại phản ứng oxi hóa khử là
Cho Cu + HNO3 → Cu(NO3)2 + NO + H2O.
Sau khi cân bằng phương trình hóa học của phản ứng, tỉ lệ các hệ số của HNO3 và NO là
Phản ứng nào sau đây vừa là phản ứng hóa hợp, vừa là phản ứng oxi hóa – khử?
Phản ứng hóa học nào cho dưới đây là phản ứng hóa hợp?
Khi cho Cl2 tác dụng với dung dịch NaOH ở nhiệt độ thường, trong phàn ứng này Cl2 đóng vai trò là
Khi cho Cl2 tác dụng với dung dịch NaOH ở nhiệt độ thường, xảy ra phản ứng:
2NaOH + Cl2 → NaCl + NaClO + H2O
Trong phản ứng này Cl2 đóng vai trò là
Loại phản ứng không phải phản ứng oxi hóa – khử trong 4 phản ứng hóa học bên dưới đây?
Thực hiện hai thí nghiệm dưới đây:
Thí nghiệm 1: Đặt một nhiệt kế vào trong cốc thủy tinh chứa khoảng 50 mL dung dịch hydrochloric acid (HCl) 1M (hình 14.1). Khi nhiệt độ trong cốc ổn định, ghi nhiệt độ ban đầu. Thêm vào cốc khoảng 1 gam magnesium oxide (MgO) rồi dùng đũa thủy tinh khuấy liên tục. Quan sát hiện tượng phản ứng và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Thí nghiệm 2: Lặp lại thí nghiệm với bộ dụng cụ và cách tiến hành như trên, nhưng thay bằng khoảng 50 mL dung dịch CH3COOH 5% (giấm ăn) và khoảng 5 gam baking soda (sodium hydrogen carbonate, NaHCO3). Quan sát và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Viết phương trình hóa học xảy ra ở hai thí nghiệm trên và cho biết phản ứng nào là tỏa nhiệt, phản ứng nào là thu nhiệt.
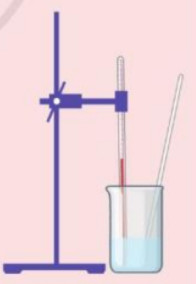
Hình 14.1. Bộ dụng cụ thí nghiệm 1,2
Khi làm thí nghiệm, làm thế nào để biết một phản ứng là tỏa nhiệt hay thu nhiệt?
Dự đoán các phản ứng sau là tỏa nhiệt hay thu nhiệt?
a) Nung NH4Cl(s) tạo ra HCl(g) và NH3(g).
b) Cồn cháy trong không khí.
c) Phản ứng thủy phân collagen thành gelatin (là một loại protein dễ tiêu hóa) diễn ra khi hầm xương động vật.
Lấy ví dụ một số phản ứng xảy ra trong tự nhiên có kèm theo sự tỏa nhiệt hoặc thu nhiệt mà em biết.
Nhiệt tỏa ra khi hình thành 1 mol Na2O(s) ở điều kiện chuẩn từ phản ứng giữa Na(s) và O3(g) có được coi là nhiệt tạo thành chuẩn của Na2O(s) không? Giả sử Na tác dụng được với O3 thu được Na2O.
Trong ví dụ 1, ở cùng điều kiện phản ứng, nếu chỉ thu được 0,5 mol Na2O thì lượng nhiệt tỏa ra là bao nhiêu kJ?
Cho phản ứng:
N2(g) + 3H2(g) → 2NH3(g)
Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ tỏa ra 92,22 kJ. Tính enthalpy tạo thành chuẩn của NH3.
Vì sao enthalpy tạo thành của một đơn chất bền lại bằng không?
Giá trị \({\Delta _r}H_{298}^0\) của phản ứng sau là bao nhiêu kJ?
½ CH4(g) + O2(g) → ½ CO2(g) + H2O(l)
Đốt cháy hoàn toàn 1 gam C2H2(g) ở điều kiện chuẩn, thu được CO2(g) và H2O(l), giải phóng 49,98 kJ. Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy 1 mol C2H2.
Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam CH4(g) để cung cấp nhiệt cho phản ứng tạo 1 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%.
Sự hô hấp cung cấp oxygen cho các phản ứng oxi hóa chất béo, chất đường, tinh bột, … trong cơ thể con người. Đó là các phản ứng giải phóng hay hấp thụ năng lượng? Năng lượng kèm theo các phản ứng này dùng để làm gì?
Những loại phản ứng nào sau đây cần phải cung cấp năng lượng trong quá trình phản ứng?
(a) Phản ứng tạo gỉ kim loại
(b) Phản ứng quang hợp
(c) Phản ứng nhiệt phân
(d) Phản ứng đốt cháy
Một số phản ứng khi xảy ra sẽ làm nóng môi trường xung quanh, một số khác lại làm lạnh môi trường xung quanh. Em hãy cho biết sự khác biệt cơ bản giữa hai loại phản ứng này.
Cho biết phản ứng sau có \({\Delta _t},H_{298}^o\) > 0 và diễn ra ở ngay nhiệt độ phòng.
2NH4NO3(s) + Ba(OH)2.8H2O(s) → 2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
Khi trộn đều một lượng ammonium nitrate (NH4NO3) rắn với một lượng barium hydroxide ngậm nước (Ba(OH)2.8H2O) ở nhiệt độ phòng thì nhiệt độ của hỗn hợp sẽ tăng hay giảm? Giải thích.
Cho biết phản ứng tạo thành 2 mol HCl(g) ở điều kiện chuẩn sau đây tỏa ra 184,6 kJ:
H2(g) + Cl2(g) → 2HCl(g) (*)
Những phát biểu sau dưới đây là đúng?
A. Nhiệt tạo thành của HCl là -184,6 kJ.mol-1.
B. Biến thiên enthalpy phản ứng (*) là -184,6 kJ.
C. Nhiệt tạo thành của HCl là -92,3 kJ.mol-1.
D. Biến thiên enthalpy phản ứng (*) là -92,3 kJ.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *