Để giúp các em học tập hiệu quả môn Hóa 10, đội ngũ DapAnHay đã biên soạn và tổng hợp nội dung Bài 3: Nguyên tố hóa học lớp 10 chương trình SGK Cánh Diều. Bài giảng gồm kiến thức cần nhớ về nguyên tố, số hiệu nguyên tử, số khối, kí hiệu, đồng vị cũng như cách tính nguyên tử trung bình... Bên cạnh đó còn có các bài tập minh họa có hướng dẫn giải chi tiết, giúp các em học tập và củng cố thật tốt kiến thức. Mời các em cùng tham khảo.
a. Khái niệm nguyên tố hoá học
- Nguyên tố hoá học là tập hợp các nguyên tử có cùng số hạt proton.
Ví dụ: Ba loại nguyên tử hydrogen (H) đều có một proton trong hạt nhân nên thuộc cùng một nguyên tố hoá học, nguyên tố hydrogen (H).
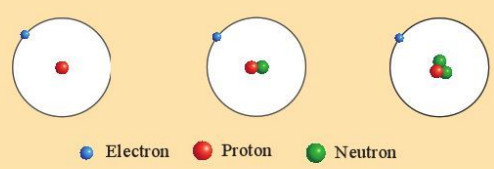
Hình 3.2. Mô hình cấu tạo các loại nguyên tử của nguyên tố hydrogen
- Kim cương và than chì có vẻ bề ngoài rất khác nhau nhưng đều được tạo nên từ các nguyên tử mà hạt nhân có 6 proton. Như vậy, kim cương và than chì đều được tạo nên từ cùng một nguyên tố hoá học, nguyên tố carbon (C).

Hình 3.3. Kim cương và than chì
- Hạt nhân nguyên tử chì (Pb) có 82 proton, hạt nhân nguyên tử vàng có 79 proton. Các tác động vật lí, hoá học thông thường không làm thay đổi hạt nhân nên không thể biến đổi chì thành vàng bằng các cách này được.
- Số proton trong một hạt nhân nguyên tử được gọi là số hiệu nguyên tử, kí hiệu là Z.
- Ví dụ: Hạt nhân nguyên tử helium (He) có 2 proton, vậy số hiệu nguyên tử của He là 2 (ZHe = 2).
- Tổng số proton (Z) và neutron (N) trong một hạt nhân nguyên tử được gọi là số khối, kí hiệu là A: A = Z + N
- Như vậy, số khối chính bằng tổng số hạt có trong hạt nhân nguyên tử. Giá trị này xấp xỉ bằng giá trị khối lượng nguyên tử (khi tính theo đơn vị amu).
- Kí hiệu nguyên tử \(_Z^AX\) cho biết kí hiệu hoá học của nguyên tố (X), số hiệu nguyên tử (Z) và số khối (A).

Hình 3.4. Kí hiệu nguyên tử của helium
- Đôi khi, người ta viết tắt kí hiệu nguyên tử. Ví dụ: sử dụng He thay cho \(_2^4He\), bởi kí hiệu He đã cho biết đây là nguyên tử nguyên tố helium, hạt nhân có 2 proton.
a. Đồng vị
- Các nguyên tử của cùng một nguyên tố hoá học có số neutron khác nhau là đồng vị của nhau.
- Do đó, các đồng vị của cùng một nguyên tố hoá học (có cùng số proton) khác nhau về số khối do có số neutron khác nhau.
- Tất cả các nguyên tố hoá học đều có nhiều đồng vị.
Ví dụ: hydrogen có các đồng vị là: 1H (kí hiệu là H), đồng vị, 2H (kí hiệu là D), 3H (kí hiệu là T).., carbon có các đồng vị là 12C, 13C,...
b. Nguyên tử khối trung bình
- Nguyên tử khối là khối lượng tương đối của một nguyên tử, cho biết khối lượng của một nguyên tử nặng gấp bao nhiêu lần 1 amu.
Ví dụ: Nguyên tử khối của 12C là 12 do khối lượng của một nguyên tử 12C là 12 amu.
- Nguyên tử khối trung bình
+ Mỗi nguyên tố hoá học đều có nhiều đồng vị. Trong tự nhiên, một nguyên tố hoá học dù ở dạng đơn chất hay hợp chất thì tỉ lệ giữa các đồng vị của nguyên tố này là không đổi. Nguyên tử khối của nguyên tố hoá học có nhiều đồng vị là nguyên tử khối trung bình của các đồng vị (kí hiệu là \(\overline A \)), có tính đến tỉ lệ số nguyên tử các đồng vị tương ứng (xác định từ phổ khối lượng).
+ Công thức tính nguyên tử khối trung bình như sau:
\(\overline A = \frac{{A.a + B.b + C.c + ...}}{{a + b + c + ...}}\)
+ Trong đó:
Ví dụ: Trong tự nhiên, bạc có hai đồng vị bền: 107Ag và 109Ag chiếm tương ứng khoảng 51,86% và 48,14% về số nguyên tử. Nguyên tử khối trung bình của bạc là:
\(\frac{{107.51,86 + 109.48,14}}{{51,86 + 51,86}} \approx 107,96\)
Bài 1: Những nguyên tử nào dưới đây thuộc cùng một nguyên tố hoá học?
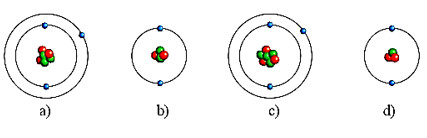
Hình 3.1. Mô hình cấu tạo của một số nguyên tử
Hướng dẫn giải
- Những nguyên tử mà hạt nhân có cùng số proton sẽ thuộc cùng một nguyên tố hóa học.
- Trong một nguyên tử trung hòa về điện, số hạt proton = số hạt electron
- Dễ dàng thấy được:
+ Hình a, hình c đều có 3 electron ở lớp vỏ => Hình a, hình c đều có 3 proton → Nguyên tử a, nguyên tử c thuộc cùng 1 nguyên tố hóa học
+ Hình b, hình d đều có 2 electron ở lớp vỏ => Hình b, hình d đều có 2 proton → Nguyên tử b, nguyên tử d thuộc cùng 1 nguyên tố hóa học
Bài 2: Nguyên tử lithium (Li) có 3 proton trong hạt nhân. Khi Li tác dụng với khí chlorine (Cl2) sẽ thu được muối lithium chlorine (LiCl), trong đó Li tồn tại ở dạng Li+. Ion Li+ có bao nhiêu proton trong hạt nhân?
Hướng dẫn giải
- Nguyên tử Li và ion Li+ đều thuộc cùng 1 nguyên tố hóa học là Li
- Li+ là nguyên tử Li sau khi mất đi 1 electron. Do vậy Li+ sẽ có 3 proton và 2 electron
→ Trong hạt nhân Li và Li+ đều có cùng số hạt proton là 3.
Bài 3: Nguyên tử Li có 3 proton, 4 neutron. Viết kí hiệu nguyên tử của nguyên tố này
Hướng dẫn giải
- Nguyên tử Li có 3 proton và 4 neutron
- Số hiệu nguyên tử = số proton
- Số khối = số proton + số neutron
→ Số hiệu nguyên tử của Li là 3 và số khối của Li = 3 + 4 = 7
→ Kí hiệu Li có 3 proton và 4 neutron là: \({}_3^7X\)
Học xong bài học này, em có thể:
- Trình bày được khái niệm về nguyên tố hoá học, số hiệu nguyên tử, số khối và kí hiệu nguyên tử.
- Phát biểu được khái niệm đồng vị, nguyên tử khối.
- Tính được nguyên tử khối trung bình (theo amu) dựa vào khối lượng nguyên tử và phần trăm số nguyên tử của các đồng vị theo phổ khối lượng được cung cấp.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Cánh Diều Bài 3 cực hay có đáp án và lời giải chi tiết.
Số hiệu của X biết khi mất 2 e ngoài cùng thì tạo X2+ thì 3p6?
Nguyên tử của X có electron lớp ngoài cùng là 5f66d17s2 nếu vị trí của X?
X có cấu hình electron là 1s22s22p3 vậy vị trí X?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Cánh Diều Bài 3để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 16 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 1 trang 17 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 2 trang 17 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 3 trang 17 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 2 trang 17 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 3 trang 18 SGK Hóa học 10 Cánh Diều - CD
Vận dụng 1 trang 18 SGK Hóa học 10 Cánh Diều - CD
Vận dụng 2 trang 18 SGK Hóa học 10 Cánh Diều - CD
Luyện tập trang 18 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 4 trang 18 SGK Hóa học 10 Cánh Diều - CD
Giải bài 1 trang 20 SGK Hóa học 10 Cánh Diều - CD
Giải bài 2 trang 20 SGK Hóa học 10 Cánh Diều - CD
Giải bài 3 trang 20 SGK Hóa học 10 Cánh Diều - CD
Giải bài 4 trang 20 SGK Hóa học 10 Cánh Diều - CD
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Số hiệu của X biết khi mất 2 e ngoài cùng thì tạo X2+ thì 3p6?
Nguyên tử của X có electron lớp ngoài cùng là 5f66d17s2 nếu vị trí của X?
X có cấu hình electron là 1s22s22p3 vậy vị trí X?
Những phát biểu sai trong 5 phát biểu dưới:
1. Trong một nguyên tử luôn luôn có số proton = số electron = số điện tích hạt nhân
2. Tổng số proton và số electron trong một hạt nhân gọi là số khối
3. Số khối A là khối lượng tuyệt đối của nguyên tử
4. Số proton = điện tích hạt nhân
5. Đồng vị là các nguyên tử có cùng số proton nhưng khác nhau về số nơtron
X có 3 đồng vị A1X (79%), A2X (10%), A3X (11%), biết tổng A của 3 đồng vị là 75, nguyên tử lượng trung bình của 3 đồng vị là 24,32. Mặt khác số nơtron của đồng vị thứ 2 nhiều hơn số nơtron đồng vị 1 là 1 đơn vị . A1, A2, A3 lần lượt là gì?
Cấu hình không tuân theo nguyên lí Pauli trong số 4 đáp án dưới đây?
Tổng số hạt cơ bản M2+ là 90, số hạt mang điện nhiều hơn số hạt không mang điện là 22. M là kim loại nào bên dưới đây?
Oxit X có công thức R2O, tổng số hạt là 92, trong đó hạt mang điện nhiều hơn không mang điện là 28. X là chất nào ?
B có tổng số hạt là 21. Số hạt không mang điện chiếm 33,33%. Nguyên tử B là gì?
Phát biểu nào sau đây không đúng về nguyên tử trong 4 ý?
Nguyên tử lithium (Li) có 3 proton trong hạt nhân. Khi Li tác dụng với khí chlorine (Cl2) sẽ thu được muối lithium chlorine (LiCl), trong đó Li tồn tại ở dạng Li+. Ion Li+ có bao nhiêu proton trong hạt nhân?
Phân tử S8 có 128 electron, hỏi số hiệu nguyên tử của lưu huỳnh (S) là bao nhiêu?
Một nguyên tử có Z hạt proton, Z hạt electron và N hạt neutron. Tính khối lượng (gần đúng, theo amu) và số khối của nguyên tử này. Nhận xét về kết quả thu được.
Hoàn thành bảng sau
| Nguyên tử | Số p | Số n | Kí hiệu nguyên tử |
| C | 6 | 6 | ? |
| ? | ? | ? | \({}_{11}^{23}X\) |
Nguyên tử Li có 3 proton, 4 neutron. Viết kí hiệu nguyên tử của nguyên tố này
Cho các nguyên tử sau: \({}_2^5X\), \({}_3^7Y\), \({}_4^9Z\), \({}_5^{11}M\), \({}_5^{12}T\)
Những nguyên tử nào là đồng vị của nhau?
Nguyên tố oxygen có 17 đồng vị, bắt đầu từ \({}_8^{12}O\), kết thúc là \({}_8^{28}O\). Các đồng vị oxygen có tỉ lệ giữa số hạt neutron (N) và số hiệu nguyên tử thỏa mãn \(1 \leqslant \frac{N}{Z} \leqslant 1,25\)thì bền vững. Hỏi trong tự nhiên thường gặp đồng vị nào của oxygen?
Em hãy tìm hiểu đồng vị nào của oxygen chiếm tỉ lệ lớn nhất trong tự nhiên.
Trong tự nhiên, argon có các đồng vị \({}^{40}{\text{Ar}}\),\(^{38}{\text{Ar}}\), \({}^{36}{\text{Ar}}\)chiếm tương ứng khoảng 99,604%; 0,063% và 0,333% số nguyên tử. Tính nguyên tử khối trung bình của Ar.
Chlorine có hai đồng vị bền là 35Cl và 37Cl. Nguyên tử khối trung bình của chlorine là 35,45. Tính tỉ lệ phần trăm số nguyên tử mỗi đồng vị của chlorine trong tự nhiên.
Hoàn thành bảng sau đây:
| Kí hiệu | Số hiệu nguyên tử | Số khối | Số proton | Số electron | Số neutron |
| \({}_{18}^{40}{\text{Ar}}\) | ? | ? | ? | ? | ? |
| ? | ? | 39 | 19 | ? | ? |
| ? | 16 | ? | ? | ? | 20 |
Những phát biểu nào sau đây là đúng?
(a) Những nguyên tử có cùng số electron thì thuộc cùng một nguyên tố hóa học
(b) Hai ion dương (ion một nguyên tử) có điện tích lần lượt là +2 và +3, đều có 26 proton. Vậy hai ion này thuộc cùng một nguyên tố hóa học
(c) Hai nguyên tử A và B đều có số khối là 14. Vậy hai nguyên tử này thuộc cùng một nguyên tố hóa học.
(d) Những nguyên tử có cùng số neutron thì thuộc cùng một nguyên tố hóa học.
Trong tự nhiên, đồng có hai đồng vị bền là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,54. Tính số mol mỗi loại đồng vị có trong 6,354 gam đồng
Phổ khối, hay phổ khối lượng (MS: Mass Spectrum) chủ yếu được sử dụng để xác định phân tử khối, nguyên tử khối của các chất và hàm lượng các đồng vị bền của một nguyên tố. Phổ khối của neon được biểu diễn như ở Hình 3.5.
Trục tung biểu thị hàm lượng phần trăm về số nguyên tử của từng đồng vị, trục hoành biểu thị tỉ số của nguyên tử khối (m) của mỗi đồng vị với điện tích của các ion đồng vị tương ứng (điện tích z của các ion đồng vị neon đều bằng +1).
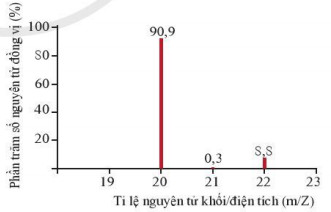
a) Neon có bao nhiêu đồng vị bền?
b) Tính nguyên tử khối trung bình của Neon.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *