Bài học Bài 17: Nguyên tố và đơn chất Halogen môn Hóa học 10 chương trình SGK Cánh Diều sẽ giúp các bạn tìm hiểu vị trí nhóm halogen trong bảng tuần hoàn, sự biến đổi độ âm điện, bán kính nguyên tử và một số tính chất vật lí của các nguyên tố trong nhóm, bên cạnh đó là cấu hình electron ngoài cùng của nguyên tử, tính chất hóa học cơ bản của các nguyên tố halogen và sự biến đổi tính chất hóa học… Mời các bạn tham khảo nội dung bài học tại đây nhé.
- Các nguyên tố nhóm VIIA gồm: fluorine, chlorine, bromine, iodine và hai nguyên tố phóng xạ là astatine, tennessine. Một số đặc điểm của các nguyên tố halogen được thể hiện trong Bảng 17.1.
Bảng 17.1. Một số đặc điểm của các nguyên tố halogen
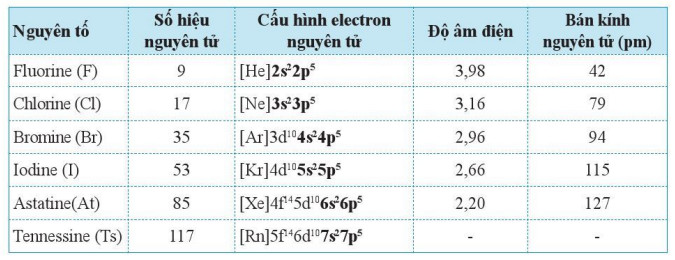
- Mỗi nguyên tử nguyên tố nhóm VIIA đều có 7 electron lớp ngoài cùng, dạng ns2np5. Vì vậy, chúng là các phi kim.
- Trong tự nhiên, các nguyên tố nhóm VIIA chủ yến tồn tại dạng muối, do đó chúng còn được gọi là nhóm halogen
+ Fluorine:
+ Chlorine
+ Bromine: Các hợp chất bromide (chứa Br-) tan trong nước biển, nước sông.
+ Iodine: Các hợp chất iodide, iodate (chứa I-, IO3-) có trong nước biển, nước sông, rong biển.
Ở điều kiện thường, đơn chất halogen tồn tại ở dạng phân tử hai nguyên tử, được kí hiệu chung là X2
a. Xu hướng biến đổi một số tính chất vật lí
- Một số tính chất vật lí của đơn chất halogen được thể hiện Bảng 17.3.
Bảng 17.3. Một số tính chất vật lí của đơn chất halogen
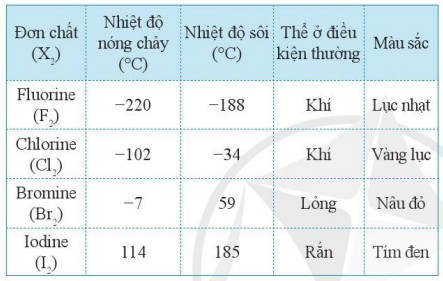
- Khi phân tử X2 có kích thước càng lớn và càng nhiều electron thì tương tác van der Waals giữa các phân tử càng mạnh. Do đó, trong các halogen, tương tác van der Waals tăng từ fluorine đến iodine. Như vậy, bên cạnh sự tăng khối lượng phân tử, thì sự tăng tương tác van der Waals đã giải thích được xu hướng biến đổi nhiệt độ sôi từ fluorine den iodine trong Bảng 17.3.
- Thể của các halogen ở điều kiện thường biển đổi từ khi (fluorine, chlorine) đến lỏng (bromine) và rắn (iodine), phù hợp với xu hướng tăng khối lượng phân tử và sự tương tác giữa các phân tử.
- Một điều lí thú là màu sắc của các đơn chất của halogen từ fluorine đến iodine cũng biến đổi theo xu hướng đậm dần.
b. Xu hướng tạo liên kết trong các phản ứng hoá học
- Nguyên tử của các nguyên tố halogen đều có 7 electron hoá trị. Vì vậy, theo quy tắc octet, halogen thường có hai xu hướng tạo liên kết khi phản ứng với các chất khác.
* Xu hướng thứ nhất: nhận thêm 1 electron từ nguyên tử khác. Xu hướng này xảy ra khi đơn chất halogen phản ứng với nhiều kim loại khác nhau. Khi đó, mỗi nguyên tử Xnhận thêm 1 electron từ nguyên tử kim loại để trở thành anion có điện tích 1-, đồng thời nguyên tử kim loại sẽ trở thành cation có điện tích n+. Cả cation và anion cùng thoả mãn quy tắc octet. Giữa chúng sẽ có tương tác tĩnh điện để tạo hợp chất có liên kết ion.
Ví dụ 1: Khi chlorine phản ứng với magnesium, có sự nhận và nhường electron như sau:
Cl2 + 2e → 2Cl-
Mg → Mg2+ + 2e
- Phương trình hoá học của phản ứng là: Mg (s) + Cl2 (g) → MgCl2 (s)
- Phương trình hoá học của phản ứng là: Mg(s) + Cl2 (8) → MgCl2(s)
* Xu hướng thứ hai: góp chung electron hoá trị với nguyên tử nguyên tố khác. Khi đơn chất halogen phản ứng với một số phi kim thì mỗi nguyên tử X có thể góp chung electron hoá trị với nguyên tử phi kim để cả hai nguyên tử đều đạt cấu hình electron thoả mãn quy tắc octet. Giữa chúng hình thành liên kết cộng hoá trị.
Ví dụ 2: Trong phản ứng giữa chlorine và hydrogen, nguyên tử của mỗi chất sẽ góp chung 1 electron độc thân để hình thành 1 liên kết cộng hoá trị. Khi đó, quanh H có 2 electron như khí hiểm helium, xung quanh C1 có 8 electron như khí hiếm neon, với mô tả theo công thức electron:
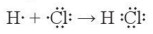
- Phương trình hoá học của phản ứng: H2(g) + Cl2 (g) → 2HCl(g)
- Hai xu hướng trên cho thấy, để thoả mãn quy tắc octet, nguyên tử halogen sẽ dễ nhận thêm 1 electron của nguyên tử khác hoặc góp chung 1 electron với nguyên tử khác.
- Vì vậy:
+ Nhóm halogen có tính phi kim mạnh hơn các nhóm phi kim còn lại trong bảng tuần hoàn.
+ Hoá trị phổ biến của các halogen là I.
c. Xu hướng thể hiện tính oxi hoá
- Ngoại trừ fluorine, các halogen còn lại thể hiện cả tính oxi hoá và tính khử trong các phản ứng hoá học. Tuy nhiên, xu hướng thể hiện tính oxi hoá phổ biến hơn rất nhiều và trở nên đặc trưng hơn so với xu hướng thể hiện tính khử.
- Do vậy, ở các nội dung dưới đây, chúng ta chủ yếu xét xu hưởng biến đổi tính oxi hoá trong dãy halogen.
- Thực nghiệm và lí thuyết đều chỉ ra rằng đơn chất halogen đều có tính oxi hoá mạnh và tính oxi hoá giảm dần từ fluorine đến iodine. a) Phản ứng với hydrogen Các đơn chất halogen đều phản ứng với hydrogen tạo hydrogen halide nhưng trong các điều kiện phản ứng và mức độ thể hiện khác nhau.
* Phản ứng với hydrogen
- Các đơn chất halogen đều phản ứng với hydrogen tạo sẽ có một phần sản phẩm tái hydrogen halide nhưng trong các điều kiện phản ứng và tạo lại các chất ban đầu, theo mức độ thể hiện khác nhau.
Bảng 17.4. Điều kiện và mức độ phản ứng của đơn chất halogen với hydrogen, năng lượng liên kết H-X

- Bảng 17.4 cho thấy, mức độ phản ứng với hydrogen giảm từ fluorine đến iodine, phù hợp với xu hướng giảm tính oxi hoá của dãy halogen từ fluorine đến iodine.
- Các phản ứng đều tạo ra phân tử HX. Giá trị năng lượng liên kết H-X giảm dần làm cho độ bền nhiệt của các phân tử giảm từ HF đến HI.
- Trong đó, phân tử HI có độ bền nhiệt thấp, dễ bị phân huỷ một phần để tái tạo lại iodine và hydrogen theo phản ứng: 2HI(g) ⇔ H2 (g) + I2 (g)
- Vì vậy, phản ứng hydrogen và iodine được trình bày trong Bảng 17.4 là phản ứng hai chiều hay phản ứng thuận nghịch.
* Phản ứng thế halogen
- Khi cho nước chlorine màu vàng rất nhạt vào dung dịch sodium bromide không màu thì tạo ra dung dịch màu vàng nâu.
- Sự chuyển màu được giải thích là do đã có sự hình thành đơn chất bromine theo phản ứng sau: Cl2 (aq) + 2NaBr (aq) → 2NaCl (aq) + Br2 (aq)
- Như vậy, nguyên tố chlorine đã thay thế bromine trong muối sodium bromide.
- Nhìn chung, trong dung dịch, các halogen có tính oxi hoá mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hoá yếu hơn để tạo ra các halogen có tính oxi hoá yếu hơn.
- Cũng cần lưu ý rằng trong dung dịch thì fluorine không có phản ứng trên. Đó là do fluorine ưu tiên phản ứng với nước.
* Phản ứng với nước, với dung dịch sodium hydroxide
- Ngoại trừ fluorine, các halogen còn lại khi phản ứng với nước hoặc dung dịch sodium hydroxide (NaOH) đều thể hiện cá tính oxi hoá và tính khử.
- Khi cho các halogen vào nước thì fluorine phản ứng mạnh, chlorine và bromine có phản ứng thuận nghịch với nước, còn iodine tan rất ít và hầu như không phản ứng.
2F(aq) + 2H2O (l) → O2 (g) + 4HF(aq)
Cl2 (aq) + H2O(l) → HCl(aq) + HClO(aq)
Br2 (aq) + H2O(l) → HBr(aq) + HBrO(aq)
- Phản ứng giữa chlorine và nước là thuận nghịch nên tạo ra dung dịch gồm nước, hydrochloric acid(HCl), hypochlorous acid (HClO, còn được viết là HOCl) cùng chlorine. Dung dịch này còn được gọi là dung dịch nước chlorine, có tính sát khuẩn. Vì vậy, nước chlorine được sử dụng để xử lí vi khuẩn trong các nguồn nước cấp, môi trường, Trong công nghiệp, người ta còn sử dụng phản ứng giữa chlorine với dung dịch sodium hydroxide lạnh (khoảng 15°C) để tạo ra nước Javel có tính oxi hoá mạnh phục vụ cho mục đích sát khuẩn. Phương trình hoá học tạo nước Javel như sau:
Cl2(aq) + 2NaOH(aq) → NaCl(aq) +NaOCl (aq) +H2O (l)

Hình 17.3. Nước Javel dùng để sát khuẩn, tẩy rửa
- Ngoài phản ứng giữa chlorine với dung dịch sodium hydroxide lạnh, người ta còn thực hiện phản ứng trên ở 70°C. Phương trình hoá học phản ứng như sau:
3Cl (aq) +6NaOH(aq) → 5NaCl(aq) + NaClO3 (aq)+3H2O (l)
- Phản ứng giữa chlorine và dung dịch sodium hydroxide thuộc loại phản ứng tự oxi hoá, tự khử. Đó là do chlorine vừa giảm số oxi hoá, vừa tăng số oxi hoá.
Bài 1: Vì sao nước chlorine được sử dụng phổ biến để khử trùng, sát khuẩn?
Hướng dẫn giải
- Nước chlorine có thành phần là HCl và HClO có tính oxi hóa mạnh
→ Nước chlorine có tính tẩy màu được dùng để khử trùng và sát khuẩn, tẩy trắng sợi, vải, giấy
Bài 2: Chất A là muối canxi halogenua. Cho dung dịch chứa 0,2 gam A tác dụng với lượng dư dung dịch bạc nitrat thì thu được 0,376 gam kết tủa bạc halogenua. Hãy xác định công thức chất A.
Hướng dẫn giải
CaX2 + 2AgNO3 → Ca(NO3)2 + 2AgX (X là halogen)
- Áp dụng phương pháp tăng giảm khối lượng:
- Theo phương trình cứ 1 mol CaX2 tham gia phản ứng tạo 2 mol AgX.
- Khối lượng AgX tăng so với khối lượng CaX2 là: (2.108 + 2MX) – (40 – 2MX) = 176
- Theo đề bài, số mol CaX2 tham gia phản ứng là: (0,376-0,2)/176 = 10-3 (mol)
→ MCaX2 = 0,2/10-3 = 200 → 40 + 2MX = 200 → MX = 80
→ Vậy X là Brom (Br). Công thức của chất A là CaBr2
Bài 3: Cho 3,87 gam hỗn hợp muối natri của hai hologen liên tiếp tác dụng với dung dịch AgNO3 dư thu được 6,63g kết tủa. Hai halogen kế tiếp là:
Hướng dẫn giải
NaX + AgNO3 → AgX + NaNO3
mNaX = 3,87 , mAgX = 6,63
Áp dụng PP tăng giảm khối lượng ⇒ nNaX = (6,63-3,87)/(108-23)=0,324 mol
MNaX = 3,87/0,324 = 119,18 ⇒ MX = 96,1
⇒ 2 Halogen liên tiếp thỏa mãn là Br2 và I2
Bài 4:Trong các phản ứng hoá học sau, brom đóng vai trò là :
(1) SO2 + Br2 + 2H2O H2SO4 + 2HBr
(2) H2S + 4Br2 + 4H2O H2SO4 + 8HBr
A. Vừa là chất oxi hoá, vừa là chất khử.
B. Chất oxi hoá.
C. Chất khử.
D. Không là chất oxi hoá, không là chất khử.
Hướng dẫn giải
Ở 2 phương trình trên Br có số oxh thay đổi từ 0 (Br2) xuống -1 (HBr)
→ Br là chất OXH
Đáp án B
Học xong bài học này, em có thể:
- Phát biểu được trạng thái tự nhiên của các nguyên tố halogen.
- Mô tả được trạng thái, màu sắc, nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen.
- Giải thích được sự biến đổi nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen dựa vào tương tác van der Waals.
- Trình bày được xu hướng nhận thêm 1 electron (từ kim loại), hoặc dùng chung electron (với phi kim) để tạo hợp chất ion, hoặc hợp chất cộng hoá trị dựa theo cấu hình electron.
- Thực hiện được (hoặc quan sát video) thí nghiệm chứng minh được xu hướng giảm dần tính oxi hoá của các halogen thông qua một số phản ứng: Thay thế halogen trong dung dịch muối bởi một halogen khác; Halogen tác dụng với hydrogen và với nước.
- Giải thích được xu hướng phản ứng của các đơn chất halogen với hydrogen theo khả năng hoạt động của halogen và năng lượng liên kết H-X (điều kiện phản ứng, hiện tượng phản ứng và hỗn hợp chất có trong bình phản ứng).
- Viết được phương trình hoá học của phản ứng tự oxi hoá - khử của chlorine trong phản ứng với dung dịch sodium hydroxide ở nhiệt độ thường và khi đun nóng; ứng dụng của phản ứng này trong sản xuất chất tẩy rửa.
- Thực hiện được (hoặc quan sát video) một số thí nghiệm chứng minh tính oxi hoá mạnh của các halogen và so sánh tính oxi hoá giữa chúng.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Cánh Diều Bài 17 cực hay có đáp án và lời giải chi tiết.
Nguyên tố halogen có bán kính nguyên tử lớn nhất là
Đặc điểm nào dưới đây không phải là đặc điểm chung cho các nguyên tố halogen (F, Cl, Br, I) ?
Brom đơn chất được điều chế trong phòng thí nghiệm và được bảo quản trong bình kín. Trạng thái của brom đơn chất ở điều kiện thường là
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Cánh Diều Bài 17để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Luyện tập 1 trang 101 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 2 trang 101 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 1 trang 102 SGK Hóa học 10 Cánh Diều - CD
Luyện tập 2 trang 102 SGK Hóa học 10 Cánh Diều - CD
Luyện tập trang 103 SGK Hóa học 10 Cánh Diều - CD
Thực hành trang 104 SGK Hóa học 10 Cánh Diều - CD
Thực hành trang 105 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 1 trang 105 SGK Hóa học 10 Cánh Diều - CD
Giải câu hỏi 2 trang 105 SGK Hóa học 10 Cánh Diều - CD
Thực hành trang 106 SGK Hóa học 10 Cánh Diều - CD
Vận dụng trang 105 SGK Hóa học 10 Cánh Diều - CD
Giải bài 1 trang 107 SGK Hóa học 10 Cánh Diều - CD
Giải bài 2 trang 107 SGK Hóa học 10 Cánh Diều - CD
Giải bài 3 trang 107 SGK Hóa học 10 Cánh Diều - CD
Giải bài 4 trang 107 SGK Hóa học 10 Cánh Diều - CD
Giải bài 5 trang 107 SGK Hóa học 10 Cánh Diều - CD
Giải bài 6 trang 108 SGK Hóa học 10 Cánh Diều - CD
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Nguyên tố halogen có bán kính nguyên tử lớn nhất là
Đặc điểm nào dưới đây không phải là đặc điểm chung cho các nguyên tố halogen (F, Cl, Br, I) ?
Brom đơn chất được điều chế trong phòng thí nghiệm và được bảo quản trong bình kín. Trạng thái của brom đơn chất ở điều kiện thường là
Ở trạng thái cơ bản, nguyên tử các halogen có số electron độc thân là
Cho 200g SO3 vào bao nhiêu gam H2SO4 49% ta được H2SO4 78,4%?
Cho 46 gam một hỗn hợp Ba và hai kim loại kiềm nào bên dưới đây biết chúng thuộc 2 chu kì kế tiếp nhau vào nước thu được C và 11,2 lít khí (đktc). Nếu thêm 0,18 mol Na2 SO4 vào C thì dung dịch sau phản ứng vẫn chưa kết tủa hết Ba. Nếu thêm 0,21 mol Na2SO4 vào dung dịch C thì dung dịch sau phản ứng còn dư Na2SO4.
Cho 1,9 gam hỗn hợp muối cacbonat và hiđrocacbonat của kim loại kiềm nào bên dưới đây sẽ tác dụng hết với dung dịch HCl (dư), sinh ra 0,448 lít khí (ở đktc).
Tìm X, Y biết X và Y là 2 nguyên tố halogen ở 2 chu kì liên tiếp. Để kết tủa hết ion chứa 4,4 gam muối natri của chúng cần 150 ml dung dịch AgNO3 0,4 M?
Khối lượng Brom cần dùng để phản ứng vừa đủ với dung dịch chứa 30 gam NaI là
Chất A là muối canxi halogenua. Cho dung dịch chứa 0,2 gam A tác dụng với lượng dư dung dịch bạc nitrat thì thu được 0,376 gam kết tủa bạc haogenua. Hãy xác định công thức chất A
Dựa vào xu hướng biến đổi tính chất của các đơn chất halogen trong bảng 17.3, hãy dự đoán về thể (trạng thái) của đơn chất astatine ở điều kiện thường. Giải thích?
Bảng 17.3. Một số tính chất vật lí của đơn chất halogen

Trong điều kiện thường, halogen nào ở thể rắn? Vì sao?
Calcium và fluorine kết hợp thành phân tử calcium fluorine, CaF2. Trong đó, nguyên tử nào đã nhường và nhường bao nhiêu electron? Nguyên tử nào đã nhận và nhận bao nhiêu electron?
Để hình thành phân tử phosphorus trichloride (PCl3) thì mỗi nguyên tử chlorine và phosphorus đã góp chung bao nhiêu electron hóa trị? Viết công thức Lewis của phân tử?
Theo độ âm điện, boron trifluoride là hợp chất ion, thực tế nó là hợp chất cộng hóa trị, với công thức Lewis như sau:
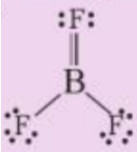
a) Viết phương trình hóa học tạo chất trên từ các đơn chất
b) Phân tử BF3 có bao nhiêu liên kết σ và bao nhiêu liên kết п?
Thí nghiệm chlorine phản ứng với hydrogen được mô tả như sau:
Bước 1: Chuẩn bị thí nghiệm như hình 17.1a với các ống nghiệm cùng đặt vào một giá thí nghiệm
Bước 2: Bơm vài giọt dung dịch hydrochloric acid (HCl) đặc từ xi – lanh chứa acid vào ống nghiệm chứa tinh thể potassium permanganate (thuốc tím, KMnO4) - ống nghiệm (1) để tạo khí chlorine. Khi pit – tông nâng lên khoảng ½ chiều cao của xi – lanh thu khí thì ngừng bơm acid (hình 17.1b)
Bước 3: Rút xi – lanh thu khí ra khỏi ống nghiệm (1), chuyển sang ghim vào ống nghiệm chứa kẽm - ống nghiệm (2) (hình 17.1c). Chuyển xi – lanh chứa dung dịch hydrochloric acid sang ống nghiệm (2)
Bước 4: Bơm vào giọt dung dịch hydrochloric acid từ xi – lanh chứa acid vào ống nghiệm (2) để tạo khí hydrogen. Đến khí pit – tông được nâng lên khoảng 2/3 xi – lanh thu khí thì ngừng bơm acid
Bước 5: Rút xi – lanh thu khí ra khỏi ống nghiệm (2). Ghim xi – lanh chứa hỗn hợp khí vào một nút cao su như hình 17.1d rồi kẹp vào giá thí nghiệm
Bước 6: Dùng đèn tử ngoại chiếu vào xi – lanh chứa hỗn hợp khí (hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi – lanh)
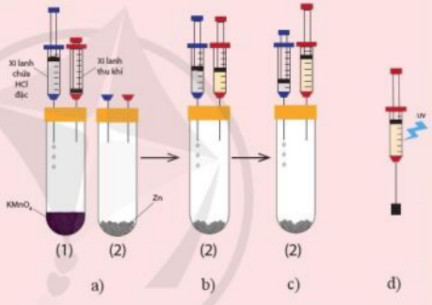
+ Quan sát và giải thích hiện tượng xảy ra khi dùng đèn tử ngoại chiếu vào xi – lanh chứa hỗn hợp khí (hoặc khi dùng ngọn lửa hơ nhẹ bên ngoài xi – lanh)
+ Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen có thể xảy ra hiện tượng như đã thấy trong thí nghiệm trên không? Giải thích
- Thí nghiệm 1:
+ Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium bromide hoặc potassium bromide loãng.
+ Nhỏ tiếp vào ống nghiệm vài giọt nước chlorine và lắc nhẹ
+ Có thể tiếp tục nhỏ vào ống nghiệm khoảng 2 mL cyclohexane
- Thí nghiệm 2:
+ Nhỏ vào ống nghiệm khoảng 2 mL dung dịch sodium iodide hoặc potassium iodide loãng
+ Nhỏ tiếp vào ống nghiệm vài giọt nước bromine loãng và lắc nhẹ. Có thể thêm tiếp vào ống nghiệm khoảng 2 mL cyclohexane
+ Thêm tiếp vào ống nghiệm vài giọt hồ tinh bột
Giải thích các hiện tượng xảy ra và minh họa bằng phương trình hóa học
Khi cho khí fluorine vào dung dịch sodium chloride thì fluorine phản ứng với nước mà không phản ứng với sodium chloride. Vậy, hãy dự đoán giá trị biến thiên enthalpy chuẩn của phản ứng nào dưới đây có thể âm hơn so với phản ứng còn lại.
F2(aq) + H2O (l) → 2HF (aq) + 1/2 O2 (g)
F2(aq) + 2NaCl (aq) → 2NaF (aq) + Cl2 (g)
Giả sử có thí nghiệm sau: Nhỏ nhanh vài giọt bromine màu nâu đỏ vào ống nghiệm chứa nước, đậy kín, lắc đều. Trong dung dịch bromine có những chất nào? Vì sao?
Thí nghiệm tính tẩy màu của khí chlorine.
Chuẩn bị thí nghiệm như hình 17.2
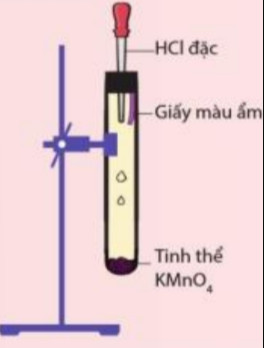
Bóp nhẹ phần cao su của ống nhỏ giọt để dung dịch hydrochloric acid chảy xuống ống nghiệm. Quan sát các hiện tượng xảy ra và giải thích.
Hãy giải thích vì sao các halogen không tồn tại tự do trong tự nhiên.
Hãy viết phương trình hóa học để chứng minh chlorine có tính oxi hóa mạnh hơn bromine
Trong công nghiệp, dung dịch sodium chlorine được đem điện phân để có phản ứng theo phương trình hóa học sau:
NaCl (aq) + H2O (l) → A (aq) + X (g) + Y (g) (*)
Từ phản ứng giữa Y với dung dịch A sẽ sản xuất được hỗn hợp tẩy rửa phổ biến.
Từ phản ứng kết hợp giữa X và Y sẽ sản xuất được hydrogen chlorine
a) Hãy cho biết công thức hóa học của A, X, Y
b) Hoàn thành phương trình hóa học (*)
Astatine là nguyên tố phóng xạ, được xếp dưới nguyên tố iodine trong nhóm VIIA. Thực tế, các nhà khoa học chỉ thu được đồng vị bền của astatine từ quá trình nghiên cứu về phóng xạ, đồng thời nó chỉ tồn tại khoảng 8 giờ
Dựa vào xu hướng biến đổi một số tính chất của nhóm halogen, hãy dự đoán:
a) Tính oxi hóa của nguyên tử astatine mạnh hơn hay yếu hơn so với nguyên tử iodine?
b) Đơn chất astatine có màu đậm hơn hay nhạt hơn so với đơn chất iodine?
Tra cứu các giá trị năng lượng liên kết ở phụ lục 2
a) Hãy tính biến thiên enthalpy chuẩn ∆rH0298 của 2 phản ứng dưới đây:
F2(g) + H2(g) → 2HF (g)
O2(g) + 2H2(g) → 2H2O(g)
b) Ở hai phản ứng trên, fluorine và oxygen đều đóng vai trò là chất oxi hóa. Dựa vào giá trị ∆rH0298, cho biết phản ứng oxi hóa – khử nào thuận lợi hơn
Một trong những ứng dụng của chlorine trong đời sống là khử trùng nước sinh hoạt tại các nhà máy xử lí và cấp nước. Trong quá trình khử trùng, người ta phải cho một lượng chlorine dư vào nước sinh hoạt. Lượng chlorine dư trong nước sinh hoạt còn có tác dụng ngăn ngừa sự tái nhiễm của vi khuẩn trong quá trình phân phối trong đường ống dẫn nước và trữ nước tại nhà.
Theo quy chuẩn kĩ thuật quốc gia (QCVN 01 – 1: 2018/BYT), hàm lượng chlorine tự do đối với nước sạch sử dụng cho mục đích sinh hoạt từ 0,2 – 1 mgL-1. Nếu hàm lượng chlorine nhỏ hơn 0,2 – 1 mgL-1 thì không tiêu diệt hết vi khuẩn và không xử lí được hết chất hữu cơ. Ngược lại, lượng chlorine trong nước lớn hơn 1,0 mgL-1 sẽ gây dị ứng
Carbon trong than hoạt tính sẽ tương tác trực tiếp với chlorine, giúp loại bỏ chlorine và các hợp chất chlorine và các hợp chất chlorine bằng cơ chế hấp thụ bề mặt. Khi chiếu tia cực tím với cường độ cao vào nước cũng làm giảm lượng chlorine. Các máy lọc nước RO (reverse osmosis: thẩm thấu ngược) cũng có thể giúp loại bỏ lượng chlorine trong nước một cách hiệu quả
Hãy trả lời các câu hỏi sau đây:
a) Dấu hiệu nào cho thấy chlorine có trong nước sinh hoạt
b) Vì sao người ta cần cho chlorine đến dư vào nước sinh hoạt
c) Cho biết một số phương pháp có thể loại bỏ khí chlorine dư trong nước sinh hoạt.
Xét các phản ứng: X2(g) + H2(g) → 2HX(g) ∆rH0298 (*)
Với X lần lượt là Cl, Br, I
Dựa vào Phụ lục 2:
a) Hãy tính biến thiên enthalpy chuẩn ∆rH0298 của mỗi phản ứng
b) Dựa vào kết quả ∆rH0298, dự đoán phản ứng của halogen nào với hydrogen thuận lợi nhất
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *