Ở bài học trước chúng ta đã tìm hiểu và biết cách tính nồng độ dung dịch. Nhưng làm thế nào để pha chế dung dịch theo nồng độ cho trước? Chúng ta cùng tìm hiểu nội dung bài học sau:
Đầu tiên ta xác định chất tan, dung môi là chất nào?
Có 2 kiểu pha chế:
Bài tập 1: Từ muối CuSO4, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 50 gam dung dịch CuSO4 10%.
a) Tính toán
Đề bài cho khối lượng chất tan là 50 gam dung dịch CuSO4 và nồng độ phần trăm của dung dịch C% = 10%.
Vận dụng công thức tính khối lượng chất tan ta có:
\(m_{CuSO_{4}} = \frac{{C\% .{m_{dd}}}}{{100\% }}\) = \(\frac{{10\%.50 }}{{100\% }} = 5(gam)\)
Các em lưu ý tới công thức tính khối lượng dung dịch là mdung dịch = mdung môi + mchất tan
Có khối lượng chất tan (5gam CuSO4), có khối lượng dung dịch (50 gam). Như vậy ta suy ra được khối lượng dung môi (nước)
mdung dịch = mdung môi + mchất tan ⇒ mdung môi = mdung dịch - mchất tan = 50 - 5 = 45 (gam)
Vậy khối lượng nước cần dùng cho sự pha chế là 45 gam.
b) Cách pha chế:
Hình 1: Quá trình pha chế 50 gam dung dịch CuSO4 10%
Bài tập 2: Từ muối CuSO4, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 50 ml dung dịch CuSO4 1M.
a) Tính toán
Từ công thức tính nồng độ mol của dung dịch nhận thấy có chứa 3 ẩn là số mol (n), thể tích (V) và nồng độ mol (CM).
Đề bài cung cấp 2 dữ kiện là thể tích dung dịch và nồng độ mol (1mol/l)
Vì đơn vị của nồng độ mol là mol/lít nên dữ kiện ml phải đổi về lít: 50 ml = \(\frac{{50}}{{1000}} = 0,05(lit)\)
Cho nguyên tử khối của Cu = 64, S = 32, O = 16
Cụ thể như sau:
Số mol CuSO4 chứa trong 50 ml dung dịch CuSO4 1M là:
\(n = {C_M}.V = 1.0,05 = 0,05(mol)\)
Khối lượng CuSO4 chứa trong 50 ml dung dịch CuSO4 1M là:
\({m_{CuS{O_4}}} = {n_{CuS{O_4}}}.{M_{CuS{O_4}}} = 0,05.(64 + 32 + 16.4) = 8(gam)\)
Vậy khối lượng CuSO4 cần thêm vào là 8 gam để tạo 50 ml dung dịch CuSO4 1M.
b) Cách pha chế
Bước 2: Tiến hành pha chế
Hình 2: Quá trình pha chế 50 ml dung dịch CuSO4 1M
Bài tập 1: Từ muối MgSO4, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 100ml dung dịch MgSO4 0,4 M từ dung dịch MgSO4 2M.
a) Tính toán
Từ công thức tính nồng độ mol của dung dịch nhận thấy có chứa 3 ẩn là số mol (n), thể tích (V) và nồng độ mol (CM).
Đề bài cung cấp 2 dữ kiện là thể tích dung dịch (100 ml) và nồng độ mol (0,4M)
Lưu ý: Vì đơn vị của nồng độ mol là (mol/lit) nên thể tích phải đổi từ ml sang lít.
Cho nguyên tử khối của Mg = 24, S = 32, O = 16
Cụ thể như sau:
Đổi 100ml thành 0,1 lít
Số mol chất tan có trong 100ml dung dịch 0,4M:
\({n_{MgS{O_4}}} = {C_M}.V = 0,4.0,1 = 0,04(mol)\)
+ Thể tích dung dịch MgSO4 2M trong đó có 0,04 mol MgSO4:
\(V' = \frac{n}{{{C_M}'}} = \frac{{0,04}}{2} = 0,02(lit)=20(ml)\)
b) Cách pha chế
Hình 3: Quá trình pha loãng dung dịch MgSO4 2M
Bài tập 2: Từ muối NaCl, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế 150g dung dịch NaCl 2,5% từ dung dịch NaCl 10%.
a) Tính toán
Khối lượng NaCl trong 150g dung dịch NaCl 2,5% là:
\({m_{NaCl}} = \frac{{C\% .{m_{{\rm{dd}}}}}}{{{\rm{100\% }}}} = \frac{{2,5.150}}{{100}} = 3,75(g)\)
Khối lượng dung dịch NaCl ban đầu chứa 3,75g NaCl là:
\({m_{{\rm{dd}}}} = \frac{{{m_{ct}}.100\% }}{{C\% }} = \frac{{3,75.100}}{{10}} = 37,5(g)\)
Khối lượng nước cần dùng là:
mdm= 150 – 37,5 = 112,5(g)
b) Cách pha chế
Lưu ý: Khi cân dung dịch ta cân cả dung dịch và bình chứa dung dịch nên ta sẽ cân riêng bình đựng, sau đó lấy tổng khối lượng trừ đi khối lượng bình là ra được khối lượng dung dịch chứa trong bình. Cụ thể như bài này. Khối lượng bình rỗng là 50 gam, tổng khối lượng bình và dung dịch là 87,8 gam. Như vậy ta vừa cân được 87,5 - 50 = 37,5 gam dung dịch.
Hình 4: Đầu tiên ta cân bình rỗng
Hình 5: Sau đó, cân cả khối lượng của bình và dung dịch
Hình 6: Quá trình pha chế dung dịch NaCl 2,5%
Sau bài học cần nắm:
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 43có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Muốn pha 300ml dung dịch NaCl 3M thì khối lượng NaCl cần lấy là:
Muốn pha 150g dung dịch CuSO4 2% từ dung dịch CuSO4 20% thì khối lượng dung dịch CuSO4 20% cần lấy là:
Có 60g dung dịch NaOH 20%. Khối lượng NaOH cần cho thêm vào dung dịch trên để được dung dịch 25% là:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 43.
Bài tập 1 trang 149 SGK Hóa học 8
Bài tập 2 trang 149 SGK Hóa học 8
Bài tập 3 trang 149 SGK Hóa học 8
Bài tập 4 trang 149 SGK Hóa học 8
Bài tập 5 trang 149 SGK Hóa học 8
Bài tập 43.1 trang 59 SBT Hóa học 8
Bài tập 43.2 trang 59 SBT Hóa học 8
Bài tập 43.3 trang 59 SBT Hóa học 8
Bài tập 43.4 trang 59 SBT Hóa học 8
Bài tập 43.5 trang 59 SBT Hóa học 8
Bài tập 43.6 trang 59 SBT Hóa học 8
Bài tập 43.7 trang 59 SBT Hóa học 8
Bài tập 43.8 trang 60 SBT Hóa học 8
Bài tập 43.9 trang 60 SBT Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa DapAnHay thảo luận và trả lời nhé.
Muốn pha 300ml dung dịch NaCl 3M thì khối lượng NaCl cần lấy là:
Muốn pha 150g dung dịch CuSO4 2% từ dung dịch CuSO4 20% thì khối lượng dung dịch CuSO4 20% cần lấy là:
Có 60g dung dịch NaOH 20%. Khối lượng NaOH cần cho thêm vào dung dịch trên để được dung dịch 25% là:
Để pha 100g dung dịch CuSO4 4% thì khối lượng nước cần lấy là:
Muốn pha 250ml dung dịch NaOH nồng độ 0,5M từ dung dịch NaOH 2M thì thể tích dung dịch NaOH 2M cần lấy là:
Bằng cách nào sau đây có thể pha chế được dung dịch NaCl 15%.
Để tính nồng độ mol của dung dịch KOH, người ta làm thế nào?
Để tính nồng độ phần trăm của dung dịch H2SO4, người ta làm thế nào?
Muốn pha 400ml dung dịch CuCl2 0,2M thì khối lượng CuCl2 cần lấy là
Cho 3 mẫu thử mất nhãn là Fe2O3,CuO, Al2O3. Để phân biệt mấy dung dịch trên, cần sử dụng mấy chất để phân biệt? là những chất nào
Làm bay hơi 60 g nước từ dung dịch có nồng độ 15% được dung dịch mới có nồng độ 18%. Hãy xác định khối lượng của dung dịch ban đầu?
Đun nhẹ 20 g dung dịch CuSO4 cho đến khi nước bày hơi hết, người ta thu được chất rắn màu trắng là CuSO4 khan. Chất này có khối lượng là 3,6 g. Hãy xác định nồng độ phần trăm của dung dịch CuSO4
Cân lấy 10,6 g Na2CO3 cho vào cốc chia độ có dung tích 500 ml. Rót từ từ nước cất vào cốc cho đến vạch 200 ml. Khuấy nhẹ cho Na2CO3 tan hết, ta được dung dịch Na2CO3. Biết 1 ml dung dịch này cho khối lượng là 1,05 g. Hãy xác định nồng độ phần trăm (C%) và nồng độ mol của dung dịch vừa pha chế được?
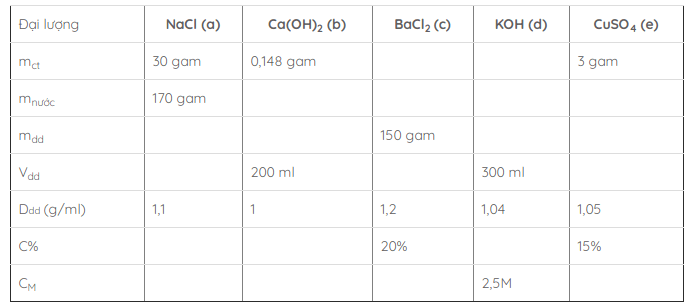
Hãy điền những giá trị chưa biết vào những ô trống trong bảng, bằng cách thực hiện các tính toán theo mỗi cột?
Tìm độ tan của một muối trong nước bằng phương pháp thực nghiệm người ta có được những kết quả sau:
- Nhiệt độ của dung dịch muỗi bão hòa là 200C.
- Chén sứ nung có khối lượng 60,26 g.
- Chén sứ đựng dung dịch muối có khối lượng 86,26 g.
- Khối lượng chén nung và muối kết tinh sau khi làm bay hết hơi nước là 66,26 g.
Hãy xác định độ tan của muối ở nhiệt độ 200C.
Từ dung dịch MgSO4 2M làm thế nào pha chế được 100ml dung dịch MgSO4 0,4M?
Từ dung dịch NaCl 1M, hãy trình bày cách pha chế 250ml dung dịch NaCl 0,2M.
Hãy trình bày cách pha chế 150ml dung dịch HNO3 0,25M bằng cách pha loãng dung dịch HNO3 5M có sẵn.
Từ glucozo (C6H12O6) vào nước cất, hãy trình bày cách pha chế 200g dung dịch glucozo 2%.
Hãy trình bày cách pha chế các dung dịch theo những yêu cầu sau:
a) 250ml dung dịch có nồng độ 0,1M của những chất sau:
- NaCl
- KNO3
- CuSO4
b) 200g dung dịch có nồng độ 10% của mỗi chất nói trên.
Có những dung dịch ban đầu như sau:
a) NaCl 2M
b) MgSO4 0,5M
c) KNO3 4M
Làm thế nào có thể pha chế được những dung dịch theo những yêu cầu sau:
- 500m dung dịch NaCl 0,5M
- 2 lit dung dịch MgSO4 0,2M
- 50ml dung dịch KNO3 0,2M.
Từ những muối và nước cất, hãy trình bày cách pha chế các dung dịch sau:
a) 2,5kg dung dịch NaCl 0,9%
b) 50g dung dịch MgCl2 4%
c) 250g dung dịch MgSO4 0,1%
Có 2 lọ đựng dung dịch H2SO4. Lọ thứ nhất có nồng độ 1mol/l, lọ thứ hai có nồng độ 3 mol/l. Hãy tính toán và trình bày cách pha chế 50ml dung dịch H2SO4 có nồng độ 1,5mol/l từ 2 dung dịch axit đã cho.
Cần dùng bao nhiêu ml dung dịch NaOH 3% có khối lượng riêng là 1,05g/ml và bao nhiêu mililit dung dịch NaOH 10% có khối lượng riêng là 1,12g/ml để pha chế được 2 lít dung dịch NaOH 8% có khối lượng riêng là 1,10g/ml.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
Gọi khối lượng dung dịch KNO3 45% và 15% cần lấy lần lượt là m1 (gam) và m2 (gam) cần pha trộn với nhau để được dung dịch KNO3 20%
\( \to {m_{KN{O_3}(1)}} = \frac{{45}}{{100}}.{m_1};{m_{KN{O_3}(2)}} = \frac{{15}}{{100}}.{m_2}\)
=> Tổng khối lượng chất tan là:
\( {m_{KN{O_3}(3)}} = {m_{KN{O_3}(1)}} + {m_{KN{O_3}(2)}} = \frac{{45.{m_1}}}{{100}} + \frac{{15.{m_2}}}{{100}} = 0,45{m_1} + 0,15{m_2}(1)\)
Tổng khối lượng dung dịch là: mdd (3) = mdd (1) + mdd (2) = m1 + m2
Dung dịch thu được có nồng độ 20% \( \to {m_{ct(3)}} = \frac{{({m_1} + {m_2}).20{\rm{\% }}}}{{100{\rm{\% }}}} = 0,2.({m_1} + {m_2})\) (2)
Từ (1) và (2) => 0,45.m1 + 0,15.m2= 0,2.(m1 + m2) => 0,25.m1 = 0,05.m2
\( = > \frac{{{m_1}}}{{{m_2}}} = \frac{{0,05}}{{0,25}} = 1:5\)
Câu trả lời của bạn
Khối lượng chất tan ở dd (1) là: \( {m_1} = {m_{dd(1)}}.C\% = \frac{{200.15{\rm{\% }}}}{{100{\rm{\% }}}} = 30{\mkern 1mu} gam\)
Khối lượng chất tan ở dd (2) là: \({m_2} = {m_{dd(2)}}.C\% = \frac{{m.5,4{\rm{\% }}}}{{100{\rm{\% }}}} = 0,054m{\mkern 1mu} gam\)
=> khối lượng chất tan dd thu được là: mct = m1 + m2 = 30 + 0,054m
Khối lượng dd thu được là: mdd = mdd (1) + mdd (2) = 200 + m
=> Nồng độ dung dịch thu được là:
\( C{\rm{\% }} = \frac{{{m_{ct}}}}{{{m_{dd}}}}.100{\rm{\% }} = \frac{{30 + 0,054m}}{{200 + m}}.100{\rm{\% }} = 11,8{\rm{\% }}\)
Vậy m=100g
Câu trả lời của bạn
Khối lượng chất tan ở dd (1) là: \( {m_{NaOH(1)}} = \frac{{300.3{\rm{\% }}}}{{100{\rm{\% }}}} = 9{\mkern 1mu} gam\)
Khối lượng chất tan ở dd (2) là: \( {m_{NaOH(2)}} = \frac{{200.10{\rm{\% }}}}{{100{\rm{\% }}}} = 20{\mkern 1mu} gam\)
=> khối lượng chất tan dd thu được là: mNaOH = mNaOH (1) + mNaOH (2) = 9 + 20 = 29 gam
Khối lượng dd thu được là: mdd = mdd (1) + mdd (2) = 300 + 200 = 500 gam
=> Nồng độ dung dịch thu được là: \( C{\rm{\% }} = \frac{{{m_{NaOH}}}}{{{m_{dd}}}}.100{\rm{\% }} = \frac{{29}}{{500}}.100{\rm{\% }} = 5,8\%\)
Câu trả lời của bạn
Khối lượng 10 lít dung dịch sau khi pha là:
mdd sau = V.d = 10.1,28 = 12,8 (kg)
Gọi thể tích cần thiết là x lít. Suy ra khối lượng nước là x (kg)
Gọi thể tích dung dịch axit là y lít. Suy ra khối lượng là 1,84y kg
=> x + y = 10 (1)
x + 1,84y = 12,8 (2)
từ (1) và (2) => x = 6,67 (lít) và y = 3,33 (lít)
Câu trả lời của bạn
Gọi khối lượng dung dịch ban đầu là m (g)
Khối lượng chất tan ban đầu là: 0,15m (g)
Sau khi làm bay hơi 20 gam nước thì khối lượng dung dịch sau là: m – 20 (g)
Nồng độ phần trăm sau phản ứng:
\( C\% = \frac{{{m_{c\tan }}}}{{{m_{{\rm{ddsau}}}}}}.100\% \to 20\% = \frac{{0,15m}}{{m - 20}}.100\% \to m = 80gam\)
Câu trả lời của bạn
200 ml = 0,2 (l)
Số mol của NaCl trước khi thêm nước là: nNaCl = CM. V = 5. 0,2 = 1 (mol)
Thể tích dung dịch sau khi thêm 50 ml nước là: Vdd sau = 200 +50 = 250 (ml) = 0,25 (l)
=> CM NaCl sau khi thêm nước là: CM = nNaCl : Vdd sau = 1 : 0,25 = 4 (M)
Câu trả lời của bạn
Khối lượng NaOH có trong dung dịch là: \( {m_{NaOH}} = \frac{{C{\rm{\% }}.{m_{dd}}}}{{100{\rm{\% }}}} = \frac{{60.25{\rm{\% }}}}{{100{\rm{\% }}}} = 15{\mkern 1mu} gam\)
Nồng độ dung dịch sau cô cạn là 30%, khối lượng chất tan là 12 gam (cô cạn không làm thay đổi khối lượng chất tan)
=> Khối lượng dung dịch sau cô cạn là: \({m_{dd}} = \frac{{{m_{NaCl}}.100{\rm{\% }}}}{{C{{\rm{\% }}_{dd\,sau}}}} = \frac{{15.100{\rm{\% }}}}{{30{\rm{\% }}}} = 50{\mkern 1mu} gam\)
Câu trả lời của bạn
Khối lượng NaCl có trong dung dịch là: \( {m_{NaCl}} = \frac{{C{\rm{\% }}.{m_{dd}}}}{{100{\rm{\% }}}} = \frac{{60.20{\rm{\% }}}}{{100{\rm{\% }}}} = 12{\mkern 1mu} gam\)
Khối lượng dung dịch sau khi cô đặc là 50 gam, khối lượng chất tan là 12 gam
=> nồng độ dung dịch sau cô đặc là: \( C{{\rm{\% }}_{dd\,sau}} = \frac{{{m_{NaCl}}}}{{{m_{dd}}}}.100{\rm{\% }} = \frac{{12}}{{50}}.100{\rm{\% }} = 24{\rm{\% }}\)
Câu trả lời của bạn
Khối lượng NaOH có chứa trong 60 gam dung dịch 30% là
\( {m_{ct}} = \frac{{C{\rm{\% }}.{m_{dd}}}}{{100{\rm{\% }}}} = \frac{{30{\rm{\% }}.60}}{{100{\rm{\% }}}} = 18{\mkern 1mu} gam\)
Gọi khối lượng NaOH thêm vào là a (gam), ta có:
Khối lượng chất tan trong dung dịch sau là: mct = 18 + a
Khối lượng dung dịch sau là: mdd = 60 + a
=> Nồng độ phần trăm của dd sau pha là
\( C{\rm{\% }} = \frac{{{m_{ct}}.100{\rm{\% }}}}{{{m_{dd}}}} = > \frac{{18 + a}}{{60 + a}}.100{\rm{\% }} = 44{\rm{\% }} = > a = 15{\mkern 1mu} gam\)
Câu trả lời của bạn
Đổi 250 ml = 0,25 lít
Pha loãng dung dịch có nồng độ 2M xuống 0,5M thì số mol NaOH không đổi
nNaOH = 0,5.0,25 = 0,125 mol
Thể tích dung dịch NaOH 2M cần lấy là:
\( V = \frac{n}{{{C_M}}} = \frac{{0,125}}{2} = 0,0625l = 62,5ml\)
Câu trả lời của bạn
Đầu tiên, ta cho NaOH, ta thấy Al2O3 tan trong dung dịch
Sau đó cho dung dịch HCl vào 2 mẫu còn lại,
- mẫu thử xuất hiện dung dịch vàng nầu => chất ban đầu là Fe2O3
- mẫu thử xuất hiện dung dịch màu xanh, chất ban đầu là CuO
Câu trả lời của bạn
Khối lượng NaOH có trong 60 gam dung dịch 20% là:
\( {m_{ct}} = \frac{{{m_{dd}}.C{\rm{\% }}}}{{100{\rm{\% }}}} = \frac{{20.60}}{{100}} = 12{\mkern 1mu} gam\)
Gọi khối lượng NaOH thêm vào là a (gam), ta có:
Khối lượng chất tan trong dung dịch sau khi thêm là: mct sau = 12 + a
Khối lượng dung dịch sau khi thêm là: mdd sau = 60 + a
=> Nồng độ dung dịch thu được là:
\(\begin{array}{l} C{\rm{\% }} = \frac{{{m_{ct\,sau}}.100{\rm{\% }}}}{{{m_{dd\,sau}}}} = \frac{{12 + a}}{{60 + a}}.100{\rm{\% }} = 25{\rm{\% }}\\ \to a = 4gam \end{array}\)
Câu trả lời của bạn
Khi pha loãng dung dịch từ 20% xuống 2% thì chỉ có khối lượng dung môi thay đổi còn khối lượng chất tan vẫn giữ nguyên.
Từ 150 gam dung dịch CuSO4 2% ta có khối lượng chất tan là:
\( C{\rm{\% }} = \frac{{{m_{ct}}}}{{{m_{dd}}}}.100{\rm{\% }} = > {m_{ct}} = \frac{{C{\rm{\% }}.{m_{dd}}}}{{100{\rm{\% }}}} = \frac{{2{\rm{\% }}.150}}{{100{\rm{\% }}}} = 3{\mkern 1mu} gam\)
Khối lượng dung dịch CuSO4 20% cần lấy là:
\( {m_{dd}} = \frac{{{m_{ct}}.100{\rm{\% }}}}{{C{\rm{\% }}}} = \frac{{3.100{\rm{\% }}}}{{20{\rm{\% }}}} = 15{\mkern 1mu} gam\)
Câu trả lời của bạn
Vì đơn vị của nồng độ mol là mol/l nên ta đổi 300 ml thành 0,3 lít
Số mol chất tan trong 0,3 lít dung dịch NaCl 3M là
\( {C_M} = \frac{n}{V} = > n = {C_M}.V = 3.0,3 = 0,9{\mkern 1mu} mol\)
Khối lượng NaCl cần lấy là: mNaCl = n.M = 0,9.58,5 = 52,65 gam
Câu trả lời của bạn
\( {n_{CuC{l_2}}}{\rm{\;}} = {C_M}.{\rm{\;}}V = 0,2.0,4 = 0,08{\rm{\;}}mol\)
=> Khối lượng CuCl2 cần lấy là:
\( {m_{CuC{l_2}}}{\rm{\;}} = 0,08.135 = 10,8{\rm{\;}}gam\)
Câu trả lời của bạn
Để tính nồng độ phần trăm của dung dịch H2SO4 ta tính số gam H2SO4 có trong 100 gam dung dịch.
Câu trả lời của bạn
Các chất tan được trong nước để tạo ra dung dịch là: KOH, NaCl, H2SO4.
Câu trả lời của bạn
Các chất tan được trong nước để tạo ra dung dịch là: NaOH, NaCl, HCl
Câu trả lời của bạn
Để tính nồng độ phần trăm của dung dịch H2SO4, người ta Tính số gam H2SO4 có trong 100 gam dung dịch
Câu trả lời của bạn
nCuCl2 = 0,4.0,2 = 0,08 mol
mCuCl2 = 0,08.135 = 10,8 gam

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *