Để sản xuất nhôm cần phải có một nguồn điện năng dồi dào. Vậy quy trình luyện nhôm đã dựa trên hiện tượng nào để đòi hỏi cần nhiều điện như vậy?
Sau khi học xong bài mới- Bài 14: Dòng điện trong chất điện phân các em sẽ trả lời được câu hỏi trên. Mời các em cùng theo dõi nội dung bài học nhé.
Trong dung dịch, các hợp chất hoá học như axit, bazơ và muối bị phân li thành các nguyên tử tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của các ion trong điện trường.
Chất điện phân không dẫn điện tốt bằng kim loại.
Dòng điện trong chất điện phân không chỉ tải điện lượng mà còn tải cả vật chất đi theo. Tới điện cực chỉ có các electron có thể đi tiếp, còn lượng vật chất đọng lại ở điện cực, gây ra hiện tượng điện phân
Ion dương (Cation) -> Catot
Ion âm (Anion) -> Anot
Các ion chuyển động về các điện cực có thể tác dụng với chất làm điện cực hoặc với dung môi tạo nên các phản ứng hoá học gọi là phản ứng phụ trong hiện tượng điện phân.
Hiện tượng dương cực tan xảy ra khi các anion đi tới anôt kéo các ion kim loại của điện cực vào trong dung dịch
Khối lượng vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
\(m = k.q\)
k: đương lượng điện hóa của chất được giải phóng
Đương lượng điện hoá k của một nguyên tố tỉ lệ với đương lượng gam \(\frac{A}{n}\) của nguyên tố đó. Hệ số tỉ lệ \(\frac{1}{F}\) , trong đó F gọi là số Faraday.
\(k = \frac{1}{F}.\frac{A}{n}\)
F = 96500 C/mol
A: khối lượng phân tử
n: hóa trị
Kết hợp hai định luật Fa-ra-đây, ta được công thức Fa-ra-đây
\(m = \frac{1}{F}.\frac{A}{n}.I.t\)
m: khối lượng chất được giải phóng (g)
F = 96500 C/mol
A: khối lượng phân tử
n: hóa trị
I: cường độ dòng điện
t: thời gian dòng điện chạy qua.
Hiện tượng điện phân có nhiều ứng dụng trong thực tế sản xuất và đời sống như luyện nhôm, tinh luyện đồng, điều chế clo, xút, mạ điện, đúc điện, …
Dựa vào hiện tượng điện phân quặng nhôm nóng chảy.
Bể điện phân có cực dương là quặng nhôm nóng chảy, cực âm bằng than, chất điện phân là muối nhôm nóng chảy, dòng điện chạy qua khoảng \({10^4}A\)
Bể điện phân có anôt là một tấm kim loại để mạ, catôt là vật cần mạ.
Chất điện phân thường là dung dịch muối kim loại để mạ. Dòng điện qua bể mạ được chọn một cách thích hợp để đảm bảo chất lượng của lớp mạ.
Phát biểu nào sau đây chính xác
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là
A. Không có thay đổi gì ở bình điện phân
B. Anôt bị ăn mòn
C. Đồng bám vào catôt
D. Đồng chạy từ anôt sang catôt
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là đồng chạy từ anôt sang catôt.
⇒ Đáp án D
Phát biểu nào là chính xác
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của
A. Các chất tan trong dung dịch
B. Các ion dương trong dung dịch
C. Các ion dương và ion âm dưới tác dụng của điện trường trong dung dịch
D. Các ion dương và ion âm theo chiều điện trường trong dung dịch
Các ion dương và ion âm dưới tác dụng của điện trwòng trong dung dịch
⇒ Đáp án C.
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Mật độ của các ion \(Na^+\) và \(Cl^-\):
\(N = 0,1.1000.6,023.10^{23} = 6,023.10^{25}/m^3\)
Điện dẫn suất của dung dịch:
\(\sigma = 1,{6.10^{ - 19}}.6,{023.10^{25}}.(4,5 + 6,8){.10^{ - 8}} = 1,088{(\Omega /m)^{ - 1}}\)
⇒ Điện trở suất \(\rho =\frac{1}{\sigma }=\frac{1}{1,088}=0,92\Omega .m\)
Người ta muốn bóc một lớp đồng dày \(d = 10 \mu m\) trên một bản đồng diện tích \(S = 1cm^2\) bằng phương pháp điện phân. Cường độ dòng điện là 0,010A. Tính thời gian cần thiết để bóc được lớp đồng. Cho biết đồng có khối lượng riêng là \(p = 8 900 kg/m^3\)
Khối lượng đồng phải bóc đi là: \(m = 8 900.1.10^{-4}.10.10^{-6} = 8,9.10^{-6} kg\)
Theo công thức Fa-ra-đây: \(m = \frac{1}{F}.\frac{A}{n}It\) ⇔ m = 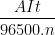 ; suy ra t =
; suy ra t = 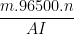
Với \(A = 64g = 6,{4.10^{ - 2}}kg;{\rm{ }}n{\rm{ }} = 2;{\rm{ }}I{\rm{ }} = {10^{ - 2}}A\) , suy ra:
t = 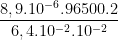 = 2 683,9 s
= 2 683,9 s
Để tách đồng ra khỏi một hỗn hợp rắn chứa 12% tạp chất khác người ta dùng thanh hỗn hợp này làm cực dương của bình điện phân đựng dung dịch \(CuS{O_4}.\) Hiệu điện thế giữa hai cực là \(U = 6(V)\). Tính điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp ?
Khối lượng đồng có trong thanh :
\({m_{Cu}} = \frac{{(100 - 12)}}{{100}}m = 0,88(kg)\)
Theo công thức Định luật Faraday :
\(\begin{array}{l}
m = \frac{1}{F}.\frac{A}{n}q\\
\Leftrightarrow 880 = \frac{1}{{96500}}.\frac{{64}}{2}q \Rightarrow q = {2654.10^3}(C)
\end{array}\)
Điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp :
\(W = qU = {2654.10^3}.6 = 15923{\rm{ }}\left( {kJ} \right) = 4,42\left( {kWh} \right)\)
Qua bài giảng Dòng điện trong chất điện phân này, các em cần hoàn thành 1 số mục tiêu mà bài đưa ra như :
Trả lời được câu hỏi thế nào là chất điện phân, hiện tượng điện phân, nêu được bản chất dòng điện trong chất điện phân
Phát biểu được định luật Fa-ra-day về điện phân.
Mô tả được hiện tượng dương cực tan
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Vật lý 11 Bài 14 cực hay có đáp án và lời giải chi tiết.
Muốn mạ đồng một tấm sắt có diện tích tổng cộng 200 cm2 , người ta dùng tấm sắt làm catôt của một bình điện phân đựng dùng dịch CuSO4 và anôt là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ \(I = 10A\) chạy qua trong thời gian 2 giờ 40 phút 50 giây. Tìm bề dày lớp đồng bám trên mặt tấm sắt. Cho biết đồng có \(A = 64; n = 2\) và có khối lượng riêng \(\rho = 8,9.103{\rm{ }}kg/{m^3}\)
Chiều dày của một lớp niken phủ lên một tấm kim loại là \(h =0,05mm\) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Biết niken có \( A = 58,n = 2\) và có khối lượng riêng là \(\rho = 8,9{\rm{ }}g/c{m^3}.\)
Một bộ nguồn điện gồm 30 pin mắc thành 3 nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động 0,9 V và điện trở trong \(0,6\Omega \). Một bình điện phân đựng dung dịch CuSO4 có điện trở \(205\Omega \) được mắc vào hai cực của bộ nguồn nói trên. Anôt của bình điện phân bằng đồng. Tính khối lượng đồng bám vào catôt của bình trong thời gian 50 phút. Biết Cu có \( A = 64; n = 2.\)
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Vật lý 11 Bài 14để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Bài tập 1 trang 85 SGK Vật lý 11
Bài tập 2 trang 85 SGK Vật lý 11
Bài tập 3 trang 85 SGK Vật lý 11
Bài tập 4 trang 85 SGK Vật lý 11
Bài tập 5 trang 85 SGK Vật lý 11
Bài tập 6 trang 85 SGK Vật lý 11
Bài tập 7 trang 85 SGK Vật lý 11
Bài tập 8 trang 85 SGK Vật lý 11
Bài tập 9 trang 85 SGK Vật lý 11
Bài tập 10 trang 85 SGK Vật lý 11
Bài tập 11 trang 85 SGK Vật lý 11
Bài tập 1 trang 100 SGK Vật lý 11 nâng cao
Bài tập 2 trang 100 SGK Vật lý 11 nâng cao
Bài tập 3 trang 100 SGK Vật lý 11 nâng cao
Bài tập 14.1 trang 35 SBT Vật lý 11
Bài tập 14.2 trang 35 SBT Vật lý 11
Bài tập 14.3 trang 36 SBT Vật lý 11
Bài tập 14.4 trang 36 SBT Vật lý 11
Bài tập 14.5 trang 36 SBT Vật lý 11
Bài tập 14.6 trang 36 SBT Vật lý 11
Bài tập 14.7 trang 37 SBT Vật lý 11
Bài tập 14.8 trang 37 SBT Vật lý 11
Bài tập 14.9 trang 37 SBT Vật lý 11
Bài tập 14.10* trang 37 SBT Vật lý 11
Bài tập 14.11 trang 37 SBT Vật lý 11
Bài tập 14.12* trang 37 SBT Vật lý 11
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Vật lý DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
-- Mod Vật Lý 11 DapAnHay
Muốn mạ đồng một tấm sắt có diện tích tổng cộng 200 cm2 , người ta dùng tấm sắt làm catôt của một bình điện phân đựng dùng dịch CuSO4 và anôt là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ \(I = 10A\) chạy qua trong thời gian 2 giờ 40 phút 50 giây. Tìm bề dày lớp đồng bám trên mặt tấm sắt. Cho biết đồng có \(A = 64; n = 2\) và có khối lượng riêng \(\rho = 8,9.103{\rm{ }}kg/{m^3}\)
Chiều dày của một lớp niken phủ lên một tấm kim loại là \(h =0,05mm\) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Biết niken có \( A = 58,n = 2\) và có khối lượng riêng là \(\rho = 8,9{\rm{ }}g/c{m^3}.\)
Một bộ nguồn điện gồm 30 pin mắc thành 3 nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động 0,9 V và điện trở trong \(0,6\Omega \). Một bình điện phân đựng dung dịch CuSO4 có điện trở \(205\Omega \) được mắc vào hai cực của bộ nguồn nói trên. Anôt của bình điện phân bằng đồng. Tính khối lượng đồng bám vào catôt của bình trong thời gian 50 phút. Biết Cu có \( A = 64; n = 2.\)
Hai bình điện phân: (CuSO4/Cu và AgNO3/Ag) mắc nối tiếp. Trong một mạch điện. Sau một thời gian điện phân, khối lượng catôt của hai bình tăng lên 2,8 g. Biết nguyên tử lượng của đồng và bạc là 64 và 108, hóa trị của đồng và bạc là 2 và 1. Tính khối lượng Ag được giải phóng ở catôt
Hai bình điện phân: \((FeC{l_3}/Fe\) và CuSO4/Cu) mắc nối tiếp. Sau một khoảng thời gian, bình thứ nhất giải phóng một lượng sắt là 1,4 g. Tính lượng đồng giải phóng ở bình thứ hai trong cùng khoảng thời gian đó. Biết nguyên tử lượng của đồng và sắt là 64 và 56, hóa trị của đồng và sắt là 2 và 3.
Một bình điện phân đựng dung dịch bạc Nitrat với Anốt làm bằng bạc. Điện trở của bình điện phân là \(R = 2\Omega \) . Hiệu điện thế đặt ở hai cực là \(U = 10(V)\). Cho \(A = 108, n = 1\). Khối lượng bạc bám vào cực âm sau 2 giờ là
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Để tách đồng ra khỏi một hỗn hợp rắn chứa 12% tạp chất khác người ta dùng thanh hỗn hợp này làm cực dương của bình điện phân đựng dung dịch \(CuS{O_4}.\) .Hiệu điện thế giữa hai cực là \(U = 6(V)\). Tính điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp ?
Nội dung của thuyết điện li là gì? Anion thường là phần nào của phân tử?
Dòng điện trong chất điện phân khác với dòng điện trong kim loại như thế nào?
Hãy nói rõ hạt tải điện nào mang dòng điện trên các phần khác nhau của mạch điện có chứa bình điện phân:
a. Dây dẫn và điện cực
b. Ở sát bề mặt hai điện cực
c. Ở trong lòng chất điện phân: ở trong lòng chất điện phân, hạt tải điện là
Chất điện phân thường dẫn điện tốt hơn hay kém hơn kim loại? Tại sao?
Hai bể điện phân: bể A để luyện nhôm, bể B để mạ niken. Hỏi bể nào có dương cực tan? Bể nào có suất phản điện?
Phát biểu định luật Pha-ra-đây, viết công thức Fa-ra-đây và đơn vị dùng trong công thức này.
Khi điện phân dung dịch \(H_2SO_4\) với điện cực bằng graphit, thì ta thu được khí oxi bay ra. Có thể dùng công thức Fa-ra-đây để tìm khối lượng oxi bay ra được không?
Phát biểu nào là chính xác
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của
A. Các chất tan trong dung dịch
B. Các ion dương trong dung dịch
C. Các ion dương và ion âm dưới tác dụng của điện trường trong dung dịch
D. Các ion dương và ion âm theo chiều điện trường trong dung dịch
Phát biểu nào sau đây chính xác
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là
A. Không có thay đổi gì ở bình điện phân
B. Anôt bị ăn mòn
C. Đồng bám vào catôt
D. Đồng chạy từ anôt sang catôt
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Người ta muốn bóc một lớp đồng dày \(d = 10 \mu m\) trên một bản đồng diện tích \(S = 1cm^2\) bằng phương pháp điện phân. Cường độ dòng điện là 0,010A. Tính thời gian cần thiết để bóc được lớp đồng. Cho biết đồng có khối lượng riêng là \(p = 8 900 kg/m^3\)
Chọn phát biểu đúng
A. Khi hòa tan axit, bazo hoặc muối vào trong nước, tất cả các phân tử của chúng đều bị phân li thành các ion.
B. Số cặp ion được tạo thành trong dung dịch điện phân không thay đổi theo nhiệt độ
C. Bình điện phân nào cũng có suất phản điện
D. Khi có hiện tượng dương cực tan, dòng điện trong chất điện phân tuân theo định luật Ôm.
Chọn đáp số đúng
Đương lượng điện hóa của niken là k = 3.10-4 g/C. Khi cho một điện lượng 10C chạy qua bình điện phân có anot bằng niken thì khối lượng niken bám vào catot là:
A. 0,3.10-4 g
B. 3.10-3 g
C. 0,3.10-3 g
D. 3.10-4 g
Chiều dày của lớp Niken phủ lên một tấm kim loại là D = 0,05mm sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Cho biết Niken có khối lượng riêng là ρ = 8,9.103kg/m3, A = 58 và n = 2.
Câu nào dưới đây nói về bản chất dòng điện trong chất điện phân là đúng ?
A. Là dòng các êlectron chuyển động có hướng ngược chiều điện trường.
B. Là dòng các ion dương-chuyển động có hướng thuận chiều điện trường.
C. Là dòng các ion âm chuyển động có hướng ngược chiều điện trường.
D. Là dòng chuyển động có hướng đồng thời của các ion dương thuận chiều điện trường và của các ion âm ngược chiều điện trường.
Câu nào dưới đây nói về hiện tượng điện phân có dương cực tan là đúng ?
A. Là hiện tượng điện phân dung dịch axit hoặc bazơ với điện cực là graphit.
B. Là hiện tượng điện phân dung dịch muối có chứa kim loại dùng làm catôt.
C. Là hiện tượng điện phân dung dịch muối có chứa kim loại dùng làm anôt. Kết quả là kim loại tan dần từ anôt tải sang catôt.
D. Là hiện tượng điện phân dung dịch muối có chứa kim loại dùng làm anôt. Kết quả là kim loại được tải dần từ catôt sang anôt.
Một bình điện phân chứa dung dịch muối niken với hai điện cực bằng niken. Xác định khối lượng niken bám vào catôt khi cho dòng điện cường độ I = 5,0 A chạy qua bình này trong khoảng thời gian t = 1 giờ. Đương lượng điện hoá của niken là 0,3.10-3 g/C.
A. 1,5 kg. B. 5,4 g.
C. 1,5 g. D. 5,4 kg.
Một bình điện phân chứa dung dịch đồng sunphat (CuS04) có anôt bằng đồng. Cho dòng điện không đổi chạy qua bình này trong thời gian 30 phút, khi đó khối lượng của catôt tăng thêm 1,143 g. Xác định cường độ dòng điện chạy qua bình điện phân. Đồng (Cu) có khối lượng mol là của A = 63,5 g/mol.
A. 0,965 A. B. 1,93 A.
C. 0,965 mA. D. 1,93 mA.
Một bình điện phân chứa dung dịch bạc nitrat (AgN03) có anôt bằng bạc và điện trở là 2,5 Ω. Hiệu điện thế giữa hai điện cực của bình này là 10 V. Bạc (Ag) có khối lượng mol là A = 108 g/mol và hoá trị n = 1. Xác định khối lượng bạc bám vào catôt sau 16 phút 5 giây.
A. 4,32 g. B. 4,32 kg.
C.2,16g. D. 2,16 kg.
Mắc nối tiếp một bình điện phân chứa dung dịch đồng sunphat (CuSO4) có anôt bằng đồng (Cu) với một bình điện phân chứa dung dịch bạc nitrat (AgNO3) có anôt bằng bạc (Ag). Sau môt khoảng thời gian có dòng điện không đổi chạy qua hai bình này, thì khối lượng anôt của bình chứa dung dịch CuSO4 bị giảm bớt 2,3 g. Xác định khối lượng bạc tới bám vào catôt của bình chứa dung dịch AgNO3. Đồng có khối lượng mol là A1 = 63,5 g/mol và hoá trị n1 = 2, bạc có khối lượng mol là A2 = 108 g/mol và hoá trị n2 = 1. Khối lượng bạc tới bám vào catot của bình chứa dung dịch AgNO3 là
A. 0,67g B. 1,95g
C. 2,66g D. 7,82g
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
)Tính cường độ dòng bazơ IB.
b)Tính cường độ dòng colectơ IC.
c)Tính hiệu điện thế giữa hai cực colectơ (C) và emitơ (E).
Câu trả lời của bạn
a)Cường độ điện bazơ IB
Ta có: IB = \(\frac{{{\text{e}}_{\text{1}}}\text{ - }{{\text{U}}_{\text{BE}}}}{{{\text{R}}_{\text{B}}}}\text{ = }\frac{4,5\text{ - 0,5}}{{{40.10}^{3}}}\) = 10-4A = 10μA.
Vậy: Cường độ điện bazơ IB là IB = 10μA.
b)Cường độ dòng colectơ IC
Ta có: IC = βIB = 100.10 = 1000μA = 10mA.
Vậy: Cường độ dòng colectơ IC là IC = 10mA.
c)Hiệu điện thế giữa hai cực colectơ (C) và emitơ (E)
Xét đoạn mạch C – RC – e2 – E, ta có: UCE = e2 – ICRC.
UCE = 12 – 10-2.103 = 2V
Vậy: Hiệu điện thế giữa hai cực colectơ (C) và emitơ (E) là uCE = 2V.
Câu trả lời của bạn
Gọi N là số nguyên tử silic.
-Ban đầu số hạt tải điện là : N1 = 2.10-13N (1)
-Khi pha P vào Si với tỉ lệ 1/106 thì số hạt tải điện tăng lên là do số electron tạo ra tăng lên. Số hạt tải điện lúc này là:
N2 = N1 + 10-6N = 2.10-13N + 10-6N (2)
-Tỉ số giữa số hạt tải điện cũ và mới là : k = \(\frac{{{\text{N}}_{\text{2}}}}{{{\text{N}}_{\text{1}}}}\)
k = \(\frac{\text{(2}\text{.1}{{\text{0}}^{\text{-13}}}\text{+1}{{\text{0}}^{\text{-6}}}\text{)N}}{\text{2}\text{.1}{{\text{0}}^{\text{-13}}}\text{N}}\text{ = 1 + 5}\text{.1}{{\text{0}}^{6}}\text{ }\approx \text{ 5}\text{.1}{{\text{0}}^{6}}\)
Vậy : Số hạt tải điện tăng lên hơn 5 triệu lần.
Câu trả lời của bạn
Giả sử các đi-ôt đều mở. Áp dụng định luật Kiêc-xôp cho các mạch vòng nhỏ, ta được:
-e1 + i1r + iR = 0 (1)
-e2 + i2r + iR = 0 (2)
Và i1 + i2 = i (3)
-e1 + 4i1 + iR = 0 (1’)
-e2 + 4i2 + iR = 0 (2’)
i1 + i2 = i (3’)
Từ (1’), (2’) và (3’): i1 = \(\frac{\text{4 - R}}{\text{10(2 + R)}}\); i2 = \(\frac{\text{8 + R}}{\text{10(2 + R)}}\); i = \(\frac{\text{12}}{\text{10(2 + R)}}\).
Vì i2 > 0 với mọi giá trị của R nên đi-ôt 2 luôn mở còn đi-ôt 1 có thể mở hoặc đóng.
a)Trường hợp R < 4Ω: i1 > 0, đi-ôt 1 mở. Lúc đó:
PR = Ri2 = R\({{\left( \frac{\text{12}}{\text{10(2 + R)}} \right)}^{2}}\text{ = }\frac{\text{1,44R}}{{{\text{(2 + R)}}^{\text{2}}}}\text{ = }\frac{\text{1,44}}{{{\left( \sqrt{\text{R}}\text{+}\frac{\text{2}}{\sqrt{\text{R}}} \right)}^{\text{2}}}}\text{ }\le \text{ }\frac{1,44}{{{(2\sqrt{2})}^{2}}}\) = 0,18W
Vậy: Công suất tỏa nhiệt trên R đạt cực đại khi \(\sqrt{\text{R}}\text{ = }\frac{\text{2}}{\sqrt{\text{R}}}\text{ = R = 2}\Omega \) và PR(max) = 0,18W.
b)Trường hợp R \(\ge \) 4Ω: i1 < 0, đi-ôt 1 đóng. Lúc đó:
PR = Ri2 = R\(\frac{\text{e}_{\text{2}}^{\text{2}}}{{{\text{(R + r)}}^{\text{2}}}}\text{ = }\frac{\text{e}_{\text{2}}^{\text{2}}}{{{\left( \sqrt{\text{R}}\text{+}\frac{\text{r}}{\sqrt{\text{R}}} \right)}^{2}}}\le \text{ }\frac{\text{e}_{\text{2}}^{\text{2}}}{\text{4r}}\) = \(\frac{1,{{6}^{2}}}{4.4}\) = 0,16W
Vậy: Công suất tỏa nhiệt trên R đạt cực đại khi \(\text{R = r = 4}\Omega \) và PR(max) = 0,16W.
a)Lắp mạch điện và đo lường để vẽ đường đặc trưng vôn – ampe của đèn bán dẫn trong phạm vi công suất tối đa 250mW. Trước khi đo, hãy nghĩ xem làm thế nào thì đèn bán dẫn không bị quá tải, ghi lập luận vào báo cáo. Vẽ sơ đồ mạch điện mà em dùng, phân tích các sai số hệ thống mắc phải khi dùng mạch ấy.
b)Tính điện trở nội (điện trở động) của đèn bán dẫn khi dòng có cường độ 25mA.
c)Dùng sơ đồ như hình vẽ bên để nghiên cứu sự phụ thuộc của điện thế ra U2 đối với điện thế vào U1. Lập bảng số liệu và vẽ đồ thị. Cho U1 biến đổi từ 0 đến 9V. Nên mắc đèn sao cho U2 thật lớn. Vẽ sơ đồ đầy đủ của mạch đã lắp và giải thích kết quả đo lường.
d)Nếu U1 tăng từ 7V lên 9V thì U2 biến đổi bao nhiêu, giải thích định tính giá trị của \(\frac{\text{ }\!\!\Delta\!\!\text{ }{{\text{U}}_{\text{1}}}}{\text{ }\!\!\Delta\!\!\text{ }{{\text{U}}_{\text{2}}}}\).
e)Đèn bán dẫn dùng trong thí nghiệm này là loại đèn gì? Nêu công dụng thực tế của sơ đồ ở câu c (tiếp theo là bảng điện trở nội của máy đo, thuộc loại chính xác 2,5Ω).
Câu trả lời của bạn
-Nguồn điện không đổi.
-Biến trở có con chạy.
-Hai đồng hồ vạn năng, dây nối và giấy kẻ ô li.
Câu trả lời của bạn
-Lắp sơ đồ theo hình II và đo dòng i ứng với các hiệu điện thế U1, U2 đặt theo hai chiều ngược nhau, ta được các giá trị:
i(U1); i(U2); i(-U1); i(-U2)
-Từ kết quả thu được ta nhận thấy:
+Dòng điện chạy được theo cả hai chiều.
+Với cùng một hiệu điện thế đặt theo hai chiều thì dòng có giá trị khác nhau.
+Theo cả hai chiều, dòng không là hàm tuyến tính của hiệu điện thế.
-Từ các đặc điểm trên, ta thấy:
+Từ đặc điểm thứ nhất, ta có thể loại bỏ các sơ đồ: a1, c1, c4, d1, e2.
+Từ đặc điểm thứ hai, ta có thể loại bỏ các sơ đồ: b2, d2.
+Từ đặc điểm thứ ba, ta có thể loại bỏ các sơ đồ: b1, c2, c3.
Từ đó, các linh kiện trong hộp phải được mắc theo sơ đồ e1.
-Giá trị của R: R = \(\frac{{{\text{U}}_{\text{R}}}\text{(i)}}{\text{i}}\text{ = }\frac{{{\text{U}}_{\text{B}}}\text{(i)-}{{\text{U}}_{\text{A}}}\text{(i)}}{\text{i}}\).
-Thực hiện phép đo nhiều lần và ghi kết quả theo bảng sau:
| STT phép đo | i(mA) | UB(mV) | UA(mV) | UB-UA | R=\(\frac{{{\text{U}}_{\text{B}}}\text{-}{{\text{U}}_{\text{A}}}}{\text{i}}\) |
| … |
-Kết quả: R = 10Ω; sai số:
\(\frac{\text{ }\!\!\Delta\!\!\text{ R}}{\text{R}}\text{ = }\frac{\text{ }\!\!\Delta\!\!\text{ }{{\text{U}}_{\text{B}}}\text{+ }\!\!\Delta\!\!\text{ }{{\text{U}}_{\text{A}}}}{{{\text{U}}_{\text{B}}}\text{-}{{\text{U}}_{\text{A}}}}\text{+}\frac{\text{ }\!\!\Delta\!\!\text{ i}}{\text{i}}\) = 10%.
a)Vẽ phác đồ thị của hàm số này với I0 = 1mA; -0,5V < U < 0,15V.
b)Tính hệ số chỉnh lưu của đi-ôt này ở hiệu điện thế 0,1V và 0,5V.
Cho hằng số Bôn-zơ-man k = 1,38.10-23(J/K); hệ số chỉnh lưu của một hiệu điện thế nào đó là tỉ số giữa dòng điện thuận và dòng điện ngược của hiệu điện thế đó; ở nhiệt độ phòng kT = 0,025eV.
Câu trả lời của bạn
a)Đồ thị của I theo U: Hình vẽ.
b)Hệ số chỉnh lưu của đi-ôt
Ta có: Ing = I0; Ith = \({{\text{I}}_{0}}{{\text{e}}^{\frac{\text{eU}}{\text{kT}}}}\) (khi U đủ lớn).
=> η = \(\frac{{{\text{I}}_{\text{th}}}}{{{\text{I}}_{\text{ng}}}}\text{ = }{{\text{e}}^{\frac{\text{eU}}{\text{kT}}}}\)
Với U = 0,1V thì η1 = \({{\text{e}}^{\frac{\text{e}\text{.0,1V}}{\text{0,025eV}}}}\text{ = }{{\text{e}}^{4}}\text{ = 55}\); với U = 0,5V thì η2 = \({{\text{e}}^{\frac{\text{e}\text{.0,5V}}{\text{0,025eV}}}}\text{ = }{{\text{e}}^{20}}\text{ = 4,9}\text{.1}{{\text{0}}^{8}}\).
Vậy: Hệ số chỉnh lưu của đi-ôt ứng với hiệu điện thế 0,1V là η1 = 55; ứng với η2 = 4,9.108.
Câu trả lời của bạn
Ta có m = ρV = ρSh = 1,335 g; \(m=\frac{1}{F}.\frac{A}{n}It\) \(\rightarrow I=\) \(\frac{mFn}{At}\) = 2,47 A.
Câu trả lời của bạn
Ta có: Eb = 3e = 2,7 V; rb = 3 \(\frac{r}{10}\) = 0,18 Ω;
I = \(\frac{E_{b}}{R+r_{b}}\) = 0,01316 A; \(m=\frac{1}{F}.\frac{A}{n}It\) = 0,013 g.
Câu trả lời của bạn
Khối lượng sắt giải phóng ở bình thứ nhất: \(m_{1}=\frac{1}{F}.\frac{A_{1}}{n_{1}}It\)
Khối lượng đồng giải phóng ở bình thứ hai: \(m_{2}=\frac{1}{F}.\frac{A_{2}}{n_{2}}It\) \(\rightarrow \frac{m_{2}}{m_{1}}=\frac{A_{2}n_{1}}{A_{1}n_{2}}m_{1}\rightarrow m_{2}=2,4g\)
Câu trả lời của bạn
Khối lượng đồng có trong thanh : \(m_{Cu}=\frac{(100-12)}{100}m=0,88(kg)\)
Định luật Faraday : \(m=\frac{1}{F}.\frac{A}{n}q \Rightarrow 880 = \frac{1}{96500}.\frac{64}{2}q\Rightarrow q=2654.10^{3}(C)\) (C )
Điện năng tiêu hao để xử lý 1 (kg) hỗn hợp : W = qU = 2654.103.6 = 15923 (kJ) = 4,42 (kWh).
Câu trả lời của bạn
- Khối lượng của hiđrô thu được ở catốt là: \(m_{1}=\frac{1}{96500}.\frac{A_{1}}{n_{1}}.I.t=\frac{1}{96500}.2,5.3860=0,1g\)
1mol khí hiđrô (H2) (đktc) có thể tích 22,4lít \(\rightarrow\) Thể tích khí hiđrô thu được: \(v_{1}=\frac{0,1}{2}.22,4=1,12\) lít
- Khối lượng của khí ôxi thu được ở anốt là: \(m_{2}=\frac{1}{96500}.\frac{A_{2}}{n_{2}}.I.t=\frac{1}{96500}.\frac{16}{2}.2,5.3860=0,8g\)
Thể tích khí hiđrô thu được: \(v_{2}=\frac{0,8}{32}.22,4=0,56\) lít
Câu trả lời của bạn
a có: \(m=\frac{1}{F}.\frac{A}{n}It\) = ρSh \(\rightarrow\) h = \(h=\frac{AIt}{Fn\rho S}=\) 0,018 cm.
Câu trả lời của bạn
+ Dòng điện qua bình : \(I=\frac{U}{R}=5(A)\)
+ Công thức pha-ra-đây về điện phân : \(m=\frac{1}{F}.\frac{A}{n}q=40,3(g)\)
Câu trả lời của bạn
Thời gian điện phân t = 30 phút = 1800 giây.
S = 30cm2 = 30.10-4 (m2)
D = 0,05 (mm) = 5.10-5 (m)
Khối lượng riêng của Niken
\(\rho \) = 8,9.103 kg/m3, A = 58, n = 2
Trước hết ta tính thể tích lớp kim loại Niken:
\(V\; = {\rm{ }}S.D{\rm{ }} = {\rm{ }}{30.10 }^{-4}{.5.10^{ - 5}} = {\rm{ }}{15.10^{ - 8}}\left( {{m^3}} \right)\)
Khối lượng lớp Niken
\(m{\rm{ }} = {\rm{ }}\rho V{\rm{ }} = {\rm{ }}8,{9.10^3}{.15.10^{ - 8}} = {\rm{ }}1,{335.10^{ - 3}}\left( {kg} \right)\)
\(=> m = 1,335\) (g)
Theo công thức Fa-ra-đây:
\(m = {1 \over {F}}.{A \over n}.I.t \Rightarrow I = {{mFn} \over {A.t}}\)
Thay số \(I = {{1,335.96500.2} \over {58.1800}} = 2,47\left( A \right)\)
Câu trả lời của bạn
Dựa vào bảng kết quả thí nghiệm (bảng 19.1) và hình 19.4.
Ta có:
| U(V) | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 |
| I (A) | 0,025 | 0,06 | 0,1 | 0,13 | 0,17 | 0,21 |
| R(Q) | 20 | 16,67 | 15 | 15,38 | 14,71 | 14,29 |
Ta nhận thấy khi U tăng, I tăng thì nhiệt độ của chất điện phân tăng vì công suất toả nhiệt tăng và điện trở R giảm.
Hay:
Bản chất dòng điện trong chất điện phân là dòng dịch chuyển có hướng của các ion dương theo chiều điện trường và các ion âm ngược chiều điện trường. Khi nhiệt độ tăng, số lượng phân tử phân li tăng dẫn đến số lượng các cặp ion được tạo thành tăng. Chính điều này làm tăng khả năng dẫn điện của dung dịch điện phân, do vậy mà điện trở của dung dịch điện phân giảm khi nhiệt độ tăng.
B. Số cặp ion được tạo thành dung dịch điện phân không thay đổi theo nhiệt độ.
C. Bình điện phân nào cũng có suất phản điện.
D. Khi có hiện tượng dương cực tan, dòng điện trong chất điện phân tuân theo định luật Ôm.
Câu trả lời của bạn
Khi có hiện tượng dương cực tan, dòng điện trong chất điện phân tuân theo định luật Ôm.
Chọn D
A.0,3.10-4g
B. 3.10-3 g
C. 0,3.10-3 g
D. 3.10-4 g
Câu trả lời của bạn
Ta có k = 3.10-4g/C, điện lượng Q = 10 (C)
Khối lượng Niken bám vào catôt theo định luật Fa-ra-đây:
\(m = kQ = {3.10^{ - 4}}.10 = {3.10^{ - 3}}(g)\)
Chọn B.
Câu trả lời của bạn
Khối lượng của niken được giải phóng ra ở điện cực của bình điện phân tuân theo định luật I Fa-ra-đây :\(m = kq = kIt\)
Trong đó k là đương lượng điện hoá của niken, \(q = It\) là điện lượng chuyển qua dung dịch điện phân.
Thay số, ta tìm được : \(m = 0,3.10^{-3}.5,0.3600 = 5,4g.\)
Câu trả lời của bạn
Áp dụng công thức Fa-ra-đây về điện phân dung dịch đồng sunphat (CuSO4) có anôt bằng đồng (Cu), ta có:
\(m = \dfrac{1}{F}.\dfrac{A}{ n}.It = \dfrac{1}{96500}.\dfrac{A}{n}.It\)
Thay số, với A = 63,5 g/mol, n = 2, t = 30 phút = 1800 giây và m = 1,143 g. ta tìm được cường độ dòng điện chạy qua dung dịch điện phân :
\(I = \dfrac{96500.nm}{At} = \dfrac{96500.2.1,143}{63,5.30.60} = 1,93A\)
Câu trả lời của bạn
Cho một ít muối ăn (NaCl) vào nước, NaCl phân li thành 2 loại ion
\(NaCl \to N{a^ + } + C{l^ - }\)
Khi chưa đặt một hiệu điện thế vào hai cực của bình điện phân thì các ion Na+và Cl- chuyển động nhiệt hỗn loạn và sau một thời gian ta có sự cân bằng động giữa quá trình phân li và tái hợp.
Đặt một hiệu điện thế xác định vào hai điện cực, trong chất điện phân hình thành một điện trường hướng từ anôt sang catôt, dưới tác dụng của điện trường, các ion lúc này chuyển động có hướng; Các ion Na+ dịch chuyển cùng chiều điện trường về catôt nhận một êlectron trở thành Na trung hoà, các ion Cl- ngược hướng điện trường về anôt cho một êlectron trở thành Cl trung hoà và kết hợp với Na tan lại vào dung dịch.
Kết quả có dòng điện qua chất điện phân.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *